L'istituto del cloro, Inc.
L'elettrolisi delle salamoie produce cloro e sostanze caustiche. Il cloruro di sodio (NaCl) è il sale principale utilizzato; produce soda caustica (NaOH). Tuttavia, l'uso di cloruro di potassio (KCl) produce potassa caustica (KOH).
2 NaCl + 2 H2O → Cl2↑+2NaOH+H2↑
sale + acqua → cloro (gas) + caustico + idrogeno (gas)
Attualmente il processo con celle a diaframma è il più utilizzato per la produzione commerciale di cloro, seguito dal processo con celle a mercurio e quindi dal processo con celle a membrana. A causa di problemi economici, ambientali e di qualità del prodotto, i produttori ora preferiscono il processo con cella a membrana per i nuovi impianti di produzione.
Il processo della cella a diaframma
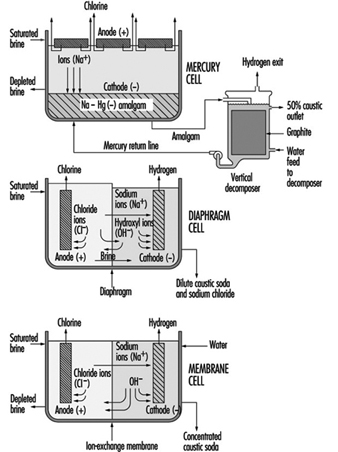
Una cella a diaframma (vedi figura 1) viene alimentata con salamoia satura in un compartimento contenente un anodo di titanio rivestito con sali di rutenio e altri metalli. Una testa della cella di plastica raccoglie il cloro gassoso caldo e umido prodotto su questo anodo. L'aspirazione da parte di un compressore aspira quindi il cloro in un collettore di raccolta per l'ulteriore lavorazione consistente in raffreddamento, essiccazione e compressione. L'acqua e la salamoia non reagita percolano attraverso un separatore a diaframma poroso nel compartimento catodico dove l'acqua reagisce su un catodo di acciaio per produrre idrossido di sodio (soda caustica) e idrogeno. Il diaframma trattiene il cloro prodotto all'anodo dall'idrossido di sodio e l'idrogeno prodotto al catodo. Se questi prodotti si combinano, il risultato è ipoclorito di sodio (candeggina) o clorato di sodio. I produttori commerciali di clorato di sodio utilizzano celle prive di separatori. Il diaframma più comune è un composto di amianto e un polimero di fluorocarburo. I moderni impianti con celle a diaframma non presentano i problemi sanitari o ambientali storicamente associati all'uso di diaframmi in amianto. Alcuni impianti impiegano diaframmi non amianto, che sono ora disponibili in commercio. Il processo della cella a diaframma produce una soluzione debole di idrossido di sodio contenente sale non reagito. Un ulteriore processo di evaporazione concentra la sostanza caustica e rimuove la maggior parte del sale per ottenere una sostanza caustica di qualità commerciale.
Figura 1. Tipi di processi cellulari cloralcali
Il processo della cella di mercurio
Una cella a mercurio consiste in realtà di due celle elettrochimiche. La reazione nella prima cella all'anodo è:
2 Cl- → DO12 + 2 e-
cloruro → cloro + elettroni
La reazione nella prima cella al catodo è:
Na+ + Hg + e- →Na·Hg
ione sodio + mercurio + elettroni → amalgama di sodio
La salamoia scorre in una vasca d'acciaio inclinata con lati rivestiti in gomma (vedi figura 4) Il mercurio, il catodo, scorre sotto la salamoia. Gli anodi di titanio rivestito sono sospesi nella salamoia per la produzione di cloro, che esce dalla cella verso un sistema di raccolta e lavorazione. Il sodio viene elettrolizzato nella cella e lascia la prima cella amalgamato con il mercurio. Questo amalgama fluisce in una seconda cella elettrochimica chiamata decompositore. Il decompositore è una cella con grafite come catodo e l'amalgama come anodo.
La reazione nel decompositore è:
2 Na•Hg + 2 H2O → 2 NaOH + 2 Hg + H2 ↑
Il processo della cella a mercurio produce NaOH commerciale (50%) direttamente dalla cella.
Il processo cellulare a membrana
Le reazioni elettrochimiche in una cella a membrana sono le stesse della cella a diaframma. Una membrana a scambio cationico viene utilizzata al posto del diaframma poroso (vedi figura 1). Questa membrana impedisce la migrazione di ioni cloruro nel catolita, producendo in tal modo sostanza caustica dal 30 al 35% essenzialmente senza sale direttamente dalla cella. L'eliminazione della necessità di rimuovere il sale rende più semplice l'evaporazione della sostanza caustica al 50% commerciale e richiede meno investimenti ed energia. Il nichel costoso viene utilizzato come catodo nella cella della membrana a causa della caustica più forte.
Rischi per la sicurezza e la salute
A temperature ordinarie, il cloro secco, liquido o gassoso, non corrode l'acciaio. Il cloro umido è altamente corrosivo perché forma acido cloridrico e ipocloroso. Devono essere prese precauzioni per mantenere il cloro e le apparecchiature per il cloro asciutte. Tubazioni, valvole e contenitori devono essere chiusi o tappati quando non in uso per tenere fuori l'umidità atmosferica. Se si utilizza acqua su una perdita di cloro, le condizioni corrosive risultanti peggioreranno la perdita.
Il volume del cloro liquido aumenta con la temperatura. Devono essere prese precauzioni per evitare la rottura idrostatica di tubazioni, recipienti, contenitori o altre apparecchiature riempite con cloro liquido.
L'idrogeno è un coprodotto di tutto il cloro prodotto dall'elettrolisi di soluzioni acquose di salamoia. Entro un intervallo di concentrazione noto, le miscele di cloro e idrogeno sono infiammabili e potenzialmente esplosive. La reazione di cloro e idrogeno può essere avviata dalla luce solare diretta, da altre fonti di luce ultravioletta, dall'elettricità statica o da un forte impatto.
Piccole quantità di tricloruro di azoto, un composto instabile e altamente esplosivo, possono essere prodotte nella produzione di cloro. Quando il cloro liquido contenente tricloruro di azoto viene evaporato, il tricloruro di azoto può raggiungere concentrazioni pericolose nel restante cloro liquido.
Il cloro può reagire, a volte in modo esplosivo, con una serie di materiali organici come olio e grasso provenienti da fonti quali compressori d'aria, valvole, pompe e strumentazione a membrana oleosa, nonché legno e stracci provenienti da lavori di manutenzione.
Non appena vi è alcuna indicazione di un rilascio di cloro, è necessario adottare misure immediate per correggere la condizione. Le perdite di cloro peggiorano sempre se non vengono tempestivamente corrette. Quando si verifica una perdita di cloro, il personale autorizzato e addestrato dotato di respiratori e altri dispositivi di protezione individuale (DPI) appropriati deve indagare e adottare le misure adeguate. Il personale non deve entrare in atmosfere contenenti concentrazioni di cloro superiori alla concentrazione immediatamente pericolosa per la vita e la salute (IDLH) (10 ppm) senza DPI adeguati e personale di supporto. Il personale non necessario deve essere tenuto lontano e l'area di pericolo deve essere isolata. Le persone potenzialmente colpite da un rilascio di cloro dovrebbero essere evacuate o riparate sul posto a seconda delle circostanze.
I monitor del cloro dell'area e gli indicatori di direzione del vento possono fornire informazioni tempestive (ad esempio, vie di fuga) per aiutare a determinare se il personale deve essere evacuato o riparato sul posto.
Quando viene utilizzata l'evacuazione, le persone potenzialmente esposte dovrebbero spostarsi in un punto sopravento rispetto alla perdita. Poiché il cloro è più pesante dell'aria, sono preferibili quote più elevate. Per fuggire nel più breve tempo possibile, le persone che si trovano già in un'area contaminata devono muoversi con vento laterale.
Quando all'interno di un edificio e viene selezionato il riparo sul posto, è possibile ottenere un riparo chiudendo tutte le finestre, porte e altre aperture e spegnendo i condizionatori d'aria e i sistemi di aspirazione dell'aria. Il personale deve spostarsi sul lato dell'edificio più lontano dal rilascio.
Si deve prestare attenzione a non posizionare il personale senza una via di fuga. Una posizione sicura può essere resa pericolosa da un cambio di direzione del vento. Potrebbero verificarsi nuove perdite o la perdita esistente potrebbe aumentare.
Se l'incendio è presente o imminente, i contenitori e le attrezzature per il cloro devono essere spostati lontano dall'incendio, se possibile. Se un contenitore o un'attrezzatura che non perde non può essere spostato, dovrebbe essere mantenuto fresco applicando acqua. L'acqua non deve essere utilizzata direttamente su una perdita di cloro. Il cloro e l'acqua reagiscono formando acidi e la perdita peggiorerà rapidamente. Tuttavia, se sono coinvolti più contenitori e alcuni perdono, può essere prudente utilizzare uno spruzzo d'acqua per aiutare a prevenire la sovrapressione dei contenitori che non perdono.
Ogni volta che i contenitori sono stati esposti alle fiamme, l'acqua di raffreddamento deve essere applicata fino a quando il fuoco non si è spento e i contenitori si sono raffreddati. I contenitori esposti al fuoco devono essere isolati e il fornitore deve essere contattato il prima possibile.
Le soluzioni di idrossido di sodio sono corrosive, specialmente se concentrate. I lavoratori a rischio di esposizione a fuoriuscite e perdite devono indossare guanti, visiera, occhiali e altri indumenti protettivi.
Ringraziamenti: Si ringrazia il Dr. RG Smerko per aver messo a disposizione le risorse del Chlorine Institute, Inc.