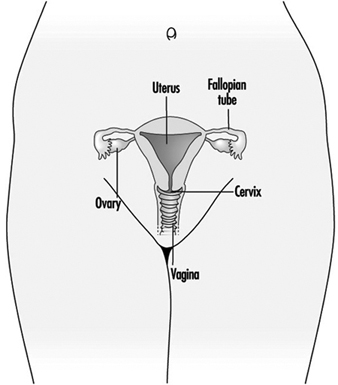
Слика 1. Женски репродуктивни систем.
Женски репродуктивни систем контролишу компоненте централног нервног система, укључујући хипоталамус и хипофизу. Састоји се од јајника, јајовода, материце и вагине (слика 1). Јајници, женске гонаде, су извор ооцита и такође синтетишу и луче естрогене и прогестагене, главне женске полне хормоне. Јајоводи транспортују ооците до материце и сперму из материце. Материца је мишићни орган крушколиког облика, чији горњи део преко јајовода комуницира са трбушном дупљом, док је доњи део суседан кроз уски канал грлића материце са вагином, који прелази ка спољашности. Табела 1 сумира једињења, клиничке манифестације, место и механизме деловања потенцијалних репродуктивних токсиканата.
Табела 1. Потенцијални репродуктивни токсиканти код жена
| Једињење | Клиничка манифестација | Сајт | Механизам/циља |
| Хемијска реактивност | |||
| Алкилирање агенти |
Промењена менструација аменореја Атрофија јајника Смањена плодност Превремена менопауза |
јајник материца |
Цитотоксичност ћелија гранулозе Цитотоксичност ооцита Цитотоксичност ћелија ендометријума |
| Довести | Абнормалне менструације Атрофија јајника Смањена плодност |
хипоталамус Хипофиза јајник |
Смањен ФСХ Смањен прогестерон |
| Меркур | Абнормалне менструације | хипоталамус јајник |
Промењена производња и лучење гонадотропина Токсичност фоликула Пролиферација гранулозних ћелија |
| Кадмијум | Фоликуларна атрезија Перзистентни диеструс |
јајник Хипофиза хипоталамус |
Васкуларна токсичност Цитотоксичност ћелија гранулозе Цитотоксичност |
| Структурна сличност | |||
| Азатиоприн | Смањен број фоликула | јајник Оогенеза |
Пурине аналог Поремећај синтезе ДНК/РНА |
| Хлордекон | Оштећена плодност | хипоталамус | Естроген агонист |
| ДДТ | Промењена менструација | Хипофиза | Поремећај ФСХ, ЛХ |
| 2,4-Д | неплодност | ||
| Линдане | аменореја | ||
| Токсафен | Хиперменореја | ||
| ПЦБ, ПББ | Абнормалне менструације | Поремећај ФСХ, ЛХ | |
Извор: из Пловцхалк, Меадовс и Маттисон 1992. Предлаже се да су ова једињења директно делујући репродуктивни токсиканти на основу испитивања токсичности на експерименталним животињама.
Хипоталамус и хипофиза
Хипоталамус се налази у диенцефалону, који се налази на врху можданог стабла и окружен је можданим хемисферама. Хипоталамус је главни посредник између нервног и ендокриног система, два главна контролна система тела. Хипоталамус регулише рад хипофизе и производњу хормона.
Механизми помоћу којих хемикалија може пореметити репродуктивну функцију хипоталамуса генерално укључује сваки догађај који би могао да модификује пулсирајуће ослобађање гонадотропин ослобађајућег хормона (ГнРХ). Ово може укључивати промену фреквенције или амплитуде ГнРХ импулса. Процеси подложни хемијским повредама су они који су укључени у синтезу и секрецију ГнРХ—тачније, транскрипција или транслација, паковање или аксонални транспорт и секреторни механизми. Ови процеси представљају места где хемијски реактивна једињења директног дејства могу да ометају хипоталмичку синтезу или ослобађање ГнРХ. Измењена фреквенција или амплитуда ГнРХ импулса може бити последица поремећаја у стимулативним или инхибиторним путевима који регулишу ослобађање ГнРХ. Истраживања регулације генератора ГнРХ импулса су показала да катехоламини, допамин, серотонин, γ-аминобутерна киселина и ендорфини имају известан потенцијал за промену ослобађања ГнРХ. Стога, ксенобиотици који су агонисти или антагонисти ових једињења могу да модификују ослобађање ГнРХ, ометајући тако комуникацију са хипофизом.
Пролактин, фоликулостимулишући хормон (ФСХ) и лутеинизирајући хормон (ЛХ) су три протеинска хормона које лучи предња хипофиза и која су неопходна за репродукцију. Они играју кључну улогу у одржавању циклуса јајника, регулишући регрутовање и сазревање фоликула, стероидогенезу, завршетак сазревања јајних ћелија, овулацију и лутеинизацију.
Прецизна, фино подешена контрола репродуктивног система се постиже од стране предње хипофизе као одговор на позитивне и негативне повратне сигнале из гонада. Одговарајуће ослобађање ФСХ и ЛХ током циклуса јајника контролише нормалан развој фоликула, а одсуство ових хормона је праћено аменорејом и атрофијом гонада. Гонадотропини играју кључну улогу у покретању промена у морфологији фоликула јајника иу њиховом стероидном микроокружењу кроз стимулацију производње стероида и индукцију популација рецептора. Правовремено и адекватно ослобађање ових гонадотропина је такође неопходно за овулаторне догађаје и функционалну лутеалну фазу. Пошто су гонадотропини неопходни за функцију јајника, измењена синтеза, складиштење или секреција могу озбиљно пореметити репродуктивни капацитет. Интерференција са експресијом гена – било у транскрипцији или транслацији, пост-транслационим догађајима или паковању, или секреторним механизмима – може да модификује ниво гонадотропина који доспева до гонада. Хемикалије које делују на основу структурне сличности или измењене ендокрине хомеостазе могу произвести ефекте мешањем у нормалне механизме повратне спреге. Агонисти и антагонисти стероидних рецептора могу иницирати неодговарајуће ослобађање гонадотропина из хипофизе, чиме индукују ензиме који метаболизирају стероиде, смањујући полуживот стероида и последично циркулишући ниво стероида који достижу хипофизу.
Тхе Овари
Јајник код примата је одговоран за контролу репродукције кроз своје главне производе, ооците и стероидне и протеинске хормоне. Фоликулогенеза, која укључује и интраоваријалне и екстраоваријске регулаторне механизме, је процес којим се производе ооцити и хормони. Сам јајник има три функционалне подјединице: фоликул, ооцит и жуто тело. Током нормалног менструалног циклуса, ове компоненте, под утицајем ФСХ и ЛХ, функционишу заједно како би произвеле одрживу јајну ћелије за оплодњу и погодно окружење за имплантацију и каснију гестацију.
Током преовулаторног периода менструалног циклуса, регрутовање и развој фоликула се дешавају под утицајем ФСХ и ЛХ. Потоњи стимулише производњу андрогена од стране текалних ћелија, док први стимулише ароматизацију андрогена у естрогене од стране гранулоза ћелија и производњу инхибина, протеинског хормона. Инхибин делује на предњу хипофизу како би смањио ослобађање ФСХ. Ово спречава прекомерну стимулацију развоја фоликула и омогућава наставак развоја доминантног фоликула - фоликула који је предодређен за овулацију. Повећава се производња естрогена, стимулишући и пораст ЛХ (које резултира овулацијом) и ћелијске и секреторне промене у вагини, грлићу материце, материци и јајоводу које побољшавају одрживост и транспорт сперматозоида.
У постовулаторној фази, текалне и гранулозне ћелије које остају у фоликуларној шупљини овулиране јајне ћелије, формирају жуто тело и луче прогестерон. Овај хормон стимулише материцу да обезбеди одговарајуће окружење за имплантацију ембриона ако дође до оплодње. За разлику од мушке гонаде, женске гонаде при рођењу имају коначан број заметних ћелија и стога су јединствено осетљиве на репродуктивне токсичне материје. Такво излагање женке може довести до смањене плодности, повећаног губитка трудноће, ране менопаузе или неплодности.
Као основна репродуктивна јединица јајника, фоликул одржава деликатно хормонско окружење неопходно да подржи раст и сазревање ооцита. Као што је раније поменуто, овај сложени процес је познат као фоликулогенеза и укључује и интраоваријалну и екстраоваријалну регулацију. Бројне морфолошке и биохемијске промене се јављају како примордијални фоликул напредује до пре-овулаторног фоликула (који садржи ооцит у развоју), а свака фаза раста фоликула показује јединствене обрасце осетљивости на гонадотропин, производњу стероида и повратне путеве. Ове карактеристике сугеришу да је на располагању низ места за интеракцију ксенобиотика. Такође, постоје различите популације фоликула унутар јајника, што додатно компликује ситуацију дозвољавајући диференцијалну токсичност фоликула. Ово ствара ситуацију у којој би обрасци неплодности изазвани хемијским агенсом зависили од типа погођеног фоликула. На пример, токсичност за примордијалне фоликуле не би произвела тренутне знаке неплодности, али би на крају скратила репродуктивни животни век. С друге стране, токсичност за антралне или преовулаторне фоликуле би резултирала тренутним губитком репродуктивне функције. Комплекс фоликула се састоји од три основне компоненте: гранулозне ћелије, текалне ћелије и ооцита. Свака од ових компоненти има карактеристике које је могу учинити јединствено подложном хемијским повредама.
Неколико истраживача је истражило методологију за скрининг ксенобиотика на токсичност гранулоза ћелија мерењем ефеката на производњу прогестерона ћелијама гранулозе у култури. Супресија производње прогестерона у ћелијама гранулозе естрадиолом је коришћена да би се верификовала реакција гранулозе ћелија. Пестицид п,п'-ДДТ и његов о,п'-ДДТ изомер производе супресију производње прогестерона очигледно са потенцијама једнаким оној естрадиола. Насупрот томе, пестициди малатион, аратион и диелдрин и фунгицид хексахлоробензен су без ефекта. Потребна је даља детаљна анализа одговора изолованих ћелија гранулозе на ксенобиотике да би се дефинисала корисност овог система испитивања. Привлачност изолованих система као што је овај је економичност и лакоћа коришћења; међутим, важно је запамтити да ћелије гранулозе представљају само једну компоненту репродуктивног система.
Текалне ћелије обезбеђују прекурсоре за стероиде које синтетишу гранулоза ћелије. Верује се да се текалне ћелије регрутују из ћелија строме јајника током формирања и раста фоликула. Регрутовање може укључивати стромалну ћелијску пролиферацију, као и миграцију у регионе око фоликула. Ксенобиотици који ометају пролиферацију ћелија, миграцију и комуникацију ће утицати на функцију ћелија. Ксенобиотици који мењају производњу андрогена могу такође оштетити функцију фоликула. На пример, андрогени који се метаболишу у естрогене у гранулозним ћелијама обезбеђују текалне ћелије. Очекује се да промене у производњи андрогена у ћелијама, било да се повећавају или смањују, имају значајан утицај на функцију фоликула. На пример, верује се да ће вишак производње андрогена од стране текалних ћелија довести до атрезије фоликула. Поред тога, оштећена производња андрогена у текалним ћелијама може довести до смањене производње поестрогена у ћелијама гранулозе. Свака од ових околности ће јасно утицати на репродуктивни учинак. За сада, мало се зна о рањивости текалних ћелија на ксенобиотике.
Иако постоји оштрина информација које дефинишу рањивост ћелија јајника на ксенобиотике, постоје подаци који јасно показују да ооцити могу бити оштећени или уништени таквим агенсима. Алкилациона средства уништавају ооците код људи и експерименталних животиња. Олово производи токсичност за јајнике. Жива и кадмијум такође производе оштећење јајника које може бити посредовано токсичношћу ооцита.
Оплодња до имплантације
Гаметогенеза, ослобађање и спајање мушких и женских заметних ћелија су прелиминарни догађаји који воде до зигота. Сперматозоиди депоновани у вагини морају да уђу у грлић материце и да се крећу кроз материцу у јајовод да би се сусрели са јајном јајом. пенетрација јајне ћелије сперматозоида и спајање њихове одговарајуће ДНК чине процес оплодње. Након оплодње почиње деоба ћелија и наставља се током наредна три или четири дана, формирајући чврсту масу ћелија која се зове морула. Ћелије моруле настављају да се деле, а док ембрион у развоју стигне до материце, то је шупља лопта која се зове бластоциста.
Након оплодње, ембрион у развоју мигрира кроз јајовод у материцу. Бластоциста улази у материцу и имплантира се у ендометријум отприлике седам дана након овулације. У овом тренутку ендометријум је у постовулаторној фази. Имплантација омогућава бластоцисти да апсорбује хранљиве материје или токсичне материје из жлезда и крвних судова ендометријума.