Le decisioni che riguardano la salute, il benessere e l'occupabilità dei singoli lavoratori o l'approccio di un datore di lavoro alle questioni di salute e sicurezza devono basarsi su dati di buona qualità. Ciò è particolarmente vero nel caso dei dati di monitoraggio biologico ed è quindi responsabilità di qualsiasi laboratorio che intraprenda un lavoro analitico su campioni biologici provenienti da popolazioni attive garantire l'affidabilità, l'accuratezza e la precisione dei suoi risultati. Questa responsabilità si estende dal fornire metodi e linee guida adeguati per la raccolta dei campioni fino a garantire che i risultati vengano restituiti all'operatore sanitario responsabile della cura del singolo lavoratore in una forma adeguata. Tutte queste attività sono coperte dall'espressione di garanzia della qualità.
L'attività centrale in un programma di garanzia della qualità è il controllo e il mantenimento dell'accuratezza e della precisione analitiche. I laboratori di monitoraggio biologico si sono spesso sviluppati in un ambiente clinico e hanno adottato tecniche e filosofie di garanzia della qualità dalla disciplina della chimica clinica. In effetti, le misurazioni delle sostanze chimiche tossiche e degli indicatori di effetti biologici nel sangue e nelle urine non sono essenzialmente diverse da quelle effettuate nei laboratori di chimica clinica e di farmacologia clinica presenti in qualsiasi grande ospedale.
Un programma di garanzia della qualità per un singolo analista inizia con la selezione e la definizione di un metodo adeguato. La fase successiva è lo sviluppo di una procedura interna di controllo della qualità per mantenere la precisione; il laboratorio deve quindi accertarsi dell'accuratezza dell'analisi, e questo può comportare una valutazione esterna della qualità (vedi sotto). È importante riconoscere, tuttavia, che la garanzia della qualità include più di questi aspetti del controllo della qualità analitica.
Selezione del metodo
Esistono diversi testi che presentano metodi analitici nel monitoraggio biologico. Sebbene questi forniscano una guida utile, molto deve essere fatto dal singolo analista prima che possano essere prodotti dati di qualità adeguata. Fondamentale per qualsiasi programma di garanzia della qualità è la produzione di un protocollo di laboratorio che deve specificare in dettaglio quelle parti del metodo che hanno la maggiore influenza sulla sua affidabilità, accuratezza e precisione. In effetti, l'accreditamento nazionale dei laboratori di chimica clinica, tossicologia e scienze forensi dipende solitamente dalla qualità dei protocolli del laboratorio. Lo sviluppo di un protocollo adatto è solitamente un processo che richiede tempo. Se un laboratorio desidera stabilire un nuovo metodo, spesso è più conveniente ottenere da un laboratorio esistente un protocollo che abbia dimostrato le sue prestazioni, ad esempio, attraverso la convalida in un programma internazionale stabilito di garanzia della qualità. Se il nuovo laboratorio è impegnato in una tecnica analitica specifica, ad esempio la gascromatografia piuttosto che la cromatografia liquida ad alta prestazione, è spesso possibile identificare un laboratorio che ha un buon record di prestazioni e che utilizza lo stesso approccio analitico. I laboratori possono spesso essere identificati tramite articoli di riviste o organizzatori di vari schemi nazionali di valutazione della qualità.
Controllo di qualità interno
La qualità dei risultati analitici dipende dalla precisione del metodo raggiunto nella pratica, e questo a sua volta dipende dalla stretta aderenza a un protocollo definito. La precisione viene valutata al meglio includendo "campioni di controllo qualità" a intervalli regolari durante un ciclo analitico. Ad esempio, per il controllo delle analisi del piombo nel sangue, i campioni di controllo della qualità vengono introdotti nella corsa ogni sei o otto campioni di lavoratori effettivi. Metodi analitici più stabili possono essere monitorati con meno campioni di controllo qualità per ciclo. I campioni di controllo qualità per l'analisi della piombemia vengono preparati da 500 ml di sangue (umano o bovino) addizionato di piombo inorganico; singole aliquote vengono conservate a bassa temperatura (Bullock, Smith e Whitehead 1986). Prima che ogni nuovo lotto venga utilizzato, 20 aliquote vengono analizzate in corse separate in diverse occasioni per stabilire il risultato medio per questo lotto di campioni di controllo di qualità, nonché la sua deviazione standard (Whitehead 1977). Queste due figure vengono utilizzate per impostare una carta di controllo di Shewhart (figura 27.2). I risultati dell'analisi dei campioni di controllo di qualità inclusi nelle esecuzioni successive vengono tracciati sul grafico. L'analista utilizza quindi regole per l'accettazione o il rifiuto di un ciclo analitico a seconda che i risultati di questi campioni rientrino in due o tre deviazioni standard (SD) della media. Una sequenza di regole, convalidata dalla modellazione al computer, è stata suggerita da Westgard et al. (1981) per l'applicazione ai campioni di controllo. Questo approccio al controllo di qualità è descritto nei libri di testo di chimica clinica e un semplice approccio all'introduzione della garanzia di qualità è esposto in Whitehead (1977). Va sottolineato che queste tecniche di controllo qualità dipendono dalla preparazione e dall'analisi di campioni di controllo qualità separatamente dai campioni di calibrazione che vengono utilizzati in ogni occasione analitica.
Figura 27.2 Carta di controllo di Shewhart per campioni di controllo qualità
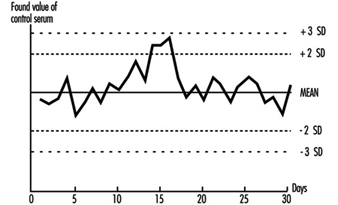
Questo approccio può essere adattato a una serie di analisi di monitoraggio biologico o di monitoraggio degli effetti biologici. È possibile preparare lotti di campioni di sangue o di urina aggiungendo il materiale tossico o il metabolita da misurare. Allo stesso modo, il sangue, il siero, il plasma o l'urina possono essere aliquotati e conservati surgelati o liofilizzati per la misurazione di enzimi o proteine. Tuttavia, occorre prestare attenzione per evitare il rischio infettivo per l'analista da campioni basati su sangue umano.
L'attenta osservanza di un protocollo ben definito e di regole per l'accettabilità è una prima fase essenziale in un programma di garanzia della qualità. Qualsiasi laboratorio deve essere preparato a discutere il controllo di qualità e le prestazioni di valutazione della qualità con gli operatori sanitari che lo utilizzano e ad indagare su risultati sorprendenti o insoliti.
Valutazione esterna della qualità
Una volta che un laboratorio ha stabilito di poter produrre risultati con adeguata precisione, la fase successiva è quella di confermare l'accuratezza ("esattezza") dei valori misurati, cioè la relazione delle misurazioni effettuate con la quantità effettiva presente. Questo è un esercizio difficile da svolgere da solo per un laboratorio, ma può essere ottenuto partecipando a un regolare programma esterno di valutazione della qualità. Questi sono stati una parte essenziale della pratica chimica clinica per qualche tempo, ma non sono stati ampiamente disponibili per il monitoraggio biologico. L'eccezione è l'analisi del piombo nel sangue, dove gli schemi sono disponibili dagli anni '1970 (ad esempio, Bullock, Smith e Whitehead 1986). Il confronto dei risultati analitici con quelli riportati da altri laboratori che analizzano campioni dello stesso lotto consente la valutazione delle prestazioni di un laboratorio rispetto ad altri, nonché una misura della sua accuratezza. Sono disponibili diversi schemi di valutazione della qualità nazionali e internazionali. Molti di questi schemi accolgono nuovi laboratori, poiché la validità della media dei risultati di un analita di tutti i laboratori partecipanti (presa come misura della concentrazione effettiva) aumenta con il numero di partecipanti. I programmi con molti partecipanti sono anche maggiormente in grado di analizzare le prestazioni di laboratorio secondo il metodo analitico e quindi consigliare alternative ai metodi con caratteristiche di prestazioni scadenti. In alcuni paesi, la partecipazione a tale schema è una parte essenziale dell'accreditamento del laboratorio. Le linee guida per la progettazione e il funzionamento del sistema di valutazione esterna della qualità sono state pubblicate dall'OMS (1981).
In assenza di schemi di valutazione esterna della qualità stabiliti, l'accuratezza può essere verificata utilizzando materiali di riferimento certificati che sono disponibili su base commerciale per una gamma limitata di analiti. I vantaggi dei campioni distribuiti da schemi esterni di valutazione della qualità sono che (1) l'analista non ha una conoscenza anticipata del risultato, (2) viene presentato un intervallo di concentrazioni e (3) poiché i metodi analitici definitivi non devono essere impiegati, i materiali coinvolti sono più economici.
Controllo di qualità pre-analitico
Lo sforzo speso per ottenere una buona accuratezza e precisione di laboratorio è sprecato se i campioni presentati al laboratorio non sono stati prelevati al momento giusto, se hanno subito contaminazione, si sono deteriorati durante il trasporto o sono stati etichettati in modo inadeguato o errato. È anche una cattiva pratica professionale sottoporre individui a campionamenti invasivi senza prendersi cura adeguata dei materiali campionati. Sebbene il campionamento spesso non sia sotto il diretto controllo dell'analista di laboratorio, un programma di monitoraggio biologico di qualità completa deve tenere conto di questi fattori e il laboratorio dovrebbe garantire che le siringhe e i contenitori dei campioni forniti siano privi di contaminazione, con chiare istruzioni sulla tecnica di campionamento e conservazione e trasporto del campione. L'importanza del corretto tempo di campionamento all'interno del turno o della settimana lavorativa e la sua dipendenza dalla tossicocinetica del materiale campionato sono ormai riconosciute (ACGIH 1993; HSE 1992), e queste informazioni dovrebbero essere messe a disposizione degli operatori sanitari responsabili della raccolta dei campioni .
Controllo qualità post-analitico
Risultati analitici di alta qualità possono essere di scarsa utilità per l'individuo o per il professionista sanitario se non vengono comunicati al professionista in una forma interpretabile e al momento giusto. Ogni laboratorio di monitoraggio biologico dovrebbe sviluppare procedure di refertazione per avvisare l'operatore sanitario che presenta i campioni di risultati anomali, inaspettati o sconcertanti in tempo per consentire l'adozione di misure appropriate. L'interpretazione dei risultati di laboratorio, in particolare le variazioni di concentrazione tra campioni successivi, dipende spesso dalla conoscenza della precisione del test. Nell'ambito della gestione totale della qualità, dalla raccolta del campione alla restituzione dei risultati, agli operatori sanitari dovrebbero essere fornite informazioni sulla precisione e l'accuratezza del laboratorio di monitoraggio biologico, nonché sugli intervalli di riferimento e sui limiti indicativi e legali, al fine di aiutarli nell'interpretazione dei risultati.
