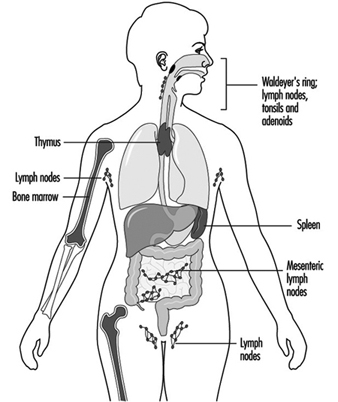
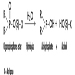Деца категорије

27. Биолошки мониторинг (6)

27. Биолошки мониторинг
Уредник поглавља: Роберт Лауверис
Преглед садржаја
Табеле и слике
Општи принципи
Вито Фоа и Лоренцо Алесио
Осигурање квалитета
Д. Гомпертз
Метали и органометална једињења
П. Хоет и Роберт Лауверис
Органски растварачи
Масаиуки Икеда
Генотоксичне хемикалије
Марја Сорса
Пестициди
Марко Марони и Адалберто Фериоли
Столови
Кликните на везу испод да видите табелу у контексту чланка.
1. АЦГИХ, ДФГ и друге граничне вредности за метале
2. Примери хемикалија и биолошког праћења
3. Биолошки мониторинг за органске раствараче
4. Генотоксичност хемикалија коју је проценио ИАРЦ
5. Биомаркери и неки узорци ћелија/ткива и генотоксичност
6. Људски карциногени, професионална изложеност и цитогенетске крајње тачке
8. Изложеност од производње и употребе пестицида
9. Акутна ОП токсичност на различитим нивоима инхибиције АЦХЕ
КСНУМКС. Варијације АЦХЕ & ПЦХЕ и одабраних здравствених стања
КСНУМКС. Активности холинестеразе неекспонираних здравих људи
КСНУМКС. Уринарни алкил фосфати и ОП пестициди
КСНУМКС. Мерење алкил фосфата у урину и ОП
КСНУМКС. Метаболити карбамата у урину
КСНУМКС. Метаболити дитиокарбамата у урину
КСНУМКС. Предложени индекси за биолошки мониторинг пестицида
КСНУМКС. Препоручене биолошке граничне вредности (од 1996.)
фигуре
Поставите показивач на сличицу да бисте видели наслов слике, кликните да бисте видели слику у контексту чланка.

28. Епидемиологија и статистика (12)

28. Епидемиологија и статистика
Уредници поглавља: Франко Мерлети, Цолин Л. Сосколне и Паоло Винеис
Преглед садржаја
Табеле и слике
Епидемиолошка метода примењена на безбедност и здравље на раду
Франко Мерлети, Цолин Л. Сосколне и Паоло Винеис
Процена изложености
М. Гералд Отт
Резиме Мере изложености током радног века
Цолин Л. Сосколне
Мерење ефеката изложености
Шелија Хоар Зам
Студија случаја: Мере
Франко Мерлети, Цолин Л. Сосколне и Паола Винеис
Опције у дизајну студија
Свен Хернберг
Питања ваљаности у дизајну студија
Анние Ј. Сасцо
Утицај случајне грешке мерења
Паоло Винеис и Колин Л. Сосколне
Статистичке методе
Аннибале Биггери и Марио Брага
Процена узрочности и етика у епидемиолошким истраживањима
Паоло Винеис
Студије случаја које илуструју методолошка питања у надзору професионалних болести
Јунг-Дер Ванг
Упитници у епидемиолошким истраживањима
Стевен Д. Стеллман и Цолин Л. Сосколне
Историјска перспектива азбеста
Лоренс Гарфинкел
Столови
Кликните на везу испод да видите табелу у контексту чланка.
1. Пет одабраних збирних мера изложености током радног века
3. Мере повезивања за кохортну студију
4. Мере повезивања за студије случаја-контроле
5. Општи изглед табеле учесталости за податке кохорте
6. Пример распореда података о контроли случајева
7. Изглед података случај-контрола - једна контрола по случају
8. Хипотетичка кохорта од 1950 особа до Т2
9. Индекси централне тенденције и дисперзије
КСНУМКС. Биномни експеримент и вероватноће
КСНУМКС. Могући исходи биномског експеримента
КСНУМКС. Биномна дистрибуција, 15 успеха/30 покушаја
КСНУМКС. Биномна расподела, п = 0.25; 30 суђења
КСНУМКС. Тип ИИ грешка и снага; x = КСНУМКС, n = 30, а = 0.05
КСНУМКС. Тип ИИ грешка и снага; x = КСНУМКС, n = 40, а = 0.05
КСНУМКС. 632 радника изложена азбесту 20 година или дуже
КСНУМКС. О/Е број умрлих међу 632 радника азбеста
фигуре
Поставите показивач на сличицу да бисте видели наслов слике, кликните да бисте видели слику у контексту чланка.

29. Ергономија (27)

29. Ергономија
Уредници поглавља: Волфганг Лауриг и Јоаким Ведер
Преглед садржаја
Табеле и слике
преглед
Волфганг Лауриг и Јоаким Ведер
Циљеви, принципи и методе
Природа и циљеви ергономије
Вилијам Т. Синглтон
Анализа активности, задатака и система рада
Вероникуе Де Кеисер
Ергономија и стандардизација
Фриедхелм Нацхреинер
цхецклистс
Пранаб Кумар Наг
Физички и физиолошки аспекти
Антропометрија
Мелцхиорре Масали
Мусцулар Ворк
Јухани Смоландер и Веикко Лухеваара
Положаји на послу
Илкка Куоринка
Биомеханика
Франк Дарби
Општи умор
Етиенне Грандјеан
Умор и опоравак
Ролф Хелбиг и Валтер Рохмерт
Психолошки аспекти
Ментал Ворклоад
Винфриед Хацкер
Будност
Херберт Хеуер
Ментални умор
Петер Рицхтер
Организациони аспекти рада
Организација рада
Еберхард Улих и Гудела Гроте
Депривација сна
Казутака Коги
Пројектовање радних система
радне станице
Роланд Кадефорс
алат
ТМ Фрасер
Контроле, индикатори и панели
Карл ХЕ Кроемер
Обрада информација и дизајн
Андриес Ф. Сандерс
Дизајнирање за свакога
Дизајнирање за одређене групе
Шала Х. Гради-ван ден Ниеувбоер
Студија случаја: Међународна класификација функционалних ограничења код људи
Културне разлике
Хоусханг Схахнаваз
Старији радници
Антоан Лавил и Серж Волкоф
Радници са посебним потребама
Шала Х. Гради-ван ден Ниеувбоер
Разноврсност и важност ергономије – два примера
Дизајн система у производњи дијаманата
Исацхар Гилад
Занемаривање принципа ергономског дизајна: Чернобил
Владимир М. Мунипов
Столови
Кликните на везу испод да видите табелу у контексту чланка.
1. Основна антропометријска језгра листа
2. Умор и опоравак зависе од нивоа активности
3. Правила комбинованог дејства два фактора стреса на напрезање
4. Разликовање између неколико негативних последица психичког оптерећења
5. Принципи оријентисани на рад за структурирање производње
6. Учешће у организационом контексту
7. Учешће корисника у технолошком процесу
8. Нередовно радно време и недостатак сна
9. Аспекти напредног, сидреног и ретардираног спавања
КСНУМКС. Контролишите покрете и очекиване ефекте
КСНУМКС. Релације контроле и ефекта уобичајених ручних контрола
КСНУМКС. Правила за уређење контрола
КСНУМКС. Смернице за етикете
фигуре
Поставите показивач на сличицу да бисте видели наслов слике, кликните да бисте видели слику у контексту чланка.

30. Хигијена рада (6)

30. Хигијена рада
Уредник поглавља: Роберт Ф. Херрицк
Преглед садржаја
Табеле и слике
Циљеви, дефиниције и опште информације
Беренице И. Феррари Гоелзер
Препознавање опасности
Линнеа Лиллиенберг
Евалуација радног окружења
Лори А. Тодд
Хигијена рада: контрола изложености кроз интервенцију
Јамес Стеварт
Биолошка основа за процену изложености
Дик Хедерик
Границе професионалне изложености
Деннис Ј. Паустенбацх
Столови
1. Опасности од хемикалија; биолошки и физички агенси
2. Границе професионалне изложености (ОЕЛс) – разне земље
фигуре

31. Лична заштита (7)

31. Лична заштита
Уредник поглавља: Роберт Ф. Херрицк
Преглед садржаја
Табеле и слике
Преглед и филозофија личне заштите
Роберт Ф. Херрицк
Штитници за очи и лице
Кикузи Кимура
Заштита стопала и ногу
Тоиохико Миура
Заштита главе
Изабел Балти и Ален Мајер
Ношење заштите
Јохн Р. Франкс и Еллиотт Х. Бергер
Заштитна одећа
С. Зацк Мансдорф
Заштита дисајних органа
Тхомас Ј. Нелсон
Столови
Кликните на везу испод да видите табелу у контексту чланка.
1. Захтеви за пренос (ИСО 4850-1979)
2. Скала заштите - гасно заваривање и лемљење
3. Ваге заштите - резање кисеоником
4. Ваге заштите - плазма лучно сечење
5. Скала заштите - електролучно заваривање или жлебљење
6. Скала заштите - заваривање плазма директним луком
7. Заштитни шлем: ИСО стандард 3873-1977
8. Оцена смањења буке штитника за уши
9. Израчунавање А-пондерисане редукције шума
КСНУМКС. Примери категорија дермалне опасности
КСНУМКС. Захтеви за физичке, хемијске и биолошке перформансе
КСНУМКС. Материјалне опасности повезане са одређеним активностима
КСНУМКС. Додељени заштитни фактори из АНСИ З88 2 (1992)
фигуре
Поставите показивач на сличицу да бисте видели наслов слике, кликните да бисте видели слику у контексту чланка.

32. Системи евиденције и надзор (9)

32. Системи евиденције и надзор
Уредник поглавља: Стевен Д. Стеллман
Преглед садржаја
Табеле и слике
Системи за надзор и пријављивање професионалних болести
Стевен Б. Марковитз
Надзор професионалних опасности
Давид Х. Вегман и Стевен Д. Стеллман
Надзор у земљама у развоју
Давид Кох и Кее-Сенг Цхиа
Развој и примена система класификације повреда и болести на раду
Елице Биддле
Анализа ризика од нефаталних повреда и болести на радном месту
Јохн В. Русер
Студија случаја: Заштита радника и статистика о незгодама и професионалним болестима - ХВБГ, Немачка
Мартин Бутз и Буркхард Хоффманн
Студија случаја: Висмут - Поновно разматрање изложености уранијуму
Хајнц Отен и Хорст Шулц
Стратегије и технике мерења за процену професионалне изложености у епидемиологији
Франк Боцхманн и Хелмут Бломе
Студија случаја: Анкете о здрављу на раду у Кини
Столови
Кликните на везу испод да видите табелу у контексту чланка.
1. Ангиосарком јетре - светски регистар
2. Професионална болест, САД, 1986. у односу на 1992
3. Смртни случајеви у САД од пнеумокониозе и мезотелиома плеуре
4. Узорак листе професионалних болести које треба пријавити
5. Структура кода за пријаву болести и повреда, САД
6. Нефаталне професионалне повреде и болести, САД 1993
7. Ризик од повреда и професионалних болести
8. Релативни ризик за услове понављања кретања
9. Несреће на радном месту, Немачка, 1981-93
КСНУМКС. Брусилице у несрећама у обради метала, Немачка, 1984-93
КСНУМКС. Професионална болест, Немачка, 1980-93
КСНУМКС. Инфективне болести, Немачка, 1980-93
КСНУМКС. Изложеност радијацији у рудницима Висмут
КСНУМКС. Професионалне болести у рудницима уранијума Висмут 1952-90
фигуре
Поставите показивач на сличицу да бисте видели наслов слике, кликните да бисте видели слику у контексту чланка.

33. Токсикологија (21)

33. Токсикологија
Уредник поглавља: Еллен К. Силбергелд
Преглед садржаја
Табеле и слике
увод
Еллен К. Силбергелд, уредница поглавља
Општи принципи токсикологије
Дефиниције и концепти
Бо Холмберг, Јохан Хогберг и Гунар Јохансон
Токсикокинетика
Душан Ђурић
Циљни орган и критични ефекти
Марек Јакубовски
Ефекти старости, пола и других фактора
Споменка Телишман
Генетске детерминанте токсичног одговора
Даниел В. Неберт и Росс А. МцКиннон
Механизми токсичности
Увод и концепти
Филип Г. Ватанабе
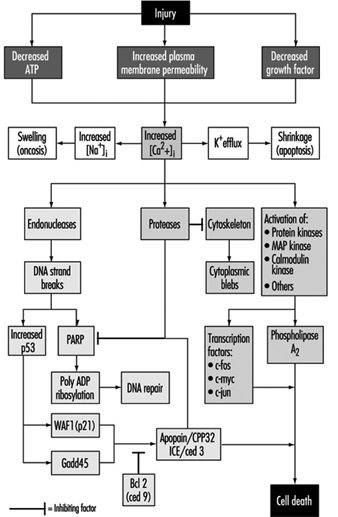
Ћелијска повреда и ћелијска смрт
Бењамин Ф. Трумп и Ирене К. Березески
Генетиц Токицологи
Р. Рита Мисра и Мицхаел П. Ваалкес
Иммунотокицологи
Јосепх Г. Вос и Хенк ван Ловерен
Токсикологија циљног органа
Еллен К. Силбергелд
Токсиколошке методе испитивања
Биомаркери
Пхилиппе Грандјеан
Процена генетске токсичности
Давид М. ДеМарини и Јамес Хуфф
Ин витро испитивање токсичности
Јоанне Зурло
Структура Активности Односи
Еллен К. Силбергелд
Регулатори Токицологи
Токсикологија у прописима о здрављу и безбедности
Еллен К. Силбергелд
Принципи идентификације опасности – јапански приступ
Масаиуки Икеда
Приступ Сједињених Држава процени ризика од репродуктивних токсичних и неуротоксичних агенаса
Еллен К. Силбергелд
Приступи идентификацији опасности - ИАРЦ
Хари Ваинио и Јулиан Вилбоурн
Додатак – Опште процене канцерогености за људе: монографије ИАРЦ, свеске 1-69 (836)
Процена ризика од карциногена: други приступи
Цеес А. ван дер Хеијден
Столови
Кликните на везу испод да видите табелу у контексту чланка.
- Примери критичних органа и критичних ефеката
- Основни ефекти могућих вишеструких интеракција метала
- Адукти хемоглобина код радника изложених анилину и ацетанилиду
- Наследни поремећаји склони раку и дефекти у поправци ДНК
- Примери хемикалија које показују генотоксичност у људским ћелијама
- Класификација тестова за имунолошке маркере
- Примери биомаркера изложености
- За и против метода за идентификацију ризика од рака код људи
- Поређење ин витро система за студије хепатотоксичности
- Поређење САР и тест података: ОЕЦД/НТП анализе
- Регулисање хемијских супстанци законима, Јапан
- Испитни предмети према Закону о контроли хемијских супстанци, Јапан
- Хемијске супстанце и закон о контроли хемијских супстанци
- Одабрани велики инциденти неуротоксичности
- Примери специјализованих тестова за мерење неуротоксичности
- Крајње тачке у репродуктивној токсикологији
- Поређење поступака екстраполације малих доза
- Често цитирани модели у карактеризацији ризика од карциногена
фигуре
Поставите показивач на сличицу да бисте видели наслов слике, кликните да бисте видели слику у контексту чланка.
Пестициди
увод
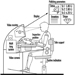
Изложеност људи пестицидима има различите карактеристике у зависности од тога да ли се јавља током индустријске производње или употребе (табела 1). Формулација комерцијалних производа (мешањем активних састојака са другим коформулантима) има неке карактеристике изложености које су заједничке са употребом пестицида у пољопривреди. У ствари, пошто формулацију обично обављају мале индустрије које производе много различитих производа у узастопним операцијама, радници су изложени сваком од неколико пестицида на кратко време. У јавном здравству и пољопривреди, употреба разних једињења је генерално правило, иако се у неким специфичним применама (на пример, дефолијација памука или програми контроле маларије) може користити само један производ.
Табела 1. Поређење карактеристика изложености током производње и употребе пестицида
|
Изложеност на производњу |
Изложеност при употреби |
|
|
Трајање излагања |
Континуирано и продужено |
Променљиво и повремено |
|
Степен изложености |
Прилично константно |
Изузетно променљиво |
|
Тип изложености |
За једно или неколико једињења |
На бројна једињења било у низу или истовремено |
|
Апсорпција коже |
Лако је контролисати |
Променљиво према радним процедурама |
|
Мониторинг амбијента |
Корисно |
Ретко информативно |
|
Биолошки мониторинг |
Комплементарно надгледању амбијента |
Веома корисно када је доступно |
Извор: СЗО 1982а, модификовано.
Мерење биолошких индикатора изложености је посебно корисно за кориснике пестицида где су конвенционалне технике процене изложености кроз мониторинг амбијенталног ваздуха једва применљиве. Већина пестицида су супстанце растворљиве у липидима које продиру у кожу. Појава перкутане (кожне) апсорпције чини употребу биолошких индикатора веома важном у процени нивоа изложености у овим околностима.
Органофосфатни инсектициди
Биолошки индикатори ефекта:
Холинестеразе су циљни ензими који узрокују токсичност органофосфата (ОП) за врсте инсеката и сисара. Постоје два главна типа холинестераза у људском организму: ацетилхолинестераза (АЦХЕ) и плазма холинестераза (ПЦХЕ). ОП изазива токсичне ефекте код људи кроз инхибицију синаптичке ацетилхолинестеразе у нервном систему. Ацетилхолинестераза је такође присутна у црвеним крвним зрнцима, где је њена функција непозната. Плазма холинестераза је генерички термин који покрива нехомогену групу ензима присутних у глијалним ћелијама, плазми, јетри и неким другим органима. ПЦХЕ инхибирају ОП, али његова инхибиција не производи познате функционалне поремећаје.
Инхибиција активности АЦХЕ и ПЦХЕ у крви је у великој корелацији са интензитетом и трајањем изложености ОП. АЦХЕ у крви, који је исти молекуларни циљ као и онај који је одговоран за акутну ОП токсичност у нервном систему, је специфичнији индикатор од ПЦХЕ. Међутим, осетљивост АЦХЕ и ПЦХЕ у крви на инхибицију ОП варира између појединачних ОП једињења: при истој концентрацији у крви, нека инхибирају више АЦХЕ, а друга више ПЦХЕ.
Постоји разумна корелација између активности АЦХЕ у крви и клиничких знакова акутне токсичности (табела 2). Корелација има тенденцију да буде боља јер је стопа инхибиције бржа. Када се инхибиција јавља споро, као код хроничне изложености на ниском нивоу, корелација са болешћу може бити ниска или потпуно непостојећа. Мора се напоменути да инхибиција АЦХЕ у крви није предиктивна за хроничне или одложене ефекте.
Табела 2. Тежина и прогноза акутне ОП токсичности на различитим нивоима инхибиције АЦХЕ
|
АЦХЕ инхибиција (%) |
Ниво од тровања |
Клинички симптоми |
Прогноза |
|
КСНУМКС-КСНУМКС |
Милд |
Слабост, главобоља, вртоглавица, мучнина, саливација, лакримација, миоза, умерени бронхијални спазам |
Реконвалесценција за 1-3 дана |
|
КСНУМКС-КСНУМКС |
Умерена |
Нагла слабост, поремећај вида, вишак саливације, знојење, повраћање, дијареја, брадикардија, хипертонија, дрхтање руку и главе, поремећен ход, миоза, бол у грудима, цијаноза слузокоже |
Реконвалесценција за 1-2 недеље |
|
КСНУМКС-КСНУМКС |
озбиљан |
Нагли тремор, генерализоване конвулзије, психички поремећаји, интензивна цијаноза, едем плућа, кома |
Смрт од респираторне или срчане инсуфицијенције |
Уочене су варијације активности АЦХЕ и ПЦХЕ код здравих људи иу специфичним физиопатолошким стањима (табела 3). Стога се осетљивост ових тестова у праћењу изложености ОП може повећати усвајањем појединачних вредности пре излагања као референтних. Активности холинестеразе након излагања се затим пореде са појединачним основним вредностима. Референтне вредности активности популације холинестеразе треба користити само када нивои холинестеразе пре излагања нису познати (табела 4).
Табела 3. Варијације активности АЦХЕ и ПЦХЕ код здравих људи иу одабраним физиопатолошким стањима
|
Услов |
АЦХЕ активност |
ПЦХЕ активност |
|
Здрави људи |
||
|
Интериндивидуална варијација1 |
10–18% |
15–25% |
|
Интраиндивидуална варијација1 |
3–7% |
6% |
|
Полне разлике |
Не |
10–15 % више код мушкараца |
|
старост |
Смањен до 6 месеци старости |
|
|
Телесна маса |
Позитивна корелација |
|
|
Серумски холестерол |
Позитивна корелација |
|
|
Сезонске варијације |
Не |
Не |
|
Циркадијална варијација |
Не |
Не |
|
Менструација |
Смањено |
|
|
Трудноћа |
Смањено |
|
|
Патолошка стања |
||
|
Смањена активност |
Леукемија, неоплазма |
Обољење јетре; уремија; рак; отказивање срца; алергијске реакције |
|
Повећана активност |
полицитемија; таласемија; друге урођене крвне дискразије |
Хипертиреоза; други услови високог метаболизма |
1 Извор: Аугустинссон 1955 и Гаге 1967.
Табела 4. Активности холинестеразе здравих особа без изложености ОП мерене одабраним методама
|
Метод |
Секс |
БОЛИ* |
ПЦХЕ* |
|
Мицхел1 (ДпХ/х) |
мушки женски |
КСНУМКС КСНУМКС ± КСНУМКС КСНУМКС ± |
КСНУМКС КСНУМКС ± КСНУМКС КСНУМКС ± |
|
Титриметријски1 (ммол/мин мл) |
мушко женски |
КСНУМКС КСНУМКС ± |
КСНУМКС КСНУМКС ± |
|
Еллман је модификован2 (УИ/мл) |
мушки женски |
КСНУМКС КСНУМКС ± КСНУМКС КСНУМКС ± |
КСНУМКС КСНУМКС ± КСНУМКС КСНУМКС ± |
* средњи резултат, ± стандардна девијација.
Извор: 1 Закони 1991. 2 Алцини и др. 1988.
Крв је пожељно узети у року од два сата након излагања. Венепункција је пожељнија од вађења капиларне крви из прста или ушне ресице јер место узорковања може бити контаминирано пестицидом који се налази на кожи изложених субјеката. Препоручују се три узастопна узорка да би се успоставила нормална почетна линија за сваког радника пре излагања (СЗО 1982б).
Постоји неколико аналитичких метода за одређивање АЦХЕ и ПЦХЕ у крви. Према СЗО, Елманова спектрофотометријска метода (Еллман ет ал. 1961) треба да послужи као референтна метода.
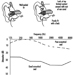
Биолошки индикатори изложености.
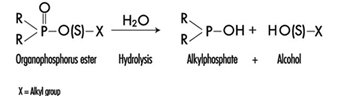
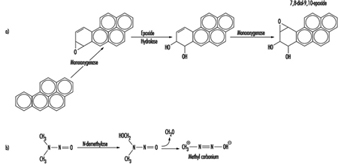
Одређивање у урину метаболита који су изведени из алкил фосфатног дела молекула ОП или остатака насталих хидролизом П–Кс везе (слика 1) коришћено је за праћење изложености ОП.
Слика 1. Хидролиза ОП инсектицида
Метаболити алкил фосфата.
Метаболити алкил фосфата који се могу детектовати у урину и главно матично једињење из којег могу настати наведени су у табели 5. Алкил фосфати у урину су осетљиви индикатори изложености ОП једињењима: излучивање ових метаболита у урину се обично може детектовати на нивоу изложености на која инхибиција холинестеразе плазме или еритроцита не може да се открије. Излучивање алкил фосфата у урину је мерено за различите услове изложености и за различита ОП једињења (табела 6). Постојање везе између спољашњих доза ОП и концентрација алкил фосфата у урину утврђено је у неколико студија. У неким студијама је такође приказана значајна веза између активности холинестеразе и нивоа алкил фосфата у урину.
Табела 5. Алкил фосфати који се могу детектовати у урину као метаболити ОП пестицида
|
Метаболит |
Скраћеница |
Главна матична једињења |
|
Монометилфосфат |
ММП |
Малатион, паратион |
|
Диметилфосфат |
ЗФМ |
Дихлорвос, трихлорфон, мевинфос, малаоксон, диметоат, фенхлорфос |
|
Диетилфосфат |
ДЕП |
Параоксон, деметон-оксон, диазинон-оксон, дихлорфентион |
|
Диметилтиофосфат |
ДМТП |
Фенитротион, фенхлорфос, малатион, диметоат |
|
Диетилтиофосфат |
ДЕТП |
Диазинон, деметон, паратхион, фенцхлорпхос |
|
Диметилдитиофосфат |
ДМДТП |
Малатион, диметоат, азинфос-метил |
|
Диетилдитиофосфат |
ДЕДТП |
Дисулфотон, форат |
|
Фенилфосфорна киселина |
Лептопхос, ЕПН |
Табела 6. Примери нивоа уринарних алкил фосфата измерених у различитим условима изложености ОП
|
Једињење |
Услов излагања |
Пут излагања |
Концентрације метаболита1 (мг/л) |
|
Паратхион2 |
Нефатално тровање |
Орално |
ДЕП = 0.5 ДЕТП = 3.9 |
|
Дисулфотон2 |
Формулатори |
Дермално/инхалација |
ДЕП = 0.01-4.40 ДЕТП = 0.01-1.57 ДЕДТП = <0.01-.05 |
|
Пхорате2 |
Формулатори |
Дермално/инхалација |
ДЕП = 0.02-5.14 ДЕТП = 0.08-4.08 ДЕДТП = <0.01-0.43 |
|
Малатхион3 |
Прскалице |
Дермално |
ДМДТП = <0.01 |
|
Фенитротион3 |
Прскалице |
Дермално |
ДМП = 0.01-0.42 ДМТП = 0.02-0.49 |
|
Моноцротопхос4 |
Прскалице |
Дермално/инхалација |
ДМП = <0.04-6.3/24 х |
1 За скраћенице видети табелу 27.12 [БМО12ТЕ].
2 Дилон и Хо 1987.
3 Рицхтер 1993.
4 Ван Ситтерт и Думас 1990.
Алкил фосфати се обично излучују урином за кратко време. Узорци прикупљени убрзо након завршетка радног дана су погодни за одређивање метаболита.
Мерење алкил фосфата у урину захтева прилично софистицирану аналитичку методу, засновану на дериватизацији једињења и детекцији гасно-течном хроматографијом (Схафик ет ал. 1973а; Реид и Ваттс 1981).
Хидролитички остаци.
p-Нитрофенол (ПНП) је фенолни метаболит паратиона, метилпаратиона и етил паратиона, ЕПН. Мерење ПНП у урину (Цранмер 1970) је широко коришћено и показало се успешним у процени изложености паратиону. ПНП у урину добро корелира са апсорбованом дозом паратиона. Са нивоима ПНП у урину до 2 мг/л, апсорпција паратиона не изазива симптоме, а примећује се мало или никакво смањење активности холинестеразе. Излучивање ПНП се дешава брзо и нивои ПНП у урину постају безначајни 48 сати након излагања. Стога, узорке урина треба прикупити убрзо након излагања.
Карбамати
Биолошки индикатори ефекта.
Карбаматни пестициди укључују инсектициде, фунгициде и хербициде. Инсектицидна токсичност карбамата је последица инхибиције синаптичког АЦХЕ, док су други механизми токсичности укључени за хербицидне и фунгицидне карбамате. Дакле, само изложеност карбаматним инсектицидима може се пратити путем анализе активности холинестеразе у црвеним крвним зрнцима (АЦХЕ) или плазми (ПЦХЕ). АЦХЕ је обично осетљивији на инхибиторе карбамата од ПЦХЕ. Холинергични симптоми су обично примећени код радника изложених карбамату са активношћу АЦХЕ у крви нижом од 70% индивидуалног основног нивоа (ВХО 1982а).
Инхибиција холинестеразе карбаматима је брзо реверзибилна. Стога се могу добити лажно негативни резултати ако протекне превише времена између излагања и биолошког узорковања или између узорковања и анализе. Да би се избегли овакви проблеми, препоручује се да се узорци крви сакупе и анализирају у року од четири сата након излагања. Предност треба дати аналитичким методама које омогућавају одређивање активности холинестеразе одмах након узорковања крви, као што је дискутовано за органофосфате.
Биолошки индикатори изложености.
Мерење излучивања метаболита карбамата у урину као метода за праћење изложености људи до сада је примењено само на неколико једињења иу ограниченим студијама. Табела 7 сумира релевантне податке. Пошто се карбамати брзо излучују урином, узорци прикупљени убрзо након завршетка излагања су погодни за одређивање метаболита. Давсон ет ал. (1964); ДеБернардинис и Варгин (1982) и Верберк ет ал. (1990).
Табела 7. Нивои метаболита карбамата у урину измерени у теренским студијама
|
Једињење |
Биолошки индекс |
Услов излагања |
Концентрације у животној средини |
Резултати |
Референце |
|
Царбарил |
а-нафтол а-нафтол а-нафтол |
формулатори миксер/апликатори неекспонирано становништво |
0.23–0.31 мг/м3 |
к=18.5 мг/л1 , мак. брзина излучивања = 80 мг/дан к=8.9 мг/л, опсег = 0.2–65 мг/л опсег = 1.5–4 мг/л |
ВХО 1982а |
|
Пиримицарб |
метаболити И2 и В3 |
апликатори |
опсег = 1–100 мг/л |
Верберк и др. 1990 |
1 Повремено су пријављивана системска тровања.
2 2-диметиламино-4-хидрокси-5,6-диметилпиримидин.
3 2-метиламино-4-хидрокси-5,6-диметилпиримидин.
к = стандардна девијација.
Дитиокарбамати
Биолошки индикатори изложености.
Дитиокарбамати (ДТЦ) су широко коришћени фунгициди, хемијски груписани у три класе: тиурами, диметилдитиокарбамати и етилен-бис-дитиокарбамати.
Угљен-дисулфид (ЦС2) и његов главни метаболит 2-тиотиазолидин-4-карбоксилна киселина (ТТЦА) су метаболити заједнички за скоро све ДТЦ. Примећено је значајно повећање концентрација ових једињења у урину за различите услове излагања и за различите ДТЦ пестициде. Етилен тиоуреа (ЕТУ) је важан уринарни метаболит етилен-бис-дитиокарбамата. Такође може бити присутан као нечистоћа у тржишним формулацијама. Пошто је утврђено да је ЕТУ тератоген и канцероген код пацова и других врста и да је повезан са токсичношћу за штитну жлезду, широко се примењује за праћење изложености етилен-бис-дитиокарбамату. ЕТУ није специфичан за једињење, јер може бити изведен од манеба, манкозеба или зинеба.
Мерење метала присутних у ДТЦ-у је предложено као алтернативни приступ у праћењу изложености ДТЦ-у. Уочено је повећано излучивање мангана у урину код радника изложених манкозебу (табела 8).
Табела 8. Нивои метаболита дитиокарбамата у урину измерени у теренским студијама
|
Једињење |
Биолошки индекс |
Цондитион оф излагање |
Концентрације у животној средини* ± стандардна девијација |
Резултати ± стандардна девијација |
Референце |
|
Зирам |
Угљен-дисулфид (ЦС2) ТТЦА1 |
формулатори формулатори |
1.03 ± 0.62 мг/м3 |
3.80 ± 3.70 мг/л 0.45 ± 0.37 мг/л |
Марони и др. 1992 |
|
Манеб/Манцозеб |
ЕТУ2 |
апликатори |
опсег = < 0.2–11.8 мг/л |
Курттио и др. 1990 |
|
|
Манцозеб |
Манган |
апликатори |
57.2 мг/м3 |
пре излагања: 0.32 ± 0.23 мг/г креатинина; после излагања: 0.53 ± 0.34 мг/г креатинина |
Цаносса и др. 1993 |
* Средњи резултат према Марони ет ал. 1992.
1 ТТЦА = 2-тиотиазолидин-4-карбонилна киселина.
2 ЕТУ = етилен тиоуреа.
CS2, ТТЦА и манган се обично налазе у урину особа које нису биле изложене. Стога се препоручује мерење нивоа ових једињења у урину пре излагања. Узорке урина треба узети ујутру након престанка излагања. Аналитичке методе за мерење ЦС2, ТТЦА и ЕТУ су пријавили Марони ет ал. (1992).
Синтетички пиретроиди
Биолошки индикатори изложености.
Синтетички пиретроиди су инсектициди слични природним пиретринима. Метаболити у урину погодни за примену у биолошком праћењу изложености идентификовани су кроз студије на људима добровољцима. Кисели метаболит 3-(2,2'-дихлоро-винил)-2,2'-диметил-циклопропан карбоксилна киселина (Цл2ЦА) излучују и субјекти који су орално дозирали перметрин и циперметрин и бромо-аналог (Бр2ЦА) од стране субјеката лечених делтаметрином. Код добровољаца лечених циперметрином, такође је идентификован фенокси метаболит, 4-хидрокси-фенокси бензојева киселина (4-ХПБА). Ови тестови, међутим, нису често примењени у праћењу професионалне изложености због сложених аналитичких техника које су потребне (Еадсфортх, Брагт и ван Ситтерт 1988; Колмодин-Хедман, Свенссон и Акерблом 1982). У апликаторима изложеним циперметрину, нивои Цл у урину2Утврђено је да се ЦА креће од 0.05 до 0.18 мг/л, док је у формулаторима изложеним а-циперметрину нивои 4-ХПБА у урину нижи од 0.02 мг/л.
За одређивање метаболита препоручује се 24-часовни период сакупљања урина који је почео након завршетка излагања.
Органоцхлоринес
Биолошки индикатори изложености.
Органохлорни (ОЦ) инсектициди су били широко коришћени 1950-их и 1960-их. Након тога, употреба многих од ових једињења је прекинута у многим земљама због њихове постојаности и последичне контаминације животне средине.
Биолошко праћење изложености ОЦ може се спровести кроз одређивање интактних пестицида или њихових метаболита у крви или серуму (Дале, Цурлеи и Цуето 1966; Баркует, Моргаде и Пфаффенбергер 1981). Након апсорпције, алдрин се брзо метаболише у диелдрин и може се мерити као диелдрин у крви. Ендрин има веома кратко време полураспада у крви. Због тога је концентрација ендрина у крви од користи само за одређивање нивоа недавне изложености. Одређивање метаболита у урину анти-12-хидрокси-ендрина се такође показало корисним у праћењу изложености ендрину (ван Ситтерт и Тордоир 1987).
За нека ОЦ једињења доказане су значајне корелације између концентрације биолошких индикатора и појаве токсичних ефеката. Случајеви токсичности услед изложености алдрину и дилдрину повезани су са нивоима дилдрина у крви изнад 200 μг/л. Концентрација линдана у крви од 20 μг/л је назначена као горњи критични ниво када су у питању неуролошки знаци и симптоми. Нису пријављени акутни нежељени ефекти код радника са концентрацијом ендрина у крви испод 50 μг/л. Одсуство раних штетних ефеката (индукција микрозомалних ензима јетре) показало се при поновљеном излагању ендрину при концентрацијама анти-12-хидрокси-ендрина у урину испод 130 μг/г креатинина и при поновљеном излагању ДДТ при концентрацијама ДДТ или ДДЕ у серуму испод 250 μг/л.
ОЦ се може наћи у ниским концентрацијама у крви или урину опште популације. Примери посматраних вредности су следећи: концентрације линдана у крви до 1 μг/л, диелдрина до 10 μг/л, ДДТ или ДДЕ до 100 μг/л и анти-12-хидрокси-ендрина до 1 μг/г креатинин. Стога се препоручује основна процена пре излагања.
За изложене субјекте, узорке крви треба узети одмах након завршетка једнократног излагања. За услове дуготрајног излагања, време узимања узорка крви није критично. Узорке мрља урина за одређивање метаболита у урину треба прикупити на крају излагања.
Триазинес
Биолошки индикатори изложености.
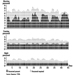
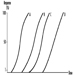
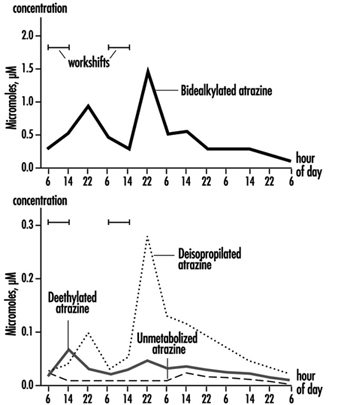
Мерење излучивања триазинских метаболита и немодификованог матичног једињења у урину примењено је на субјекте изложене атразину у ограниченим студијама. Слика 2 приказује профиле излучивања метаболита атразина у урину производног радника са дермалним излагањем атразину у распону од 174 до 275 μмол/радној смени (Цатенацци ет ал. 1993). Пошто други хлоротриазини (симазин, пропазин, тербутилазин) прате исти пут биотрансформације атразина, нивои деалкилованих триазинских метаболита се могу одредити да би се пратила изложеност свим хербицидима хлоротриазина.
Слика 2. Профили излучивања у урину метаболита атразина
Одређивање немодификованих једињења у урину може бити корисно као квалитативна потврда природе једињења које је изазвало излагање. За одређивање метаболита препоручује се 24-часовни период сакупљања урина започет на почетку излагања.
Недавно је коришћењем ензимског имуносорбентног теста (ЕЛИСА тест), коњугат атразина меркаптурне киселине идентификован као његов главни метаболит у урину код изложених радника. Ово једињење је пронађено у концентрацијама које су најмање 10 пута веће од оних било ког деалкилованог производа. Примећен је однос између кумулативне дермалне и инхалационе изложености и укупне количине коњугата меркаптурне киселине излученог током периода од 10 дана (Луцас ет ал. 1993).
Деривати кумарина
Биолошки индикатори ефекта.
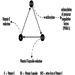
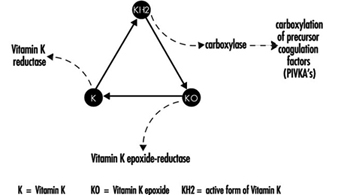
Кумарински родентициди инхибирају активност ензима циклуса витамина К у јетри сисара, укључујући и људе (слика 3), узрокујући на тај начин смањење у зависности од дозе синтезе фактора згрушавања зависних од витамина К, односно фактора ИИ (протромбина) , ВИИ, ИКС и Кс. Антикоагулантни ефекти се јављају када нивои фактора згрушавања у плазми падну испод приближно 20% нормалног.
Слика 3. Циклус витамина К
Ови антагонисти витамина К су груписани у такозвана једињења „прве генерације“ (нпр. варфарин) и једињења „друге генерације“ (нпр. бродифакум, дифенакум), а ове последње карактерише веома дуг биолошки полуживот (100 до 200 дана). ).
Одређивање протромбинског времена се широко користи у праћењу изложености кумаринима. Међутим, овај тест је осетљив само на смањење фактора згрушавања за приближно 20% нормалних нивоа у плазми. Тест није погодан за откривање раних ефеката излагања. У ту сврху се препоручује одређивање концентрације протромбина у плазми.
У будућности би ови тестови могли бити замењени одређивањем прекурсора фактора коагулације (ПИВКА), а то су супстанце које се у крви могу детектовати само у случају блокаде циклуса витамина К кумаринима.
Са условима продужене експозиције, време узимања крви није критично. У случајевима акутног прекомерног излагања, биолошки мониторинг треба спровести најмање пет дана након догађаја, с обзиром на латентност антикоагулансног дејства. Да би се повећала осетљивост ових тестова, препоручује се мерење основних вредности пре излагања.
Биолошки индикатори изложености.
Мерење немодификованих кумарина у крви је предложено као тест за праћење изложености људи. Међутим, искуство у примени ових индекса је веома ограничено углавном због тога што су аналитичке технике много сложеније (и мање стандардизоване) у поређењу са онима које су потребне за праћење ефеката на систем коагулације (Цхалермцхаикит, Фелице и Мурпхи 1993).
фенокси хербициди
Биолошки индикатори изложености.
Фенокси хербициди се једва биотрансформишу код сисара. Код људи, више од 95% дозе 2,4-дихлорофеноксисирћетне киселине (2,4-Д) се излучује непромењено урином у року од пет дана, а 2,4,5-триклорофеноксисирћетна киселина (2,4,5-Т) и 4-хлоро-2-метилфеноксисирћетна киселина (МЦПА) се такође излучују углавном непромењене урином у року од неколико дана након оралне апсорпције. Мерење непромењених једињења у урину примењено је у праћењу професионалне изложености овим хербицидима. У теренским студијама, утврђено је да се нивои урина код изложених радника крећу од 0.10 до 8 μг/л за 2,4-Д, од 0.05 до 4.5 μг/л за 2,4,5-Т и испод 0.1 μг/л до 15 μг/л за МЦПА. За одређивање непромењених једињења препоручује се 24-часовни период сакупљања урина који почиње на крају излагања. Аналитичке методе за мерење фенокси хербицида у урину известио је Драпер (1982).
Квартерна једињења амонијума
Биолошки индикатори изложености.
Дикват и паракват су хербициди које људски организам једва биотрансформише. Због њихове високе растворљивости у води, лако се излучују непромењени урином. Концентрације у урину испод аналитичке границе детекције (0.01 μг/л) често су примећене код радника изложених параквату; док су у тропским земљама мерене концентрације до 0.73 μг/л после неправилног руковања паракватом. Концентрације диквата у урину ниже од аналитичке границе детекције (0.047 μг/л) су пријављене за субјекте са дермалним излагањем од 0.17 до 1.82 μг/х и инхалационим излагањем мањим од 0.01 μг/х. Идеално би било да се за анализу користи 24-часовно узорковање урина прикупљеног на крају излагања. Када је то непрактично, може се користити спот узорак на крају радног дана.
Одређивање нивоа параквата у серуму је корисно у прогностичке сврхе у случају акутног тровања: пацијенти са нивоом параквата у серуму до 0.1 μг/л двадесет четири сата након ингестије вероватно ће преживети.
Аналитичке методе за одређивање параквата и диквата прегледао је Суммерс (1980).
Разни пестициди
4,6-динитро-о-крезол (ДНОЦ).
ДНОЦ је хербицид уведен 1925. године, али је употреба овог једињења прогресивно смањена због његове високе токсичности за биљке и људе. Пошто концентрације ДНОЦ у крви у одређеној мери корелирају са озбиљношћу штетних ефеката на здравље, предложена је мера непромењеног ДНОЦ у крви за праћење професионалне изложености и за процену клиничког тока тровања.
Пентацхлоропхенол.
Пентаклорофенол (ПЦП) је биоцид широког спектра са пестицидним деловањем против корова, инсеката и гљивица. Мерења непромењеног ПЦП у крви или урину су препоручена као одговарајући индекси у праћењу професионалне изложености (Цолосио ет ал. 1993), јер су ови параметри у значајној корелацији са оптерећењем ПЦП тела. Код радника са продуженим излагањем ПЦП-у време узимања крви није критично, док узорке мрља урина треба узети ујутру након излагања.
Методу са више остатака за мерење халогенизованих и нитрофенолних пестицида описали су Схафик ет ал. (1973б).
Остали тестови предложени за биолошко праћење изложености пестицидима наведени су у табели 9.
Табела 9. Остали индекси предложени у литератури за биолошки мониторинг изложености пестицидима
|
Једињење |
Биолошки индекс |
|
|
Урин |
Крв |
|
|
Бромопхос |
Бромопхос |
Бромопхос |
|
Капетане |
Тетрахидрофталимид |
|
|
Царбофуран |
3-Хидроксикарбофуран |
|
|
Цхлордимеформ |
4-hloro-o-деривати толуидина |
|
|
Хлоробензилат |
п,п-1-дихлоробензофенон |
|
|
дихлоропропен |
Метаболити Мерцаптуриц ацид |
|
|
Фенитротион |
p-Нитрокрезол |
|
|
Фербам |
Тхирам |
|
|
Флуазифоп-Бутил |
Флуазифоп |
|
|
Флуфенокурон |
Флуфенокурон |
|
|
глифосат |
глифосат |
|
|
Малатхион |
Малатхион |
Малатхион |
|
Органокалај једињења |
Калај |
Калај |
|
Трифеноморф |
Морфолин, трифенилкарбинол |
|
|
Зирам |
Тхирам |
|
Закључци
Биолошки индикатори за праћење изложености пестицидима примењени су у бројним експерименталним и теренским студијама.
Неки тестови, као што су они за холинестеразу у крви или за одабране немодификоване пестициде у урину или крви, потврђени су великим искуством. За ова испитивања су предложене границе биолошке изложености (табела 10). Други тестови, посебно они за метаболите у крви или урину, пате од већих ограничења због аналитичких потешкоћа или због ограничења у интерпретацији резултата.
Табела 10. Препоручене биолошке граничне вредности (од 1996. године)
|
Једињење |
Биолошки индекс |
ЕИБ1 |
БАТ2 |
ХББЛ3 |
БЛВ4 |
|
АЦХЕ инхибитори |
БОЛИ у крви |
100% |
100% |
КСНУМКС% |
|
|
ДНОЦ |
ДНОЦ у крви |
20 мг/л, |
|||
|
Линдане |
Линдан у крви |
0.02мг / л |
0.02мг / л |
||
|
Паратхион |
ПНП у урину |
0.5мг / л |
0.5мг / л |
||
|
Пентахлорофенол (ПЦП) |
ПЦП у урину ПЦП у плазми |
КСНУМКС мг / л КСНУМКС мг / л |
0.3мг / л КСНУМКС мг / л |
||
|
Диелдрин/Алдрин |
Диелдрин у крви |
КСНУМКС мг / л |
|||
|
Ендрин |
Анти-12-хидрокси-ендрин у урину |
КСНУМКС мг / л |
|||
|
ДДТ |
ДДТ и ДДЕ у серуму |
КСНУМКС мг / л |
|||
|
Кумарини |
Протромбинско време у плазми Концентрација протромбина у плазми |
10% изнад основне линије 60% од основне вредности |
|||
|
МЦПА |
МЦПА у урину |
КСНУМКС мг / л |
|||
|
2,4-Д |
2,4-Д у урину |
КСНУМКС мг / л |
1 Индексе биолошке изложености (БЕИ) препоручује Америчка конференција владиних индустријских хигијеничара (АЦГИХ 1995).
2 Вредности биолошке толеранције (БАТ) препоручује Немачка комисија за испитивање опасности по здравље хемијских једињења у радном подручју (ДФГ 1992).
3 Биолошке границе засноване на здрављу (ХББЛ) препоручује студијска група СЗО (СЗО 1982а).
4 Биолошке граничне вредности (БЛВ) су предложене од стране Студијске групе Научног комитета за пестициде Међународне комисије за здравље на раду (Тордоир ет ал. 1994). Процена услова рада захтева се ако је ова вредност прекорачена.
Ова област је у брзом развоју и, с обзиром на огроман значај коришћења биолошких индикатора за процену изложености овим супстанцама, нови тестови ће се континуирано развијати и валидирати.
Епидемиолошка метода примењена на безбедност и здравље на раду
Епидемиологија
Епидемиологија је препозната и као наука која је основа превентивне медицине и као наука која даје информације о процесу политике јавног здравља. Предложено је неколико оперативних дефиниција епидемиологије. Најједноставније је да је епидемиологија проучавање појаве болести или других здравствених карактеристика код људи и животиња. Епидемиолози проучавају не само учесталост болести, већ и да ли се учесталост разликује међу групама људи; тј. проучавају узрочно-последични однос између изложености и болести. Болести се не јављају насумично; они имају узроке – врло често узроке које је створио човек – које је могуће избећи. Тако би се многе болести могле спречити ако би се знали узроци. Методе епидемиологије биле су кључне за идентификацију многих узрочних фактора који су, заузврат, довели до здравствених политика дизајнираних да спрече болести, повреде и прерану смрт.
Шта је задатак епидемиологије и које су њене предности и слабости када се дефиниције и концепти епидемиологије примењују на здравље на раду? Ово поглавље се бави овим питањима и начинима на које се опасности по здравље на раду могу истражити коришћењем епидемиолошких техника. Овај чланак представља идеје које се налазе у узастопним чланцима у овом поглављу.
Оццупатионал Епидемиологи
Епидемиологија рада је дефинисана као проучавање ефеката изложености на радном месту на учесталост и дистрибуцију болести и повреда у популацији. Дакле, то је дисциплина оријентисана на изложеност која има везе и са епидемиологијом и са здрављем на раду (Цхецковаи ет ал. 1989). Као такав, користи методе сличне онима које користи епидемиологија уопште.
Основни циљ епидемиологије рада је превенција кроз идентификовање последица изложености на радном месту по здравље. Ово наглашава превентивни фокус епидемиологије рада. Заиста, сва истраживања у области здравља и безбедности на раду треба да служе у превентивне сврхе. Дакле, епидемиолошко знање може и треба да се лако примени. Док интерес јавног здравља увек треба да буде примарна брига епидемиолошког истраживања, интереси могу да врше утицај, и мора се водити рачуна да се такав утицај минимизира у формулисању, спровођењу и/или тумачењу студија (Сосколне 1985; Сосколне 1989).
Други циљ епидемиологије рада је да користи резултате из специфичних окружења да би се смањиле или елиминисале опасности у популацији у целини. Стога, осим што пружају информације о здравственим ефектима изложености на радном месту, резултати студија епидемиологије рада такође играју улогу у процени ризика повезаног са истим изложеностима, али на нижим нивоима које генерално доживљава општа популација. Контаминација животне средине индустријским процесима и производима обично би резултирала нижим нивоима изложености од оних на радном месту.
Нивои примене епидемиологије рада су:
- надзор како би се описала појава болести код различитих категорија радника и тако пружили сигнали раног упозорења о непрепознатим професионалним опасностима
- стварање и тестирање хипотезе да дато излагање може бити штетно и квантификација ефекта
- евалуација интервенције (на пример, превентивне акције као што је смањење нивоа изложености) мерењем промена у здравственом статусу популације током времена.
Узрочна улога коју професионална изложеност може одиграти у развоју болести, повреда и преране смрти идентификована је давно и део је историје епидемиологије. Треба се осврнути на Бернардина Рамацинија, оснивача медицине рада и једног од првих који је оживео и додао Хипократову традицију зависности здравља од препознатљивих природних спољашњих фактора. Године 1700. написао је у свом „Де Морбис Артифицум Диатриба“ (Рамаззини 1705; Сараци 1995):
Лекар мора да поставља многа питања пацијентима. Хипократ наводи у Де Аффецтионибус: „Када се суочите са болесним човеком, питајте га од чега болује, из ког разлога, колико дана, шта једе и каква му је црева. На сва ова питања треба додати: 'Којим послом он ради?'.
Ово поновно буђење клиничког посматрања и пажње на околности у вези са појавом болести, навело је Рамацинија да идентификује и опише многе професионалне болести које су касније проучавали лекари рада и епидемиолози.
Користећи овај приступ, Пот је први 1775. године (Потт 1775.) пријавио могућу везу између рака и занимања (Цлаисон 1962). Његова запажања о раку скротума међу оџачарима почела су описом болести и наставила:
Чини се да је судбина ових људи изузетно тешка: у раном детињству према њима се најчешће поступа с великом бруталношћу, а скоро изгладњели од хладноће и глади; избачени су у уске, а понекад и ужарене димњаке, где су натучене, изгорене и скоро угушене; а када дођу у пубертет, постају посебно подложни најгрознијој, најболнијој и фаталној болести.
У вези са овом последњом околношћу нема ни најмање сумње, иако јој се можда није довољно водило рачуна да би била опште позната. Други људи имају рак истих делова; као и други, осим водећих радника, Поитоу колике и последичне парализе; али је то ипак болест којој су они посебно подложни; а тако и оџачари до рака скротума и тестиса.
Чини се да болест код ових људи води порекло од нагомилавања чађи у рубовима скротума и у почетку није болест навике... али овде су субјекти млади, опште доброг здравља, барем прво; болест коју им је донело њихово занимање, и по свој прилици локална; за коју последњу околност се, мислим, може поштено претпоставити да увек заузима исте делове; све ово чини (у почетку) сасвим другачијим случајем од рака који се јавља код старијег човека.
Овај први приказ професионалног рака и даље остаје модел луцидности. Природа болести, занимање и вероватни узрочник су јасно дефинисани. Примјећује се повећана инциденција рака скротума међу димњачарима иако нису дати квантитативни подаци који би поткријепили тврдњу.
Прошло је још педесет година пре него што је Аиртон-Парис 1822. године (Аиртон-Парис 1822.) приметио чест развој рака скротума међу топионицама бакра и калаја у Корнволу и претпоставио да би паре арсена могле бити узрочник. Фон Волкман је 1874. пријавио туморе коже код парафинских радника у Саксонији, а недуго затим, Бел је 1876. године сугерисао да је уље из шкриљаца одговорно за рак коже (Вон Волкманн 1874; Белл 1876). Извештаји о професионалном пореклу рака тада су постали релативно чешћи (Цлаисон 1962).
Међу раним запажањима професионалних болести била је повећана појава рака плућа код Шнебергових рудара (Хартинг и Хессе 1879). Занимљиво је (и трагично) да недавна студија случаја показује да је епидемија рака плућа у Шнебергу и даље велики јавноздравствени проблем, више од једног века након првог посматрања 1879. Приступ да се идентификује „повећање“ болести па чак и да се квантификује био је присутан у историји медицине рада. На пример, као што је Акелсон (1994) истакао, ВА Гуи је 1843. проучавао „плућну потрошњу“ у штампачима за писму и открио већи ризик међу композиторима него међу новинарима; ово је урађено применом дизајна сличног приступу случај-контрола (Лилиенфелд и Лилиенфелд 1979). Ипак, тек почетком 1950-их је савремена епидемиологија занимања и њена методологија почела да се развија. Највећи допринос који је обележио овај развој биле су студије о раку бешике код фарбара (Цасе и Хоскер 1954) и рака плућа међу радницима на гасу (Долл 1952).
Питања епидемиологије рада
Чланци у овом поглављу уводе и филозофију и алате епидемиолошког истраживања. Они се фокусирају на процену искуства изложености радника и на болести које се јављају у овим популацијама. У овом поглављу обрађена су питања у доношењу ваљаних закључака о могућим узрочно-последичким везама на путу од изложености опасним супстанцама до развоја болести.
Утврђивање искуства изложености појединца у радном животу чини срж епидемиологије занимања. Информативност епидемиолошке студије зависи, у првом реду, од квалитета и обима доступних података о изложености. Друго, здравствени ефекти (или болести) од којих се брине епидемиолог занимања морају се тачно одредити међу добро дефинисаном и приступачном групом радника. Коначно, епидемиологу треба да буду доступни подаци о другим потенцијалним утицајима на болест од интереса, тако да се сви ефекти професионалне изложености који се утврде из студије могу приписати професионалној изложености по себи него на друге познате узроке дотичне болести. На пример, у групи радника који могу да раде са хемикалијом за коју се сумња да изазива рак плућа, неки радници могу такође имати историју пушења дувана, што је још један узрок рака плућа. У потоњој ситуацији, епидемиолози рада морају утврдити која је изложеност (или, који фактор ризика – хемикалија или дуван, или, заиста, ова два у комбинацији) одговорна за било какво повећање ризика од рака плућа у групи радника који проучавао.
Процена изложености
Ако студија има приступ само чињеници да је радник био запослен у одређеној индустрији, онда резултати такве студије могу повезати здравствене ефекте само са том индустријом. Исто тако, ако постоји сазнање о изложености занимања радника, закључци се могу директно изводити само у погледу занимања. Могу се направити индиректни закључци о изложености хемикалијама, али њихова поузданост се мора процењивати од ситуације до ситуације. Међутим, ако студија има приступ информацијама о одељењу и/или називу радног места сваког радника, тада ће се моћи донети закључци о том бољем нивоу искуства на радном месту. Када су информације о стварним супстанцама са којима особа ради познате епидемиологу (у сарадњи са индустријским хигијеничарем), онда би то био најбољи ниво информација о изложености који је доступан у одсуству ретко доступне дозиметрије. Штавише, налази из таквих студија могу пружити корисније информације индустрији за стварање сигурнијих радних места.
Епидемиологија је до сада била нека врста дисциплине „црне кутије“, јер је проучавала однос између изложености и болести (два екстрема узрочног ланца), не узимајући у обзир средње механичке кораке. Овај приступ, упркос његовом очигледном недостатку префињености, био је изузетно користан: у ствари, сви познати узроци рака код људи, на пример, откривени су помоћу епидемиолошких алата.
Епидемиолошка метода се заснива на доступним подацима — упитницима, називима послова или другим „проксијима“ изложености; ово чини спровођење епидемиолошких студија и тумачење њихових налаза релативно једноставним.
Ограничења грубљег приступа процени изложености, међутим, постала су очигледна последњих година, при чему се епидемиолози суочавају са сложенијим проблемима. Ограничавајући наше разматрање на професионалну епидемиологију рака, већина добро познатих фактора ризика је откривена због високог нивоа изложености у прошлости; ограничен број изложености за сваки посао; велике популације изложених радника; и јасна кореспонденција између „проки“ информација и изложености хемикалијама (нпр. обућарски радници и бензол, бродоградилишта и азбест, итд.). Данас је ситуација битно другачија: нивои изложености су знатно нижи у западним земљама (ту квалификацију увек треба истицати); радници су изложени многим различитим хемикалијама и смешама на истом радном месту (нпр. пољопривредни радници); хомогене популације изложених радника теже је пронаћи и обично су мале; и, кореспонденција између „проки“ информација и стварне изложености постаје све слабија. У овом контексту, епидемиолошки инструменти имају смањену осетљивост због погрешне класификације изложености.
Поред тога, епидемиологија се ослањала на „тврде“ крајње тачке, као што је смрт у већини кохортних студија. Међутим, радници би можда више волели да виде нешто другачије од „броја тела” када се проучавају потенцијални здравствени ефекти изложености на радном месту. Стога би употреба директнијих индикатора и изложености и раног одговора имала неке предности. Биолошки маркери могу бити само средство.
Биолошки маркери
Употреба биолошких маркера, као што су нивои олова у крви или тестовима функције јетре, није новост у епидемиологији рада. Међутим, коришћење молекуларних техника у епидемиолошким студијама омогућило је коришћење биомаркера за процену изложености циљним органима, за одређивање осетљивости и за утврђивање ране болести.
Потенцијалне употребе биомаркера у контексту епидемиологије занимања су:
- процена изложености у случајевима у којима су традиционална епидемиолошка средства недовољна (нарочито за мале дозе и ниске ризике)
- да раздвоји узрочну улогу појединачних хемијских агенаса или супстанци у вишеструким излагањима или смешама
- процена укупног терета изложености хемикалијама које имају исти механички циљ
- истраживање патогенетских механизама
- проучавање индивидуалне осетљивости (нпр. метаболички полиморфизми, поправка ДНК) (Винеис 1992)
- да прецизније класификују изложеност и/или болест, чиме се повећава статистичка моћ.
У научној заједници се појавио велики ентузијазам о овим употребама, али, као што је горе наведено, методолошка сложеност употребе ових нових „молекуларних алата“ треба да послужи као упозорење од претераног оптимизма. Биомаркери хемијског излагања (као што су адукти ДНК) имају неколико недостатака:
- Они обично одражавају недавна излагања и стога су од ограничене употребе у студијама случај-контрола, док захтевају поновљено узорковање током дужих периода да би се користили у кохортним истраживањима.
- Иако могу бити веома специфични и на тај начин побољшати погрешну класификацију изложености, налазе је често тешко протумачити.
- Када се истражује сложена хемијска изложеност (нпр. загађење ваздуха или дувански дим из животне средине) могуће је да би биомаркер одражавао једну одређену компоненту смеше, док би биолошки ефекат могао бити последица друге.
- У многим ситуацијама није јасно да ли биомаркер одражава релевантну изложеност, корелацију релевантне изложености, индивидуалну осетљивост или рану фазу болести, чиме се ограничава узрочни закључак.
- Одређивање већине биомаркера захтева скуп тест или инвазивну процедуру или обоје, чиме се стварају ограничења за адекватну величину студије и статистичку моћ.
- Биомаркер изложености није ништа више од замене за прави циљ епидемиолошког истраживања, које се, по правилу, фокусира на изложеност животне средине која се може избећи (Трицхопоулос 1995; Пеарце ет ал. 1995).
Још важније од методолошких недостатака је разматрање да би молекуларне технике могле да доведу до тога да преусмеримо фокус са идентификовања ризика у егзогеном окружењу, на идентификацију високоризичних појединаца, а затим на персонализоване процене ризика мерењем фенотипа, оптерећења адукта и стечених мутација. Ово би усмерило наш фокус, као што је приметио МцМицхаел, на облик клиничке евалуације, а не на епидемиологију јавног здравља. Фокусирање на појединце могло би да нас одврати од важног циља јавног здравља стварања мање опасног окружења (МцМицхаел 1994).
Појављују се још два важна питања у вези са употребом биомаркера:
- Употреба биомаркера у епидемиологији рада мора бити праћена јасном политиком када је у питању информисани пристанак. Радник може имати више разлога да одбије сарадњу. Један веома практичан разлог је тај што идентификација, рецимо, промене у маркеру раног одговора, као што је размена сестринских хроматида, подразумева могућност дискриминације од стране здравствених и животних осигуравача и послодаваца који би могли да избегавају радника јер је он или она склонији до болести. Други разлог се тиче генетског скрининга: пошто дистрибуција генотипова и фенотипова варира у зависности од етничке групе, могућности занимања за мањине могу бити отежане генетским скринингом. Треће, могу се појавити сумње у предвидљивост генетских тестова: пошто предиктивна вредност зависи од преваленције стања које тест има за циљ да идентификује, ако је ово друго ретко, предиктивна вредност ће бити ниска и практична употреба скрининга тест ће бити упитан. До сада, ниједан од генетских скрининг тестова није био применљив на терену (Асхфорд ет ал. 1990).
- Пре употребе биомаркера морају се применити етички принципи. Ови принципи су процењени за биомаркере који се користе за идентификацију индивидуалне осетљивости на болести од стране интердисциплинарне радне групе Техничке канцеларије европских синдиката, уз подршку Комисије Европских заједница (Ван Дамме ет ал. 1995); њихов извештај је учврстио став да се тестови могу спроводити само са циљем превенције болести код радне снаге. Између осталог, коришћење тестова мора никад.
- служе као средство за "избор најспособнијих"
- користити за избегавање спровођења ефикасних превентивних мера, као што је идентификација и замена фактора ризика или побољшања услова на радном месту
- стварају, потврђују или појачавају друштвену неједнакост
- створити јаз између етичких принципа који се поштују на радном месту и етичких принципа који се морају поштовати у демократском друштву
- обавезују особу која тражи посао да открије личне податке осим оних који су стриктно неопходни за добијање посла.
Коначно, гомилају се докази да метаболичка активација или инактивација опасних супстанци (а посебно канцерогених) значајно варира у људској популацији и да је делимично генетски условљена. Штавише, интер-индивидуална варијабилност у осетљивости на карциногене може бити посебно важна при ниским нивоима изложености на радном месту и околини (Винеис ет ал. 1994). Такви налази могу снажно утицати на регулаторне одлуке које фокусирају процес процене ризика на најосјетљивије (Винеис и Мартоне 1995).
Дизајн студије и валидност
Хернбергов чланак о дизајну епидемиолошких студија и њиховој примени у медицини рада концентрише се на концепт „базе студија“, дефинисаног као искуство морбидитета (у односу на неку изложеност) популације док се оно прати током времена. Дакле, основа проучавања није само популација (тј. група људи), већ искуство појаве болести ове популације током одређеног временског периода (Миеттинен 1985, Хернберг 1992). Ако се усвоји овај обједињујући концепт базе истраживања, онда је важно препознати да су различити дизајни студија (нпр., контрола случајева и дизајн кохорте) једноставно различити начини „прикупљања“ информација о изложености и болести из исте студије. база; нису дијаметрално различити приступи.
Сасцоов чланак о валидности у дизајну студија бави се дефиницијама и значајем збуњивања. Истраживачи студија морају увек да размотре могућност збуњивања у студијама занимања, и никада се не може довољно нагласити да је идентификација потенцијално збуњујућих варијабли саставни део сваког дизајна и анализе студије. У епидемиологији занимања морају се позабавити два аспекта збуњивања:
- Требало би истражити негативне недоумице: на пример, неке индустријске популације имају ниску изложеност факторима ризика везаним за начин живота због радног места без пушења; дувачи стакла имају тенденцију да пуше мање од опште популације.
- Када се узме у обзир збуњивање, требало би да се процени процена његовог правца и његовог потенцијалног утицаја. Ово је посебно тачно када су подаци за контролу збуњујућих оскудни. На пример, пушење је важан збуњујући фактор у епидемиологији занимања и увек га треба узети у обзир. Ипак, када подаци о пушењу нису доступни (као што је често случај у кохортним студијама), мало је вероватно да пушење може објаснити велики вишак ризика који се налази у групи занимања. Ово је лепо описано у раду Акелсон-а (1978), а даље о томе говори Гренланд (1987). Када су у литератури били доступни детаљни подаци и о занимању и о пушењу, чинило се да збуњујуће није у великој мери искривило процене о повезаности рака плућа и занимања (Винеис и Симонато 1991). Штавише, сумња на збуњивање не уводи увек неважеће асоцијације. Пошто су истраживачи такође изложени ризику да буду одведени на странпутицу другим неоткривеним пристрасностима у посматрању и селекцији, њима треба дати исти нагласак као и питању збуњивања у дизајнирању студије (Стеллман 1987).
Временске и временски повезане варијабле као што су ризична старост, календарски период, време од запошљавања, време од првог излагања, трајање изложености и њихов третман у фази анализе, спадају међу најкомплекснија методолошка питања у епидемиологији занимања. Они нису обухваћени у овом поглављу, али су забележене две релевантне и новије методолошке референце (Пеарце 1992; Робинс ет ал. 1992).
Статистика
Чланак о статистици Бигерија и Браге, као и наслов овог поглавља, указују да се статистичке методе не могу одвојити од епидемиолошких истраживања. То је зато што: (а) добро разумевање статистике може пружити вредан увид у правилан дизајн истраге и (б) статистика и епидемиологија имају заједничко наслеђе, а целокупна квантитативна основа епидемиологије је заснована на појму вероватноће ( Цлаитон 1992; Цлаитон анд Хиллс 1993). У многим чланцима који следе, емпиријски докази и докази о претпостављеним узрочно-последичној вези процењују се коришћењем аргумената вероватноће и одговарајућег дизајна студија. На пример, нагласак је стављен на процену мере ризика камате, као што су стопе или релативни ризици, и на изградњу интервала поверења око ових процена уместо на извршење статистичких тестова вероватноће (Пооле 1987; Гарднер и Алтман 1989; Гренланд 1990. ). Дат је кратак увод у статистичко резоновање коришћењем биномне дистрибуције. Статистика треба да буде пратилац научног расуђивања. Али то је безвредно у недостатку правилно осмишљених и спроведених истраживања. Статистичари и епидемиолози су свесни да избор метода одређује шта и у којој мери вршимо запажања. Стога је промишљен избор опција дизајна од фундаменталне важности како би се осигурала ваљана запажања.
Етика
Последњи чланак, аутора Винеиса, бави се етичким питањима у епидемиолошким истраживањима. Тачке које треба поменути у овом уводу односе се на епидемиологију као дисциплину која по дефиницији подразумева превентивно деловање. Специфични етички аспекти у погледу заштите радника и становништва у целини захтевају признање да:
- Епидемиолошке студије на радном месту ни на који начин не би требало да одлажу превентивне мере на радном месту.
- Епидемиологија рада се не односи на факторе начина живота, већ на ситуације у којима се обично мало или нимало лична улога игра у избору изложености. Ово подразумева посебну посвећеност ефикасној превенцији и тренутном преношењу информација радницима и јавности.
- Истраживања откривају опасности по здравље и пружају знање за превентивно деловање. Треба размотрити етичке проблеме неспровођења истраживања, када је то изводљиво.
- Обавештавање радника о резултатима епидемиолошких студија је и етичко и методолошко питање у комуникацији о ризику. Истраживању у процени потенцијалног утицаја и ефикасности обавештења треба дати високи приоритет (Сцхулте ет ал. 1993).
Обука из епидемиологије рада
Људи различитог порекла могу пронаћи свој пут до специјализације из области епидемиологије рада. Медицина, медицинска сестра и статистика су неке од вероватнијих позадина које се виде међу онима који су специјализовани за ову област. У Северној Америци, око половина свих обучених епидемиолога има научну позадину, док ће друга половина наставити путем доктора медицине. У земљама ван Северне Америке, већина специјалиста за епидемиологију рада напредоваће кроз звање доктора медицине. У Северној Америци, они са медицинском обуком се обично сматрају „стручњацима за садржај“, док се они који су обучени кроз научну руту сматрају „методолошким стручњацима“. Често је корисно да се стручњак за садржај удружи са стручњаком за методологију како би осмислио и спровео најбољу могућу студију.
Не само да је познавање епидемиолошких метода, статистике и компјутера потребно за специјалност из области епидемиологије рада, већ је потребно и познавање токсикологије, индустријске хигијене и регистара болести (Мерлетти и Цомба 1992). Пошто велике студије могу захтевати повезивање са регистрима болести, познавање извора података о популацији је корисно. Познавање рада и корпоративне организације је такође важно. Тезе на нивоу магистара и дисертације на нивоу докторских студија оспособљавају студенте са знањем потребним за спровођење великих студија заснованих на евиденцији и интервјуима међу радницима.
Пропорција болести која се може приписати занимању
Пропорција болести која се може приписати професионалној изложености, било у групи изложених радника или у општој популацији, покривена је барем у односу на рак у другом делу ове Енциклопедија. Овде треба да запамтимо да ако се израчунава процена, то би требало да буде за одређену болест (и специфично место у случају рака), одређени временски период и специфично географско подручје. Штавише, требало би да се заснива на тачним мерама пропорције изложених људи и степена изложености. Ово имплицира да пропорција болести која се може приписати занимању може варирати од веома ниске или нуле у одређеним популацијама до веома високог у другим лоцираним у индустријским областима где се, на пример, чак 40% карцинома плућа може приписати професионалној изложености (Винеис и Симонато 1991). Процене које нису засноване на детаљном прегледу добро осмишљених епидемиолошких студија могу се, у најбољем случају, сматрати утемељеним нагађањима и имају ограничену вредност.
Трансфер опасних индустрија
Већина епидемиолошких истраживања се спроводи у развијеном свету, где је регулација и контрола познатих професионалних опасности смањила ризик од болести у последњих неколико деценија. У исто време, међутим, дошло је до великог трансфера опасних индустрија у свет у развоју (Јеиаратнам 1994). Хемикалије које су раније биле забрањене у Сједињеним Државама или Европи сада се производе у земљама у развоју. На пример, млевење азбеста је пребачено из САД у Мексико, а производња бензидина из европских земаља у бившу Југославију и Кореју (Симонато 1986; ЛаДоу 1991; Пеарце ет ал. 1994).
Индиректан знак степена професионалног ризика и услова рада у земљама у развоју је епидемија акутног тровања која се дешава у неким од ових земаља. Према једној процени, сваке године у свету има око 20,000 смртних случајева од акутне интоксикације пестицидима, али је вероватно да је то значајно потцењено (Когевинас ет ал. 1994). Процењује се да се 99% свих смртних случајева од акутног тровања пестицидима дешава у земљама у развоју, где се користи само 20% светских агрохемикалија (Когевинас ет ал. 1994). То значи да чак и ако се чини да епидемиолошко истраживање указује на смањење професионалних опасности, то би једноставно могло бити због чињенице да се већина ових истраживања спроводи у развијеном свету. Професионалне опасности су се можда једноставно пренијеле на земље у развоју и укупни терет изложености на радном мјесту у свијету се могао повећати (Винеис ет ал. 1995).
Ветеринарска епидемиологија
Из очигледних разлога, ветеринарска епидемиологија није директно релевантна за здравље и епидемиологију рада. Ипак, назнаке еколошких и професионалних узрока болести могу доћи из епидемиолошких студија на животињама из неколико разлога:
- Животни век животиња је релативно кратак у поређењу са људским, а период латенције за болести (нпр. већина карцинома) је краћи код животиња него код људи. Ово имплицира да болест која се јавља код дивљих животиња или кућних љубимаца може послужити као надзорни догађај који ће нас упозорити на присуство потенцијалног токсичног или канцерогеног материја за животну средину за људе пре него што би било идентификовано на други начин (Глицкман 1993).
- Маркери изложености, као што су адукти хемоглобина или нивои апсорпције и излучивања токсина, могу се мерити код дивљих животиња и кућних љубимаца да би се проценила контаминација животне средине из индустријских извора (Блондин и Виау 1992; Реинолдс ет ал. 1994; Хунгерфорд ет ал. 1995) .
- Животиње нису изложене неким факторима који могу деловати као збуњујући у студијама на људима, па се истраживања на животињским популацијама стога могу спроводити без обзира на ове потенцијалне збуњујуће факторе. На пример, студија рака плућа код паса кућних љубимаца може открити значајне везе између болести и изложености азбесту (нпр. преко занимања власника везаних за азбест и близине индустријских извора азбеста). Јасно је да би таква студија уклонила ефекат активног пушења као збуњујућег фактора.
Ветеринари говоре о епидемиолошкој револуцији у ветеринарској медицини (Сцхвабе 1993) и појавили су се уџбеници о овој дисциплини (Тхрусфиелд 1986; Мартин ет ал. 1987). Свакако, трагови еколошких и професионалних опасности дошли су од заједничких напора епидемиолога људи и животиња. Између осталог, ефекат феноксихербицида код оваца и паса (Невелл ет ал. 1984; Хаиес ет ал. 1990), магнетних поља (Реиф ет ал. 1995) и пестицида (посебно препарата против бува) контаминираних једињењима сличним азбесту код паса (Глицкман ет ал. 1983) су значајни доприноси.
Партиципативно истраживање, саопштавање резултата и превенција
Важно је препознати да су многе епидемиолошке студије у области здравља на раду покренуте кроз искуство и бригу самих радника (Олсен ет ал. 1991). Често су радници — они који су историјски и/или тренутно изложени — веровали да нешто није у реду много пре него што је то потврђено истраживањем. Епидемиологија рада се може сматрати начином „давања смисла“ радничком искуству, прикупљања и груписања података на систематски начин и омогућавања закључивања о професионалним узроцима њиховог лошег здравља. Штавише, сами радници, њихови представници и људи задужени за здравље радника су најприкладније особе за тумачење података који се прикупљају. Они стога увек треба да буду активни учесници у било којој истрази која се спроводи на радном месту. Само њихово директно учешће ће гарантовати да ће радно место остати безбедно након што истраживачи оду. Циљ сваке студије је коришћење резултата у превенцији болести и инвалидитета, а успех тога у великој мери зависи од тога да ли изложени учествују у добијању и тумачењу резултата студије. Улога и употреба налаза истраживања у судском процесу док радници траже компензацију за штету проузроковану изложеношћу на радном месту је ван оквира овог поглавља. За неки увид у ово, читалац је упућен на друго место (Сосколне, Лилиенфелд и Блацк 1994).
Партиципативни приступи обезбеђивању спровођења епидемиолошких истраживања занимања су на неким местима постали стандардна пракса у виду управних одбора основаних да надгледају истраживачку иницијативу од њеног почетка до њеног завршетка. Ови комитети су вишепартитни по својој структури, укључујући рад, науку, менаџмент и/или владу. Са представницима свих заинтересованих група у процесу истраживања, комуникација резултата ће бити ефикаснија захваљујући њиховом повећаном кредибилитету јер би „један од њих“ надгледао истраживање и саопштавао резултате својим изборна јединица. На овај начин је вероватан највећи ниво ефикасне превенције.
Ови и други партиципативни приступи у истраживању здравља на раду предузимају се уз укључивање оних који доживљавају или су на други начин погођени проблемом који изазива забринутост. Ово би требало чешће да се види у свим епидемиолошким истраживањима (Лаурелл ет ал. 1992). Важно је запамтити да док је у епидемиолошком раду циљ анализе процена величине и дистрибуције ризика, у партиципативном истраживању, превенција ризика је такође циљ (Лоевенсон и Биоцца 1995). Ова комплементарност епидемиологије и ефикасне превенције је део поруке овога Енциклопедија и овог поглавља.
Одржавање значаја за јавно здравље
Иако су нови развоји у епидемиолошкој методологији, анализи података и процени и мерењу изложености (као што су нове молекуларне биолошке технике) добродошли и важни, они такође могу допринети редукционистичком приступу који се фокусира на појединце, а не на популације. Речено је да:
… епидемиологија је у великој мери престала да функционише као део мултидисциплинарног приступа разумевању узрока болести у популацијама и постала је скуп генеричких метода за мерење повезаности изложености и болести код појединаца… Тренутно постоји занемаривање друштвених, економских, културних питања. , историјски, политички и други популациони фактори као главни узроци болести... Епидемиологија се мора реинтегрисати у јавно здравље и мора поново открити перспективу становништва (Пеарце 1996).
Професионални и еколошки епидемиолози имају важну улогу, не само у развоју нових епидемиолошких метода и примене ових метода, већ иу обезбеђивању да ове методе увек буду интегрисане у одговарајућу перспективу становништва.
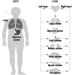
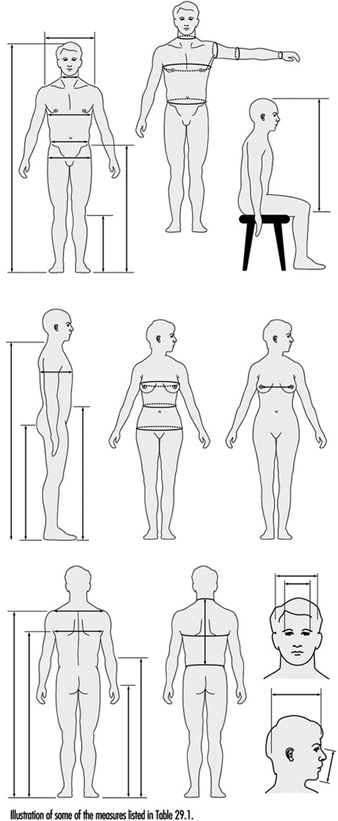
Антропометрија
Овај чланак је преузет из 3. издања Енциклопедије здравља и безбедности на раду.
Антропометрија је фундаментална грана физичке антропологије. Представља квантитативни аспект. Широк систем теорија и праксе посвећен је дефинисању метода и варијабли за повезивање циљева у различитим областима примене. У областима здравља, безбедности и ергономије на раду, антропометријски системи се углавном баве грађом тела, композицијом и конституцијом, као и димензијама међуодноса људског тела са димензијама радног места, машинама, индустријским окружењем и одећом.
Антропометријске варијабле
Антропометријска варијабла је мерљива карактеристика тела која се може дефинисати, стандардизовати и односити на јединицу мере. Линеарне варијабле су генерално дефинисане оријентирима који се могу прецизно пратити до тела. Оријентири су генерално два типа: скелетно-анатомски, који се могу пронаћи и пратити опипањем коштаних избочина кроз кожу, и виртуелни оријентири који се једноставно пронађу као максималне или минималне удаљености помоћу грана калипера.
Антропометријске варијабле имају и генетске компоненте и компоненте животне средине и могу се користити за дефинисање индивидуалне и популацијске варијабилности. Избор варијабли мора бити везан за конкретну сврху истраживања и стандардизован са другим истраживањима из исте области, пошто је број варијабли описаних у литератури изузетно велик, до 2,200 описаних за људско тело.
Антропометријске варијабле су углавном линеаран мере, као што су висине, удаљености од оријентира са субјектом који стоји или седи у стандардизованом положају; пречника, као што су удаљености између билатералних оријентира; дужине, као што су растојања између два различита оријентира; закривљене мере, односно лукови, као што су растојања на површини тела између два оријентира; и обимови, као што су затворене свеобухватне мере на површини тела, генерално постављене на најмање један оријентир или на дефинисаној висини.
Друге варијабле могу захтевати посебне методе и инструменте. На пример, дебљина набора се мери помоћу специјалних мерача константног притиска. Запремине се мере прорачуном или потапањем у воду. Да би се добиле потпуне информације о карактеристикама површине тела, компјутерска матрица површинских тачака се може нацртати коришћењем биостереометријских техника.
Инструменти
Иако су софистицирани антропометријски инструменти описани и коришћени у циљу аутоматизованог прикупљања података, основни антропометријски инструменти су прилично једноставни и лаки за употребу. Мора се посветити много пажње да се избегну уобичајене грешке које су резултат погрешног тумачења оријентира и неправилних положаја субјеката.
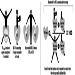
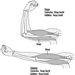
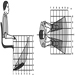
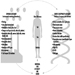
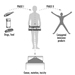
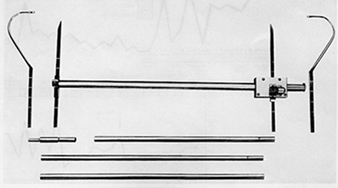
Стандардни антропометријски инструмент је антропометар — крута шипка дужине 2 метра, са две скале за контра-читање, помоћу којих се могу узети вертикалне димензије тела, као што су висина оријентира од пода или седишта, и попречне димензије, као што су пречници.
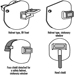
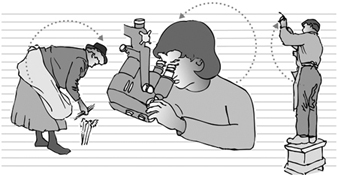
Штап се обично може поделити на 3 или 4 дела који се уклапају један у други. Клизна грана са равном или закривљеном канџом омогућава мерење удаљености од пода за висине, или од фиксне гране за пречнике. Сложенији антропометри имају једну скалу за висине и пречнике да би се избегле грешке на скали, или су опремљени дигиталним механичким или електронским уређајима за очитавање (слика 1).
Стадиометар је фиксни антропометар, који се углавном користи само за раст и често је повезан са скалом.
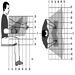
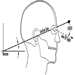
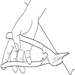
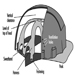
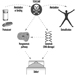
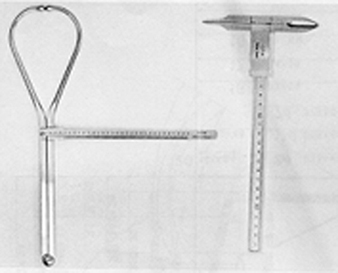
За попречне пречнике може се користити серија чељусти: пелвиметар за мере до 600 мм и цефалометар до 300 мм. Ово последње је посебно погодно за мерење главе када се користи заједно са клизним компасом (слика 2).
Слика 2. Кефалометар заједно са клизним компасом
Подножје се користи за мерење стопала, а узглавље даје картезијанске координате главе када је оријентисано у „Франкфортској равни“ (хоризонтална раван која пролази кроз порион орбитални оријентири главе).Рука се може мерити калипером или посебним уређајем састављеним од пет клизних лењира.
Дебљина кожног набора се мери помоћу калипера кожног набора са константним притиском обично са притиском од 9.81 к 104 Pa (притисак наметнут тежином од 10 г на површину од 1 мм2).
За лукове и обимове користи се уска, флексибилна челична трака са равним пресеком. Морају се избегавати самоисправљајуће челичне траке.
Системи варијабли
Систем антропометријских варијабли је кохерентан скуп телесних мерења за решавање неких специфичних проблема.
У области ергономије и безбедности, главни проблем је прилагођавање опреме и радног простора људима и кројење одеће одговарајуће величине.
Опрема и радни простор захтевају углавном линеарне мере удова и сегмената тела које се лако могу израчунати из оријентирних висина и пречника, док се величине за кројење заснивају углавном на луковима, обимима и флексибилним дужинама траке. Оба система се могу комбиновати према потреби.
У сваком случају, апсолутно је неопходно имати прецизну референцу простора за свако мерење. Оријентири, према томе, морају бити повезани висинама и пречницима и сваки лук или обим мора имати дефинисану референцу оријентира. Висине и нагиби морају бити назначени.
У одређеном истраживању, број варијабли мора бити ограничен на минимум како би се избегао непотребни стрес на субјекта и оператера.
Основни скуп варијабли за радни простор је смањен на 33 измерене варијабле (слика 3) плус 20 изведених једноставним прорачуном. За војно истраживање опште намене, Херцберг и сарадници користе 146 варијабли. За одећу и опште биолошке сврхе Италијански модни одбор (Енте Италиано делла Мода) користи скуп од 32 варијабле опште намене и 28 техничких. Немачка норма (ДИН 61 516) за димензије контролног тела за одећу укључује 12 варијабли. Препорука Међународне организације за стандардизацију (ИСО) за антропометрију укључује основну листу од 36 варијабли (види табелу 1). Међународне табеле података о антропометрији које је објавила ИЛО наводе 19 телесних димензија за популације 20 различитих региона света (Јургенс, Ауне и Пиепер 1990).
Слика 3. Основни скуп антропометријских варијабли
Табела 1. Листа основних антропометријских језгара
1.1 Дохват напред (за хватање руком са субјектом који стоји усправно уза зид)
1.2 Раст (вертикална удаљеност од пода до темена главе)
1.3 Висина очију (од пода до унутрашњег угла ока)
1.4 Висина рамена (од пода до акромиона)
1.5 Висина лакта (од пода до радијалне депресије лакта)
1.6 Висина препона (од пода до стидне кости)
1.7 Висина врха прста (од пода до осе шаке)
1.8 Ширина рамена (биакромијални пречник)
1.9 Ширина кукова, стојећи (максимално растојање преко кукова)
2.1 Висина седења (од седишта до темена главе)
2.2 Висина очију, седење (од седишта до унутрашњег угла ока)
2.3 Висина рамена, седење (од седишта до акромиона)
2.4 Висина лакта, седење (од седишта до најниже тачке савијеног лакта)
2.5 Висина колена (од ослонца за стопала до горње површине бутина)
2.6 Дужина потколенице (висина површине седења)
2.7 Дужина подлактице и шаке (од задње стране савијеног лакта до осе хватања)
2.8 Дубина тела, седење (дубина седишта)
2.9 Дужина задњице до колена (од капе за колена до крајње задње тачке задњице)
2.10 Ширина од лакта до лакта (растојање између бочних површина лактова)
2.11 Ширина кукова, седење (ширина седишта)
3.1 Ширина кажипрста, проксимална (на споју између медијалне и проксималне фаланге)
3.2 Ширина кажипрста, дистална (на споју између дисталне и медијалне фаланге)
3.3 Дужина кажипрста
3.4 Дужина руке (од врха средњег прста до стилоида)
3.5 Ширина шаке (на метакарпалима)
3.6 Обим зглоба
4.1 Ширина стопала
4.2 Дужина стопала
5.1 Топлотни обим (код глабеле)
5.2 Сагитални лук (од глабеле до иниона)
5.3 Дужина главе (од глабеле до опистокраниона)
5.4 Ширина главе (максимално изнад уха)
5.5 Битрагион лук (преко главе између ушију)
6.1 Обим струка (код пупка)
6.2 Висина тибије (од пода до највише тачке на антеромедијалној ивици гленоида тибије)
6.3 Цервикална висина седења (до врха спинозног наставка 7. вратног пршљена).
Извор: Прилагођено према ИСО/ДП 7250 1980).
Прецизност и грешке
Прецизност димензија живог тела мора се посматрати на стохастички начин јер је људско тело веома непредвидиво, и као статична и као динамичка структура.
Једна особа може расти или променити мишићну масу и дебљину; подвргнути променама скелета као последицама старења, болести или незгода; или модификовати понашање или држање. Различити предмети се разликују по пропорцијама, а не само по општим димензијама. Високи субјекти нису само увећања ниских; конституцијски типови и соматотипови вероватно варирају више од општих димензија.
Употреба манекена, посебно оних који представљају стандардне 5., 50. и 95. перцентиле за тестове уклапања, може бити веома погрешна ако се не узму у обзир варијације тела у пропорцијама тела.
Грешке су резултат погрешног тумачења оријентира и погрешне употребе инструмената (лична грешка), непрецизних или нетачних инструмената (инструментална грешка) или промена у држању субјекта (грешка субјекта – ово последње може бити последица потешкоћа у комуникацији ако културна или језичка позадина субјект се разликује од субјекта оператера).
Статистички третман
Антропометријски подаци се морају третирати статистичким процедурама, углавном у области метода закључивања применом униваријатних (средња вредност, мод, перцентили, хистограми, анализа варијансе, итд.), биваријатних (корелација, регресија) и мултиваријантних (вишеструка корелација и регресија, факторска анализа , итд.) методе. За класификацију људских типова (антропометрограми, морфосоматограми) осмишљене су различите графичке методе засноване на статистичким применама.
Узорковање и анкетирање
Како се антропометријски подаци не могу прикупити за целу популацију (осим у ретким случајевима посебно мале популације), узорковање је генерално неопходно. У основи насумичан узорак треба да буде полазна тачка сваког антропометријског истраживања. Да би се број мерених субјеката одржао на разумном нивоу, генерално је неопходно прибећи вишестепеном стратификованом узорковању. Ово омогућава најхомогенију поделу становништва на одређени број класа или слојева.
Становништво се може поделити по полу, старосној групи, географском подручју, друштвеним варијаблама, физичкој активности и тако даље.
Обрасци анкете морају бити дизајнирани имајући у виду и поступак мерења и третман података. Треба направити тачну ергономску студију поступка мерења како би се смањио замор оператера и могуће грешке. Из тог разлога, варијабле се морају груписати према инструменту који се користи и поредати у редоследу како би се смањио број савијања тела које оператер мора да изврши.
Да би се смањио ефекат личне грешке, анкету треба да спроведе један оператер. Ако се мора користити више од једног оператера, неопходна је обука да би се осигурала поновљивост мерења.
Популациона антропометрија
Без обзира на веома критикован концепт „расе“, људске популације су ипак веома варијабилне по величини појединаца и дистрибуцији величине. Генерално, људска популација није стриктно менделовска; обично су резултат мешања. Понекад две или више популација, различитог порекла и прилагођавања, живе заједно на истом подручју без укрштања. Ово компликује теоријску дистрибуцију особина. Са антропометријског становишта, полови су различите популације. Популације запослених можда неће тачно одговарати биолошкој популацији истог подручја као последица могућег одабира склоности или ауто-селекције због избора посла.
Популације из различитих области могу се разликовати као последица различитих услова адаптације или биолошких и генетских структура.
Када је блиско уклапање важно, потребно је испитивање на случајном узорку.
Испитивања и регулација уклапања
Прилагођавање радног простора или опреме кориснику може зависити не само од телесних димензија, већ и од варијабли као што су толеранција непријатности и природа активности, одећа, алати и услови околине. Може се користити комбинација контролне листе релевантних фактора, симулатора и серије одговарајућих испитивања користећи узорак субјеката одабраних да представљају распон величина тела очекиване корисничке популације.
Циљ је пронаћи опсег толеранције за све предмете. Ако се опсези преклапају, могуће је изабрати ужи коначни опсег који није ван граница толеранције ниједног субјекта. Ако нема преклапања, биће потребно структуру подесити или обезбедити у различитим величинама. Ако је подесиво више од две димензије, субјект можда неће моћи да одлучи које од могућих подешавања ће му најбоље одговарати.
Прилагодљивост може бити компликована ствар, посебно када неудобни положаји доводе до умора. Стога се морају дати прецизне индикације кориснику који често зна мало или нимало о својим антропометријским карактеристикама. Генерално, тачан дизајн треба да смањи потребу за прилагођавањем на минимум. У сваком случају, треба стално имати на уму да је у питању антропометрија, а не само инжењерство.
Динамичка антропометрија
Статичка антропометрија може дати широке информације о кретању ако је одабран адекватан скуп варијабли. Ипак, када су покрети компликовани и када је пожељно блиско уклапање са индустријским окружењем, као у већини интерфејса корисник-машина и човек-возило, неопходан је тачан преглед положаја и покрета. Ово се може урадити помоћу одговарајућих макета које омогућавају праћење линија досега или фотографисањем. У овом случају, камера опремљена телефото сочивом и антропометријском шипком, постављена у сагиталној равни субјекта, омогућава стандардизоване фотографије са малим изобличењем слике. Мале ознаке на артикулацији субјеката омогућавају тачно праћење покрета.
Други начин проучавања покрета је формализовање постуралних промена према низу хоризонталних и вертикалних равни које пролазе кроз артикулације. Опет, коришћење компјутеризованих људских модела са системима компјутерски потпомогнутог дизајна (ЦАД) је изводљив начин да се динамичка антропометрија укључи у ергономски дизајн радног места.
Увод и концепти
Механистичка токсикологија је студија о томе како хемијски или физички агенси интерагују са живим организмима да изазову токсичност. Познавање механизма токсичности неке супстанце побољшава способност спречавања токсичности и дизајнирања пожељнијих хемикалија; представља основу за терапију прекомерног излагања и често омогућава даље разумевање основних биолошких процеса. За потребе овога Енциклопедија нагласак ће бити стављен на животиње да би се предвидела токсичност за људе. Различите области токсикологије укључују механистичку, дескриптивну, регулаторну, форензичку и еколошку токсикологију (Клаассен, Амдур и Доулл 1991). Све ово има користи од разумевања основних механизама токсичности.
Зашто разумети механизме токсичности?
Разумевање механизма којим супстанца изазива токсичност побољшава различите области токсикологије на различите начине. Механистичко разумевање помаже владином регулатору да успостави правно обавезујуће безбедне границе за излагање људи. Помаже токсиколозима у препоруци правца деловања у вези са чишћењем или санацијом контаминираних места и, заједно са физичким и хемијским својствима супстанце или смеше, може се користити за одабир степена потребне заштитне опреме. Механистичко знање је такође корисно у формирању основе за терапију и дизајн нових лекова за лечење људских болести. За форензичког токсиколога механизам токсичности често пружа увид у то како хемијски или физички агенс може изазвати смрт или онеспособљење.
Ако се разуме механизам токсичности, дескриптивна токсикологија постаје корисна у предвиђању токсичних ефеката сродних хемикалија. Важно је схватити, међутим, да недостатак механичких информација не спречава здравствене раднике да заштите људско здравље. Разборите одлуке засноване на студијама на животињама и људском искуству се користе за утврђивање безбедних нивоа изложености. Традиционално, маргина сигурности је утврђена коришћењем „нивоа без штетних ефеката“ или „најнижег нивоа штетних ефеката“ из студија на животињама (користећи дизајне са поновљеном изложеношћу) и дељењем тог нивоа са фактором 100 за професионалну изложеност или 1,000 за друга изложеност људи животне средине. Успех овог процеса је очигледан из неколико инцидената штетних ефеката на здравље који се приписују излагању хемикалијама код радника где су у прошлости постављене и поштоване одговарајуће границе изложености. Поред тога, људски животни век наставља да расте, као и квалитет живота. Свеукупно коришћење података о токсичности довело је до ефикасне регулаторне и добровољне контроле. Детаљно познавање токсичних механизама ће побољшати предвидљивост новијих модела ризика који се тренутно развијају и резултираће сталним побољшањем.
Разумевање механизама животне средине је сложено и претпоставља познавање поремећаја екосистема и хомеостазе (равнотеже). Иако се о томе не говори у овом чланку, боље разумевање токсичних механизама и њихових крајњих последица у екосистему би помогло научницима да донесу мудре одлуке у вези са руковањем комуналним и индустријским отпадом. Управљање отпадом је растућа област истраживања и биће веома важно у будућности.
Технике проучавања механизама токсичности
Већина механичких студија почиње дескриптивном токсиколошком студијом на животињама или клиничким опсервацијама код људи. У идеалном случају, студије на животињама укључују пажљиво понашање и клиничка посматрања, пажљиво биохемијско испитивање елемената крви и урина на знакове штетне функције главних биолошких система у телу и постморталну процену свих система органа микроскопским прегледом да би се проверило да ли постоје повреда (видети смернице ОЕЦД-а за испитивање; директиве ЕЦ о процени хемикалија; правила тестирања ЕПА САД; прописе о хемикалијама Јапана). Ово је аналогно темељном физичком прегледу људи који би се обавио у болници током периода од два до три дана, осим обдукције.
Разумевање механизама токсичности је уметност и наука посматрања, креативност у одабиру техника за тестирање различитих хипотеза и иновативна интеграција знакова и симптома у узрочно-последичној вези. Механистичке студије почињу са излагањем, прате временску дистрибуцију и судбину у телу (фармакокинетика) и мере резултујући токсични ефекат на неком нивоу система и на неком нивоу дозе. Различите супстанце могу деловати на различитим нивоима биолошког система изазивајући токсичност.
Излагање
Пут излагања у механичким студијама је обично исти као код излагања људи. Пут је важан јер могу постојати ефекти који се јављају локално на месту излагања поред системских ефеката након што се хемикалија апсорбује у крв и дистрибуира по целом телу. Једноставан, али убедљив пример локалног ефекта би била иритација и евентуална корозија коже након наношења јаких киселих или алкалних раствора дизајнираних за чишћење тврдих површина. Слично томе, иритација и ћелијска смрт се могу јавити у ћелијама које облажу нос и/или плућа након излагања иритантним парама или гасовима као што су оксиди азота или озона. (Обоје су састојци загађења ваздуха или смога). Након апсорпције хемикалије у крв кроз кожу, плућа или гастроинтестинални тракт, концентрацију у било ком органу или ткиву контролишу многи фактори који одређују фармакокинетику хемикалије у телу. Тело има способност активирања и детоксикације разних хемикалија као што је наведено у наставку.
Улога фармакокинетике у токсичности
Фармакокинетика описује временске односе за хемијску апсорпцију, дистрибуцију, метаболизам (биохемијске промене у телу) и елиминацију или излучивање из тела. У односу на механизме токсичности, ове фармакокинетичке варијабле могу бити веома важне и у неким случајевима одређују да ли ће се токсичност појавити или неће. На пример, ако се материјал не апсорбује у довољној количини, неће доћи до системске токсичности (унутар тела). Супротно томе, високо реактивна хемикалија која се брзо (секунде или минуте) детоксифицира помоћу дигестивних или јетрених ензима можда неће имати времена да изазове токсичност. Неке полицикличне халогенисане супстанце и смеше, као и одређени метали као што је олово, не би изазвали значајну токсичност ако би излучивање било брзо; али акумулација до довољно високих нивоа одређује њихову токсичност пошто излучивање није брзо (понекад се мери годинама). На срећу, већина хемикалија се не задржава тако дуго у телу. Акумулација безопасног материјала и даље не би изазвала токсичност. Брзина елиминације из тела и детоксикације се често назива полуживотом хемикалије, што је време да се 50% хемикалије излучи или промени у нетоксични облик.
Међутим, ако се хемикалија акумулира у одређеној ћелији или органу, то може бити разлог за даље испитивање њене потенцијалне токсичности у том органу. Недавно су развијени математички модели за екстраполацију фармакокинетичких варијабли са животиња на људе. Ови фармакокинетички модели су изузетно корисни у генерисању хипотеза и тестирању да ли експериментална животиња може бити добра репрезентација за људе. О овој теми написана су бројна поглавља и текстови (Гехринг ет ал. 1976; Реитз ет ал. 1987; Нолан ет ал. 1995). Поједностављени пример физиолошког модела је приказан на слици 1.
Слика 1. Поједностављени фармакокинетички модел
Могу негативно утицати на различите нивое и системе
Токсичност се може описати на различитим биолошким нивоима. Повреда се може проценити на целој особи (или животињи), органском систему, ћелији или молекулу. Системи органа обухватају имунолошки, респираторни, кардиоваскуларни, бубрежни, ендокрини, дигестивни, мусколо-скелетни, крвни, репродуктивни и централни нервни систем. Неки кључни органи укључују јетру, бубреге, плућа, мозак, кожу, очи, срце, тестисе или јајнике и друге главне органе. На ћелијском/биохемијском нивоу, нежељени ефекти укључују ометање нормалне функције протеина, функције ендокриних рецептора, инхибицију метаболичке енергије или инхибицију или индукцију ксенобиотских (страних супстанци) ензима. Нежељени ефекти на молекуларном нивоу укључују промену нормалне функције ДНК-РНК транскрипције, специфичног везивања за цитоплазматске и нуклеарне рецепторе и гена или генских производа. На крају, дисфункција у главном органском систему је вероватно узрокована молекуларном променом у одређеној циљној ћелији унутар тог органа. Међутим, није увек могуће пратити механизам уназад до молекуларног порекла узрочности, нити је то неопходно. Интервенција и терапија се могу осмислити без потпуног разумевања молекуларне мете. Међутим, знање о специфичном механизму токсичности повећава предиктивну вредност и тачност екстраполације на друге хемикалије. Слика 2 је дијаграмски приказ различитих нивоа на којима се може открити интерференција нормалних физиолошких процеса. Стрелице показују да се последице по појединца могу одредити одозго надоле (изложеност, фармакокинетика токсичности система/органа) или одоздо према горе (молекуларна промена, ћелијски/биохемијски ефекат до токсичности система/органа).
Слика 2. Репрезентација механизама токсичности
Примери механизама токсичности
Механизми токсичности могу бити једноставни или веома сложени. Често постоји разлика између врсте токсичности, механизма токсичности и нивоа ефекта, у зависности од тога да ли су штетни ефекти последица појединачне, акутне високе дозе (попут случајног тровања) или ниже дозе. поновљено излагање (од професионалне изложености или изложености околини). Класично, у сврху тестирања, акутна, појединачна висока доза се даје директном интубацијом у стомак глодара или излагањем атмосфери гаса или паре у трајању од два до четири сата, шта год највише личи на излагање људи. Животиње се посматрају током периода од две недеље након излагања, а затим се прегледају главни спољни и унутрашњи органи на повреде. Тестирање поновљених доза се креће од месеци до година. За врсте глодара, две године се сматрају хроничном (доживотном) студијом која је довољна за процену токсичности и канцерогености, док би се за нељудске примате две године сматрале субхроничном (мање од животног века) студијом за процену токсичности поновљених доза. Након излагања, врши се комплетан преглед свих ткива, органа и течности како би се утврдили нежељени ефекти.
Механизми акутне токсичности
Следећи примери су специфични за високе дозе, акутне ефекте који могу довести до смрти или тешке онеспособљености. Међутим, у неким случајевима, интервенција ће довести до пролазних и потпуно реверзибилних ефеката. Доза или тежина изложености ће одредити резултат.
Једноставни асфиксанти. Механизам токсичности за инертне гасове и неке друге нереактивне супстанце је недостатак кисеоника (аноксија). Ове хемикалије, које узрокују недостатак кисеоника у централном нервном систему (ЦНС), називају се једноставни асфиксанти. Ако особа уђе у затворени простор који садржи азот без довољно кисеоника, долази до тренутног исцрпљивања кисеоника у мозгу и доводи до несвести и коначне смрти ако се особа брзо не уклони. У екстремним случајевима (близу нулте вредности кисеоника) може доћи до несвести за неколико секунди. Спасавање зависи од брзог уклањања у окружење богато кисеоником. Преживљавање са иреверзибилним оштећењем мозга може настати од одложеног спасавања, због одумирања неурона, који не могу да се регенеришу.
Хемијска средства за гушење. Угљенмоноксид (ЦО) се такмичи са кисеоником за везивање за хемоглобин (у црвеним крвним зрнцима) и стога лишава ткива кисеоника за енергетски метаболизам; може доћи до ћелијске смрти. Интервенција обухвата уклањање са извора ЦО и третман кисеоником. Директна употреба кисеоника заснива се на токсичном деловању ЦО. Још један снажан хемијски гушилац је цијанид. Јон цијанида омета ћелијски метаболизам и коришћење кисеоника за енергију. Третман натријум нитритом изазива промену хемоглобина у црвеним крвним зрнцима у метхемоглобин. Метхемоглобин има већи афинитет везивања за јон цијанида него ћелијска мета цијанида. Сходно томе, метхемоглобин везује цијанид и држи цијанид подаље од циљних ћелија. Ово чини основу за антидоталну терапију.
Депресиви централног нервног система (ЦНС).. Акутну токсичност карактерише седација или губитак свести за низ материјала као што су растварачи који нису реактивни или који се трансформишу у реактивне интермедијере. Претпоставља се да је седација/анестезија последица интеракције растварача са мембранама ћелија у ЦНС-у, што нарушава њихову способност да преносе електричне и хемијске сигнале. Иако седација може изгледати као благи облик токсичности и била је основа за развој раних анестетика, „доза и даље ствара отров”. Ако се довољна доза даје гутањем или удисањем, животиња може угинути услед застоја дисања. Ако не дође до смрти од анестетика, ова врста токсичности је обично лако реверзибилна када се субјект уклони из околине или се хемикалија редистрибуира или елиминише из тела.
Ефекти коже. Штетни ефекти на кожу могу варирати од иритације до корозије, у зависности од супстанце на коју се сусреће. Јаке киселине и алкални раствори су некомпатибилни са живим ткивом и корозивни су, изазивајући хемијске опекотине и могуће ожиљке. Ожиљци настају услед смрти дермалних, дубоких ћелија коже одговорних за регенерацију. Ниже концентрације могу само изазвати иритацију првог слоја коже.
Још један специфичан токсични механизам коже је хемијска сензибилизација. На пример, сензибилизација се јавља када се 2,4-динитрохлоробензен веже са природним протеинима у кожи и имуни систем препознаје измењени комплекс везан за протеине као страни материјал. Реагујући на ову страну материју, имуни систем активира посебне ћелије да елиминишу страну супстанцу ослобађањем медијатора (цитокина) који изазивају осип или дерматитис (погледајте „Имунотоксикологију“). Ово је иста реакција имуног система када дође до излагања отровном бршљану. Имунолошка сензибилизација је веома специфична за одређену хемикалију и потребна је најмање два излагања пре него што се изазове одговор. Прво излагање сензибилизира (подешава ћелије да препознају хемикалију), а накнадно излагање покреће одговор имуног система. Уклањање контакта и симптоматска терапија антиинфламаторним кремама које садрже стероиде обично су ефикасне у лечењу сензибилизованих појединаца. У озбиљним или рефракторним случајевима, системски делујући имуносупресив попут преднизона користи се у комбинацији са локалним лечењем.
Сензибилизација плућа. Толуен диизоцијанат (ТДИ) изазива имуни одговор на сензибилизацију, али циљно место су плућа. Прекомерно излагање ТДИ код осетљивих особа изазива едем плућа (нагомилавање течности), бронхијално стезање и оштећење дисања. Ово је озбиљно стање и захтева уклањање појединца из потенцијалног накнадног излагања. Лечење је првенствено симптоматско. Сензибилизација коже и плућа прати одговор на дозу. Прекорачење нивоа одређеног за професионалну изложеност може изазвати штетне ефекте.
Ефекти ока. Повреда ока се креће од црвенила спољашњег слоја (црвенило у базену) преко формирања катаракте на рожњачи до оштећења шаренице (обојени део ока). Тестови иритације очију се спроводе када се верује да неће доћи до озбиљне повреде. Многи механизми који изазивају корозију коже такође могу изазвати повреду очију. Материјали корозивни за кожу, попут јаких киселина (пХ мањи од 2) и алкалија (пХ већи од 11.5), нису тестирани у очима животиња јер ће већина изазвати корозију и слепило због механизма сличног оном који изазива корозију коже . Поред тога, површински активни агенси попут детерџената и сурфактаната могу изазвати повреде ока у распону од иритације до корозије. Група материјала која захтева опрез су позитивно наелектрисани (катјонски) сурфактанти, који могу изазвати опекотине, трајно замућење рожњаче и васкуларизацију (формирање крвних судова). Друга хемикалија, динитрофенол, има специфичан ефекат стварања катаракте. Чини се да је ово повезано са концентрацијом ове хемикалије у оку, што је пример фармакокинетичке дистрибуционе специфичности.
Иако је горенаведена листа далеко од исцрпне, она је дизајнирана да пружи читаоцу уважавање различитих механизама акутне токсичности.
Механизми субхроничне и хроничне токсичности
Када се дају као појединачна висока доза, неке хемикалије немају исти механизам токсичности као када се дају више пута као нижа, али и даље токсична доза. Када се даје једна велика доза, увек постоји могућност да се прекорачи способност особе да детоксикује или излучи хемикалију, а то може довести до другачијег токсичног одговора него када се дају мање дозе које се понављају. Алкохол је добар пример. Високе дозе алкохола доводе до примарних ефеката на централни нервни систем, док мање дозе које се понављају доводе до повреде јетре.
Инхибиција антихолинестеразе. Већина органофосфатних пестицида, на пример, има малу токсичност за сисаре док се метаболички не активирају, првенствено у јетри. Примарни механизам деловања органофосфата је инхибиција ацетилхолинестеразе (АЦхЕ) у мозгу и периферном нервном систему. АЦхЕ је нормални ензим који прекида стимулацију неуротрансмитера ацетилхолина. Лагана инхибиција АЦхЕ током дужег периода није повезана са нежељеним ефектима. При високим нивоима изложености, немогућност да се прекине ова неуронска стимулација доводи до прекомерне стимулације холинергичког нервног система. Холинергична прекомерна стимулација на крају доводи до низа симптома, укључујући респираторни застој, праћен смрћу ако се не лечи. Примарни третман је примена атропина, који блокира ефекте ацетилхолина, и примена пралидоксим хлорида, који реактивира инхибирани АЦхЕ. Стога се и узрок и третман токсичности органофосфата разматрају разумевањем биохемијске основе токсичности.
Метаболичка активација. Многе хемикалије, укључујући угљен-тетрахлорид, хлороформ, ацетиламинофлуорен, нитрозамине и паракват се метаболички активирају до слободних радикала или других реактивних интермедијера који инхибирају и ометају нормалну ћелијску функцију. При високим нивоима изложености ово доводи до смрти ћелије (погледајте „Повреда ћелије и ћелијска смрт“). Док специфичне интеракције и ћелијски циљеви остају непознати, системи органа који имају способност да активирају ове хемикалије, као што су јетра, бубрези и плућа, су потенцијалне мете за повреде. Конкретно, одређене ћелије унутар органа имају већи или мањи капацитет да активирају или детоксикују ове интермедијере, а овај капацитет одређује интрацелуларну осетљивост унутар органа. Метаболизам је један од разлога зашто је разумевање фармакокинетике, која описује ове врсте трансформација и дистрибуцију и елиминацију ових интермедијера, важно за препознавање механизма деловања ових хемикалија.
Механизми рака. Рак је мноштво болести, и док се разумевање одређених врста рака убрзано повећава због многих молекуларно биолошких техника које су развијене од 1980. године, има још много тога да се научи. Међутим, јасно је да је развој рака процес у више фаза, а критични гени су кључни за различите врсте рака. Промене у ДНК (соматске мутације) у великом броју ових критичних гена могу изазвати повећану осетљивост или канцерогене лезије (погледајте „Генетичка токсикологија”). Изложеност природним хемикалијама (у куваној храни попут говедине и рибе) или синтетичким хемикалијама (као што је бензидин, који се користи као боја) или физичким агенсима (ултраљубичасто светло од сунца, радон из земље, гама зрачење из медицинских процедура или индустријских активности) су све доприносе мутацијама соматских гена. Међутим, постоје природне и синтетичке супстанце (као што су антиоксиданти) и процеси поправке ДНК који штите и одржавају хомеостазу. Јасно је да је генетика важан фактор у настанку рака, пошто синдроми генетских болести као што је пигментна ксеродерма, где постоји недостатак нормалне поправке ДНК, драматично повећавају осетљивост на рак коже услед излагања ултраљубичастом зрачењу сунца.
Репродуктивни механизми. Слично као код рака, познати су многи механизми репродуктивне и/или развојне токсичности, али много тога треба научити. Познато је да ће одређени вируси (као што је рубеола), бактеријске инфекције и лекови (као што су талидомид и витамин А) негативно утицати на развој. Недавно, рад Кхере (1991), који је прегледао Царнеи (1994), показује добре доказе да се абнормални развојни ефекти у тестовима на животињама са етилен гликолом могу приписати метаболичким метаболитима код мајке. Ово се дешава када се етилен гликол метаболише у киселе метаболите укључујући гликолну и оксалну киселину. Чини се да су накнадни ефекти на плаценту и фетус последица овог процеса метаболичке токсичности.
Zakljucak
Намера овог чланка је да пружи перспективу о неколико познатих механизама токсичности и потреби за будућом студијом. Важно је схватити да механичко знање није апсолутно неопходно за заштиту здравља људи или животне средине. Ово знање ће побољшати способност стручњака да боље предвиди и управља токсичношћу. Стварне технике које се користе у разјашњавању било ког посебног механизма зависе од колективног знања научника и размишљања оних који доносе одлуке у вези са људским здрављем.
Процена изложености
Процена изложености је критичан корак у идентификацији опасности на радном месту путем епидемиолошке истраге. Процес процене изложености може се поделити на низ активности. Ови укључују:
- састављање инвентара потенцијално токсичних агенаса и смеша присутних у циљаном радном окружењу
- утврђивање начина на који долази до изложености и колика је вероватноћа да ће варирати међу запосленима
- избор одговарајућих мера или индекса за квантификацију изложености
- прикупљање података који ће омогућити учесницима студије да буду додељене квалитативне или квантитативне вредности изложености за сваку меру. Кад год је могуће, ове активности треба да се спроводе под вођством квалификованог индустријског хигијеничара.
Студије медицине рада су често критиковане због неадекватности у процени изложености. Неадекватности могу довести до диференцијалне или недиференцијалне погрешне класификације изложености и накнадне пристрасности или губитка прецизности у анализама ефеката изложености. О настојањима да се ситуација побољша сведочи неколико недавних међународних конференција и текстова посвећених овој теми (АЦГИХ 1991; Армстронг ет ал. 1992; Процеедингс оф тхе Цонференце он Ретроспецтиве Ассессмент оф Оццупатионал Екпосурес ин Епидемиологи 1995). Јасно је да технички развој пружа нове могућности за унапређење процене изложености. Ови развоји укључују побољшања у аналитичкој инструментацији, боље разумевање фармакокинетичких процеса и откривање нових биомаркера изложености. Пошто студије здравља на раду често зависе од историјских информација о изложености за које не би било предузето посебно праћење, потреба за ретроспективном проценом изложености додаје додатну димензију сложености овим студијама. Међутим, и даље се развијају побољшани стандарди за процену и за обезбеђивање поузданости таквих процена (Сиемиатицки ет ал. 1986). Процене потенцијалне изложености, наравно, могу се лакше потврдити.
Термин излагање односи се на концентрацију агенса на граници између појединца и околине. Изложеност се обично претпоставља када је познато да је агент присутан у радном окружењу и постоји разумно очекивање да ће запослени имати контакт са тим агентом. Изложеност се може изразити као 8-часовна временско пондерисана просечна концентрација (ТВА), која је мера интензитета изложености који је усредсређен током 8-часовне радне смене. Максималне концентрације су интензитети усредњени у краћим временским периодима као што је 15 минута. Кумулативна изложеност је мера производа просечног интензитета и трајања (нпр. средња 8-часовна ТВА концентрација помножена годинама рада на тој средњој концентрацији). У зависности од природе студије и здравствених исхода од интереса, може бити пожељна процена вршне, просечног интензитета, кумулативне или закашњеле изложености.
Насупрот томе, доза односи се на таложење или апсорпцију агенса у јединици времена. Доза или дневни унос агенса може се проценити комбиновањем података мерења животне средине са стандардним претпоставкама у вези, између осталих фактора, брзине дисања и пенетрације у кожу. Алтернативно, унос се може проценити на основу података биомониторинга. Идеално би било да се доза мери на циљном органу од интереса.
Важни фактори процене изложености укључују:
- идентификацију релевантних агената
- одређивање њиховог присуства и концентрација у одговарајућим срединама животне средине (нпр. ваздух, контактне површине)
- процена вероватних путева уласка (удисање, апсорпција кожом, гутање), временски ток изложености (дневне варијације) и кумулативно трајање изложености изражено у недељама, месецима или годинама
- евалуација ефикасности инжењерских и личних контрола (нпр. употреба заштитне одеће и респираторне заштите може да посредује у изложености) и, коначно
- домаћин и друга разматрања која могу модулирати концентрацију циљних органа.
То укључује физички ниво радне активности и претходно здравствено стање појединаца. Посебну пажњу треба посветити процени изложености агенсима који су постојани или имају тенденцију биоакумулације (нпр. одређени метали, радионуклиди или стабилна органска једињења). Са овим материјалима, унутрашње оптерећење тела може се подмукло повећати чак и када се чини да су концентрације у животној средини ниске.
Иако ситуација може бити прилично сложена, често није. Свакако, многи вредни доприноси идентификацији опасности на раду потичу из студија које користе здраворазумске приступе процени изложености. Извори информација који могу бити од помоћи у идентификацији и категоризацији изложености укључују:
- интервјуи са запосленима
- евиденција о особљу послодавца и производњи (ово укључује радне евиденције, описе послова, историју постројења и процеса и хемијске инвентаре)
- стручни суд
- евиденција о индустријској хигијени (надзор подручја, личне природе и усклађености, и узорци брисања површине, заједно са здравственим опасностима или свеобухватним извештајима истраживања)
- интервјуи са дугогодишњим или пензионисаним запосленима и
- подаци о биомониторингу.
Постоји неколико предности категоризације појединачних експозиција на што је могуће више детаља. Јасно је да ће информативност студије бити побољшана у мери у којој су релевантне изложености адекватно описане. Друго, кредибилитет налаза може бити повећан јер се потенцијал за збуњивање може решити на задовољавајући начин. На пример, референти и изложени појединци ће се разликовати у погледу статуса изложености, али се такође могу разликовати у односу на друге мерене и неизмерене факторе објашњења за болест од интереса. Међутим, ако се градијент изложености може утврдити унутар испитиване популације, мања је вероватноћа да ће исти степен збуњивања опстати унутар подгрупа изложености, чиме се јачају укупни налази студије.
Матрице изложености посла
Један од практичнијих и често коришћених приступа процени изложености био је индиректна процена изложености на основу назива радних места. Употреба матрице изложености послу може бити ефикасна када су доступне комплетне радне историје и постоји разумна константност и у задацима и у изложеностима повезаним са пословима који се проучавају. У најширој скали, стандардна груписања по делатностима и називима радних места осмишљена су на основу рутински прикупљених пописних података или података о занимањима датих у умрлицама. Нажалост, информације које се чувају у овим великим системима евиденције често су ограничене на „тренутно“ или „уобичајено“ занимање. Штавише, пошто стандардне групе не узимају у обзир услове присутне на одређеним радним местима, они се обично морају сматрати сурогатима изложености сировој сировини.
За студије контроле случајева засноване на заједници и регистру, детаљнија процена изложености је постигнута коришћењем стручног мишљења за превођење података о историји посла добијених личним интервјуом у полу-квантитативне процене вероватне изложености одређеним агенсима (Сиемиатицки ет ал. 1986. ). Стручњаци, попут хемичара и индустријских хигијеничара, бирају се да помогну у процени изложености због њиховог знања и познавања различитих индустријских процеса. Комбиновањем детаљних података из упитника са познавањем индустријских процеса, овај приступ је био од помоћи у карактеризацији разлика у изложености између радних објеката.
Приступ матрице изложености посла је такође успешно примењен у студијама специфичним за индустрију и компанију (Гамбле и Спиртас 1976). Појединачне историје послова (хронолошки списак прошлих одељења и радних задатака за сваког запосленог) се често чувају у досијеима особља компаније и, када су доступне, пружају комплетну историју послова за запослене док раде у том објекту. Ови подаци се могу проширити личним интервјуима учесника студије. Следећи корак је инвентаризација свих назива послова и ознака одељења или радних области коришћених током периода студирања. Они се лако могу кретати у стотинама или чак хиљадама у великим, вишепроцесним објектима или међу компанијама у оквиру индустрије, када се производња, одржавање, истраживање, инжењеринг, услуге подршке постројењима и административни послови разматрају током времена (често неколико деценија), омогућавајући промене у индустријским процесима. Консолидација података може бити олакшана креирањем компјутерске датотеке са свим записима о историји рада, а затим коришћењем рутина за уређивање ради стандардизације терминологије назива посла. Они послови који укључују релативно хомогене изложености могу се комбиновати да би се поједноставио процес повезивања изложености са појединачним пословима. Међутим, груписање послова и радних локација треба да буде подржано где год је то могуће мерним подацима прикупљеним у складу са добром стратегијом узорковања.
Чак и са компјутеризованим радним историјама, ретроспективно повезивање података о изложености појединцима може бити тежак задатак. Свакако, услови на радном месту ће се мењати како се технологије мењају, потражња за производима се мења и постављају се нови прописи. Такође може доћи до промена у формулацијама производа и сезонским обрасцима производње у многим индустријама. О неким променама може се водити стална евиденција. Међутим, мање је вероватно да ће се задржати евиденција у вези са сезонским и другим маргиналним променама процеса и производње. Запослени такође могу бити обучени да обављају више послова, а затим да се ротирају између послова како се захтеви производње мењају. Све ове околности чине сложеност профилима изложености запослених. Ипак, постоје и радне поставке које су остале релативно непромењене дуги низ година. У коначној анализи, свако радно окружење мора бити процењено за себе.
На крају, биће неопходно сумирати историју изложености сваке особе током радног века у студији. Показан је значајан утицај на коначне мере изложености-ефекат ризика (Суарез-Алмазор ет ал. 1992), па се стога мора посветити велика пажња у одабиру најприкладније збирне мере изложености.
Индустријска хигијена — мерење животне средине
Праћење изложености на раду је основна стална активност у заштити здравља запослених. Дакле, евиденција о индустријској хигијени можда већ постоји у време када се планира епидемиолошка студија. Ако је тако, ове податке треба прегледати како би се утврдило колико је добро обухваћена циљна популација, колико година су подаци представљени у датотекама и колико лако се мерења могу повезати са пословима, радним подручјима и појединцима. Ова одређивања ће бити од помоћи како у процени изводљивости епидемиолошке студије, тако иу идентификацији недостатака у подацима који би се могли отклонити додатним узорковањем изложености.
Питање како најбоље повезати податке мерења са одређеним пословима и појединцима је посебно важно. Узорковање подручја и зона дисања може бити од помоћи индустријским хигијеничарима у идентификацији извора емисије за корективне мере, али би могло бити мање корисно у карактеризацији стварне изложености запослених осим ако се не изврше пажљиве временске студије радних активности запослених. На пример, континуирано праћење подручја може да идентификује изложеност екскурзијама у одређено доба дана, али остаје питање да ли су запослени били у радном подручју у то време.
Подаци личног узорковања генерално дају тачније процене изложености запослених све док се узорковање обавља у репрезентативним условима, ако се правилно узме у обзир употреба личне заштитне опреме, а задаци посла и услови процеса су релативно константни из дана у дан. Лични узорци се могу лако повезати са појединачним запосленим коришћењем личних идентификатора. Ови подаци се могу генерализовати на друге запослене на истим пословима и на друге временске периоде како је то оправдано. Међутим, на основу сопственог искуства, Раппапорт ет ал. (1993) су упозорили да концентрације изложености могу бити веома варијабилне чак и међу запосленима који су распоређени у оно што се сматра хомогеним групама изложености. Опет, потребна је стручна процена да би се одлучило да ли се могу претпоставити хомогене групе изложености или не.
Истраживачи су успешно комбиновали приступ матрице изложености посла са коришћењем података мерења животне средине за процену изложености унутар ћелија матрице. Када се утврди да подаци мерења недостају, можда ће бити могуће попунити празнине у подацима коришћењем моделирања изложености. Генерално, ово укључује развој модела за повезивање концентрација у животној средини са лакше процењивим детерминантама концентрација изложености (нпр. обим производње, физичке карактеристике објекта укључујући употребу система издувне вентилације, испарљивост агенаса и природа радне активности). Модел је конструисан за радна окружења са познатим концентрацијама у животној средини, а затим се користи за процену концентрација у сличним радним окружењима којима недостају мерни подаци, али имају информације о таквим параметрима као што су састојци и обим производње. Овај приступ може бити посебно користан за ретроспективну процену изложености.
Друго важно питање процене је руковање изложеношћу смешама. Прво, са аналитичке тачке гледишта, одвојена детекција хемијски сродних једињења и елиминација сметњи од других супстанци присутних у узорку можда неће бити у могућностима аналитичког поступка. Потребно је проценити различита ограничења у аналитичким процедурама које се користе за обезбеђивање мерних података и у складу са тим модификовати циљеве студије. Друго, може бити да се одређени агенси скоро увек користе заједно и да се стога јављају у приближно истим релативним размерама у радном окружењу које се проучава. У овој ситуацији интерне статистичке анализе по себи неће бити од користи у разликовању да ли су ефекти последица једног или другог агенса или комбинације агенаса. Такве просудбе би биле могуће само на основу прегледа екстерних студија у којима није било истих комбинација агенаса. Коначно, у ситуацијама када се различити материјали користе наизменично у зависности од спецификација производа (нпр. употреба различитих боја за добијање жељених контраста боја), можда ће бити немогуће приписати ефекте било ком специфичном агенсу.
Биолошки мониторинг
Биомаркери су молекуларне, биохемијске или ћелијске промене које се могу мерити у биолошким медијима као што су људско ткиво, ћелије или течности. Примарни разлог за развој биомаркера изложености је да се обезбеди процена унутрашње дозе за одређени агенс. Овај приступ је посебно користан када су могући вишеструки путеви излагања (нпр. удисање и апсорпција коже), када се заштитна опрема носи повремено или када су услови излагања непредвидиви. Биомониторинг може бити посебно користан када се зна да агенси од интереса имају релативно дуг биолошки полуживот. Из статистичке перспективе, предност биолошког праћења над мониторингом ваздуха може се видети код агенаса који имају полувреме елиминације од само десет сати, у зависности од степена варијабилности животне средине (Дроз и Ву 1991). Изузетно дуг период полураспада материјала као што су хлоровани диоксини (мерено у годинама) чини ова једињења идеалним кандидатима за биолошко праћење. Као и код аналитичких метода за мерење концентрација у ваздуху, мора се бити свестан потенцијалних сметњи. На пример, пре употребе одређеног метаболита као биомаркера, треба утврдити да ли се друге уобичајене супстанце, као што су оне које се налазе у одређеним лековима и диму цигарета, могу метаболисати до исте крајње тачке. Уопштено говорећи, потребно је основно познавање фармакокинетике неког агенса пре него што се биолошки мониторинг користи као основа за процену изложености.
Најчешће тачке мерења су алвеоларни ваздух, урин и крв. Узорци алвеоларног ваздуха могу бити од помоћи у карактеризацији високог краткотрајног излагања растварачу које је настало у року од неколико минута или сати након што је узорак сакупљен. Узорци урина се обично сакупљају да би се одредиле стопе излучивања метаболита једињења од интереса. Узорци крви се могу сакупљати за директно мерење једињења, за мерење метаболита или за одређивање протеина или адуката ДНК (нпр. адукти албумина или хемоглобина и ДНК адукти у циркулишућим лимфоцитима). Доступне ћелије ткива, као што су епителне ћелије из букалне области уста, такође могу бити узорковане за идентификацију адуката ДНК.
Одређивање активности холинестеразе у црвеним крвним зрнцима и плазми представља пример употребе биохемијских промена као мере изложености. Органофосфорни пестициди инхибирају активност холинестеразе и стога мерење те активности пре и после вероватног излагања овим једињењима може бити користан индикатор интензитета излагања. Међутим, како се напредује кроз спектар биолошких промена, постаје све теже разликовати биомаркере изложености и оне ефекта. Уопштено говорећи, мере ефекта имају тенденцију да буду неспецифичне за супстанцу од интереса и стога ће можда бити потребно проценити друга потенцијална објашњења ефекта како би се подржало коришћење тог параметра као мере изложености. Мере изложености треба да буду или директно везане за агента од интереса или треба да постоји добра основа за повезивање било које индиректне мере са агентом. Упркос овим квалификацијама, биолошки мониторинг има много обећања као средство за побољшање процене изложености у прилог епидемиолошким студијама.
Закључци
Приликом поређења у студијама о епидемиологији рада, потреба је да се група радника са изложеношћу упореди са групом радника без изложености. Такве разлике су грубе, али могу бити од помоћи у идентификацији проблематичних области. Јасно је, међутим, да што је мера изложености прецизнија, то ће студија бити кориснија, посебно у смислу њене способности да идентификује и развије одговарајуће циљане програме интервенције.
Мусцулар Ворк
Мишићни рад у професионалним активностима
У индустријализованим земљама око 20% радника је још увек запослено на пословима који захтевају мишићни напор (Рутенфранз ет ал. 1990). Број конвенционалних тешких физичких послова је смањен, али су, с друге стране, многи послови постали статичнији, асиметрични и стационарни. У земљама у развоју, мишићни рад свих облика је и даље веома чест.
Мишићни рад у професионалним активностима може се грубо поделити у четири групе: тежак динамички рад мишића, ручно руковање материјалима, статички рад и рад који се понавља. Тешки динамички радни задаци налазе се на пример у шумарству, пољопривреди и грађевинарству. Руковање материјалима је уобичајено, на пример, у неги, транспорту и складиштењу, док статична оптерећења постоје у канцеларијском раду, електронској индустрији и задацима поправке и одржавања. Радни задаци који се понављају могу се наћи у прехрамбеној и дрвопрерађивачкој индустрији, на пример.
Важно је напоменути да су ручно руковање материјалима и рад који се понавља у основи или динамички или статични мишићни рад, или комбинација ова два.
Физиологија мишићног рада
Динамичан рад мишића
У динамичном раду, активни скелетни мишићи се ритмично контрахују и опуштају. Проток крви у мишиће се повећава како би одговарао метаболичким потребама. Повећани проток крви се постиже појачаним пумпањем срца (срчани минутни волумен), смањеним протоком крви у неактивна подручја, као што су бубрези и јетра, и повећаним бројем отворених крвних судова у радној мускулатури. Пулс, крвни притисак и екстракција кисеоника у мишићима се линеарно повећавају у односу на интензитет рада. Такође, плућна вентилација је појачана због дубљег дисања и повећане фреквенције дисања. Сврха активације целог кардио-респираторног система је да се побољша испорука кисеоника активним мишићима. Ниво потрошње кисеоника измерен током тешког динамичког рада мишића указује на интензитет рада. Максимална потрошња кисеоника (ВОКСНУМКСмак) означава максималан капацитет особе за аеробни рад. Вредности потрошње кисеоника се могу превести у потрошњу енергије (1 литар потрошње кисеоника у минути одговара приближно 5 кцал/мин или 21 кЈ/мин).
У случају динамичког рада, када је активна мишићна маса мања (као на рукама), максимални радни капацитет и вршна потрошња кисеоника су мањи него код динамичког рада са великим мишићима. При истој спољашњој радној снази, динамички рад са малим мишићима изазива веће кардио-респираторне одговоре (нпр. број откуцаја срца, крвни притисак) него рад са великим мишићима (слика 1).
Слика 1. Статички наспрам динамичког рада
Статички рад мишића
У статичком раду, контракција мишића не производи видљиво кретање, као, на пример, у уду. Статички рад повећава притисак унутар мишића, који заједно са механичком компресијом делимично или потпуно блокира циркулацију крви. Испорука хранљивих материја и кисеоника до мишића и уклањање крајњих метаболичких производа из мишића су отежани. Тако се у статичком раду мишићи лакше замарају него у динамичком раду.
Најистакнутија циркулаторна карактеристика статичког рада је пораст крвног притиска. Откуцаји срца и минутни волумен се не мењају много. Изнад одређеног интензитета напора, крвни притисак расте у директној вези са интензитетом и трајањем напора. Штавише, при истом релативном интензитету напора, статички рад са великим мишићним групама производи већи одговор крвног притиска него рад са мањим мишићима. (Види слику 2)
Слика 2. Модел проширеног напрезања и деформације модификован од Рохмерта (1984)
У принципу, регулација вентилације и циркулације у статичком раду је слична оној у динамичком раду, али су метаболички сигнали из мишића јачи и изазивају другачији образац одговора.
Последице мишићног преоптерећења у професионалним активностима
Степен физичког напора који радник доживљава при мишићном раду зависи од величине радне мишићне масе, врсте мишићних контракција (статичке, динамичке), интензитета контракција и индивидуалних карактеристика.
Када мишићно оптерећење не прелази физичке капацитете радника, тело ће се прилагодити оптерећењу и опоравак је брз када се рад прекине. Ако је мишићно оптерећење превелико, наступиће замор, радни капацитет је смањен, а опоравак се успорава. Вршна оптерећења или продужено преоптерећење могу довести до оштећења органа (у облику професионалних болести или болести повезаних са радом). С друге стране, мишићни рад одређеног интензитета, учесталости и трајања такође може резултирати ефектима тренинга, јер, с друге стране, претерано ниски мишићни захтеви могу изазвати ефекте детренинга. Ове односе представљају тзв проширени концепт напрезања развио Рохмерт (1984) (слика 3).
Слика 3. Анализа прихватљивих оптерећења
Генерално, мало је епидемиолошких доказа да је преоптерећење мишића фактор ризика за болести. Међутим, лоше здравље, инвалидитет и субјективна преоптерећеност на послу конвергирају се у физички захтевним пословима, посебно код старијих радника. Штавише, многи фактори ризика за болести мишићно-скелетног система у вези са радом повезани су са различитим аспектима мишићног оптерећења, као што су напор снаге, лоши радни положаји, подизање и изненадна вршна оптерећења.
Један од циљева ергономије је одређивање прихватљивих граница за мишићно оптерећење које би се могло применити за превенцију умора и поремећаја. Док је превенција хроничних ефеката у фокусу епидемиологије, физиологија рада се углавном бави краткорочним ефектима, односно умором у радним задацима или током радног дана.
Прихватљиво оптерећење у тешком динамичком мишићном раду
Процена прихватљивог оптерећења у динамичким радним задацима традиционално се заснива на мерењу потрошње кисеоника (или, сходно томе, утрошка енергије). Потрошња кисеоника се може релативно лако мерити на терену помоћу преносивих уређаја (нпр. Доуглас торба, Мак Планцк респирометар, Окилог, Цосмед), или се може проценити на основу снимака откуцаја срца, који се могу поуздано направити на радном месту, нпр. , са уређајем СпортТестер. Употреба пулса у процени потрошње кисеоника захтева да се он индивидуално калибрише у односу на измерену потрошњу кисеоника у стандардном режиму рада у лабораторији, односно, истраживач мора да зна потрошњу кисеоника појединачног субјекта при датом пулсу. Снимке откуцаја срца треба третирати са опрезом јер на њих утичу и фактори као што су физичка спремност, температура околине, психолошки фактори и величина активне мишићне масе. Дакле, мерења срчане фреквенције могу довести до прецењивања потрошње кисеоника на исти начин на који вредности потрошње кисеоника могу довести до потцењивања глобалног физиолошког напрезања одражавајући само енергетске потребе.
Релативни аеробни напор (РАС) се дефинише као део (изражен у процентима) радникове потрошње кисеоника измерен на послу у односу на његову или њену ВОКСНУМКСмак мерено у лабораторији. Ако су доступна само мерења откуцаја срца, блиска апроксимација РАС се може направити израчунавањем вредности за процентуални опсег откуцаја срца (% ХР опсега) помоћу такозване Карвоненове формуле као на слици 3.
VOКСНУМКСмак се обично мери на бициклистичком ергометру или траци за трчање, код којих је механичка ефикасност висока (20-25%). Када је активна мишићна маса мања или је статичка компонента већа, ВОКСНУМКСмак а механичка ефикасност ће бити мања него у случају вежбања са великим мишићним групама. На пример, утврђено је да у сортирању поштанских пакета ВОКСНУМКСмак радника била је само 65% од максимума измереног на бициклергометру, а механичка ефикасност задатка била је мања од 1%. Када се смернице заснивају на потрошњи кисеоника, режим тестирања у максималном тесту треба да буде што је могуће ближи стварном задатку. Овај циљ је, међутим, тешко постићи.
Према класичној студији Астранда (1960), РАС не би требало да пређе 50% током осмочасовног радног дана. У њеним експериментима, при оптерећењу од 50% телесна тежина се смањила, пулс није достигао стабилно стање и субјективна нелагодност се повећала током дана. Препоручила је ограничење РАС од 50% и за мушкарце и за жене. Касније је открила да су грађевински радници спонтано изабрали просечан ниво РАС од 40% (распон 25-55%) током радног дана. Неколико новијих студија је показало да је прихватљиви РАС нижи од 50%. Већина аутора препоручује 30-35% као прихватљив ниво РАС за цео радни дан.
Првобитно, прихватљиви нивои РАС су развијени за чист динамички рад мишића, који се ретко дешава у стварном радном животу. Може се десити да прихватљиви нивои РАС не буду прекорачени, на пример, у задатку дизања, али локално оптерећење на леђима може у великој мери премашити прихватљиве нивое. Упркос својим ограничењима, РАС одређивање се широко користи у процени физичког напрезања на различитим пословима.
Поред мерења или процене потрошње кисеоника, доступне су и друге корисне физиолошке методе на терену за квантификацију физичког стреса или напрезања при тешком динамичком раду. Технике посматрања се могу користити у процени потрошње енергије (нпр. уз помоћ Едхолмова скала) (Едхолм 1966). Оцена уоченог напора (РПЕ) указује на субјективно накупљање умора. Нови системи за амбулантно праћење крвног притиска омогућавају детаљније анализе одговора циркулације.
Прихватљиво радно оптерећење у ручном руковању материјалима
Ручно руковање материјалима обухвата такве радне задатке као што су подизање, ношење, гурање и повлачење различитих спољашњих терета. Већина истраживања у овој области фокусирана је на проблеме доњег дела леђа у задацима дизања, посебно са биомеханичке тачке гледишта.
Ниво РАС од 20-35% је препоручен за задатке дизања, када се задатак упореди са индивидуалном максималном потрошњом кисеоника добијеном тестом на бициклергометру.
Препоруке за максималну дозвољену брзину откуцаја срца су или апсолутне или повезане са пулсом у мировању. Апсолутне вредности за мушкарце и жене су 90-112 откуцаја у минути при континуираном ручном руковању материјалима. Ове вредности су отприлике исте као и препоручене вредности за повећање броја откуцаја срца изнад нивоа мировања, односно 30 до 35 откуцаја у минути. Ове препоруке важе и за тежак динамички рад мишића за младе и здраве мушкарце и жене. Међутим, као што је раније поменуто, са подацима о пулсу треба поступати са опрезом, јер на њих утичу и други фактори осим рада мишића.
Смернице за прихватљиво оптерећење за ручно руковање материјалима на основу биомеханичких анализа обухватају неколико фактора, као што су тежина терета, учесталост руковања, висина подизања, удаљеност терета од тела и физичке карактеристике особе.
У једној великој теренској студији (Лоухеваара, Хакола и Оллила 1990) откривено је да здрави мушки радници могу да рукују поштанским пакетима тежине 4 до 5 килограма током смене без икаквих знакова објективног или субјективног умора. Већина руковања се одвијала испод нивоа рамена, просечна учесталост руковања била је мања од 8 пакета у минути, а укупан број пакета мањи од 1,500 по смени. Просечна брзина откуцаја срца радника била је 101 откуцај у минути, а средња потрошња кисеоника 1.0 л/мин, што је одговарало 31% РАС у односу на бициклистички максимум.
Посматрања радних положаја и употребе силе која се обављају на пример према ОВАС методи (Карху, Канси и Куоринка 1977), оцене уоченог напора и амбулантна снимања крвног притиска су такође погодне методе за процену стреса и напрезања при ручном руковању материјалима. Електромиографија се може користити за процену локалних одговора на напрезање, на пример у мишићима руку и леђа.
Прихватљиво оптерећење за статички мишићни рад
Статички мишићни рад је потребан углавном у одржавању радних положаја. Време издржљивости статичке контракције експоненцијално зависи од релативне силе контракције. То значи, на пример, да када је статичка контракција захтева 20% максималне силе, време издржљивости је 5 до 7 минута, а када је релативна сила 50%, време издржљивости је око 1 минут.
Старије студије су показале да се неће развити замор када је релативна сила испод 15% максималне силе. Међутим, новије студије су показале да је прихватљива релативна сила специфична за мишић или мишићну групу и износи 2 до 5% максималне статичке снаге. Ова ограничења силе су, међутим, тешка за коришћење у практичним радним ситуацијама јер захтевају електромиографске снимке.
За практичаре је доступно мање теренских метода за квантификацију напрезања у статичком раду. Постоје неке опсервационе методе (нпр. ОВАС метода) за анализу пропорције лоших радних положаја, односно положаја који одступају од нормалних средњих положаја главних зглобова. Мерење крвног притиска и оцена уоченог напора могу бити корисни, док број откуцаја срца није толико применљив.
Прихватљиво оптерећење у раду који се понавља
Понављајући рад са малим мишићним групама подсећа на статички рад мишића са становишта циркулаторних и метаболичких одговора. Типично, у раду који се понавља, мишићи се контрахују преко 30 пута у минути. Када релативна сила контракције пређе 10% максималне силе, време издржљивости и мишићна сила почињу да се смањују. Међутим, постоје велике индивидуалне варијације у временима издржљивости. На пример, време издржљивости варира између два до педесет минута када се мишић контрахује 90 до 110 пута у минути при релативном нивоу силе од 10 до 20% (Лауриг 1974).
Веома је тешко поставити било какве дефинитивне критеријуме за рад који се понавља, јер чак и веома лагани нивои рада (као код употребе микрорачунарског миша) могу изазвати повећање интрамускуларног притиска, што понекад може довести до отицања мишићних влакана, бола и смањења у мишићној снази.
Понављајући и статични рад мишића ће узроковати умор и смањен радни капацитет при веома ниским релативним нивоима силе. Стога, ергономске интервенције треба да имају за циљ да минимизирају број понављајућих покрета и статичких контракција колико год је то могуће. Врло мало теренских метода је доступно за процену напрезања у раду који се понавља.
Превенција мишићног преоптерећења
Постоји релативно мало епидемиолошких доказа који показују да је оптерећење мишића штетно по здравље. Међутим, физиолошке и ергономске студије рада показују да преоптерећење мишића доводи до умора (тј. смањење радног капацитета) и може смањити продуктивност и квалитет рада.
Превенција мишићног преоптерећења може бити усмерена на садржај рада, радно окружење и радника. Оптерећење се може подесити техничким средствима, која се фокусирају на радно окружење, алате и/или методе рада. Најбржи начин да се регулише мишићно оптерећење је повећање флексибилности радног времена на индивидуалној основи. То значи осмишљавање режима рада и одмора који узимају у обзир радно оптерећење и потребе и капацитете појединачног радника.
Статички и понављајући мишићни рад треба свести на минимум. Повремене тешке динамичке фазе рада могу бити корисне за одржавање физичке спремности типа издржљивости. Вероватно најкориснији облик физичке активности који се може уградити у радни дан је брзо ходање или пењање уз степенице.
Превенција мишићног преоптерећења је, међутим, веома тешка ако су физичке способности или радне вештине радника лоше. Одговарајућа обука ће побољшати радне вештине и може смањити мишићно оптерећење на послу. Такође, редовно физичко вежбање током рада или слободног времена повећаће мишићне и кардио-респираторне капацитете радника.
Ћелијска повреда и ћелијска смрт
Практично цела медицина је посвећена или спречавању ћелијске смрти, код болести као што су инфаркт миокарда, можданог удара, трауме и шока, или њеном изазивању, као у случају заразних болести и рака. Стога је неопходно разумети природу и механизме који су укључени. Ћелијска смрт је класификована као „случајна“, односно узрокована токсичним агенсима, исхемијом и тако даље, или „програмирана“, као што се дешава током ембриолошког развоја, укључујући формирање цифара и ресорпцију репа пуноглавца.
Повреда ћелије и ћелијска смрт су, стога, важни и у физиологији и у патофизиологији. Физиолошка смрт ћелија је изузетно важна током ембриогенезе и ембрионалног развоја. Проучавање ћелијске смрти током развоја довело је до важних и нових информација о укљученој молекуларној генетици, посебно кроз проучавање развоја бескичмењака. Код ових животиња, прецизна локација и значај ћелија које су предодређене за ћелијску смрт су пажљиво проучаване и, уз коришћење класичних техника мутагенезе, сада је идентификовано неколико укључених гена. Код одраслих органа, равнотежа између ћелијске смрти и пролиферације ћелије контролише величину органа. У неким органима, као што су кожа и црева, постоји непрекидан обрт ћелија. У кожи, на пример, ћелије се диференцирају како стигну до површине и коначно пролазе кроз терминалну диференцијацију и ћелијску смрт док кератинизација наставља са формирањем умрежених омотача.
Многе класе токсичних хемикалија су способне да изазову акутне повреде ћелија праћене смрћу. То укључује аноксију и исхемију и њихове хемијске аналоге као што је калијум цијанид; хемијски карциногени, који формирају електрофиле који се ковалентно везују за протеине у нуклеинским киселинама; оксидативне хемикалије, што доводи до стварања слободних радикала и повреде оксиданса; активација комплемента; и разне калцијум јонофоре. Ћелијска смрт је такође важна компонента хемијске канцерогенезе; многи потпуни хемијски карциногени, у канцерогеним дозама, производе акутну некрозу и упалу праћену регенерацијом и пренеоплазијом.
Дефиниције
Повреда ћелије
Повреда ћелије се дефинише као догађај или стимулус, као што је токсична хемикалија, која ремети нормалну хомеостазу ћелије, изазивајући тако низ догађаја (слика 1). Илустровани главни циљеви смртоносне повреде су инхибиција синтезе АТП-а, поремећај интегритета плазма мембране или повлачење есенцијалних фактора раста.
Смртоносне повреде доводе до смрти ћелије након променљивог временског периода, у зависности од температуре, типа ћелије и стимулуса; или могу бити сублеталне или хроничне – то јест, повреда доводи до измењеног хомеостатског стања које, иако абнормално, не доводи до смрти ћелије (Трамп и Арстила 1971; Трумп и Березески 1992; Трумп и Березески 1995; Трумп, Березески и Осорнио-Варгас 1981). У случају смртоносне повреде, постоји фаза пре времена смрти ћелије
током овог времена, ћелија ће се опоравити; међутим, након одређеног временског периода („тачка без повратка“ или тачка смрти ћелије), уклањање повреде не резултира опоравком, већ уместо тога ћелија пролази кроз деградацију и хидролизу, на крају достижући физичко-хемијску равнотежу са Животна средина. Ово је фаза позната као некроза. Током прелеталне фазе долази до неколико главних типова промена, у зависности од ћелије и врсте повреде. Они су познати као апоптоза и онкоза.
Апоптоза
Апоптоза је изведена из грчких речи или, што значи далеко од, и птосис, што значи пасти. Термин отпадајући од произилази из чињенице да се, током ове врсте прелеталне промене, ћелије смањују и подлежу изразитом мехурићу на периферији. Мехурићи се затим одвајају и испливавају. Апоптоза се јавља у различитим типовима ћелија након различитих врста токсичних повреда (Виллие, Керр и Цуррие 1980). Посебно је изражен у лимфоцитима, где је преовлађујући механизам за промет клонова лимфоцита. Добијени фрагменти резултирају базофилним телима која се виде унутар макрофага у лимфним чворовима. У другим органима, апоптоза се обично јавља у појединачним ћелијама које се брзо уклањају пре и после смрти фагоцитозом фрагмената од стране суседних паренхимских ћелија или макрофага. Апоптоза која се јавља у појединачним ћелијама са накнадном фагоцитозом обично не доводи до упале. Пре смрти, апоптотичке ћелије показују веома густ цитосол са нормалним или кондензованим митохондријама. Ендоплазматски ретикулум (ЕР) је нормалан или само благо проширен. Нуклеарни хроматин је изразито скупљен дуж нуклеарног омотача и око нуклеола. Нуклеарна контура је такође неправилна и долази до нуклеарне фрагментације. Кондензација хроматина је повезана са фрагментацијом ДНК која се, у многим случајевима, дешава између нуклеозома, дајући карактеристичан изглед лествице на електрофорези.
У апоптози, повећана [Ца2+]i може стимулисати К+ ефлукс који доводи до смањења ћелија, што вероватно захтева АТП. Повреде које потпуно инхибирају синтезу АТП-а, стога, вероватније ће довести до апоптозе. Константно повећање од [Ца2+]i има низ штетних ефеката укључујући активацију протеаза, ендонуклеаза и фосфолипаза. Активација ендонуклеазе доводи до прекида једноструких и двоструких ланаца ДНК који, заузврат, стимулишу повећане нивое п53 и поли-АДП рибозилацију, као и нуклеарних протеина који су неопходни за поправку ДНК. Активација протеаза модификује бројне супстрате укључујући актин и сродне протеине што доводи до формирања мехурића. Други важан супстрат је поли(АДП-рибоза) полимераза (ПАРП), која инхибира поправку ДНК. Повећана [ца2+]i је такође повезан са активацијом бројних протеин киназа, као што су МАП киназа, калмодулин киназа и друге. Такве киназе су укључене у активацију фактора транскрипције који иницирају транскрипцију непосредно раних гена, на пример, ц-фос, ц-јун и ц-миц, и у активацији фосфолипазе А2 што резултира пермеабилизацијом плазма мембране и интрацелуларних мембрана као што је унутрашња мембрана митохондрија.
Онкоза
Онкоза, изведена од грчке речи онкос, да отекне, назван је тако јер у овој врсти прелеталне промене ћелија почиње да отиче скоро одмах након повреде (Мајно и Јорис 1995). Разлог за отицање је повећање катјона у води унутар ћелије. Главни одговорни катјон је натријум, који је нормално регулисан за одржавање запремине ћелије. Међутим, у одсуству АТП-а или ако је На-АТПаза плазмалеме инхибирана, контрола запремине се губи због интрацелуларног протеина, а натријум у води наставља да расте. Међу раним догађајима у онкози су, дакле, повећани [На+]i што доводи до ћелијског отока и повећања [Ца2+]i који настају или услед прилива из екстрацелуларног простора или ослобађања из интрацелуларних складишта. То доводи до отицања цитосола, отицања ендоплазматског ретикулума и Голгијевог апарата и формирања водених мехурића око површине ћелије. Митохондрије су у почетку подвргнуте кондензацији, али касније и оне показују отицање велике амплитуде због оштећења унутрашње митохондријалне мембране. У овој врсти прелеталне промене, хроматин се подвргава кондензацији и на крају деградацији; међутим, не види се карактеристична лествица апоптозе.
Некроза
Некроза се односи на низ промена које се јављају након смрти ћелије када се ћелија претвара у остатке који се обично уклањају инфламаторним одговором. Могу се разликовати две врсте: онкотска некроза и апоптотичка некроза. Онкотична некроза се обично јавља у великим зонама, на пример, у инфаркту миокарда или регионално у органу након хемијске токсичности, као што је проксимални тубул бубрега након примене ХгЦл2. Укључене су широке зоне органа и некротичне ћелије брзо подстичу инфламаторну реакцију, прво акутну, а затим хроничну. У случају да организам преживи, у многим органима некроза је праћена уклањањем мртвих ћелија и регенерацијом, на пример, у јетри или бубрезима након хемијске токсичности. Насупрот томе, апоптотичка некроза се обично јавља на бази једне ћелије и некротични остаци се формирају унутар фагоцита макрофага или суседних паренхимских ћелија. Најраније карактеристике некротичних ћелија укључују прекиде у континуитету плазма мембране и појаву густине флокулента, што представља денатурисане протеине унутар митохондријалног матрикса. Код неких облика повреда који у почетку не ометају акумулацију калцијума у митохондријима, депозити калцијум фосфата се могу видети унутар митохондрија. Други мембрански системи се слично фрагментирају, као што су ЕР, лизозоми и Голгијев апарат. На крају, нуклеарни хроматин се подвргава лизи, што је резултат напада лизозомалних хидролазе. Након смрти ћелије, лизозомалне хидролазе играју важну улогу у чишћењу остатака катепсина, нуклеолаза и липаза, јер оне имају оптимални кисели пХ и могу да преживе низак пХ некротичних ћелија док су други ћелијски ензими денатурисани и инактивирани.
Механизми
Почетни стимулус
У случају смртоносних повреда, најчешће почетне интеракције које доводе до повреде које доводе до смрти ћелије су сметње у енергетском метаболизму, као што су аноксија, исхемија или инхибитори дисања, и гликолиза као што су калијум цијанид, угљен моноксид, јодоацетат и ускоро. Као што је горе поменуто, високе дозе једињења која инхибирају енергетски метаболизам обично доводе до онкозе. Други уобичајени тип почетне повреде која резултира акутном смрћу ћелије је модификација функције плазма мембране (Трумп и Арстила 1971; Трумп, Березески и Осорнио-Варгас 1981). То може бити или директно оштећење и пермеабилизација, као у случају трауме или активације Ц5б-Ц9 комплекса комплемента, механичко оштећење ћелијске мембране или инхибиција натријум-калијума (На+-K+) пумпа са гликозидима као што је оуабаин. Калцијум јонофори као што су јономицин или А23187, који брзо носе [Ца2+] низ градијент у ћелију, такође изазивају акутну смртоносну повреду. У неким случајевима, образац прелеталне промене је апоптоза; код других је онкоза.
Сигнални путеви
Код многих врста повреда, митохондријално дисање и оксидативна фосфорилација су брзо погођени. У неким ћелијама, ово стимулише анаеробну гликолизу, која је способна да одржи АТП, али код многих повреда то је инхибирано. Недостатак АТП-а доводи до неуспеха да се активирају бројни важни хомеостатски процеси, посебно контрола интрацелуларне хомеостазе јона (Трумп и Березески 1992; Трумп, Березески и Осорнио-Варгас 1981). Ово доводи до брзог повећања [Ца2+]i, и повећана [На+] и [Цл-] резултира отицањем ћелија. Повећава [ца2+]i резултирају активацијом низа других сигналних механизама о којима се говори у наставку, укључујући низ киназа, што може резултирати повећаном тренутном раном транскрипцијом гена. Повећана [ца2+]i такође модификује функцију цитоскелета, делом резултирајући формирањем мехурића и активацијом ендонуклеаза, протеаза и фосфолипаза. Чини се да они изазивају многе од важних ефеката о којима је горе дискутовано, као што су оштећење мембране кроз активацију протеазе и липазе, директна деградација ДНК од активације ендонуклеазе и активација киназа као што су МАП киназа и калмодулин киназа, које делују као фактори транскрипције.
Кроз опсежан рад на развоју код бескичмењака Ц. елеганс Дросопхила, као и људске и животињске ћелије, идентификован је низ гена за смрт. Утврђено је да неки од ових гена бескичмењака имају пандане сисара. На пример, ген цед-3, који је неопходан за програмирану ћелијску смрт Ц. елеганс, има активност протеазе и јаку хомологију са ензимом који конвертује интерлеукин сисара (ИЦЕ). Блиско сродни ген који се зове апопаин или прИЦЕ недавно је идентификован са још ближом хомологијом (Ницхолсон ет ал. 1995). Ин Дросопхила, чини се да је ген жетеоца укључен у сигнал који води до програмиране ћелијске смрти. Остали гени за смрт укључују протеин Фас мембране и важан ген супресор тумора, п53, који је широко очуван. п53 се индукује на нивоу протеина након оштећења ДНК и када је фосфорилисан делује као фактор транскрипције за друге гене као што су гадд45 и ваф-1, који су укључени у сигнализацију смрти ћелије. Чини се да су и други непосредни рани гени као што су ц-фос, ц-јун и ц-миц укључени у неке системе.
У исто време, постоје гени против смрти који изгледа да се супротстављају генима за смрт. Први од њих који је идентификован био је цед-9 из Ц. елеганс, који је хомологан бцл-2 код људи. Ови гени делују на још непознат начин да спрече убијање ћелија било генетским или хемијским токсинима. Неки недавни докази указују да бцл-2 може деловати као антиоксиданс. Тренутно се улаже много напора да се развије разумевање укључених гена и да се развију начини за активирање или инхибицију ових гена, у зависности од ситуације.
Резиме Мере изложености током радног века
Истраживачи су срећни када имају на располагању детаљну хронологију радног века радника која пружа историјски преглед послова које су обављали током времена. За ове раднике а матрица изложености послу затим се може подесити тако да омогућава да се свака промена посла кроз коју је радник прошао да буде повезана са специфичним информацијама о изложености.
Детаљне историје изложености морају бити сумиране у сврху анализе како би се утврдило да ли су евидентни обрасци који би могли бити повезани са здравственим и безбедносним проблемима на радном месту. Можемо да визуализујемо листу од, рецимо, 20 промена посла које је радник доживео током свог радног века. Затим постоји неколико алтернативних начина на које се детаљи о изложености (за сваку од 20 промена посла у овом примеру) могу сумирати, узимајући у обзир трајање и/или концентрацију/дозу/степен излагања.
Важно је напоменути, међутим, да се различити закључци из студије могу донети у зависности од одабране методе (Суарез-Алмазор ет ал. 1992). Пример пет збирних мера изложености током радног века приказан је у табели 1.
Табела 1. Формуле и димензије или јединице пет одабраних збирних мера изложености током радног века
|
Мера експозиције |
Формула |
Димензије/Јединице |
|
Кумулативни индекс изложености (ЦЕИ) |
Σ (оцена к време изложености) |
разред и време |
|
Средња оцена (МГ) |
Σ (оцена к време изложености)/укупно време изложености |
разред |
|
Највиша оцена икада (ХГ) |
највиши степен којем је био изложен ≥ 7 дана |
разред |
|
Временски пондерисана просечна оцена (ТВА). |
Σ (оцена к време изложено)/укупно запослено време |
разред |
|
Укупно време изложености (ТТЕ) |
Σ време изложено |
време |
Прилагођено из Суарез-Алмазор ет ал. 1992.
Индекс кумулативне изложености. Кумулативни индекс изложености (ЦЕИ) је еквивалентан „дози“ у токсиколошким студијама и представља збир, током радног века, производа степена изложености и трајања изложености за свако следеће радно место. Укључује време у своје јединице.
Средња оцена. Средња оцена (МГ) кумулира производе степена изложености и трајања изложености за сваки узастопни назив радног места (тј. ЦЕИ) и дели се са укупним временом изложености у било ком степену већем од нуле. МГ је независан од времена у својим јединицама; збирна мера за особу изложену дуготрајно високој концентрацији биће слична оној за особу изложену кратком периоду у високој концентрацији. Унутар било ког усклађеног скупа у дизајну са контролом случаја, МГ је просечна оцена експозиције по јединици изложеног времена. То је просечна оцена за време стварно изложено агенсу који се разматра.
Највиша оцена икада. Највиша оцена икада (ХГ) утврђује се скенирањем радне историје за задавање највише оцене у периоду посматрања коме је радник био изложен најмање седам дана. ХГ би могао погрешно представити изложеност особе током радног века јер је, по самој својој формулацији, заснована на максимизирању, а не на поступку усредњавања и стога је независна од трајања изложености у својим јединицама.
Временски пондерисана просечна оцена. Временски пондерисани просек (ТВА) је кумулативни индекс изложености (ЦЕИ) подељен укупним утрошеним временом. Унутар било ког упареног скупа у дизајну контроле случаја, ТВА оцена је просечна у односу на укупно утрошено време. Разликује се од МГ, који представља просек само за укупно време стварно изложеног. Дакле, ТВА оцена се може посматрати као просечна изложеност по јединици времена током пуног радног стажа без обзира на изложеност по себи.
Укупно време изложено. Укупно време изложености (ТТЕ) акумулира све временске периоде повезане са изложеношћу у јединицама времена. ТТЕ је привлачна због своје једноставности. Међутим, добро је прихваћено да здравствени ефекти морају бити повезани не само са трајањем излагања хемикалијама, већ и са интензитетом те изложености (тј. концентрацијом или степеном).
Јасно је да је корисност збирне мере изложености одређена одговарајућом тежином коју приписује или трајању или концентрацији изложености или обоје. Стога различите мере могу произвести различите резултате (Валкер и Блеттнер 1985). У идеалном случају, одабрана збирна мера треба да се заснива на скупу одбрањивих претпоставки у вези са постулираним биолошким механизмом за узрочник или повезаност болести која се проучава (Смитх 1987). Међутим, овај поступак није увек могућ. Врло често је непознат биолошки ефекат трајања излагања или концентрације испитиваног агенса. У овом контексту, употреба различитих мера изложености може бити корисна да се предложи механизам помоћу којег изложеност остварује свој ефекат.
Препоручује се да се, у недостатку доказаних модела за процену изложености, користе различите сумарне мере изложености током радног века за процену ризика. Овај приступ би олакшао поређење налаза у различитим студијама.
Положаји на послу
Положај особе на послу — међусобна организација трупа, главе и екстремитета — може се анализирати и разумети са неколико тачака гледишта. Положаји имају за циљ унапређење рада; тако, они имају коначност која утиче на њихову природу, њихов временски однос и њихову цену (физиолошку или другу) за особу о којој је реч. Постоји блиска интеракција између физиолошких капацитета и карактеристика тела и захтева рада.
Мишићно-скелетно оптерећење је неопходан елемент у функцијама тела и неопходан за добробит. Са становишта дизајна дела, поставља се питање проналажења оптималне равнотеже између неопходног и прекомерног.
Ставови су заинтересовали истраживаче и практичаре из најмање следећих разлога:
- Положај је извор мишићно-скелетног оптерећења. Осим опуштеног стајања, седења и лежања хоризонтално, мишићи морају да стварају силе за балансирање држања и/или контролу покрета. У класичним тешким задацима, на пример у грађевинској индустрији или у ручном руковању тешким материјалима, спољашње силе, динамичке и статичке, доприносе унутрашњим силама у телу, понекад стварајући велика оптерећења која могу премашити капацитет ткива. (Погледајте слику 1) Чак и у опуштеним положајима, када се рад мишића приближи нули, тетиве и зглобови могу бити оптерећени и показивати знаке умора. Посао са ниским привидним оптерећењем – пример је онај микроскописта – може постати досадан и напоран када се обавља током дужег временског периода.
- Држање је уско повезано са равнотежом и стабилношћу. У ствари, држање се контролише помоћу неколико неуронских рефлекса где унос тактилних сензација и визуелних знакова из околине играју важну улогу. Неки положаји, попут досезања предмета из даљине, су инхерентно нестабилни. Губитак равнотеже је чест непосредан узрок несрећа на раду. Неки радни задаци се обављају у окружењу где стабилност не може увек да се гарантује, на пример, у грађевинској индустрији.
- Држање је основа вештих покрета и визуелног посматрања. Многи задаци захтевају фине, веште покрете руку и пажљиво посматрање предмета рада. У таквим случајевима, држање постаје платформа ових акција. Пажња се усмерава на задатак, а постурални елементи се ангажују да подрже задатке: држање постаје непомично, мишићно оптерећење се повећава и постаје статичније. Француска истраживачка група је у својој класичној студији показала да се непокретност и мишићно-скелетни терет повећавају када се стопа рада повећава (Теигер, Лавилле и Дураффоург 1974).
- Држање је извор информација о догађајима који се дешавају на послу. Посматрање положаја може бити намерно или несвесно. Познато је да вешти надзорници и радници користе постурална посматрања као индикаторе радног процеса. Често посматрање информација о положају није свесно. На пример, на бушотини за бушење нафте, постурални знакови су коришћени за преношење порука између чланова тима током различитих фаза задатка. Ово се дешава у условима када друга средства комуникације нису могућа.
Слика 1. Превисоки положаји руку или савијање напред су један од најчешћих начина стварања „статичног“ оптерећења
Безбедност, здравље и радни положаји
Са безбедносне и здравствене тачке гледишта, сви горе описани аспекти држања могу бити важни. Ипак, највише пажње су привукли положаји као извор мишићно-скелетних болести као што су болести доњег дела леђа. Мишићно-скелетни проблеми у вези са радом који се понавља су такође повезани са положајима.
Ниска бол у леђима (ЛБП) је генерички термин за различите болести доњег дела леђа. Има много узрока и држање је један од могућих узрочних елемената. Епидемиолошке студије су показале да је физички тежак рад погодан за ЛБП и да су положаји један од елемената у овом процесу. Постоји неколико могућих механизама који објашњавају зашто одређени положаји могу изазвати ЛБП. Положаји савијања унапред повећавају оптерећење кичме и лигамената, који су посебно осетљиви на оптерећења у уврнутом положају. Спољашња оптерећења, посебно динамичка, као што су трзаји и клизање, могу значајно повећати оптерећење на леђима.
Са становишта безбедности и здравља, важно је идентификовати лоше држање и друге постуралне елементе као део анализе безбедности и здравља на раду уопште.
Снимање и мерење радних положаја
Положаји се могу снимити и објективно мерити коришћењем визуелног посматрања или мање или више софистицираних техника мерења. Такође се могу снимити коришћењем шема самооцењивања. Већина метода сматра да је држање један од елемената у ширем контексту, на пример, као део садржаја посла—као и АЕТ и Ренаулт Лес профилс дес постес (Ландау и Рохмерт 1981; РНУР 1976)—или као полазна тачка за биомеханичке прорачуне који такође узимају у обзир друге компоненте.
Упркос напретку у технологији мерења, визуелно посматрање остаје, у теренским условима, једино практично средство за систематско бележење положаја. Међутим, прецизност таквих мерења је и даље ниска. Упркос томе, постурална запажања могу бити богат извор информација о раду уопште.
Следећа кратка листа мерних метода и техника представља одабране примере:
- Упитници и дневници за самоизвештавање. Упитници и дневници за самоизвештавање су економична средства за прикупљање информација о положају. Самоизвештавање се заснива на перцепцији субјекта и обично у великој мери одступа од „објективно” посматраних положаја, али ипак може да пренесе важне информације о досадности посла.
- Посматрање положаја. Посматрање положаја укључује чисто визуелно снимање положаја и њихових компоненти, као и методе којима интервју употпуњује информације. Рачунарска подршка је обично доступна за ове методе. Доступне су многе методе за визуелно посматрање. Метода може једноставно да садржи каталог акција, укључујући положаје трупа и удова (нпр. Кеисерлинг 1986; Ван дер Беек, Ван Гаален и Фрингс-Дресен 1992). ОВАС метода предлаже структурирану шему за анализу, оцењивање и евалуацију држања трупа и екстремитета дизајнираних за теренске услове (Карху, Канси и Куоринка 1977). Метода снимања и анализе може садржати шеме нотације, неке од њих прилично детаљне (као код методе циљања положаја, Цорлетт и Бисхоп 1976), и могу да обезбеде нотацију за положај многих анатомских елемената за сваки елемент задатка ( Друри 1987).
- Компјутерски потпомогнуте постуралне анализе. Компјутери су помогли постуралној анализи на много начина. Преносиви рачунари и специјални програми омогућавају лако снимање и брзу анализу положаја. Перссон и Килбом (1983) развили су програм ВИРА за проучавање горњих екстремитета; Кергуелен (1986) је направио комплетан пакет за снимање и анализу за радне задатке; Киви и Маттила (1991) су дизајнирали компјутеризовану ОВАС верзију за снимање и анализу.
Видео је обично саставни део процеса снимања и анализе. Амерички национални институт за безбедност и здравље на раду (НИОСХ) представио је смернице за коришћење видео метода у анализи опасности (НИОСХ 1990).
Биомеханички и антропометријски компјутерски програми нуде специјализоване алате за анализу неких постуралних елемената у радној активности иу лабораторији (нпр. Цхаффин 1969).
Фактори који утичу на радне положаје
Радни положаји служе циљу, коначности изван њих самих. Због тога се везују за спољне услове рада. Постурална анализа која не узима у обзир радно окружење и сам задатак је од ограниченог интереса за ергономисте.
Димензионалне карактеристике радног места у великој мери дефинишу положаје (као у случају седећег задатка), чак и за динамичке задатке (на пример, руковање материјалом у скученом простору). Оптерећења којима се рукује терају тело у одређени положај, као и тежина и природа радног алата. Неки задаци захтевају да се телесна тежина користи за подупирање алата или за примену силе на предмет рада, као што је приказано, на пример на слици 2.
Слика 2. Ергономски аспекти стајања
Индивидуалне разлике, године и пол утичу на положаје. У ствари, откривено је да је „типично“ или „најбоље“ држање, на пример при ручном руковању, углавном измишљено. За сваког појединца и сваку радну ситуацију постоји низ алтернативних „најбољих“ положаја са становишта различитих критеријума.
Помагала за посао и потпоре за радне положаје
Појасеви, лумбални ослонци и ортозе су препоручени за задатке са ризиком од болова у доњем делу леђа или мишићно-скелетних повреда горњих екстремитета. Претпоставља се да ови уређаји пружају подршку мишићима, на пример, контролом интраабдоминалног притиска или покрета руку. Такође се очекује да ограниче опсег покрета лакта, ручног зглоба или прстију. Нема доказа да би модификација постуралних елемената помоћу ових уређаја помогла да се избегну мишићно-скелетни проблеми.
Постурални ослонци на радном месту и на машинама, као што су ручке, потпорни јастучићи за клечање и помагала за седење, могу бити корисни у ублажавању постуралних оптерећења и болова.
Прописи о безбедности и здрављу који се односе на постуралне елементе
Положаји или постурални елементи нису били предмет регулаторних активности по себи. Међутим, неколико докумената или садржи изјаве које се односе на држање или укључују питање држања као саставни елемент прописа. Потпуна слика постојећег регулаторног материјала није доступна. Следеће референце су представљене као примери.
- Међународна организација рада објавила је 1967. године Препоруку о максималним оптерећењима којима се треба руковати. Иако Препорука не регулише постуралне елементе као такве, она има значајан утицај на постурално оптерећење. Препорука је сада застарела, али је служила важној сврси у фокусирању пажње на проблеме у ручном руковању материјалом.
- Смернице за подизање НИОСХ-а (НИОСХ 1981), као такве, такође нису прописи, али су добиле тај статус. Смернице изводе ограничења тежине за оптерећења користећи локацију оптерећења — постурални елемент — као основу.
- У Међународној организацији за стандардизацију, као иу Европској заједници, постоје стандарди и директиве ергономије које садрже материју која се односи на постуралне елементе (ЦЕН 1990. и 1991.).
Генетиц Токицологи
Генетска токсикологија, по дефиницији, је студија о томе како хемијски или физички агенси утичу на замршени процес наслеђа. Генотоксичне хемикалије се дефинишу као једињења која су способна да модификују наследни материјал живих ћелија. Вероватноћа да ће одређена хемикалија изазвати генетско оштећење неизбежно зависи од неколико варијабли, укључујући ниво изложености организма хемикалији, дистрибуцију и задржавање хемикалије када уђе у тело, ефикасност метаболичке активације и/или система детоксикације у циљна ткива, и реактивност хемикалије или њених метаболита са критичним макромолекулима унутар ћелија. Вероватноћа да ће генетско оштећење изазвати болест на крају зависи од природе оштећења, способности ћелије да поправи или појача генетско оштећење, могућности да изрази било коју промену која је изазвана, и способности тела да препозна и потисне умножавање аберантне ћелије.
У вишим организмима, наследне информације су организоване у хромозомима. Хромозоми се састоје од чврсто кондензованих ланаца ДНК повезане са протеинима. У оквиру једног хромозома, сваки молекул ДНК постоји као пар дугих, неразгранатих ланаца нуклеотидних подјединица повезаних фосфодиестарским везама које спајају 5 угљеника једног дела дезоксирибозе са 3 угљеника следећег (слика 1). Поред тога, једна од четири различите нуклеотидне базе (аденин, цитозин, гванин или тимин) је везана за сваку подјединицу дезоксирибозе као перле на нити. Тродимензионално, сваки пар ланаца ДНК формира двоструку спиралу са свим базама оријентисаним ка унутрашњости спирале. Унутар хеликса, свака база је повезана са својом комплементарном базом на супротном ДНК ланцу; водонична веза диктира снажно, нековалентно упаривање аденина са тимином и гванина са цитозином (слика 1). Пошто је секвенца нуклеотидних база комплементарна целом дужином молекула дуплекс ДНК, оба ланца носе у суштини исте генетске информације. У ствари, током репликације ДНК сваки ланац служи као шаблон за производњу новог партнерског ланца.
Слика 1. (а) примарна, (б) секундарна и (ц) терцијарна организација људских наследних информација
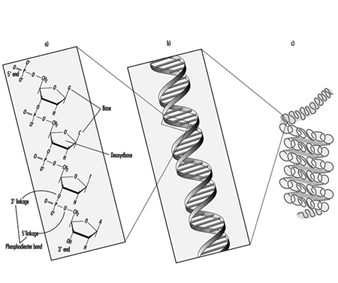 Користећи РНК и низ различитих протеина, ћелија на крају дешифрује информације кодиране линеарном секвенцом база унутар специфичних региона ДНК (гена) и производи протеине који су неопходни за опстанак основних ћелија, као и за нормалан раст и диференцијацију. У суштини, нуклеотиди функционишу као биолошка абецеда која се користи за кодирање аминокиселина, градивних блокова протеина.
Користећи РНК и низ различитих протеина, ћелија на крају дешифрује информације кодиране линеарном секвенцом база унутар специфичних региона ДНК (гена) и производи протеине који су неопходни за опстанак основних ћелија, као и за нормалан раст и диференцијацију. У суштини, нуклеотиди функционишу као биолошка абецеда која се користи за кодирање аминокиселина, градивних блокова протеина.
Када се уметну нетачни нуклеотиди или се нуклеотиди изгубе, или када се додају непотребни нуклеотиди током синтезе ДНК, грешка се назива мутација. Процењено је да се на сваких 10 јавља мање од једне мутације9 нуклеотиди уграђени током нормалне репликације ћелија. Иако мутације нису нужно штетне, промене које изазивају инактивацију или прекомерну експресију важних гена могу довести до разних поремећаја, укључујући рак, наследне болести, развојне абнормалности, неплодност и ембрионалну или перинаталну смрт. Веома ретко, мутација може довести до побољшаног преживљавања; такве појаве су основа природне селекције.
Иако неке хемикалије реагују директно са ДНК, већина захтева метаболичку активацију. У последњем случају, електрофилни интермедијери као што су епоксиди или јони угљеника су на крају одговорни за изазивање лезија на различитим нуклеофилним местима унутар генетског материјала (слика 2). У другим случајевима, генотоксичност је посредована нуспроизводима интеракције једињења са интрацелуларним липидима, протеинима или кисеоником.
Слика 2. Биоактивација: а) бензо(а)пирена; и б) Н-нитрозодиметиламин
Због њиховог релативног обиља у ћелијама, протеини су најчешћа мета интеракције токсичних супстанци. Међутим, модификација ДНК изазива већу забринутост због централне улоге овог молекула у регулисању раста и диференцијације кроз више генерација ћелија.
На молекуларном нивоу, електрофилна једињења имају тенденцију да нападају кисеоник и азот у ДНК. Локације које су најсклоне модификацијама илустроване су на слици 3. Иако су кисеоник унутар фосфатних група у ДНК кичми такође мета за хемијску модификацију, сматра се да је оштећење база биолошки релевантније јер се ове групе сматрају примарним информативним елемената у молекулу ДНК.
Слика 3. Примарна места хемијски изазваних оштећења ДНК
Једињења која садрже један електрофилни део обично испољавају генотоксичност тако што производе моно-адукте у ДНК. Слично томе, једињења која садрже два или више реактивних делова могу да реагују са два различита нуклеофилна центра и на тај начин произведу интра- или интер-молекуларне попречне везе у генетском материјалу (слика 4). Унакрсне везе између ДНК-ДНК и ДНК-протеина могу бити посебно цитотоксичне јер могу формирати потпуне блокове за репликацију ДНК. Из очигледних разлога, смрт ћелије елиминише могућност да ће бити мутирана или неопластично трансформисана. Генотоксични агенси такође могу деловати тако што изазивају прекиде у фосфодиестарској кичми, или између база и шећера (производећи абазична места) у ДНК. Такви прекиди могу бити директан резултат хемијске реактивности на месту оштећења или се могу јавити током поправке једног од горе наведених типова лезија ДНК.
Слика 4. Разне врсте оштећења комплекса протеин-ДНК
Током протеклих тридесет до четрдесет година развијене су различите технике за праћење врсте генетских оштећења изазваних разним хемикалијама. Такви тестови су детаљно описани на другом месту у овом поглављу и Енциклопедија.
Погрешна репликација „микролезија“ као што су моно-адукти, абазична места или прекиди једног ланца може на крају довести до супституција нуклеотидних базних парова, или уметања или брисања кратких полинуклеотидних фрагмената у хромозомској ДНК. Насупрот томе, „макролезије“, као што су гломазни адукти, унакрсне везе или прекиди двоструког ланца, могу изазвати добијање, губитак или преуређење релативно великих делова хромозома. У сваком случају, последице могу бити погубне по организам јер било који од ових догађаја може довести до смрти ћелије, губитка функције или малигне трансформације ћелија. Како тачно оштећење ДНК узрокује рак је углавном непознато. Тренутно се верује да процес може укључивати неодговарајућу активацију прото-онкогена као што је нпр миц Рас, и/или инактивација недавно идентификованих гена супресора тумора као што је п53. Абнормална експресија било ког типа гена укида нормалне ћелијске механизме за контролу пролиферације и/или диференцијације ћелија.
Превласт експерименталних доказа указује да је развој канцера након излагања електрофилним једињењима релативно редак догађај. Ово се делимично може објаснити интринзичном способношћу ћелије да препозна и поправи оштећену ДНК или неуспехом ћелија са оштећеном ДНК да преживе. Током поправке, оштећена база, нуклеотид или кратак део нуклеотида који окружује место оштећења се уклања и (користећи супротни ланац као шаблон) нови део ДНК се синтетише и спаја на место. Да би била ефикасна, поправка ДНК мора да се деси са великом тачношћу пре деобе ћелије, пре него што дође до могућности за ширење мутације.
Клиничке студије су показале да људи са наследним дефектима у способности да поправе оштећену ДНК често развију рак и/или развојне абнормалности у раном добу (табела 1). Такви примери пружају снажне доказе који повезују акумулацију оштећења ДНК са људским болестима. Слично, агенси који промовишу пролиферацију ћелија (као што је тетрадеканоилфорбол ацетат) често појачавају карциногенезу. За ова једињења, повећана вероватноћа неопластичне трансформације може бити директна последица смањења времена доступног ћелији да изврши адекватну поправку ДНК.
Табела 1. Наследни поремећаји склони карциному за које се чини да укључују дефекте у поправци ДНК
| Синдром | simptomi | Ћелијски фенотип |
| Атаксија телангиектазија | Неуролошко погоршање Иммунодефициенци Висока инциденција лимфома |
Преосетљивост на јонизујуће зрачење и одређене алкилирајуће агенсе. Дисрегулисана репликација оштећене ДНК (може указивати на скраћено време за поправку ДНК) |
| Блоомов синдром | Абнормалности у развоју Лезије на изложеној кожи Висока инциденција тумора имуног система и гастроинтестиналног тракта |
Висока учесталост хромозомских аберација Дефектна лигација прекида повезаних са поправком ДНК |
| Фанцонијева анемија | Заостајање у расту Висока учесталост леукемије |
Преосетљивост на средства за умрежавање Висока учесталост хромозомских аберација Дефектна поправка унакрсних веза у ДНК |
| Наследни неполипозни рак дебелог црева | Висока учесталост рака дебелог црева | Дефект у поправци неусклађености ДНК (када се убаци погрешан нуклеотид током репликације) |
| Ксеродерма пигментосум | Висока инциденца епителиома на изложеним деловима коже Неуролошко оштећење (у многим случајевима) |
Преосетљивост на УВ светлост и многе хемијске карциногене Дефекти у поправци ексцизије и/или репликацији оштећене ДНК |
Најраније теорије о томе како хемикалије интерагују са ДНК могу се пратити до студија спроведених током развоја иперита за употребу у рату. Даље разумевање је произашло из напора да се идентификују агенси против рака који би селективно зауставили репликацију туморских ћелија које се брзо деле. Повећана забринутост јавности због опасности у нашем окружењу подстакла је додатна истраживања механизама и последица хемијске интеракције са генетским материјалом. Примери различитих врста хемикалија које испољавају генотоксичност су представљени у табели 2.
Табела 2. Примери хемикалија које показују генотоксичност у људским ћелијама
| Класа хемикалија | Пример | Извор излагања | Вероватна генотоксична лезија |
| Афлатоксини | Афлатоксин Б1 | Контаминирана храна | Крупни ДНК адукти |
| Ароматични амини | 2-Ацетиламинофлуорен | еколошки | Крупни ДНК адукти |
| Азиридин кинони | Митомицин Ц | Хемотерапија рака | Моно-адукти, међуланчане унакрсне везе и једноланчани прекиди у ДНК. |
| Хлоровани угљоводоници | Винил хлорид | еколошки | Моно-адукти у ДНК |
| Метали и једињења метала | Цисплатин | Хемотерапија рака | Унакрсне везе унутар и међу ланцима у ДНК |
| Једињења никла | еколошки | Моно-адукти и једноланчани прекиди у ДНК | |
| Азотни сенф | Циклофосфамид | Хемотерапија рака | Моно-адукти и међуланчане умрежене везе у ДНК |
| Нитросамини | Н-нитрозодиметиламин | Контаминирана храна | Моно-адукти у ДНК |
| Полицикличних ароматичних угљоводоника | Бензо (а) пирене | еколошки | Крупни ДНК адукти |
Више...
Мерење ефеката изложености
Епидемиологија укључује мерење појаве болести и квантификовање повезаности између болести и изложености.
Мере појаве болести
Појава болести се може мерити помоћу фреквенције (броји) али га боље описује Стопе, који се састоје од три елемента: броја погођених особа (бројилац), броја људи у изворној или основној популацији (тј. ризичној популацији) из које потичу погођене особе и обухваћени временски период. Именилац стопе је укупно људско време које је искусила изворна популација. Стопе омогућавају информативнија поређења између популација различитих величина од самог бројања. Ризик, вероватноћа да ће појединац развити болест у одређеном временском периоду, је пропорција, у распону од 0 до 1, и није стопа по себи. Стопа напада, удео људи у популацији који су погођени у одређеном временском периоду, технички је мера ризика, а не стопа.
Морбидитет специфичан за болест укључује учесталост, који се односи на број особа код којих је новодијагностикована болест од интереса. Преваленција односи се на број постојећих предмета. морталитет односи се на број особа које су умрле.
Учесталост се дефинише као број новодијагностикованих случајева у одређеном временском периоду, док је стопа инциденције да ли је овај број подељен укупним личним временом које је доживјела изворна популација (табела 1). За рак, стопе се обично изражавају као годишње стопе на 100,000 људи. Стопе за друге чешће болести могу се исказати на мањи број људи. На пример, стопе урођених мана се обично изражавају на 1,000 живорођених. Кумулативна инциденција, проценат људи који су оболели у одређеном временском периоду, је мера просечног ризика за популацију.
Табела 1. Мере појаве болести: Хипотетичка популација посматрана за петогодишњи период
|
Новооткривени случајеви |
10 |
|
Раније дијагностиковани живи случајеви |
12 |
|
Смрт, сви узроци* |
5 |
|
Смрт, болест од интереса |
3 |
|
Особе у становништву |
100 |
|
Посматране године |
5 |
|
Учесталост |
КСНУМКС лица |
|
Годишња стопа инциденције |
|
|
Преваленција поена (на крају 5. године) |
(10 + 12 - 3) = 19 особа |
|
Преваленција периода (петогодишњи период) |
(10 + 12) = 22 особе |
|
Годишња стопа смртности |
|
|
Годишња стопа морталитета |
|
*Да бисмо поједноставили прорачуне, овај пример претпоставља да су се сви умрли догодили на крају петогодишњег периода тако да је свих 100 особа у популацији било живо пуних пет година.
Преваленција обухвата преваленција тачке, број случајева болести у одређеном тренутку, и преваленција периода, укупан број случајева болести за које се зна да су постојали у неком тренутку током одређеног периода.
морталитет, који се тиче смрти, а не новодијагностикованих случајева болести, одражава факторе који узрокују болест, као и факторе који се односе на квалитет медицинске неге, као што су скрининг, приступ медицинској нези и доступност ефикасних третмана. Сходно томе, напори за генерисање хипотеза и етиолошка истраживања могу бити информативнији и лакши за тумачење када се заснивају на инциденци, а не на подацима о морталитету. Међутим, подаци о морталитету су често доступнији за велике популације него подаци о инциденци.
Термин морталитет опште прихваћено да означава стопу смрти од свих узрока заједно, док стопа смртности је стопа смрти од једног специфичног узрока. За дату болест, стопа смртности (технички пропорција, а не стопа) је број особа које умиру од болести током одређеног временског периода подељен са бројем особа са болешћу. Допуна стопи смртних случајева је степен опстанка. Петогодишња стопа преживљавања је уобичајено мерило за хроничне болести као што је рак.
Појава болести може варирати међу подгрупама становништва или током времена. Мера болести за целу популацију, без разматрања било које подгрупе, назива се а сирова стопа. На пример, стопа инциденције за све старосне групе заједно је груба стопа. Стопе за појединачне старосне групе су старосне стопе. Да упоредимо две или више популација са различитим старосним дистрибуцијама, прилагођен узрасту (или, старосно стандардизовано) стопе треба израчунати за сваку популацију множењем сваке старосне стопе са процентом стандардне популације (нпр. једна од популација која се проучава, популација САД из 1970. године) у тој старосној групи, а затим сабирањем свих старосних група на произвести укупну стопу прилагођену старости. Стопе се могу прилагодити факторима који нису узраст, као што су раса, пол или пушачки статус, ако су познате стопе специфичне за категорију.
Надзор и евалуација дескриптивних података могу пружити назнаке етиологије болести, идентификовати подгрупе високог ризика које би могле бити прикладне за интервенције или програме скрининга и пружити податке о ефикасности таквих програма. Извори информација који су коришћени за активности надзора укључују изводе из матичне књиге умрлих, медицинске картоне, регистре рака, регистре других болести (нпр. регистре урођених мана, регистре бубрежних болести у завршној фази), регистре изложености на радном месту, евиденцију здравственог или инвалидског осигурања и накнаде за раднике записи.
Мере удруживања
Епидемиологија покушава да идентификује и квантификује факторе који утичу на болест. У најједноставнијем приступу, појава болести код особа изложених сумњивом фактору упоређује се са појавом међу неекспонираним особама. Величина повезаности између изложености и болести може се изразити на било који начин апсолутан or релативан услови. (Такође погледајте „Студија случаја: Мере“).
Апсолутни ефекти се мере са стопе разлике разлике у ризику (табела 2). А разлика у стопи је једна стопа минус друга стопа. На пример, ако је стопа инциденције леукемије међу радницима изложеним бензену 72 на 100,000 човеко-година, а стопа међу неекспонираним радницима 12 на 100,000 човеко-година, онда је разлика у стопи 60 на 100,000 човеко-година. А разлика у ризику је разлика у ризицима или кумулативној инциденци и може се кретати од -1 до 1.
Табела 2. Мере повезивања за кохортну студију
|
slučajevi |
Особа-година у опасности |
Стопа на 100,000 |
|
|
Изложен |
100 |
20,000 |
500 |
|
Неекспонирани |
200 |
80,000 |
250 |
|
укупан |
300 |
100,000 |
300 |
Разлика у стопи (РД) = 500/100,000 - 250/100,000
= 250/100,000 годишње
(146.06/100,000 - 353.94/100,000)*
Стопа (или релативни ризик) (РР) = ![]()
Приписиви ризик у изложеном (АРe) = 100/20,000 - 200/80,000
= 250/100,000 годишње
Проценат ризика који се може приписати у изложеним (АРe%) =![]()
Ризик који се може приписати становништву (ПАР) = 300/100,000 - 200/80,000
= 50/100,000 годишње
Проценат ризика који се може приписати популацији (ПАР%) =
![]()
* У заградама 95% интервала поверења израчунатих коришћењем формула у пољима.
Релативни ефекти заснивају се на односима стопа или мерама ризика, уместо на разликама. А однос стопа је однос стопе у једној популацији према стопи у другој. Однос стопа се такође назива однос ризика, релативни ризик, релативна стопа, и учесталост (Или морталитет) однос стопа. Мера је бездимензионална и креће се од 0 до бесконачности. Када је стопа у две групе слична (тј. нема ефекта од изложености), тј однос стопа једнак је јединици (1). Изложеност која повећава ризик дала би однос стопе већи од јединице, док би заштитни фактор дао однос између 0 и 1. вишак релативног ризика је релативни ризик минус 1. На пример, релативни ризик од 1.4 се такође може изразити као вишак релативног ризика од 40%.
У студијама случај-контрола (такође назване студије о случајевима), идентификују се особе са болестима (случајеви) и идентификују се особе без болести (контроле или референти). Упоређене су претходне изложености две групе. Шансе да будете откривени случај се упоређују са изгледима да будете изложени контроли. Комплетан број изворних популација изложених и неизложених особа није доступан, тако да се стопе болести не могу израчунати. Уместо тога, изложени случајеви се могу упоредити са изложеним контролама израчунавањем од релативне шансеИли Однос квота (табела 3).
Табела 3. Мере повезивања за студије случај-контрола: Изложеност дрвеној прашини и аденокарциному носне дупље и параназалних синуса
|
slučajevi |
Контроле |
|
|
Изложен |
18 |
55 |
|
Неекспонирани |
5 |
140 |
|
укупан |
23 |
195 |
Релативне шансе (однос шансе) (ИЛИ) = ![]()
Проценат ризика који се може приписати у изложеним (![]() ) =
) = ![]()
Проценат ризика који се може приписати популацији (ПАР%) = ![]()
где ![]() = пропорција изложених контрола = 55/195 = 0.28
= пропорција изложених контрола = 55/195 = 0.28
* У заградама 95% интервала поверења израчунатих коришћењем формула у оквиру на полеђини.
Извор: Прилагођено из Хаиес ет ал. 1986.
Релативне мере ефекта се користе чешће од апсолутних за извештавање о снази асоцијације. Апсолутне мере, међутим, могу пружити бољу индикацију утицаја удружења на јавно здравље. Мало релативно повећање уобичајене болести, као што је болест срца, може утицати на више особа (велика разлика у ризику) и имати већи утицај на јавно здравље него велико релативно повећање (али мала апсолутна разлика) код ретких болести, као нпр. ангиосарком јетре.
Тестирање значаја
Тестирање статистичке значајности се често врши на мерама ефекта како би се проценила вероватноћа да се уочени ефекат разликује од нулте хипотезе (тј. нема ефекта). Док многе студије, посебно у другим областима биомедицинских истраживања, могу изразити значај п-вредности, епидемиолошке студије су типично присутне интервали поверења (ЦИ) (такође се зове границе поверења). Интервал поузданости од 95%, на пример, је опсег вредности за меру ефекта који укључује процењену меру добијену из података студије и ону за коју постоји 95% вероватноћа укључивања праве вредности. Сматра се да је мало вероватно да вредности изван интервала укључују праву меру ефекта. Ако ЦИ за однос стопа укључује јединицу, онда нема статистички значајне разлике између група које се пореде.
Интервали поверења су информативнији од самих п-вредности. Величина п-вредности је одређена једним или оба разлога. Или је мера повезаности (нпр. однос стопа, разлика у ризику) велика или су популације које се проучавају велике. На пример, мала разлика у стопама болести примећена у великој популацији може дати високо значајну п-вредност. Разлози за велику п-вредност не могу се идентификовати само из п-вредности. Међутим, интервали поверења нам омогућавају да раздвојимо два фактора. Прво, величина ефекта се може уочити по вредностима мере ефекта и бројевима обухваћеним интервалом. Већи коефицијент ризика, на пример, указује на јачи ефекат. Друго, величина популације утиче на ширину интервала поверења. Мале популације са статистички нестабилним проценама стварају шире интервале поверења од веће популације.
Ниво поверења изабран да изрази варијабилност резултата („статистички значај“) је произвољан, али је традиционално био 95%, што одговара п-вредности од 0.05. Интервал поверења од 95% има вероватноћу од 95% да садржи праву меру ефекта. Повремено се користе и други нивои поверења, као што је 90%.
Изложености могу бити дихотомне (нпр. изложене и неекспониране) или могу укључивати много нивоа изложености. Мере ефекта (тј. одговор) могу да варирају у зависности од нивоа изложености. Евалуатинг експозиција-одговор односи су важан део тумачења епидемиолошких података. Аналог експозицији-одговор у студијама на животињама је „доза-одговор”. Ако се одговор повећава са нивоом изложености, већа је вероватноћа да ће повезаност бити узрочна него ако се не примећује никакав тренд. Статистички тестови за процену односа између изложености и одговора укључују Мантелов тест екстензије и тест тренда хи-квадрат.
стандардизација
Да би се узели у обзир други фактори осим примарне изложености од интереса и болести, могу бити мере повезивања стандардизован кроз технике стратификације или регресије. Стратификација значи поделу становништва на хомогене групе у односу на фактор (нпр. полне групе, старосне групе, пушачке групе). Односи ризика или коефицијент шанси се израчунавају за сваки стратум и израчунавају се укупни пондерисани просеци коефицијента ризика или односа шансе. Ове укупне вредности одражавају везу између примарне изложености и болести, прилагођене фактору стратификације, тј. повезаност са ефектима уклоњеног фактора стратификације.
A стандардизовани однос стопа (СРР) је однос две стандардизоване стопе. Другим речима, СРР је пондерисани просек односа стопа специфичних за стратум где су пондери за сваки стратум дистрибуција особа-време неекспониране групе или референтне групе. СРР за две или више група се могу поредити ако се користе исте тежине. Интервали поверења се могу конструисати за СРР као и за стопе.
стандардизовани однос морталитета (СМР) је пондерисани просек односа стопа специфичних за узраст где пондери (нпр. особа-време у ризику) долазе из групе која се проучава, а стопе потичу од референтне популације, што је супротно од ситуације у СРР. Уобичајена референтна популација је општа популација, чије стопе морталитета могу бити лако доступне и засноване на великим бројевима и стога су стабилније него коришћење стопа из неекспониране кохорте или подгрупе професионалне популације која се проучава. Коришћење пондера из кохорте уместо референтне популације назива се индиректна стандардизација. СМР је однос посматраног броја смртних случајева у кохорти и очекиваног броја, на основу стопа из референтне популације (однос се обично множи са 100 за презентацију). Ако не постоји веза, СМР је једнак 100. Треба напоменути да, пошто стопе потичу из референтне популације, а пондери долазе из студијске групе, два или више СМР обично нису упоредиви. Ова неупоредивост се често заборавља у тумачењу епидемиолошких података и могу се извући погрешни закључци.
Ефекат здравог радника
Веома је уобичајено да професионалне кохорте имају нижи укупни морталитет од опште популације, чак и ако су радници под повећаним ризиком за одабране узроке смрти од изложености на радном месту. Овај феномен, тзв ефекат здравог радника, одражава чињеницу да ће било која група запослених вероватно бити здравија, у просеку, од опште популације, што укључује раднике и особе неспособне за рад због болести и инвалидитета. Укупна стопа морталитета у општој популацији има тенденцију да буде виша од стопе код радника. Ефекат варира по јачини у зависности од узрока смрти. На пример, чини се да је мање важан за рак уопште него за хроничну опструктивну болест плућа. Један од разлога за то је тај што је вероватно да се већина карцинома не би развила из било какве предиспозиције према избору посла/каријере у основи рака у млађој доби. Ефекат здравог радника у датој групи радника има тенденцију да се смањи током времена.
Пропорционална смртност
Понекад потпуна табела кохорте (тј. ризично радно време) није доступна и постоје информације само о смртима или неким подскуповима смрти које је доживела кохорта (нпр. смрти међу пензионерима и активним запосленима, али не и међу радницима који су напустили радни однос пре него што су стекли право на пензију). Рачунање особа-година захтева посебне методе за бављење проценом личног времена, укључујући методе животних табела. Без информација о укупном времену за све чланове кохорте, без обзира на статус болести, СМР и СРР се не могу израчунати. Уместо тога, пропорционални односи морталитета (ПМР) се могу користити. ПМР је однос посматраног броја смртних случајева услед специфичног узрока у поређењу са очекиваним бројем, заснован на пропорцији укупних смртних случајева услед специфичног узрока у референтној популацији, помноженог са бројем укупних смртних случајева у студији група, помножено са 100.
Пошто удео смртних случајева од свих узрока заједно мора бити једнак 1 (ПМР=100), неки ПМР могу изгледати као вишак, али су заправо вештачки надувани због стварних дефицита у другим узроцима смрти. Слично томе, неки очигледни дефицити могу само да одражавају стварне ексцесе других узрока смрти. На пример, ако апликатори пестицида из ваздуха имају велики стварни вишак смртних случајева услед несрећа, математички захтев да је ПМР за све узроке заједно једнак 100 може довести до тога да неки од узрока смрти изгледају мањкаво чак и ако је смртност превелика. Да би ублажили овај потенцијални проблем, истраживачи заинтересовани првенствено за рак могу израчунати пропорционалне стопе морталитета од рака (ПЦМРс). ПЦМР упоређују уочени број смртних случајева од рака са бројем који се очекује на основу пропорције укупних смртних случајева од рака (а не свих смртних случајева) за рак од интереса у референтној популацији помноженог укупним бројем смртних случајева од рака у студијској групи, помноженог са 100. Дакле, на ПЦМР неће утицати аберација (вишак или дефицит) у узроку смрти који није од рака, као што су несреће, болести срца или немалигне болести плућа.
ПМР студије се могу боље анализирати коришћењем коефицијенти морталитета (МОРс), у суштини анализирајући податке као да су из студије случај-контрола. „Контроле“ су смрти из подскупа свих смрти за које се сматра да нису повезане са изложеношћу која се проучава. На пример, ако је главни интерес студије био рак, односи шансе за смртност би се могли израчунати упоређујући изложеност међу смртним случајевима од рака са изложеношћу међу смртним случајевима од кардиоваскуларних болести. Овај приступ, као и ПЦМР, избегава проблеме са ПМР који настају када флуктуација у једном узроку смрти утиче на очигледан ризик другог једноставно зато што укупни ПМР мора бити једнак 100. Избор контролних узрока смрти је, међутим, критичан . Као што је горе поменуто, они не смеју бити повезани са изложеношћу, али могући однос између изложености и болести можда није познат за многе потенцијалне контролне болести.
Приписиви ризик
Постоје доступне мере које изражавају количину болести која би се могла приписати изложености да је уочена повезаност између изложености и болести узрочна. Тхе приписиви ризик у изложеним (АРe) је стопа болести код изложених минус стопа код неекспонираних. Пошто се стопе болести не могу мерити директно у студијама случај-контрола, АРe може се израчунати само за кохортне студије. Сродна, интуитивнија мера, проценат ризика који се може приписати у изложеним (АРe%), може се добити из било којег дизајна студије. Тхе АРe% је проценат случајева који се јављају у изложеној популацији који се може приписати изложености (види табелу 2 и табелу 3 за формулу). Тхе АРe% је однос стопе (или однос шансе) минус 1, подељен односом стопе (или односом шансе), помножен са 100.
ризик који се може приписати популацији (ПАР) и проценат ризика који се може приписати популацији (ПАР%), или етиолошка фракција, изражавају количину болести у укупној популацији коју чине изложене и неекспониране особе, односно због изложености ако је уочена повезаност узрочна. ПАР се може добити из кохортних студија (табела 28.3), а ПАР% се може израчунати иу кохортним иу студијама случај-контрола (табела 2 и табела 3).
Репрезентативност
Постоји неколико мера ризика које су описане. Сваки претпоставља основне методе за бројање догађаја и представнике ових догађаја у дефинисану групу. Када се резултати упореде у различитим студијама, разумевање коришћених метода је од суштинског значаја за објашњење свих уочених разлика.
Биомеханика
Циљеви и принципи
Биомеханика је дисциплина која приступа проучавању тела као да је то само механички систем: сви делови тела су упоређени са механичким структурама и проучавају се као такви. На пример, могу се повући следеће аналогије:
- кости: полуге, структурни чланови
- месо: запремине и масе
- зглобови: носеће површине и зглобови
- облоге зглобова: мазива
- мишићи: мотори, опруге
- нерви: механизми контроле повратних информација
- органи: напајања
- тетиве: ужад
- ткиво: опруге
- телесне шупљине: балони.
Главни циљ биомеханике је проучавање начина на који тело производи силу и покреће кретање. Дисциплина се првенствено ослања на анатомију, математику и физику; сродне дисциплине су антропометрија (проучавање мерења људског тела), физиологија рада и кинезиологија (проучавање принципа механике и анатомије у односу на кретање човека).
У разматрању здравља радника на раду, биомеханика помаже да се разуме зашто неки задаци изазивају повреде и лоше здравље. Неке релевантне врсте штетног утицаја на здравље су напрезање мишића, проблеми са зглобовима, проблеми са леђима и умор.
Натегнућа и уганућа леђа и озбиљнији проблеми који укључују интервертебралне дискове су уобичајени примери повреда на радном месту које се могу избећи. Они се често јављају због изненадног посебног преоптерећења, али могу такође одражавати напрезање прекомерних сила од стране тела током много година: проблеми се могу појавити изненада или може требати време да се развију. Пример проблема који се временом развија је „прст кројачице”. Недавни опис описује руке жене која је, након 28 година рада у фабрици одеће, као и шивења у слободно време, развила очврснулу задебљану кожу и неспособност да савија прсте (Пооле 1993). (Конкретно, патила је од флексијног деформитета десног кажипрста, истакнутих Хеберденових чворова на кажипрсту и палцу десне руке и израженог жуљевости на десном средњем прсту услед сталног трења од маказа.) Рендгенски снимак. филмови на њеним рукама су показали тешке дегенеративне промене у крајњим зглобовима њеног десног кажипрста и средњег прста, са губитком зглобног простора, артикуларном склерозом (отврдњавање ткива), остеофити (коштане израслине на зглобу) и коштане цисте.
Инспекција на радном месту показала је да су ови проблеми настали због поновљене хиперекстензије (савијања) крајњег спољашњег зглоба прста. Механичко преоптерећење и ограничење протока крви (видљиво као избељивање прста) би било максимално преко ових зглобова. Ови проблеми су се развили као одговор на поновљени напор мишића на месту које није мишић.
Биомеханика помаже да се предложе начини дизајнирања задатака да се избегну ове врсте повреда или да се побољшају лоше осмишљени задаци. Лекови за ове конкретне проблеме су редизајнирање маказа и измена задатака шивања како би се уклонила потреба за извршеним радњама.
Два важна принципа биомеханике су:
- Мишићи долазе у паровима. Мишићи се могу само контраховати, тако да за сваки зглоб мора постојати један мишић (или мишићна група) да га помера у једном правцу и одговарајући мишић (или мишићна група) да га помера у супротном смеру. Слика 1 илуструје тачку за зглоб лакта.
- Мишићи се најефикасније контрахују када је пар мишића у опуштеној равнотежи. Мишић делује најефикасније када се савија у средини зглоба. Ово је тако из два разлога: прво, ако мишић покуша да се контрахује када се скрати, он ће повући издужени супротни мишић. Пошто је потоњи истегнут, примениће еластичну противсилу коју контрахујући мишић мора да савлада. Слика 2 показује начин на који мишићна сила варира са дужином мишића.
Слика 1. Скелетни мишићи се јављају у паровима да би покренули или преокренули покрет
Слика 2. Напетост мишића варира са дужином мишића
Друго, ако мишић покуша да се контрахује у другом опсегу осим у средњем опсегу покрета зглоба, он ће функционисати у механичком недостатку. Слика 3 илуструје промену механичке предности за лакат у три различита положаја.
Слика 3. Оптималне позиције за кретање зглоба
Важан критеријум за дизајн рада произилази из ових принципа: Рад треба да буде распоређен тако да се одвија са супротним мишићима сваког зглоба у опуштеној равнотежи. За већину зглобова, то значи да би зглоб требало да буде отприлике у средини кретања.
Ово правило такође значи да ће напетост мишића бити минимална док се задатак обавља. Један пример кршења правила је синдром прекомерне употребе (РСИ, или повреда од понављајућег напрезања) која утиче на мишиће врха подлактице код оператера на тастатури који уобичајено раде са савијеним зглобом. Често се ова навика намеће оператеру дизајном тастатуре и радне станице.
aplikacije
Следе неки примери који илуструју примену биомеханике.
Оптимални пречник дршке алата
Пречник дршке утиче на силу коју мишићи шаке могу применити на алат. Истраживања су показала да оптимални пречник дршке зависи од употребе на коју се алат користи. За вршење потиска дуж линије дршке, најбољи пречник је онај који омогућава прстима и палцу да преузму хват који се благо преклапа. Ово је око 40 мм. Да би се извршио обртни момент, оптималан је пречник од око 50-65 мм. (Нажалост, за обе сврхе већина ручки је мања од ових вредности.)
Употреба клешта
Као посебан случај дршке, могућност примене силе помоћу клешта зависи од одвајања дршке, као што је приказано на слици 4.
Слика 4. Снага хватања чељусти клешта коју врше корисници мушког и женског пола као функција раздвајања дршке
Седећи положај
Електромиографија је техника која се може користити за мерење напетости мишића. У студији о напетости у ерецтор спинае мишића (леђа) седећих субјеката, утврђено је да наслон (са нагнутим наслоном) смањује напетост у овим мишићима. Ефекат се може објаснити јер наслон преузима већи део тежине горњег дела тела.
Рендгенске студије испитаника у различитим положајима показале су да положај опуштене равнотеже мишића који отварају и затварају зглоб кука одговара углу кука од око 135º. Ово је близу положаја (128º) који овај зглоб природно усваја у бестежинским условима (у свемиру). У седећем положају, са углом од 90º у куку, мишићи колена који прелазе преко зглобова колена и кука теже да повуку сакрум (део кичменог стуба који се повезује са карлицом) у вертикални положај. Ефекат је уклањање природне лордозе (закривљености) лумбалне кичме; столице треба да имају одговарајуће наслоне за леђа како би се исправио овај напор.
Одвртање
Зашто су шрафови уметнути у смеру казаљке на сату? Пракса је вероватно настала из несвесног препознавања да су мишићи који ротирају десну руку у смеру казаљке на сату (већина људи су дешњаци) већи (и самим тим моћнији) од мишића који је ротирају супротно од казаљке на сату.
Имајте на уму да ће леворуки људи бити у неповољном положају када ручно убацују шрафове. Око 9% популације су леворуки и стога ће у неким ситуацијама бити потребни специјални алати: маказе и отварачи за конзерве су два таква примера.
Студија људи који користе шрафцигере у задатку монтаже открила је суптилнију везу између одређеног покрета и одређеног здравственог проблема. Утврђено је да што је већи угао лакта (што је рука равнија), то је више људи имало упалу на лакту. Разлог за овај ефекат је тај што мишић који ротира подлактицу (бицепс) такође повлачи главу радијуса (кост доње руке) на капитулум (заобљена глава) хумеруса (кост надлактице). Повећана сила код већег угла лакта изазвала је већу силу трења у лакту, са последичним загревањем зглоба, што је довело до упале. Под већим углом, мишић је такође морао да вуче са већом силом да би извршио акцију завртња, тако да је примењена већа сила него што би била потребна са лактом под углом од око 90º. Решење је било да се задатак помери ближе оператерима како би се смањио угао лакта на око 90º.
Горе наведени случајеви показују да је потребно правилно разумевање анатомије за примену биомеханике на радном месту. Дизајнери задатака ће можда морати да консултују стручњаке за функционалну анатомију како би предвидели врсте проблема о којима се расправља. (Тхе Поцкет Ергономист (Бровн и Митцхелл 1986) на основу електромиографског истраживања, предлаже многе начине смањења физичке нелагодности на послу.)
Ручно руковање материјалом
Термин ручно управљање обухвата подизање, спуштање, гурање, повлачење, ношење, померање, држање и везивање и обухвата велики део активности радног века.
Биомеханика има очигледну директну важност за рад ручног руковања, пошто мишићи морају да се крећу да би извршили задатке. Поставља се питање: колико физичког рада се може разумно очекивати од људи? Одговор зависи од околности; постоје заиста три питања која треба поставити. Сваки од њих има одговор који се заснива на научно истраженим критеријумима:
- Колико се може носити без оштећења тела (у облику, на пример, напрезања мишића, повреде диска или проблема са зглобовима)? Ово се зове биомеханички критеријум.
- Колико се може издржати без преоптерећења плућа (отежано дисање до тачке дахтања)? Ово се зове физиолошки критеријум.
- Колико се људи осећају способним за удобно руковање? Ово се зове психофизички критеријум.
Постоји потреба за ова три различита критеријума јер постоје три широко различите реакције које се могу јавити на подизање задатака: ако посао траје цео дан, брига ће бити како ће особа осећа о задатку — психофизичком критеријуму; ако је сила коју треба применити велика, забринутост би била да су мишићи и зглобови није преоптерећен до тачке оштећења — биомеханички критеријум; и ако је стопа рада је превелика, онда може премашити физиолошки критеријум или аеробни капацитет особе.
Многи фактори одређују обим оптерећења на тело приликом ручног руковања. Сви они сугеришу могућности за контролу.
Положај и покрети
Ако задатак захтева од особе да се уврне или посегне напред са теретом, ризик од повреде је већи. Радна станица се често може редизајнирати како би се спречиле ове радње. Више повреда леђа се дешава када подизање почиње на нивоу тла у поређењу са нивоом средине бутина, што сугерише једноставне мере контроле. (Ово се односи и на високо подизање.)
Учитавање.
Сам терет може утицати на руковање због своје тежине и своје локације. Други фактори, као што су његов облик, стабилност, величина и клизавост, могу утицати на лакоћу руковања.
Организација и окружење.
Начин на који је рад организован, како физички тако и временски (временски), такође утиче на руковање. Боље је да се терет истовара камиона у испоруци распореди на неколико људи на сат времена него да тражите од једног радника да проведе цео дан на задатку. Окружење утиче на руковање—лоше осветљење, претрпани или неравни подови и лоше одржавање могу довести до тога да се особа спотакне.
Лични фактори.
Личне вештине руковања, старост особе и одећа која се носи такође могу утицати на захтеве руковања. Образовање за обуку и дизање је потребно како да пружи неопходне информације, тако и да омогући време за развој физичких вештина руковања. Млађи људи су више изложени ризику; с друге стране, старији људи имају мању снагу и мањи физиолошки капацитет. Уска одећа може повећати снагу мишића потребну у задатку док се људи напрежу на уску тканину; класични примери су униформа медицинске сестре и уски комбинезони када људи раде изнад главе.
Препоручена ограничења тежине
Горе поменуте тачке указују на то да је немогуће навести тежину која ће бити „безбедна“ у свим околностима. (Ограничења тежине имају тенденцију да варирају од земље до земље на произвољан начин. Индијским докерима је, на пример, некада било „дозвољено“ да подигну 110 кг, док су њихови колеге у бившој Народној Демократској Републици Немачкој били „ограничени“ на 32 кг .) Ограничења тежине су такође имала тенденцију да буду превелика. 55 кг предложених у многим земљама сада се сматра превеликим на основу недавних научних доказа. Национални институт за безбедност и здравље на раду (НИОСХ) у Сједињеним Државама усвојио је 23 кг као границу оптерећења 1991. године (Ватерс ет ал. 1993).
Сваки задатак дизања треба проценити на основу његових заслуга. Користан приступ одређивању границе тежине за задатак дизања је једначина коју је развио НИОСХ:
РВЛ = ЛЦ к ХМ к ВМ к ДМ к АМ к ЦМ к FM
Где
РВЛ = препоручено ограничење тежине за предметни задатак
HM = хоризонтално растојање од центра гравитације терета до средине између чланака (минимално 15 цм, максимално 80 цм)
VM = вертикално растојање између центра гравитације терета и пода на почетку подизања (максимално 175 цм)
DM = вертикални ход лифта (минимално 25 цм, максимално 200 цм)
AM = фактор асиметрије – угао од којег задатак одступа право испред тела
CM = множилац спојнице – способност доброг држања предмета који треба да се подигне, што се налази у референтној табели
FM = множитељи фреквенције – фреквенција подизања.
Све варијабле дужине у једначини су изражене у јединицама центиметра. Треба напоменути да је 23 кг максимална тежина коју НИОСХ препоручује за дизање. Ово је смањено са 40 кг након што је посматрање многих људи који обављају многе задатке дизања открило да је просечна удаљеност од тела почетка дизања 25 цм, а не 15 цм претпостављених у ранијој верзији једначине (НИОСХ 1981. ).
Индекс подизања.
Упоређујући тежину коју треба подићи у задатку и РВЛ, индекс дизања (LI) може се добити према односу:
LI=(тежина којом се рукује)/РВЛ.
Стога је посебно драгоцена употреба НИОСХ једначине постављање задатака подизања по тежини, коришћењем индекса подизања за постављање приоритета за акцију. (Међутим, једначина има бројна ограничења која треба разумети за њену најефикаснију примену. Видети Ватерс ет ал. 1993).
Процена компресије кичме коју намеће задатак
Доступан је компјутерски софтвер за процену компресије кичме коју производи ручни задатак. 2Д и 3Д програми за предвиђање статичке снаге са Универзитета у Мичигену („Бацксофт“) процењују компресију кичме. Уноси потребни за програм су:
- држање у коме се обавља руководна активност
- уложена сила
- смер напрезања силе
- број руку које врше силу
- проценат популације која се проучава.
2Д и 3Д програми се разликују по томе што 3Д софтвер омогућава прорачуне који се примењују на положаје у три димензије. Излаз програма даје податке о компресији кичме и наводи проценат одабране популације која би била у стању да уради одређени задатак без прекорачења предложених ограничења за шест зглобова: скочни зглоб, колено, кук, први лумбални диск-сацрум, раме и лакат. Овај метод такође има низ ограничења која треба у потпуности разумети да би се из програма извукла максимална вредност.
Иммунотокицологи
Функције имуног система су да заштити тело од инвазије инфективних агенаса и да обезбеди имунолошки надзор против туморских ћелија које настају. Има прву линију одбране која је неспецифична и која сама може да покрене ефекторске реакције и стечену специфичну грану, у којој лимфоцити и антитела носе специфичност препознавања и накнадне реактивности према антигену.
Имунотоксикологија је дефинисана као „дисциплина која се бави проучавањем догађаја који могу довести до нежељених ефеката као резултат интеракције ксенобиотика са имунолошким системом. Ови нежељени догађаји могу резултирати као последица (1) директног и/или индиректног ефекта ксенобиотика (и/или његовог производа биотрансформације) на имуни систем, или (2) имунолошки заснованог одговора домаћина на једињење и/или његов метаболит(и), или антигени домаћина модификовани једињењем или његовим метаболитима” (Берлин ет ал. 1987).
Када имуни систем делује као пасивна мета хемијских увреда, резултат може бити смањена отпорност на инфекцију и одређене облике неоплазије, или имунолошка дисрегулација/стимулација која може погоршати алергију или ауто-имунитет. У случају да имуни систем реагује на антигенску специфичност ксенобиотика или антигена домаћина модификованог једињењем, токсичност се може манифестовати као алергије или аутоимуне болести.
Развијени су животињски модели за испитивање супресије имунитета изазване хемикалијама, а један број ових метода је потврђен (Бурлесон, Мунсон и Деан 1995; ИПЦС 1996). За потребе тестирања, следи вишестепени приступ како би се направио адекватан избор од огромног броја доступних тестова. Генерално, циљ првог нивоа је да идентификује потенцијалне имунотоксичне супстанце. Ако се идентификује потенцијална имунотоксичност, врши се други ниво тестирања да би се потврдиле и даље карактерисале уочене промене. Истраживања трећег нивоа укључују посебне студије о механизму деловања једињења. Неколико ксенобиотика је идентификовано као имунотоксиканти који изазивају имуносупресију у таквим студијама на лабораторијским животињама.
База података о поремећајима имунолошке функције код људи услед хемикалија из животне средине је ограничена (Десцотес 1986; НРЦ Подкомитет за имунотоксикологију 1992). Употреба маркера имунотоксичности је добила мало пажње у клиничким и епидемиолошким студијама да би се истражио ефекат ових хемикалија на здравље људи. Такве студије нису рађене често, а њихово тумачење често не дозвољава да се донесу недвосмислени закључци, на пример због неконтролисане природе излагања. Стога, тренутно процена имунотоксичности код глодара, са накнадном екстраполацијом на човека, чини основу за доношење одлука о опасности и ризику.
Реакције преосетљивости, посебно алергијска астма и контактни дерматитис, су важни здравствени проблеми у индустријализованим земљама (Вос, Иоунес и Смитх 1995). Феномен контактне сензибилизације је прво истражен код заморца (Андерсен и Маибацх 1985). До недавно је ово била врста избора за предиктивно тестирање. Доступне су многе методе тестирања заморчића, а најчешће коришћени су тест максимизације заморчића и Буехлеров тест оклудираних закрпа. Тестови на заморцима и новији приступи развијени на мишевима, као што су тестови отицања уха и тест локалних лимфних чворова, пружају токсикологу алате за процену опасности од сензибилизације коже. Ситуација у погледу сензибилизације респираторног тракта је веома различита. Још увек не постоје добро потврђене или широко прихваћене методе за идентификацију хемијских респираторних алергена, иако је напредак у развоју животињских модела за испитивање хемијских респираторних алергија постигнут код заморца и миша.
Подаци о људима показују да хемијски агенси, посебно лекови, могу изазвати аутоимуне болести (Каммуллер, Блоксма и Сеинен 1989). Постоји велики број експерименталних животињских модела људских аутоимуних болести. Оне обухватају и спонтану патологију (на пример системски еритематозни лупус код новозеландских црних мишева) и аутоимуне феномене изазване експерименталном имунизацијом унакрсним реактивним аутоантигеном (на пример, артритис изазван Х37Ра адјувансом код пацова соја Левис). Ови модели се примењују у претклиничкој евалуацији имуносупресивних лекова. Врло мало студија бавило се потенцијалом ових модела за процену да ли ксенобиотик погоршава индуковану или урођену аутоимуност. Животињски модели који су погодни за истраживање способности хемикалија да изазову аутоимуне болести практично недостају. Један модел који се користи у ограниченој мери је тест поплитеалних лимфних чворова код мишева. Као и ситуација код људи, генетски фактори играју кључну улогу у развоју аутоимуне болести (АД) код лабораторијских животиња, што ће ограничити предиктивну вредност таквих тестова.
Имунски систем
Главна функција имуног система је одбрана од бактерија, вируса, паразита, гљивица и неопластичних ћелија. Ово се постиже деловањем различитих типова ћелија и њихових растворљивих медијатора у фино подешеном концерту. Одбрана домаћина може се грубо поделити на неспецифичну или урођену резистенцију и специфичан или стечени имунитет посредован лимфоцитима (Роитт, Бростофф и Мале 1989).
Компоненте имуног система присутне су у целом телу (Јонес ет ал. 1990). Компартмент за лимфоците се налази у лимфоидним органима (слика 1). Коштана срж и тимус су класификовани као примарни или централни лимфоидни органи; секундарни или периферни лимфоидни органи обухватају лимфне чворове, слезину и лимфоидно ткиво дуж секреторних површина као што су гастроинтестинални и респираторни тракт, такозвано лимфоидно ткиво повезано са слузницом (МАЛТ). Отприлике половина телесних лимфоцита налази се у било ком тренутку у МАЛТ-у. Поред тога, кожа је важан орган за индукцију имунолошких одговора на антигене присутне на кожи. Важне у овом процесу су епидермалне Лангерхансове ћелије које имају функцију презентовања антигена.
Слика 1. Примарни и секундарни лимфоидни органи и ткива
Фагоцитне ћелије лозе моноцита/макрофага, назване мононуклеарни фагоцитни систем (МПС), јављају се у лимфоидним органима и такође на екстранодалним местима; екстранодални фагоцити укључују Купферове ћелије у јетри, алвеоларне макрофаге у плућима, мезангијалне макрофаге у бубрезима и глијалне ћелије у мозгу. Полиморфонуклеарни леукоцити (ПМН) су углавном присутни у крви и коштаној сржи, али се акумулирају на местима упале.
Неспецифична одбрана
Прву линију одбране од микроорганизама врши физичка и хемијска баријера, као што су кожа, респираторни и пробавни тракт. Ова баријера је потпомогнута неспецифичним заштитним механизмима укључујући фагоцитне ћелије, као што су макрофаги и полиморфонуклеарни леукоцити, који су у стању да убијају патогене, и природне ћелије убице, које могу да лизирају ћелије тумора и ћелије инфициране вирусом. Систем комплемента и одређени микробни инхибитори (нпр. лизозим) такође учествују у неспецифичном одговору.
Специфични имунитет
Након почетног контакта домаћина са патогеном, индукују се специфични имуни одговори. Обележје ове друге линије одбране је специфично препознавање детерминанти, такозваних антигена или епитопа, патогена помоћу рецептора на површини ћелије Б- и Т-лимфоцита. Након интеракције са специфичним антигеном, ћелија која носи рецептор се стимулише да се подвргне пролиферацији и диференцијацији, производећи клон ћелија потомака који су специфични за изазивајући антиген. Специфични имуни одговори помажу неспецифичној одбрани представљеној патогенима стимулишући ефикасност неспецифичних одговора. Основна карактеристика специфичног имунитета је да се памћење развија. Секундарни контакт са истим антигеном изазива бржи и снажнији, али добро регулисан одговор.
Геном нема капацитет да носи кодове низа антигенских рецептора који су довољни да препознају број антигена који се могу срести. Репертоар специфичности се развија процесом преуређивања гена. Ово је случајан процес, током којег се јављају различите специфичности. Ово укључује специфичности сопствених компоненти, које су непожељне. Процес селекције који се одвија у тимусу (Т ћелије) или коштаној сржи (Б ћелије) ради на брисању ових непожељних специфичности.
Нормална имунолошка ефекторска функција и хомеостатска регулација имуног одговора зависе од низа растворљивих производа, познатих као цитокини, које синтетишу и луче лимфоцити и други типови ћелија. Цитокини имају плеиотропне ефекте на имуне и инфламаторне одговоре. Сарадња између различитих ћелијских популација је неопходна за имуни одговор — регулацију одговора антитела, акумулацију имуних ћелија и молекула на местима упале, иницирање одговора акутне фазе, контролу цитотоксичне функције макрофага и многе друге процесе који су централни за отпорност домаћина. . На њих утичу и у многим случајевима зависе од цитокина који делују појединачно или заједно.
Препознају се два крака специфичног имунитета—хуморални имунитет и ћелијски посредован или ћелијски имунитет:
Хуморални имунитет. У хуморалном краку Б-лимфоцити се стимулишу након што рецептори на ћелијској површини препознају антиген. Антигенски рецептори на Б-лимфоцитима су имуноглобулини (Иг). Зреле Б ћелије (плазма ћелије) започињу производњу антиген-специфичних имуноглобулина који делују као антитела у серуму или дуж мукозних површина. Постоји пет главних класа имуноглобулина: (1) ИгМ, пентамерни Иг са оптималним капацитетом аглутинације, који се прво производи након антигенске стимулације; (2) ИгГ, главни Иг у циркулацији, који може да прође кроз плаценту; (3) ИгА, секреторни Иг за заштиту мукозних површина; (4) ИгЕ, Иг фиксирање за мастоците или базофилне гранулоците укључене у непосредне реакције преосетљивости и (5) ИгД, чија је главна функција рецептор на Б-лимфоцитима.
Ћелијски посредован имунитет. Ћелијски крак специфичног имуног система је посредован Т-лимфоцитима. Ове ћелије такође имају рецепторе за антиген на својим мембранама. Они препознају антиген ако су представљени ћелијама које представљају антиген у контексту антигена хистокомпатибилности. Дакле, ове ћелије имају ограничење поред специфичности антигена. Т ћелије функционишу као помоћне ћелије за различите (укључујући хуморалне) имуне одговоре, посредују у регрутовању инфламаторних ћелија и могу, као цитотоксичне Т ћелије, да убијају циљне ћелије након антиген-специфичног препознавања.
Механизми имунотоксичности
Имуносупресија
Ефективна резистенција домаћина зависи од функционалног интегритета имуног система, што заузврат захтева да компоненте ћелија и молекула који оркестрирају имуни одговор буду доступни у довољном броју иу оперативном облику. Урођене имунодефицијенције код људи често се карактеришу дефектима одређених линија матичних ћелија, што доводи до поремећене или одсутне производње имуних ћелија. По аналогији са урођеним и стеченим болестима хумане имунодефицијенције, хемијски изазвана имуносупресија може бити резултат једноставног смањења броја функционалних ћелија (ИПЦС 1996). Одсуство или смањен број лимфоцита може имати више или мање дубоке ефекте на имунолошки статус. Нека стања имунодефицијенције и тешка имуносупресија, који се могу јавити у трансплантацији или цитостатичкој терапији, повезани су посебно са повећаном инциденцом опортунистичких инфекција и одређених неопластичних болести. Инфекције могу бити бактеријске, вирусне, гљивичне или протозојске, а преовлађујући тип инфекције зависи од придружене имунодефицијенције. Може се очекивати да ће излагање имуносупресивним хемикалијама из животне средине довести до суптилнијих облика имуносупресије, што може бити тешко открити. Ово може довести, на пример, до повећане инциденције инфекција као што су грип или обична прехлада.
С обзиром на сложеност имуног система, са широким спектром ћелија, медијатора и функција које чине компликовану и интерактивну мрежу, имунотоксична једињења имају бројне могућности да испоље дејство. Иако природа почетних лезија изазваних многим имунотоксичним хемикалијама још увек није разјашњена, све је више доступних информација, углавном изведених из студија на лабораторијским животињама, у вези са имунобиолошким променама које доводе до депресије имунолошке функције (Деан ет ал. 1994.) . Токсични ефекти могу се јавити на следећим критичним функцијама (и дати су неки примери имунотоксичних једињења која утичу на ове функције):
- развој и ширење различитих популација матичних ћелија (бензен испољава имунотоксичне ефекте на нивоу матичних ћелија, изазивајући лимфоцитопенију)
- пролиферација различитих лимфоидних и мијелоидних ћелија, као и потпорних ткива у којима ове ћелије сазревају и функционишу (имунотоксична органокалајна једињења сузбијају пролиферативну активност лимфоцита у тимусној кортексу путем директне цитотоксичности; тимотоксично дејство 2,3,7,8-тетрахлоро -дибензо-п-диоксин (ТЦДД) и сродна једињења су вероватно због поремећене функције епителних ћелија тимуса, а не због директне токсичности за тимоците)
- преузимање, процесирање и презентација антигена од стране макрофага и других ћелија које представљају антиген (једна од мета 7,12-диметилбенз(а)антрацена (ДМБА) и олова је презентација антигена од стране макрофага; мета ултраљубичастог зрачења је антиген- представљање Лангерхансове ћелије)
- регулаторна функција Т-помоћних и Т-супресорских ћелија (функција Т-помоћних ћелија је оштећена органотинима, алдикарбом, полихлорисаним бифенилима (ПЦБ), ТЦДД и ДМБА; функција Т-супресорских ћелија је смањена третманом ниским дозама циклофосфамида)
- производња различитих цитокина или интерлеукина (бензо(а)пирен (БП) потискује производњу интерлеукина-1; ултраљубичасто зрачење мења производњу цитокина од стране кератиноцита)
- синтеза различитих класа имуноглобулина ИгМ и ИгГ је потиснута након третмана ПЦБ и трибутилкалај оксидом (ТБТ), и повећана након излагања хексахлоробензену (ХЦБ).
- регулација и активација комплемента (под утицајем ТЦДД)
- цитотоксична функција Т ћелија (3-метилхолантрен (3-МЦ), ДМБА и ТЦДД потискују цитотоксичну активност Т ћелија)
- функција природних ћелија убица (НК) (плућна НК активност је потиснута озоном; НК активност слезине је оштећена никлом)
- хемотаксија макрофага и полиморфонуклеарних леукоцита и цитотоксичне функције (озон и азот-диоксид нарушавају фагоцитну активност алвеоларних макрофага).
Алергија
Алергија могу се дефинисати као штетни здравствени ефекти који су резултат индукције и изазивања специфичних имуних одговора. Када се реакције преосетљивости јављају без укључивања имуног система термин псеудо-алергија се користи. У контексту имунотоксикологије, алергија је резултат специфичног имунолошког одговора на хемикалије и лекове који су од интереса. Способност хемикалије да сензибилизира појединце је генерално повезана са њеном способношћу да се ковалентно везује за телесне протеине. Алергијске реакције могу имати различите облике и оне се разликују у односу на основне имунолошке механизме и брзину реакције. Препознате су четири главне врсте алергијских реакција: Реакције преосетљивости типа И, које изазивају ИгЕ антитело и код којих се симптоми манифестују у року од неколико минута након излагања сензибилизоване особе. Реакције преосетљивости типа ИИ су резултат оштећења или уништења ћелија домаћина антителом. У овом случају симптоми постају очигледни у року од неколико сати. Реакције преосетљивости типа ИИИ или Артусове реакције су такође посредоване антителима, али против растворљивог антигена, и резултат су локалног или системског деловања имуних комплекса. На реакције типа ИВ, или преосетљивост одложеног типа, утичу Т-лимфоцити и обично се симптоми развијају 24 до 48 сати након излагања сензибилизоване особе.
Две врсте хемијских алергија од највећег значаја за здравље на раду су осетљивост на контакт или алергија коже и алергија респираторног тракта.
Контактна преосетљивост. Велики број хемикалија може изазвати сензибилизацију коже. Након локалног излагања осетљиве особе хемијском алергену, одговор Т-лимфоцита се индукује у дренирајућим лимфним чворовима. У кожи алерген директно или индиректно ступа у интеракцију са епидермалним Лангерхансовим ћелијама, које транспортују хемикалију до лимфних чворова и представљају је у имуногеном облику Т-лимфоцитима који реагују. Т-лимфоцити активирани алергеном пролиферирају, што доводи до клоналне експанзије. Појединац је сада сензибилизиран и реаговаће на друго дермално излагање истој хемикалији агресивнијим имунолошким одговором, што резултира алергијским контактним дерматитисом. Кожна инфламаторна реакција која карактерише алергијски контактни дерматитис је секундарна у односу на препознавање алергена у кожи од стране специфичних Т-лимфоцита. Ови лимфоцити се активирају, ослобађају цитокине и изазивају локалну акумулацију других мононуклеарних леукоцита. Симптоми се развијају око 24 до 48 сати након излагања сензибилизоване особе, па стога алергијски контактни дерматитис представља облик преосетљивости одложеног типа. Уобичајени узроци алергијског контактног дерматитиса укључују органске хемикалије (као што је 2,4-динитрохлоробензен), метале (као што су никл и хром) и биљне производе (као што је урушиол из отровног бршљана).
Респираторна преосетљивост. Респираторна преосетљивост се обично сматра реакцијом преосетљивости типа И. Међутим, реакције у касној фази и хроничнији симптоми повезани са астмом могу укључити ћелијски посредоване (тип ИВ) имуне процесе. На акутне симптоме повезане са респираторном алергијом утиче ИгЕ антитело, чија производња се провоцира након излагања осетљиве особе индукујућем хемијском алергену. ИгЕ антитело се дистрибуира системски и везује се, преко мембранских рецептора, за мастоците које се налазе у васкуларизованим ткивима, укључујући респираторни тракт. Након удисања исте хемикалије долази до реакције респираторне преосетљивости. Алерген се повезује са протеином и везује се за ИгЕ антитела везана за мастоците и унакрсно повезује. Ово заузврат изазива дегранулацију мастоцита и ослобађање инфламаторних медијатора као што су хистамин и леукотриени. Такви медијатори изазивају бронхоконстрикцију и вазодилатацију, што резултира симптомима респираторне алергије; астма и/или ринитис. Хемикалије за које се зна да изазивају респираторну преосетљивост код људи укључују анхидриде киселине (као што је тримелитни анхидрид), неке диизоцијанате (као што је толуен диизоцијанат), соли платине и неке реактивне боје. Такође, познато је да хронична изложеност берилијуму изазива преосетљивост плућа.
Аутоимунитет
Аутоимунитет може се дефинисати као стимулација специфичних имуних одговора усмерених против ендогених „самосталних” антигена. Индукована аутоимуност може бити резултат или промена у равнотежи регулаторних Т-лимфоцита или због повезаности ксенобиотика са компонентама нормалног ткива тако да их чини имуногеним („измењено ја“). Лекови и хемикалије за које се зна да случајно изазивају или погоршавају ефекте попут оних код аутоимуне болести (АД) код осетљивих појединаца су једињења мале молекулске тежине (молекулске тежине 100 до 500) за која се генерално сматра да сама по себи нису имуногена. Механизам АД услед излагања хемикалијама углавном је непознат. Болест се може произвести директно помоћу циркулишућих антитела, индиректно кроз формирање имунских комплекса, или као последица ћелијски посредованог имунитета, али се вероватно јавља комбинацијом механизама. Патогенеза је најпознатија код имунолошких хемолитичких поремећаја изазваних лековима:
- Лек се може везати за мембрану црвених ћелија и ступити у интеракцију са антителом специфичним за лек.
- Лек може да промени мембрану црвених ћелија тако да имуни систем сматра ћелију страном.
- Лек и његово специфично антитело формирају имуне комплексе који се везују за мембрану црвених ћелија и изазивају повреде.
- Сензибилизација црвених ћелија настаје услед производње аутоантитела црвених ћелија.
Утврђено је да разне хемикалије и лекови, посебно ове последње, изазивају аутоимуне реакције (Камуллер, Блоксма и Сеинен 1989). Професионална изложеност хемикалијама може случајно довести до синдрома сличних АД. Излагање мономерном винил хлориду, трихлоретилену, перхлоретилену, епоксидним смолама и силицијум прашини може изазвати синдроме сличне склеродерми. Синдром сличан системском еритематозусу (СЛЕ) описан је након излагања хидразину. Излагање толуен диизоцијанату је повезано са индукцијом тромбоцитопеничне пурпуре. Тешки метали као што је жива су укључени у неке случајеве имунокомплексног гломерулонефритиса.
Процена људског ризика
Процена имуног статуса човека се врши углавном коришћењем периферне крви за анализу хуморалних супстанци као што су имуноглобулини и комплемент, и леукоцита крви за састав подскупа и функционалност субпопулација. Ове методе су обично исте као оне које се користе за испитивање хуморалног и ћелијски посредованог имунитета, као и неспецифичне резистенције пацијената са сумњом на болест урођене имунодефицијенције. За епидемиолошке студије (нпр. професионално изложене популације) параметре треба изабрати на основу њихове предиктивне вредности у људским популацијама, валидираних животињских модела и основне биологије маркера (видети табелу 1). Стратегија скрининга на имунотоксичне ефекте након (случајног) излагања загађивачима животне средине или другим токсичним супстанцама у великој мери зависи од околности, као што су тип имунодефицијенције који се очекује, време између излагања и процене имунолошког статуса, степен изложености и број изложених особа. Процес процене имунотоксичног ризика од одређеног ксенобиотика код људи је изузетно тежак и често немогућ, углавном због присуства различитих збуњујућих фактора ендогеног или егзогеног порекла који утичу на одговор појединаца на токсично оштећење. Ово посебно важи за студије које истражују улогу излагања хемикалијама у аутоимуним болестима, где генетски фактори играју кључну улогу.
Табела 1. Класификација тестова за имунолошке маркере
| Тест категорија | karakteristike | Специфични тестови |
| Основно-опште Требало би да буде укључено у опште панеле |
Индикатори општег здравља и стања органа | Азот уреје у крви, глукоза у крви итд. |
| Басиц-имуне Требало би да буде укључено у опште панеле |
Општи показатељи имунолошког статуса Релативно ниска цена Методе испитивања су стандардизоване међу лабораторијама Резултати изван референтних опсега се клинички могу интерпретирати |
Комплетна крвна слика Нивои ИгГ, ИгА, ИгМ у серуму Фенотипови површинских маркера за главне подгрупе лимфоцита |
| Фокусирано/рефлексно Треба укључити када то указују клинички налази, сумњива изложеност или претходни резултати тестова |
Индикатори специфичних имунолошких функција/догађаја Цена варира Методе испитивања су стандардизоване међу лабораторијама Резултати изван референтних опсега се клинички могу интерпретирати |
Генотип хистокомпатибилности Антитела на инфективне агенсе Укупни серумски ИгЕ Алерген-специфични ИгЕ Аутоантитела Кожни тестови за преосетљивост Оксидативна експлозија гранулоцита Хистопатологија (биопсија ткива) |
| истраживање Треба укључити само контролне популације и пажљив дизајн студије |
Индикатори општих или специфичних имунолошких функција/догађаја Цена варира; често скупо Методе анализе обично нису стандардизоване међу лабораторијама Резултати изван референтних опсега често се не могу клинички интерпретирати |
Ин витро тестови стимулације Маркери површине за активацију ћелија Концентрације цитокина у серуму Тестови клоналности (антитела, ћелијска, генетска) Тестови цитотоксичности |
Пошто су адекватни подаци о људима ретко доступни, процена ризика за имуносупресију изазвану хемикалијама код људи се у већини случајева заснива на студијама на животињама. Идентификација потенцијалних имунотоксичних ксенобиотика се спроводи првенствено у контролисаним студијама на глодарима. Студије изложености ин виво представљају, у том погледу, оптималан приступ за процену имунотоксичног потенцијала једињења. Ово је због мултифакторске и сложене природе имуног система и имунолошких одговора. Ин витро студије су све веће вредности у разјашњавању механизама имунотоксичности. Поред тога, истраживањем ефеката једињења коришћењем ћелија животињског и људског порекла, могу се добити подаци за поређење врста, који се могу користити у „паралелограмском“ приступу за побољшање процеса процене ризика. Ако су доступни подаци за три камена темељца паралелограма (ин виво животиње, ин витро животиње и људи), можда ће бити лакше предвидети исход на преосталом камену темељцу, односно ризик код људи.
Када се процена ризика за имуносупресију изазвану хемикалијама мора ослањати искључиво на податке из студија на животињама, може се следити приступ у екстраполацији на човека применом фактора несигурности на ниво без уочених штетних ефеката (НОАЕЛ). Овај ниво се може заснивати на параметрима одређеним у релевантним моделима, као што су тестови резистенције домаћина и ин виво процена реакција преосетљивости и производње антитела. У идеалном случају, релевантност овог приступа у процени ризика захтева потврду студија на људима. Такве студије треба да комбинују идентификацију и мерење токсичности, епидемиолошке податке и процену имунолошког статуса.
Да би се предвидела контактна преосетљивост, доступни су модели заморчића који се користе у процени ризика од 1970-их. Иако су осетљиви и поновљиви, ови тестови имају ограничења јер зависе од субјективне процене; ово се може превазићи новијим и квантитативнијим методама развијеним у мишу. Што се тиче хемијске индуковане преосетљивости изазване удисањем или гутањем алергена, тестове треба развити и проценити у смислу њихове предиктивне вредности код човека. Када је у питању постављање безбедних нивоа изложености потенцијалним алергенима на радном месту, мора се узети у обзир двофазна природа алергије: фаза сензибилизације и фаза изазивања. Концентрација потребна за изазивање алергијске реакције код претходно сензибилизоване особе је знатно нижа од концентрације неопходне да се изазове сензибилизација код имунолошки наивне, али осетљиве особе.
Како животињски модели за предвиђање аутоимуности изазване хемикалијама практично недостају, нагласак треба дати развоју таквих модела. За развој таквих модела, наше знање о хемијском индукованој аутоимуности код људи требало би да се унапреди, укључујући проучавање генетских маркера и маркера имуног система за идентификацију осетљивих појединаца. Људи који су изложени лековима који изазивају аутоимуност нуде такву прилику.
Опције у дизајну студија
Епидемиолога занимају односи између варијабли, углавном изложености и варијабли исхода. Типично, епидемиолози желе да утврде да ли је појава болести повезана са присуством одређеног агенса (изложености) у популацији. Начини на које се ови односи проучавају могу се значајно разликовати. Може се идентификовати све особе које су изложене том агенсу и пратити их како би се измерила учесталост болести, упоређујући такву инциденцу са појавом болести у одговарајућој неекспонираној популацији. Алтернативно, може се једноставно узорковати између изложених и неекспонираних, без њиховог потпуног набрајања. Или, као трећа алтернатива, може се идентификовати све особе које развију болест од интереса у дефинисаном временском периоду („случајеви“) и одговарајућу групу појединаца без болести (узорак изворне популације случајева) и утврдити да ли се обрасци изложености разликују између две групе. Праћење учесника у студији је једна од опција (у такозваним лонгитудиналним студијама): у овој ситуацији постоји временски размак између појаве излагања и почетка болести. Једна алтернативна опција је пресек популације, где се и изложеност и болест мере у истом временском тренутку.
У овом чланку, пажња је посвећена уобичајеним дизајнима студија—кохорта, случај-референца (контрола случаја) и попречни пресек. Да бисте поставили сцену за ову дискусију, узмите у обзир велику фабрику вискозног рајона у малом граду. Покренута је истрага о томе да ли изложеност угљен-дисулфиду повећава ризик од кардиоваскуларних болести. Истрага има неколико избора дизајна, неке више, а неке мање очигледне. Прва стратегија је да се идентификују сви радници који су били изложени угљен-дисулфиду и да се прате због кардиоваскуларног морталитета.
Кохортне студије
Кохортна студија обухвата учеснике истраживања који деле заједнички догађај, изложеност. Класична кохортна студија идентификује дефинисану групу изложених људи, а затим се свако прати и региструје њихово искуство морбидитета и/или морталитета. Поред заједничке квалитативне изложености, кохорту треба дефинисати и на другим критеријуми, као што су узраст, пол (мушки или женски или обоје), минимално трајање и интензитет изложености, слобода од других изложености и слично, како би се побољшала валидност и ефикасност студије. На улазу, сви чланови кохорте треба да буду слободни од болести која се проучава, у складу са емпиријским скупом критеријума који се користе за мерење болести.
Ако се, на пример, у кохортној студији о ефектима угљен-дисулфида на коронарни морбидитет, коронарна болест срца емпиријски мери као клинички инфаркт, они који су на почетку имали историју коронарног инфаркта морају бити искључени из кохорте. Насупрот томе, електрокардиографске абнормалности без анамнезе инфаркта могу се прихватити. Међутим, ако је појава нових електрокардиографских промена емпиријска мера исхода, чланови кохорте такође треба да имају нормалне електрокардиограме на почетној линији.
Морбидитет (у смислу инциденције) или морталитет изложене кохорте треба упоредити са референтном кохортом која би у идеалном случају требало да буде што сличнија изложеној кохорти у свим релевантним аспектима, осим у погледу изложености, како би се одредио релативни ризик од болест или смрт од изложености. Коришћење сличне, али неекспониране кохорте као пружаоца референтног искуства је пожељније у односу на уобичајену (не)праксу упоређивања морбидитета или морталитета изложене кохорте са националним подацима стандардизованим по годинама, јер општа популација не испуњава чак ни највише елементарни захтеви за валидност поређења. Стандардизовани однос морбидитета (или морталитета) (СМР), који је резултат таквог поређења, обично генерише потцењивање стварног односа ризика због пристрасности која делује у изложеној кохорти, што доводи до недостатка упоредивости између две популације. Ова пристрасност поређења је названа „Ефекат здравог радника“. Међутим, то заиста није прави „ефекат“, већ пристрасност због негативног збуњивања, које је заузврат проистекло из здравствено селективне флуктуације код запослене популације. (Људи са лошим здравственим стањем имају тенденцију да се иселе или никада не улазе у „изложене“ групе, а њихова крајња дестинација често је незапослени део опште популације.)
Зато што се „изложена“ кохорта дефинише као да има само одређену изложеност ефекте изазване том једном изложеношћу (или мешавина експозиција) могу се проучавати истовремено. С друге стране, дизајн кохорте дозвољава проучавање неколико болести у исто време. Такође се могу проучавати истовремено различите манифестације исте болести – на пример, ангина, ЕКГ промене, клинички инфаркт миокарда и коронарни морталитет. Иако је добро прилагођен за тестирање специфичних хипотеза (нпр. „изложеност угљен-дисулфиду изазива коронарну болест“), кохортна студија такође даје одговоре на општије питање: „Које болести су узроковане овом изложеношћу?“
На пример, у кохортној студији која истражује ризик од умирања од рака плућа за раднике ливнице, подаци о смртности се добијају из националног регистра узрока смрти. Иако је студија требало да утврди да ли ливачка прашина изазива рак плућа, извор података, уз исти напор, такође даје информације о свим другим узроцима смрти. Стога се истовремено могу проучавати и други могући здравствени ризици.
Време кохортне студије може бити ретроспективно (историјско) или проспективно (истовремено). У оба случаја структура дизајна је иста. Потпуни попис изложених људи се дешава у неком тренутку или временском периоду, а исход се мери за све појединце кроз дефинисану крајњу тачку у времену. Разлика између проспективног и ретроспективног је у времену трајања студије. Ако је ретроспективно, крајња тачка се већ догодила; ако је перспективно, мора се сачекати.
У ретроспективном дизајну, кохорта је дефинисана у неком тренутку у прошлости (на пример, они који су били изложени 1. јануара 1961. или они који су преузели изложени рад између 1961. и 1970.). Морбидитет и/или морталитет од сви чланови кохорте се затим прати до садашњости. Иако „сви“ значи да се морају пронаћи и они који су напустили посао, у пракси се ретко може постићи 100-постотна покривеност. Међутим, што је потпуније праћење, то је студија валиднија.
У проспективном дизајну, кохорта се дефинише у садашњости, или током неког будућег периода, а затим се морбидитет прати у будућности.
Када се раде кохортне студије, мора се оставити довољно времена за праћење како би крајње тачке забринутости имале довољно времена да се манифестују. Понекад, пошто историјски записи могу бити доступни само за кратак период у прошлост, ипак је пожељно искористити овај извор података јер то значи да би био потребан краћи период проспективног праћења пре него што би резултати студије могли бити на располагању. У овим ситуацијама, комбинација дизајна ретроспективних и проспективних кохортних студија може бити ефикасна. Општи изглед табела учесталости које представљају кохортне податке приказан је у табели 1.
Табела 1. Општи изглед табела учесталости које представљају кохортне податке
|
Компонента стопе болести |
Изложена кохорта |
Неекспонирана кохорта |
|
Случајеви болести или смрти |
c1 |
c0 |
|
Број људи у кохорти |
N1 |
N0 |
Уочени проценат оболелих у изложеној кохорти израчунава се на следећи начин:
![]()
и то референтне кохорте као:
![]()
Однос стопа је тада изражен као:

N0 N1 се обично изражавају у јединицама личност-време уместо као број људи у популације. Особа-година се рачунају за сваког појединца посебно. Различити људи често улазе у кохорту током одређеног временског периода, а не на исти датум. Стога њихово време праћења почиње на различите датуме. Слично, након њихове смрти, или након што се десио догађај од интереса, они више нису „у опасности“ и не би требало да наставе да доприносе имениоцу личних година.
Ако је РР већи од 1, морбидитет изложене кохорте је већи од оног у референтној кохорти, и обрнуто. РР је тачка процене и за њу треба израчунати интервал поверења (ЦИ). Што је студија већа, интервал поверења ће постати ужи. Ако РР = 1 није укључен у интервал поверења (нпр. ЦИ од 95% је 1.4 до 5.8), резултат се може сматрати „статистички значајним“ на изабраном нивоу вероватноће (у овом примеру, α = 0.05).
Ако се општа популација користи као референтна популација, c0 замењује се „очекиваном“ цифром, Е(ц1 ), изведено из старосно стандардизованих стопа морбидитета или морталитета те популације (тј. броја случајева који би се десили у кохорти да није дошло до изложености интересу). Ово даје стандардизовани однос морталитета (или морбидитета), СМР. Тако,
![]()
Такође за СМР треба израчунати интервал поверења. Боље је дати ову меру у публикацији него п-вредност, јер је тестирање статистичке значајности бесмислено ако је општа популација референтна категорија. Такво поређење подразумева значајну пристрасност ( ефекат здравог радника горе наведено), а тестирање статистичке значајности, првобитно развијено за експериментално истраживање, доводи у заблуду у присуству систематске грешке.
Претпоставимо да је питање да ли кварцна прашина изазива рак плућа. Обично се кварцна прашина јавља заједно са другим канцерогенима — као што су радонске кћери и издувни гасови дизела у рудницима, или полиароматични угљоводоници у ливницама. Каменоломи гранита не излажу каменоломце овим другим канцерогенима. Стога се проблем најбоље проучава међу каменоломцима запосленим у каменоломима гранита.
Претпоставимо онда да је свих 2,000 радника, који су били запослени у 20 каменолома између 1951. и 1960. године, уписани у кохорту и да се прати њихова учесталост рака (алтернативно само смртност) почевши од десет година након првог излагања (да би се омогућило време индукције) и који се завршава 1990. Ово је 20 до 30 година (у зависности од године уласка) или, рецимо, у просеку 25 година праћења морталитета (или морбидитета) од рака међу 1,000 радника каменолома који били су конкретно радници на граниту. Историја изложености сваког члана кохорте мора бити забележена. Мора се ући у траг онима који су напустили каменоломе и евидентирати њихову каснију историју излагања. У земљама у којима сви становници имају јединствене матичне бројеве, ово је једноставан поступак, који се углавном регулише националним законима о заштити података. Тамо где такав систем не постоји, праћење запослених у сврху праћења може бити изузетно тешко. Тамо где постоје одговарајући регистри смрти или болести, морталитет од свих узрока, свих карцинома и специфичних места рака може се добити из националног регистра узрока смрти. (За смртност од рака, национални регистар рака је бољи извор јер садржи тачније дијагнозе. Поред тога, могу се добити и подаци о инциденци (или морбидитету).) Стопе смртности (или стопе инциденције рака) се могу упоредити са „ очекивани бројеви“, израчунати из националних стопа користећи особе-године изложене кохорте као основу.
Претпоставимо да је у кохорти пронађено 70 смртоносних случајева рака плућа, док је очекивани број (број који би се десио да није било изложености) 35. Затим:
c1 = КСНУМКС, Е(ц1) = КСНУМКС
![]()
Дакле, СМР = 200, што указује на двоструко повећање ризика од умирања од рака плућа међу изложеним. Ако су доступни детаљни подаци о изложености, смртност од рака се може проучавати као функција различитих времена латенције (рецимо, 10, 15, 20 година), рада у различитим типовима каменолома (различите врсте гранита), различитих историјских периода, различите изложености интензитета и тако даље. Међутим, 70 случајева се не може поделити у превише категорија, јер број који спада у сваки од њих брзо постаје премали за статистичку анализу.
Обе врсте дизајна кохорте имају предности и недостатке. Ретроспективно истраживање може, по правилу, да мери само морталитет, јер подаци за блаже манифестације обично недостају. Регистри за рак су изузетак, а можда и неколико других, као што су регистри можданог удара и регистри отпуста из болнице, у којима су доступни и подаци о инциденци. Процена претходне изложености је увек проблем и подаци о изложености су обично прилично слаби у ретроспективним студијама. Ово може довести до ефекта маскирања. С друге стране, пошто су се случајеви већ десили, резултати студије постају доступни много раније; за, рецимо, две до три године.
Проспективна кохортна студија може се боље планирати како би била у складу са потребама истраживача, а подаци о изложености могу се прикупљати тачно и систематски. Може се измерити неколико различитих манифестација болести. Мерења и експозиције и исхода могу се поновити, а сва мерења могу бити стандардизована и њихова валидност се може проверити. Међутим, ако болест има дугу латенцију (као што је рак), мораће да прође много времена — чак 20 до 30 година — пре него што се могу добити резултати студије. Много тога се може догодити за ово време. На пример, флуктуација истраживача, побољшања техника за мерење изложености, ремоделирање или затварање биљака изабраних за проучавање и тако даље. Све ове околности угрожавају успех студије. Трошкови проспективне студије су такође обично већи од трошкова ретроспективне студије, али то је углавном због много већег броја мерења (поновљено праћење изложености, клинички прегледи и тако даље), а не због скупље регистрације смрти. Стога трошкови по јединици информације не морају нужно премашити оне ретроспективне студије. С обзиром на све ово, проспективне студије су погодније за болести са прилично кратком латенцијом, које захтевају кратко праћење, док су ретроспективне студије боље за болести са дугом латенцијом.
Студије контроле случајева (или референтне студије случаја).
Вратимо се на фабрику вискозне рајоне. Ретроспективна кохортна студија можда неће бити изводљива ако су спискови изложених радника изгубљени, док би проспективна кохортна студија дала добре резултате за веома дуго времена. Алтернатива би тада била поређење умрлих од коронарне болести срца у граду, у одређеном временском периоду, и узорка укупне популације у истој старосној групи.
Класични дизајн за контролу случаја (или, случај-референца) заснован је на узорковању из динамичке (отворене, коју карактерише промена чланства) популације. Ова популација може бити популација целе земље, округа или општине (као у нашем примеру), или може бити административно дефинисана популација из које се пацијенти примају у болницу. Дефинисана популација обезбеђује и случајеве и контроле (или референтне).
Техника је да се сакупе сви случајеви дотичне болести који постоје у а тачка у времену (превладавајући случајеви), или су се десили током дефинисаног период времена (случајеви инцидената). Случајеви се стога могу извући из регистара морбидитета или морталитета, или директно из болница или других извора који имају валидну дијагностику. Контроле су нацртане као а узорак из исте популације, било из реда не-случајева или из целе популације. Друга опција је да одабрати пацијенти са другом болешћу као контрола, али онда ти пацијенти морају бити репрезентативни за популацију из које су случајеви дошли. Може постојати једна или више контрола (тј. референти) за сваки случај. Приступ узорковања се разликује од кохортних студија, које испитују целокупну популацију. Подразумева се да су добици у смислу нижих трошкова дизајна контроле случајева значајни, али је важно да узорак буде представник целокупне популације из које су случајеви потекли (тј. „база студија“) – у супротном студија може бити пристрасна.
Када се идентификују случајеви и контроле, њихове историје изложености се прикупљају путем упитника, интервјуа или, у неким случајевима, из постојећих евиденција (нпр. евиденција платног списка из које се може закључити историјат рада). Подаци се могу добити или од самих учесника или, ако су преминули, од блиских рођака. Да би се обезбедило симетрично присећање, важно је да пропорција мртвих и живих случајева и референта буде једнака, јер блиски рођаци обично дају мање детаљну историју изложености од самих учесника. Информације о обрасцу изложености међу случајевима упоређују се са онима међу контролама, дајући процену Однос квота (ИЛИ), индиректна мера за ризик међу изложенима да задобију болест у односу на ону неекспонираних.
Будући да се дизајн контроле случаја ослања на информације о изложености добијене од пацијената са одређеном болешћу (тј. случајева) заједно са узорком људи који нису оболели (тј. контрола) из популације из које су случајеви потекли, веза са изложеношћу може се истражити само за једна болест. Насупрот томе, овај дизајн омогућава истовремено проучавање ефекта неколико различитих експозиција. Референтна студија случаја је веома погодна да се бави специфичним истраживачким питањима (нпр. „Да ли је коронарна болест срца узрокована излагањем угљен-дисулфиду?“), али такође може помоћи да се одговори на општије питање: „Која изложеност може изазвати ову болест ?”
Питање да ли излагање органским растварачима изазива примарни рак јетре поставља се (као пример) у Европи. Случајеви примарног рака јетре, релативно ретке болести у Европи, најбоље се прикупљају из националног регистра рака. Претпоставимо да сви случајеви рака који се јављају током три године чине серију случајева. Популациона база за студију је затим трогодишње праћење целокупне популације у дотичној европској земљи. Контроле су извучене као узорак особа без рака јетре из исте популације. Из практичних разлога (што значи да се исти извор може користити за узорковање контрола) пацијенти са другим типом рака, који није повезан са излагањем растварачу, могу се користити као контроле. Рак дебелог црева нема познату везу са излагањем растварачу; стога се овај тип рака може укључити међу контроле. (Коришћење контрола рака минимизира пристрасност присећања у смислу да је тачност историје коју дају случајеви и контроле у просеку симетрична. Међутим, ако би се касније открила нека тренутно непозната веза између рака дебелог црева и излагања растварачима, ова врста контроле би изазвала потцењивање правог ризика - а не претеривање.)
За сваки случај рака јетре извлаче се две контроле како би се постигла већа статистичка моћ. (Могло би се повући још више контрола, али расположива средства могу бити ограничавајући фактор. Да средства нису ограничена, можда би чак четири контроле биле оптималне. Осим четири, примењује се закон о смањењу приноса.) Након добијања одговарајуће дозволе од података. органима заштите, предметима и контролама, или њиховим блиским сродницима, обраћа се, обично путем упитника посланог поштом, тражећи детаљну историју занимања са посебним нагласком на хронолошки списак имена свих послодаваца, одељења за рад, радних задатака у различитим пословима и период запослења на сваком поједином задатку. Ови подаци се са извесним потешкоћама могу добити од рођака; међутим, рођаци обично не памте одређене хемикалије или трговачка имена. Упитник такође треба да садржи питања о могућим збуњујућим подацима, као што су употреба алкохола, изложеност намирницама које садрже афлатоксине и инфекција хепатитисом Б и Ц. Да би се добила довољно висока стопа одговора, два подсетника се шаљу нереспондентима у интервалима од три недеље. Ово обично резултира коначном стопом одговора већом од 70%. Професионални историјат затим прегледа индустријски хигијеничар, без знања о случају испитаника или контролном статусу, а изложеност се класификује на високу, средњу, ниску, никакву и непознату изложеност растварачима. Десет година излагања непосредно пре дијагнозе карцинома се занемарују, јер није биолошки уверљиво да карциногени иницијаторског типа могу бити узрок рака ако је време латенције тако кратко (иако би промотери, у ствари, могли). У овој фази такође је могуће разликовати различите врсте изложености растварачу. Пошто је дата комплетна историја запослења, могуће је истражити и друге изложености, иако почетна хипотеза студије није укључивала ове. Односи шансе се затим могу израчунати за излагање било ком растварачу, специфичним растварачима, смешама растварача, различитим категоријама интензитета излагања и за различите временске оквире у односу на дијагнозу рака. Препоручљиво је искључити из анализе оне са непознатом изложеношћу.
Случајеви и контроле се могу узорковати и анализирати као независне серије or подударне групе. Подударање значи да се контроле бирају за сваки случај на основу одређених карактеристика или атрибута, како би се формирали парови (или скупови, ако је више од једне контроле изабрано за сваки случај). Упаривање се обично врши на основу једног или више таквих фактора, као што су старост, витални статус, историја пушења, календарско време дијагнозе случаја и слично. У нашем примеру, случајеви и контроле се затим упарују на основу старости и виталног статуса. (Витални статус је важан, јер сами пацијенти обично дају тачнију историју изложености од блиских рођака, а симетрија је неопходна из разлога валидности.) Данас је препорука да се буде рестриктиван са подударањем, јер ова процедура може да уведе негативан ефекат (маскирање ефекта). ) збуњујуће.
Ако је једна контрола усклађена са једним случајем, дизајн се назива а дизајн упарених парова. Под условом да трошкови проучавања више контрола нису превисоки, више од једног референта по случају побољшава стабилност процене ОР, што чини студију ефикаснијом у величини.
Изглед резултата неупоредиве студије случај-контрола приказан је у табели 2.
Табела 2. Пример изгледа података о контроли случајева
|
Класификација изложености |
||
|
Изложен |
Неекспонирани |
|
|
slučajevi |
c1 |
c0 |
|
Не-случајеви |
n1 |
n0 |
Из ове табеле, шансе за изложеност међу случајевима, и шансе за изложеност међу популацијом (контроле), могу се израчунати и поделити да би се добио однос шансе за изложеност, ОР. За случајеве, шансе за изложеност су c1 / c0, а за контроле јесте n1 / n0. Процена ОР је тада:
![]()
Ако је изложено релативно више случајева него контрола, ОР је већи од 1 и обрнуто. Интервали поверења се морају израчунати и обезбедити за ОР, на исти начин као и за РР.
Као још један пример, центар здравља рада велике компаније опслужује 8,000 запослених изложених разним прашинама и другим хемијским агенсима. Занима нас веза између мешовитог излагања прашини и хроничног бронхитиса. Студија укључује праћење ове популације током једне године. Дијагностичке критеријуме за хронични бронхитис поставили смо као „јутарњи кашаљ и стварање слузи три месеца током две узастопне године“. Критеријуми за „позитивну“ изложеност прашини дефинисани су пре почетка студије. Сваки пацијент који посети Дом здравља и испуни ове критеријуме у периоду од годину дана је случај, а следећи пацијент који тражи лекарски савет због неплућних тегоба се дефинише као контрола. Претпоставимо да је 100 случајева и 100 контрола уписано током периода истраживања. Нека се 40 случајева и 15 контрола класификују као изложени прашини. Онда
c1 = КСНУМКС, c0 = КСНУМКС, n1 = КСНУМКС, и n0 = КСНУМКС.
Сходно томе,
![]()
У претходном примеру, није узета у обзир могућност збуњивања, што може довести до изобличења ОР због систематских разлика између случајева и контрола у варијабли као што је старост. Један од начина да се умањи ова пристрасност је усклађивање контрола са случајевима старости или другим сумњивим факторима. Ово резултира распоредом података приказаним у табели 3.
Табела 3. Изглед података контроле случаја ако је једна контрола упарена са сваким случајем
|
Референти |
||
|
slučajevi |
Експозиција (+) |
Изложеност (-) |
|
Експозиција (+) |
f+ + |
f+ - |
|
Изложеност (-) |
f- + |
f- - |
Анализа се фокусира на нескладне парове: то јест, „изложен случај, неекспонирана контрола“ (f+–); и „случај неекспониран, контрола изложена“ (f–+). Када су оба члана пара изложена или неекспонирана, пар се занемарује. ОР у дизајну студије са подударним паровима је дефинисан као
![]()
У студији о повезаности рака носа и изложености дрвној прашини, било је укупно 164 пара случај-контрола. У само једном пару откривени су и кућиште и контрола, а код 150 парова ни кућиште ни контрола нису били изложени. Ови парови се даље не разматрају. Случај, али не и контрола, био је изложен у 12 парова, а контрола, али не и случај, у једном пару. Стога,
![]()
и пошто јединица није укључена у овај интервал, резултат је статистички значајан—то јест, постоји статистички значајна повезаност између рака носа и изложености дрвној прашини.
Студије случај-контрола су ефикасније од кохортних студија када су болест је ретка; они заправо могу пружити једину опцију. Међутим, уобичајене болести се такође могу проучавати овом методом. Ако је излагање је ретко, кохорта заснована на изложености је пожељнији или једини изводљиви епидемиолошки дизајн. Наравно, кохортне студије се такође могу спровести на уобичајеним изложеностима. Избор између кохорте и дизајна контроле случаја када су и изложеност и болест уобичајени се обично одлучује узимајући у обзир ваљаност.
Пошто се студије контроле случајева ослањају на ретроспективне податке о изложености, обично засноване на сећању учесника, њихова слаба тачка је нетачност и грубост информација о изложености, што резултира маскирањем ефекта кроз недиференцијални (симетрична) погрешна класификација статуса изложености. Штавише, понекад опозив може бити асиметричан између случајева и контрола, случајеви за које се обично верује да памте „боље“ (тј. пристрасност опозива).
Селективно подсећање може изазвати пристрасност која повећава ефекат диференцијал (асиметрична) погрешна класификација статуса изложености. Предности студија случај-контрола леже у њиховој исплативости и њиховој способности да релативно брзо пруже решење проблема. Због стратегије узорковања, они омогућавају истраживање веома великих циљних популација (нпр. кроз националне регистре рака), чиме се повећава статистичка моћ студије. У земљама у којима закон о заштити података или недостатак добрих регистара становништва и морбидитета омета извођење кохортних студија, студије случаја-контроле засноване на болницама могу бити једини практичан начин за спровођење епидемиолошког истраживања.
Узорковање случаја-контроле унутар кохорте (угнежђени дизајн студија контроле случајева)
Кохортна студија такође може бити дизајнирана за узорковање уместо потпуног праћења. Овај дизајн је раније назван „угнежђеном“ студијом контроле случаја. Приступ узорковања унутар кохорте поставља различите захтеве у погледу подобности кохорте, јер се поређења сада врше унутар исте кохорте. Ово стога треба да укључује не само јако изложене раднике, већ и мање изложене, па чак и неекспониране раднике, како би се обезбедило контрасти експозиције унутар себе. Важно је схватити ову разлику у условима подобности приликом састављања кохорте. Ако се потпуна кохортна анализа прво изврши на кохорти чији су критеријуми подобности били на „великој“ изложености, а „угнежђена“ студија случај-контрола се уради касније на истој кохорти, студија постаје неосетљива. Ово уводи маскирање ефеката јер су контрасти експозиције недовољни „по дизајну“ због недостатка варијабилности у искуству експозиције међу члановима кохорте.
Међутим, под условом да кохорта има широк спектар искуства у изложености, приступ угнежђене контроле случајева је веома привлачан. Један окупља све случајеве који су настали у кохорти током периода праћења да би се формирао низ случајева, док само узорак од неслучајева се црта за контролну серију. Истраживачи затим, као у традиционалном дизајну контроле случаја, прикупљају детаљне информације о искуству изложености интервјуисањем случајева и контрола (или њихових блиских рођака), испитивањем спискова особља послодавца, конструисањем матрица изложености послу, или комбиновањем два или више ових приступа. Контроле се могу или ускладити са случајевима или се могу третирати као независна серија.
Приступ узорковања може бити јефтинији у поређењу са прикупљањем исцрпних информација о сваком члану кохорте. Посебно, пошто се проучава само узорак контрола, више ресурса се може посветити детаљној и тачној процени изложености за сваки случај и контролу. Међутим, исти проблеми статистичке моћи преовладавају као у класичним кохортним студијама. Да би се постигла адекватна статистичка моћ, кохорта увек мора да садржи „адекватан“ број изложених случајева у зависности од величине ризика који треба да се открије.
Дизајн студија попречног пресека
У научном смислу, дизајн пресека је пресек популације која се проучава, без икаквог разматрања времена. И изложеност и морбидитет (преваленција) се мере у истом временском тренутку.
Са етиолошке тачке гледишта, овај дизајн студије је слаб, делимично зато што се бави преваленцијом, а не инциденцијом. Преваленција је сложена мера, која зависи и од инциденције и од трајања болести. Ово такође ограничава употребу студија пресека на болести дугог трајања. Још озбиљнија је јака негативна пристрасност узрокована елиминацијом која зависи од здравља из групе изложене изложености оних људи који су осетљивији на ефекте изложености. Због тога се етиолошки проблеми најбоље решавају уздужним дизајном. Заиста, студије пресека не дозвољавају никакве закључке о томе да ли је изложеност претходила болести или обрнуто. Попречни пресек је етиолошки значајан само ако постоји прави временски однос између изложености и исхода, што значи да садашња изложеност мора имати тренутне ефекте. Међутим, изложеност се може мерити попречним пресеком тако да представља дужи прошли временски период (нпр. ниво олова у крви), док је мера исхода преваленција (нпр. брзине нервне проводљивости). Студија је тада мешавина лонгитудиналног и попречног пресека, а не пуки попречни пресек испитиване популације.
Попречна дескриптивна истраживања
Истраживања попречним пресецима су често корисна у практичне и административне, а не у научне сврхе. Епидемиолошки принципи се могу применити на активности систематског надзора у окружењу здравља на раду, као што су:
- посматрање морбидитета у вези са занимањем, радним подручјем или одређеним изложеностима
- редовне анкете радника изложених познатим професионалним опасностима
- преглед радника који долазе у контакт са новим опасностима по здравље
- програми биолошког мониторинга
- истраживања изложености да би се идентификовале и квантификовале опасности
- скрининг програма различитих радничких група
- процена удела радника којима је потребна превенција или редовна контрола (нпр. крвни притисак, коронарна болест срца).
Важно је одабрати репрезентативне, валидне и специфичне индикаторе морбидитета за све врсте истраживања. Анкета или скрининг програм може да користи само мали број тестова, за разлику од клиничке дијагностике, и стога је предиктивна вредност скрининг теста важна. Неосетљиве методе не успевају да открију болест од интереса, док високо осетљиве методе дају превише лажно позитивних резултата. Не исплати се вршити скрининг на ретке болести у радном окружењу. Све активности проналажења случајева (тј. скрининга) такође захтевају механизам за збрињавање људи који имају „позитивне“ налазе, како у погледу дијагностике тако иу погледу терапије. У супротном, само фрустрација ће резултирати потенцијалом за више штете него добра.
" ОДРИЦАЊЕ ОД ОДГОВОРНОСТИ: МОР не преузима одговорност за садржај представљен на овом веб порталу који је представљен на било ком другом језику осим енглеског, који је језик који се користи за почетну производњу и рецензију оригиналног садржаја. Одређене статистике нису ажуриране од продукција 4. издања Енциклопедије (1998).“