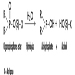Categorias crianças

27. Monitoramento Biológico (6)

27. Monitoramento Biológico
Editor do Capítulo: Robert Lauwerys
Conteúdo
Tabelas e Figuras
Princípios gerais
Vito Foà e Lorenzo Alessio
Garantia da Qualidade
D. Gompertz
Metais e Compostos Organometálicos
P. Hoet e Robert Lauwerys
Solventes orgânicos
Masayuki Ikeda
Químicos Genotóxicos
marja sorsa
Pesticidas
Marco Maroni e Adalberto Ferioli
Tabelas
Clique em um link abaixo para ver a tabela no contexto do artigo.
1. ACGIH, DFG e outros valores limite para metais
2. Exemplos de produtos químicos e monitoramento biológico
3. Monitoramento biológico para solventes orgânicos
4. Genotoxicidade de produtos químicos avaliados pela IARC
5. Biomarcadores e algumas amostras de células/tecidos e genotoxicidade
6. Carcinógenos humanos, exposição ocupacional e pontos finais citogenéticos
8. Exposição da produção e uso de pesticidas
9. Toxicidade aguda de OP em diferentes níveis de inibição de ACHE
10. Variações de DOR e PCHE e condições de saúde selecionadas
11. Atividades da colinesterase de pessoas saudáveis não expostas
12. Fosfatos de alquil urinários e pesticidas OP
13. Medições de alquil fosfatos urinários e OP
14. Metabólitos de carbamato urinário
15. Metabólitos de ditiocarbamato urinário
16. Índices propostos para monitoramento biológico de agrotóxicos
17. Valores-limite biológicos recomendados (a partir de 1996)
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

28. Epidemiologia e Estatística (12)

28. Epidemiologia e Estatística
Editores de Capítulo: Franco Merletti, Colin L. Soskolne e Paolo Vineis
Conteúdo
Tabelas e Figuras
Método Epidemiológico Aplicado à Saúde e Segurança Ocupacional
Franco Merletti, Colin L. Soskolne e Paolo Vineis
Avaliação de exposição
M. Gerald Ott
Medidas resumidas de exposição na vida profissional
Colin L. Soskolne
Medindo os efeitos das exposições
Shelia Hoar Zahm
Estudo de Caso: Medidas
Franco Merletti, Colin L. Soskolne e Paola Vineis
Opções no Projeto de Estudo
Sven Hernberg
Questões de validade no desenho do estudo
Annie J. Sasco
Impacto do erro de medição aleatória
Paolo Vineis e Colin L. Soskolne
Métodos estatísticos
Annibale Biggeri e Mário Braga
Avaliação de causalidade e ética na pesquisa epidemiológica
Paulo Vineis
Estudos de Caso Ilustrando Questões Metodológicas na Vigilância de Doenças Profissionais
Jung-Der Wang
Questionários em Pesquisa Epidemiológica
Steven D. Stellman e Colin L. Soskolne
Perspectiva Histórica do Amianto
Lawrence Garfinkel
Tabelas
Clique em um link abaixo para ver a tabela no contexto do artigo.
1. Cinco medidas resumidas selecionadas de exposição na vida profissional
2. Medidas de ocorrência da doença
3. Medidas de associação para um estudo de coorte
4. Medidas de associação para estudos de caso-controle
5. Layout geral da tabela de frequência para dados de coorte
6. Exemplo de layout de dados de controle de caso
7. Dados de controle de caso de layout - um controle por caso
8. Coorte hipotética de 1950 indivíduos para T2
9. Índices de tendência central e dispersão
10. Um experimento binomial e probabilidades
11. Possíveis resultados de um experimento binomial
12. Distribuição binomial, 15 sucessos/30 tentativas
13. Distribuição binomial, p = 0.25; 30 tentativas
14. Erro e potência tipo II; x = 12, n = 30, a = 0.05
15. Erro e potência tipo II; x = 12, n = 40, a = 0.05
16. 632 trabalhadores expostos ao amianto por 20 anos ou mais
17. O/E número de mortes entre 632 trabalhadores do amianto
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

29. Ergonomia (27)

29. Ergonomia
Editores de Capítulo: Wolfgang Laurig e Joachim Vedder
Conteúdo
Tabelas e Figuras
Visão geral
Wolfgang Laurig e Joachim Vedder
Objetivos, Princípios e Métodos
A natureza e os objetivos da ergonomia
William T.Singleton
Análise de Atividades, Tarefas e Sistemas de Trabalho
Véronique De Keyser
Ergonomia e Padronização
Friedhelm Nachreiner
Lista de verificação
Pranab Kumar Nag
Aspectos Físicos e Fisiológicos
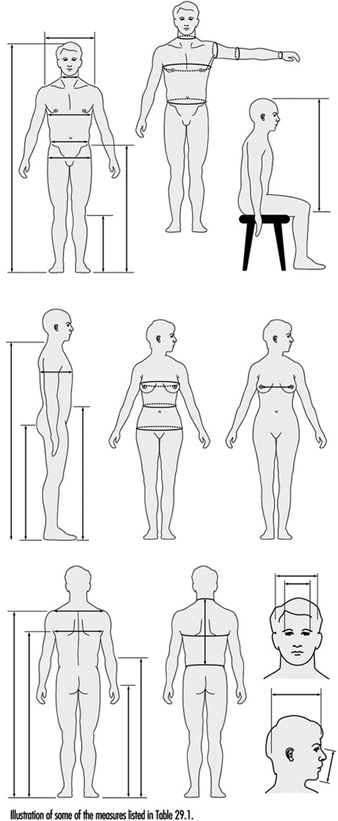
Antropometria
Melchiorre Masali
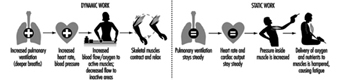
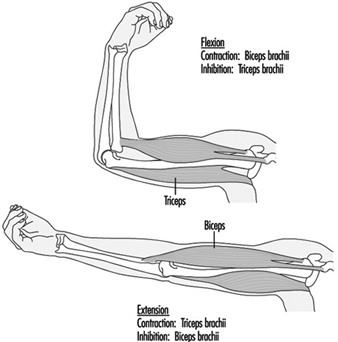
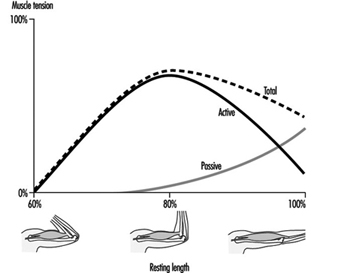
trabalho muscular
Juhani Smolander e Veikko Louhevaara
Posturas no Trabalho
Ilkka Kuorinka
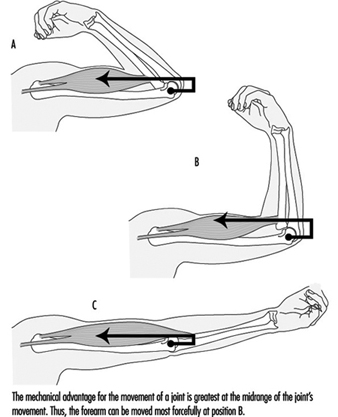
Biomecânica
Frank darby
Fadiga Geral
Étienne Grandjean
Fadiga e Recuperação
Rolf Helbig e Walter Rohmert
Aspectos psicológicos
carga de trabalho mental
Hacker Winfried
vigilância
Herbert Heuer
Fadiga mental
Pedro Richter
Aspectos Organizacionais do Trabalho
Organização do Trabalho
Eberhard Ulich e Gudela Grote
Privação de sono
Kazutaka Kogi
Projeto de sistemas de trabalho
workstations
Roland Kadefors
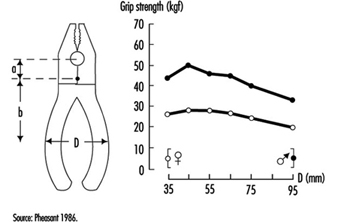
Ferramentas
TM Fraser
Controles, Indicadores e Painéis
Karl HE Kroemer
Processamento e Design de Informação
Andries F. Sanders
Projetando para todos
Projetando para grupos específicos
Piada H. Grady-van den Nieuwboer
Estudo de Caso: A Classificação Internacional de Limitação Funcional em Pessoas
Diferenças culturais
Houshang Shahnavaz
Trabalhadores Idosos
Antoine Laville e Serge Volkoff
Trabalhadores com Necessidades Especiais
Piada H. Grady-van den Nieuwboer
Diversidade e importância da ergonomia - dois exemplos
Projeto de sistema na fabricação de diamantes
Issacar Gilad
Desconsiderando os princípios de design ergonômico: Chernobyl
Vladimir M. Munipov
Tabelas
Clique em um link abaixo para ver a tabela no contexto do artigo.
1. Lista central antropométrica básica
2. Fadiga e recuperação dependentes dos níveis de atividade
3. Regras de efeitos de combinação de dois fatores de tensão na deformação
4. Diferenciando entre várias consequências negativas da tensão mental
5. Princípios orientados ao trabalho para a estruturação da produção
6. Participação no contexto organizacional
7. Participação do usuário no processo de tecnologia
8. Jornada de trabalho irregular e privação de sono
9. Aspectos do sono de avanço, âncora e retardo
10. Movimentos de controle e efeitos esperados
11. Relações controle-efeito de controles manuais comuns
12. Regras para arranjo de controles
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

30. Higiene Ocupacional (6)

30. Higiene Ocupacional
Editor de Capítulo: Robert F. Herrick
Conteúdo
Tabelas e Figuras
Objetivos, Definições e Informações Gerais
Berenice I. Ferrari Goelzer
Reconhecimento de perigos
Linnea Lillienberg
Avaliação do Ambiente de Trabalho
Lori A. Todd
Higiene Ocupacional: Controle de Exposições por Intervenção
James Stewart
A base biológica para avaliação de exposição
Dick Heederik
limites de exposição ocupacional
Dennis J. Paustenbach
Tabelas
1. Perigos de produtos químicos; agentes biológicos e físicos
2. Limites de exposição ocupacional (OELs) - vários países
figuras

31. Proteção Pessoal (7)

31. Proteção Pessoal
Editor de Capítulo: Robert F. Herrick
Conteúdo
Tabelas e Figuras
Visão geral e filosofia de proteção pessoal
Robert F. Herrick
Protetores oculares e faciais
Kikuzi Kimura
Proteção para Pés e Pernas
Toyohiko Miura
Proteção de cabeça
Isabelle Balty e Alain Mayer
Proteção auditiva
John R. Franks e Elliott H. Berger
Roupa de proteção
S. Zack Mansdorf
Proteção respiratória
Thomas J Nelson
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Requisitos de transmissão (ISO 4850-1979)
2. Escalas de proteção - soldagem a gás e soldagem por brasagem
3. Escalas de proteção - corte de oxigênio
4. Escalas de proteção - corte a arco de plasma
5. Escalas de proteção - soldagem a arco elétrico ou goivagem
6. Escalas de proteção - soldagem a arco plasma direta
7. Capacete de segurança: Norma ISO 3873-1977
8. Classificação de redução de ruído de um protetor auditivo
9. Calculando a redução de ruído ponderada A
10. Exemplos de categorias de perigo dérmico
11. Requisitos de desempenho físico, químico e biológico
12. Perigos materiais associados a atividades específicas
13. Fatores de proteção atribuídos de ANSI Z88 2 (1992)
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

32. Sistemas de Registro e Vigilância (9)

32. Sistemas de Registro e Vigilância
Editor de Capítulo: Steven D. Stellman
Conteúdo
Tabelas e Figuras
Sistemas de Vigilância e Notificação de Doenças Ocupacionais
Steven B. Markowitz
Vigilância de Riscos Ocupacionais
David H. Wegman e Steven D. Stellman
Vigilância em países em desenvolvimento
David Koh e Kee-Seng Chia
Desenvolvimento e Aplicação de um Sistema de Classificação de Lesões e Doenças Ocupacionais
Elyce Biddle
Análise de risco de lesões e doenças não fatais no local de trabalho
John W. Ruser
Estudo de Caso: Proteção ao Trabalhador e Estatísticas de Acidentes e Doenças Profissionais - HVBG, Alemanha
Martin Butz e Burkhard Hoffmann
Estudo de caso: Wismut - uma exposição de urânio revisitada
Heinz Otten e Horst Schulz
Estratégias e Técnicas de Medição para Avaliação da Exposição Ocupacional em Epidemiologia
Frank Bochmann e Helmut Blome
Estudo de caso: pesquisas de saúde ocupacional na China
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Angiossarcoma do fígado - registro mundial
2. Doença ocupacional, EUA, 1986 versus 1992
3. Mortes nos EUA por pneumoconiose e mesotelioma pleural
4. Exemplo de lista de doenças ocupacionais de notificação obrigatória
5. Estrutura do código de relatórios de doenças e lesões, EUA
6. Lesões e doenças ocupacionais não fatais, EUA 1993
7. Risco de lesões e doenças ocupacionais
8. Risco relativo para condições de movimento repetitivo
9. Acidentes de trabalho, Alemanha, 1981-93
10. Retificadores em acidentes de trabalho em metal, Alemanha, 1984-93
11. Doença ocupacional, Alemanha, 1980-93
12. Doenças infecciosas, Alemanha, 1980-93
13. Exposição à radiação nas minas de Wismut
14. Doenças ocupacionais nas minas de urânio de Wismut 1952-90
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

33. Toxicologia (21)

33. Toxicologia
Editora do Capítulo: Ellen K. Silbergeld
Conteúdo
Tabelas e Figuras
Introdução
Ellen K. Silbergeld, Editora do Capítulo
Princípios Gerais de Toxicologia
Definições e Conceitos
Bo Holmberg, Johan Hogberg e Gunnar Johanson
Toxicocinética
Dušan Djuríc
Órgão alvo e efeitos críticos
Marek Jakubowski
Efeitos da idade, sexo e outros fatores
Spomenka Telišman
Determinantes Genéticos da Resposta Tóxica
Daniel W. Nebert e Ross A. McKinnon
Mecanismos de Toxicidade
Introdução e Conceitos
Philip G. Watanabe
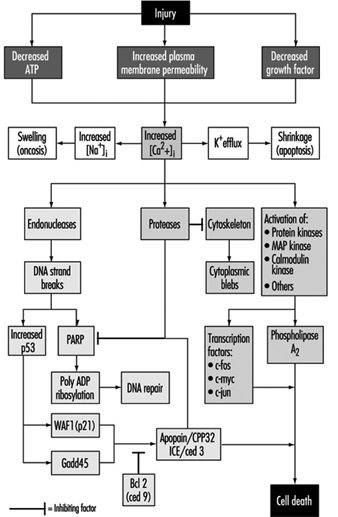
Lesão celular e morte celular
Benjamin F. Trump e Irene K. Berezsky
Toxicologia Genética
R. Rita Misra e Michael P. Waalkes
Imunotoxicologia
Joseph G. Vos e Henk van Loveren
Toxicologia de órgãos-alvo
Ellen K. Silbergeld
Métodos de Teste Toxicológico
Biomarcadores
Philippe Grandjean
Avaliação de Toxicidade Genética
David M. DeMarini e James Huff
Teste de Toxicidade In Vitro
Joanne Zurlo
Relacionamentos de atividade de estrutura
Ellen K. Silbergeld
Toxicologia Regulatória
Regulação de Toxicologia em Saúde e Segurança
Ellen K. Silbergeld
Princípios de Identificação de Perigos - A Abordagem Japonesa
Masayuki Ikeda
A Abordagem dos Estados Unidos para Avaliação de Risco de Tóxicos Reprodutivos e Agentes Neurotóxicos
Ellen K. Silbergeld
Abordagens para identificação de perigos - IARC
Harri Vainio e Julian Wilbourn
Apêndice - Avaliações gerais de carcinogenicidade para humanos: IARC Monographs Volumes 1-69 (836)
Avaliação de risco cancerígeno: outras abordagens
Cees A. van der Heijden
Tabelas
Clique em um link abaixo para ver a tabela no contexto do artigo.
- Exemplos de órgãos críticos e efeitos críticos
- Efeitos básicos de possíveis interações múltiplas de metais
- Adutos de hemoglobina em trabalhadores expostos a anilina e acetanilida
- Distúrbios hereditários, propensos ao câncer e defeitos no reparo do DNA
- Exemplos de produtos químicos que exibem genotoxicidade em células humanas
- Classificação de testes para marcadores imunológicos
- Exemplos de biomarcadores de exposição
- Prós e contras de métodos para identificar riscos de câncer humano
- Comparação de sistemas in vitro para estudos de hepatotoxicidade
- Comparação de SAR e dados de teste: análises OCDE/NTP
- Regulamentação de substâncias químicas por leis, Japão
- Itens de teste sob a Lei de Controle de Substâncias Químicas, Japão
- Substâncias químicas e a Lei de Controle de Substâncias Químicas
- Principais incidentes de neurotoxicidade selecionados
- Exemplos de testes especializados para medir a neurotoxicidade
- Endpoints em toxicologia reprodutiva
- Comparação de procedimentos de extrapolação de baixa dose
- Modelos frequentemente citados na caracterização do risco cancerígeno
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.
Pesticidas
Introdução
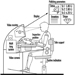
A exposição humana aos agrotóxicos tem características diferentes conforme ocorre durante a produção industrial ou uso (tabela 1). A formulação de produtos comerciais (por meio da mistura de princípios ativos com outros coformulantes) apresenta algumas características de exposição em comum com o uso de agrotóxicos na agricultura. De fato, uma vez que a formulação é normalmente realizada por pequenas indústrias que fabricam muitos produtos diferentes em operações sucessivas, os trabalhadores são expostos a cada um dos vários pesticidas por um curto período de tempo. Na saúde pública e na agricultura, o uso de uma variedade de compostos é geralmente a regra, embora em algumas aplicações específicas (por exemplo, desfolha do algodão ou programas de controle da malária) um único produto possa ser usado.
Tabela 1. Comparação das características de exposição durante a produção e uso de agrotóxicos
|
Exposição na produção |
Exposição no uso |
|
|
Duração da exposição |
Contínuo e prolongado |
Variável e intermitente |
|
Grau de exposição |
Razoavelmente constante |
Extremamente variável |
|
Tipo de exposição |
Para um ou poucos compostos |
A numerosos compostos em sequência ou concomitantemente |
|
Absorção cutânea |
Fácil de controlar |
Variável de acordo com os procedimentos de trabalho |
|
Monitoramento de ambiente |
Útil |
Raramente informativo |
|
Monitorização Biológica |
Complementar ao monitoramento ambiental |
Muito útil quando disponível |
Fonte: OMS 1982a, modificado.
A medição de indicadores biológicos de exposição é particularmente útil para usuários de pesticidas onde as técnicas convencionais de avaliação de exposição através do monitoramento do ar ambiente são pouco aplicáveis. A maioria dos pesticidas são substâncias lipossolúveis que penetram na pele. A ocorrência de absorção percutânea (pele) torna o uso de indicadores biológicos muito importante na avaliação do nível de exposição nessas circunstâncias.
Inseticidas Organofosforados
Indicadores biológicos de efeito:
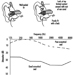
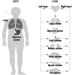
As colinesterases são as enzimas alvo responsáveis pela toxicidade dos organofosforados (OP) para espécies de insetos e mamíferos. Existem dois tipos principais de colinesterases no organismo humano: acetilcolinesterase (ACHE) e colinesterase plasmática (PCHE). OP causa efeitos tóxicos em humanos através da inibição da acetilcolinesterase sináptica no sistema nervoso. A acetilcolinesterase também está presente nos glóbulos vermelhos, onde sua função é desconhecida. A colinesterase plasmática é um termo genérico que abrange um grupo não homogêneo de enzimas presentes nas células gliais, plasma, fígado e alguns outros órgãos. PCHE é inibido por OPs, mas sua inibição não produz desarranjos funcionais conhecidos.
A inibição da atividade de ACHE e PCHE no sangue está altamente correlacionada com a intensidade e a duração da exposição ao OP. Blood ACHE, sendo o mesmo alvo molecular responsável pela toxicidade aguda de OP no sistema nervoso, é um indicador mais específico do que PCHE. No entanto, a sensibilidade do sangue ACHE e PCHE à inibição de OP varia entre os compostos OP individuais: na mesma concentração sanguínea, alguns inibem mais ACHE e outros mais PCHE.
Existe uma correlação razoável entre a atividade de ACHE no sangue e os sinais clínicos de toxicidade aguda (tabela 2). A correlação tende a ser melhor à medida que a taxa de inibição é mais rápida. Quando a inibição ocorre lentamente, como nas exposições crônicas de baixo nível, a correlação com a doença pode ser baixa ou totalmente inexistente. Deve-se notar que a inibição de ACHE no sangue não é preditiva para efeitos crônicos ou tardios.
Tabela 2. Gravidade e prognóstico da toxicidade aguda de OP em diferentes níveis de inibição da ACE
|
DOR inibição (%) |
Nível de envenenamento |
Sintomas clínicos |
Prognóstico |
|
50-60 |
Suave |
Fraqueza, dor de cabeça, tontura, náusea, salivação, lacrimejamento, miose, espasmo brônquico moderado |
Convalescença em 1-3 dias |
|
60-90 |
Moderado |
Fraqueza abrupta, distúrbios visuais, salivação excessiva, sudação, vómitos, diarreia, bradicardia, hipertonia, tremores das mãos e da cabeça, marcha perturbada, miose, dor no peito, cianose das membranas mucosas |
Convalescença em 1-2 semanas |
|
90-100 |
Grave |
Tremor abrupto, convulsões generalizadas, distúrbios psíquicos, cianose intensa, edema pulmonar, coma |
Morte por insuficiência respiratória ou cardíaca |
Variações nas atividades da DOR e da PCHE foram observadas em pessoas saudáveis e em condições fisiopatológicas específicas (tabela 3). Assim, a sensibilidade desses testes no monitoramento da exposição ao OP pode ser aumentada adotando-se valores individuais de pré-exposição como referência. As atividades da colinesterase após a exposição são então comparadas com os valores basais individuais. Deve-se usar os valores de referência da atividade da colinesterase populacional apenas quando os níveis de colinesterase pré-exposição não são conhecidos (tabela 4).
Tabela 3. Variações das atividades de ACHE e PCHE em pessoas saudáveis e em condições fisiopatológicas selecionadas
|
Condição |
atividade ACHE |
atividade PCHE |
|
Pessoas saudáveis |
||
|
variação interindividual1 |
10-18% |
15-25% |
|
variação intraindividual1 |
3-7% |
6% |
|
Diferenças sexuais |
Não |
10-15% maior no sexo masculino |
|
Idade |
Reduzido até 6 meses |
|
|
Body Mass |
Correlação positiva |
|
|
colesterol sérico |
Correlação positiva |
|
|
Variação sazonal |
Não |
Não |
|
variação circadiana |
Não |
Não |
|
Menstruação |
Diminuição |
|
|
Gravidez |
Diminuição |
|
|
Condições patológicas |
||
|
Atividade reduzida |
Leucemia, neoplasia |
Doença hepática; uremia; Câncer; insuficiência cardíaca; Reações alérgicas |
|
Atividade aumentada |
Policitemia; talassemia; outras discrasias sanguíneas congênitas |
Hipertireoidismo; outras condições de alta taxa metabólica |
1 Fonte: Augustinsson 1955 e Gage 1967.
Tabela 4. Atividades de colinesterase de pessoas saudáveis sem exposição a OP medidas com métodos selecionados
|
Método |
Sexo |
DOR* |
PCCHE* |
|
Michel1 (DpH/h) |
masculina feminina |
0.77 0.08 ± 0.75 0.08 ± |
0.95 0.19 ± 0.82 0.19 ± |
|
Titular1 (mmol/min ml) |
masculino feminino |
13.2 0.31 ± |
4.90 0.02 ± |
|
Ellman's modificado2 (UI/ml) |
masculina feminina |
4.01 0.65 ± 3.45 0.61 ± |
3.03 0.66 ± 3.03 0.68 ± |
* resultado médio, ± desvio padrão.
Fonte: 1 Leis 1991. 2 Alcini et ai. 1988.
O sangue deve preferencialmente ser amostrado dentro de duas horas após a exposição. A punção venosa é preferível à extração de sangue capilar de um dedo ou lóbulo da orelha porque o ponto de amostragem pode ser contaminado com pesticida residente na pele de indivíduos expostos. Três amostras sequenciais são recomendadas para estabelecer uma linha de base normal para cada trabalhador antes da exposição (OMS 1982b).
Vários métodos analíticos estão disponíveis para a determinação de ACHE e PCHE no sangue. Segundo a OMS, o método espectrofotométrico de Ellman (Ellman et al. 1961) deve servir como método de referência.
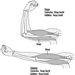
Indicadores biológicos de exposição.
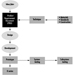
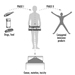
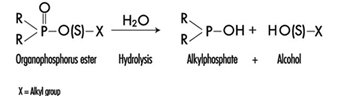
A determinação na urina de metabólitos derivados da porção alquil fosfato da molécula de OP ou dos resíduos gerados pela hidrólise da ligação P-X (figura 1) tem sido utilizada para monitorar a exposição ao OP.
Figura 1. Hidrólise de inseticidas OP
Metabolitos de fosfato de alquil.
Os metabólitos de fosfato de alquil detectáveis na urina e o principal composto original do qual eles podem se originar estão listados na tabela 5. Os fosfatos de alquil urinários são indicadores sensíveis de exposição a compostos de OP: a excreção desses metabólitos na urina geralmente é detectável em um nível de exposição em qual a inibição da colinesterase plasmática ou eritrocitária não pode ser detectada. A excreção urinária de fosfatos de alquila foi medida para diferentes condições de exposição e para vários compostos OP (tabela 6). A existência de uma relação entre as doses externas de OP e as concentrações urinárias de alquil fosfato foi estabelecida em alguns estudos. Em alguns estudos, também foi demonstrada uma relação significativa entre a atividade da colinesterase e os níveis de alquil fosfato na urina.
Tabela 5. Fosfatos de alquil detectáveis na urina como metabólitos de pesticidas OP
|
Metabólito |
Abreviatura |
Principais compostos parentais |
|
Monometilfosfato |
MMP |
malatião, paratião |
|
Dimetilfosfato |
DMP |
Diclorvos, triclorfom, mevinfos, malaoxon, dimetoato, fenclorfos |
|
Dietilfosfato |
DEP |
Paraoxon, demeton-oxon, diazinon-oxon, diclorfentiona |
|
Dimetiltiofosfato |
DMTP |
Fenitrotiona, fenclorfos, malatião, dimetoato |
|
Dietiltiofosfato |
DETP |
Diazinon, demeton, paration, fenclorfos |
|
Dimetilditiofosfato |
DMDTP |
Malatião, dimetoato, azinfos-metil |
|
Dietilditiofosfato |
DEDTP |
Dissulfoton, forato |
|
ácido fenilfosfórico |
Leptofos, EPN |
Tabela 6. Exemplos de níveis de alquil fosfatos urinários medidos em várias condições de exposição a OP
|
Compound |
Condição de exposição |
Via de exposição |
Concentrações de metabólitos1 (mg/L) |
|
Paratião2 |
Envenenamento não fatal |
Oral |
DEP = 0.5 DETP = 3.9 |
|
Dissulfoton2 |
Formuladores |
Dérmico/inalação |
DEP = 0.01-4.40 DETP = 0.01-1.57 DEDTP = <0.01-05 |
|
Forado2 |
Formuladores |
Dérmico/inalação |
DEP = 0.02-5.14 DETP = 0.08-4.08 DEDTP = <0.01-0.43 |
|
Malatião3 |
Pulverizadores |
Dérmica |
DMDTP = <0.01 |
|
Fenitrotion3 |
Pulverizadores |
Dérmica |
DMP = 0.01-0.42 DMTP = 0.02-0.49 |
|
Monocrotophos4 |
Pulverizadores |
Dérmico/inalação |
DMP = <0.04-6.3/24 h |
1 Para abreviações, consulte a tabela 27.12 [BMO12TE].
2 Dillon e Ho 1987.
3 Richer 1993.
4 van Sittert e Dumas 1990.
Os fosfatos de alquil são geralmente excretados na urina em um curto período de tempo. Amostras coletadas logo após o final da jornada de trabalho são adequadas para determinação de metabólitos.
A medição de fosfatos de alquila na urina requer um método analítico bastante sofisticado, baseado na derivatização dos compostos e na detecção por cromatografia gás-líquido (Shafik et al. 1973a; Reid e Watts 1981).
Resíduos hidrolíticos.
p-Nitrofenol (PNP) é o metabólito fenólico do paration, metilparation e etil paration, EPN. A medição de PNP na urina (Cranmer 1970) tem sido amplamente utilizada e provou ser bem-sucedida na avaliação da exposição ao paration. A PNP urinária correlaciona-se bem com a dose absorvida de paration. Com níveis urinários de PNP de até 2 mg/l, a absorção do paration não causa sintomas e observa-se pouca ou nenhuma redução das atividades da colinesterase. A excreção de PNP ocorre rapidamente e os níveis urinários de PNP tornam-se insignificantes 48 horas após a exposição. Assim, amostras de urina devem ser coletadas logo após a exposição.
Carbamatos
Indicadores biológicos de efeito.
Os pesticidas carbamato incluem inseticidas, fungicidas e herbicidas. A toxicidade dos carbamatos inseticidas é devida à inibição da ACHE sináptica, enquanto outros mecanismos de toxicidade estão envolvidos para carbamatos herbicidas e fungicidas. Assim, apenas a exposição aos inseticidas carbamato pode ser monitorada através do ensaio da atividade da colinesterase em hemácias (ACHE) ou plasma (PCHE). ACHE é geralmente mais sensível aos inibidores de carbamato do que a PCHE. Os sintomas colinérgicos foram geralmente observados em trabalhadores expostos ao carbamato com uma atividade de ACHE no sangue inferior a 70% do nível basal individual (OMS 1982a).
A inibição das colinesterases pelos carbamatos é rapidamente reversível. Portanto, resultados falsos negativos podem ser obtidos se decorrer muito tempo entre a exposição e a amostragem biológica ou entre a amostragem e a análise. Para evitar tais problemas, recomenda-se que as amostras de sangue sejam coletadas e analisadas em até quatro horas após a exposição. Deve-se dar preferência aos métodos analíticos que permitem a determinação da atividade da colinesterase imediatamente após a coleta de sangue, conforme discutido para os organofosforados.
Indicadores biológicos de exposição.
A medição da excreção urinária de metabólitos de carbamato como um método para monitorar a exposição humana até agora foi aplicada apenas a alguns compostos e em estudos limitados. A Tabela 7 resume os dados relevantes. Uma vez que os carbamatos são prontamente excretados na urina, amostras coletadas logo após o término da exposição são adequadas para determinação de metabólitos. Métodos analíticos para as medições de metabólitos de carbamato na urina foram relatados por Dawson et al. (1964); DeBernardinis e Wargin (1982) e Verberk et al. (1990).
Tabela 7. Níveis de metabólitos urinários de carbamato medidos em estudos de campo
|
Compound |
índice biológico |
Condição de exposição |
Concentrações ambientais |
Resultados |
Referências |
|
Carbaryl |
a-naftol a-naftol a-naftol |
formuladores misturador/aplicadores população não exposta |
0.23–0.31 mg/m3 |
x=18.5 mg/l1 , máx. taxa de excreção = 80 mg/dia x=8.9 mg/l, faixa = 0.2–65 mg/l faixa = 1.5–4 mg/l |
OMS 1982a |
|
Pirimicarbe |
metabólitos I2 e V3 |
aplicadores |
faixa = 1–100 mg/l |
Verberk et ai. 1990 |
1 Intoxicações sistêmicas foram ocasionalmente relatadas.
2 2-dimetilamino-4-hidroxi-5,6-dimetilpirimidina.
3 2-metilamino-4-hidroxi-5,6-dimetilpirimidina.
x = desvio padrão.
Ditiocarbamatos
Indicadores biológicos de exposição.
Os ditiocarbamatos (DTC) são fungicidas amplamente utilizados, agrupados quimicamente em três classes: tiurames, dimetilditiocarbamatos e etileno-bis-ditiocarbamatos.
Dissulfeto de carbono (CS2) e seu principal metabólito ácido 2-tiotiazolidina-4-carboxílico (TTCA) são metabólitos comuns a quase todos os CDT. Um aumento significativo nas concentrações urinárias desses compostos foi observado para diferentes condições de exposição e para vários pesticidas DTC. A etileno tioureia (ETU) é um importante metabólito urinário dos etileno-bis-ditiocarbamatos. Também pode estar presente como uma impureza em formulações de mercado. Uma vez que o ETU foi determinado como um teratógeno e um carcinógeno em ratos e em outras espécies e tem sido associado à toxicidade da tireoide, ele tem sido amplamente aplicado para monitorar a exposição ao etileno-bis-ditiocarbamato. A ETU não é específica de um composto, pois pode ser derivada de maneb, mancozeb ou zineb.
A medição dos metais presentes no DTC foi proposta como uma abordagem alternativa no monitoramento da exposição ao DTC. Aumento da excreção urinária de manganês foi observado em trabalhadores expostos ao mancozebe (tabela 8).
Tabela 8. Níveis de metabólitos urinários de ditiocarbamato medidos em estudos de campo
|
Compound |
índice biológico |
Condição de exposição |
Concentrações ambientais* ± desvio padrão |
Resultados ± desvio padrão |
Referências |
|
Ziram |
Dissulfeto de carbono (CS2) TTCA1 |
formuladores formuladores |
1.03 ± 0.62 mg/m3 |
3.80 ± 3.70 mg/l 0.45 ± 0.37 mg/l |
Maroni et ai. 1992 |
|
Manebe/Mancozebe |
ETU2 |
aplicadores |
faixa = < 0.2–11.8 mg/l |
Kurttio et al. 1990 |
|
|
Mancozeb |
Manganês |
aplicadores |
57.2 mg/m3 |
pré-exposição: 0.32 ± 0.23 mg/g de creatinina; pós-exposição: 0.53 ± 0.34 mg/g de creatinina |
Canosa et al. 1993 |
* Resultado médio segundo Maroni et al. 1992.
1 TTCA = ácido 2-tiotiazolidina-4-carbonílico.
2 ETU = etileno tioureia.
CS2, TTCA e manganês são comumente encontrados na urina de indivíduos não expostos. Assim, recomenda-se a medição dos níveis urinários desses compostos antes da exposição. As amostras de urina devem ser coletadas na manhã seguinte ao término da exposição. Métodos analíticos para as medições de CS2, TTCA e ETU foram relatados por Maroni et al. (1992).
Piretroides Sintéticos
Indicadores biológicos de exposição.
Os piretróides sintéticos são inseticidas semelhantes às piretrinas naturais. Metabólitos urinários adequados para aplicação no monitoramento biológico da exposição foram identificados por meio de estudos com voluntários humanos. O metabólito ácido 3-(2,2'-dicloro-vinil)-2,2'-dimetil-ciclopropano ácido carboxílico (Cl2CA) é excretado tanto por indivíduos administrados oralmente com permetrina e cipermetrina quanto pelo bromo-análogo (Br2CA) por indivíduos tratados com deltametrina. Nos voluntários tratados com cipermetrina, também foi identificado um metabólito fenoxi, o ácido 4-hidroxifenoxibenzóico (4-HPBA). Esses testes, no entanto, não têm sido frequentemente aplicados no monitoramento de exposições ocupacionais por causa das complexas técnicas analíticas necessárias (Eadsforth, Bragt e van Sittert 1988; Kolmodin-Hedman, Swensson e Akerblom 1982). Em aplicadores expostos a cipermetrina, os níveis urinários de Cl2Verificou-se que CA varia de 0.05 a 0.18 mg/l, enquanto em formuladores expostos a a-cipermetrina, os níveis urinários de 4-HPBA foram encontrados abaixo de 0.02 mg/l.
Um período de coleta de urina de 24 horas iniciado após o término da exposição é recomendado para determinações de metabólitos.
Organoclorados
Indicadores biológicos de exposição.
Os inseticidas organoclorados (OC) foram amplamente utilizados nas décadas de 1950 e 1960. Posteriormente, o uso de muitos desses compostos foi descontinuado em muitos países devido à sua persistência e consequente contaminação do meio ambiente.
O monitoramento biológico da exposição a OC pode ser realizado através da determinação de pesticidas intactos ou seus metabólitos no sangue ou soro (Dale, Curley e Cueto 1966; Barquet, Morgade e Pfaffenberger 1981). Após a absorção, o aldrin é rapidamente metabolizado em dieldrin e pode ser medido como dieldrin no sangue. Endrin tem uma meia-vida muito curta no sangue. Portanto, a concentração sanguínea de endrina é útil apenas para determinar os níveis de exposição recente. A determinação do metabólito urinário anti-12-hidroxi-endrina também provou ser útil no monitoramento da exposição à endrina (van Sittert e Tordoir 1987).
Correlações significativas entre a concentração de indicadores biológicos e o início de efeitos tóxicos foram demonstradas para alguns compostos OC. Casos de toxicidade devido à exposição a aldrin e dieldrin foram relacionados a níveis de dieldrin no sangue acima de 200 μg/l. Uma concentração de lindano no sangue de 20 μg/l foi indicada como o nível crítico superior no que diz respeito aos sinais e sintomas neurológicos. Nenhum efeito adverso agudo foi relatado em trabalhadores com concentrações de endrina no sangue abaixo de 50 μg/l. A ausência de efeitos adversos precoces (indução de enzimas microssomais hepáticas) foi demonstrada em exposições repetidas a endrina em concentrações urinárias de anti-12-hidroxiendrina abaixo de 130 μg/g de creatinina e em exposições repetidas a DDT em concentrações séricas de DDT ou DDE abaixo de 250 mg/l.
OC pode ser encontrado em baixas concentrações no sangue ou na urina da população em geral. Exemplos de valores observados são os seguintes: concentrações sanguíneas de lindano até 1 μg/l, dieldrin até 10 μg/l, DDT ou DDE até 100 μg/l e anti-12-hidroxiendrina até 1 μg/g creatinina. Assim, recomenda-se uma avaliação inicial antes da exposição.
Para indivíduos expostos, as amostras de sangue devem ser coletadas imediatamente após o término de uma única exposição. Para condições de exposição prolongada, o tempo de coleta da amostra de sangue não é crítico. Amostras pontuais de urina para determinação de metabólitos urinários devem ser coletadas no final da exposição.
Triazinas
Indicadores biológicos de exposição.
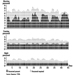
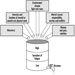
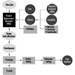
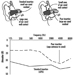
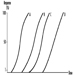
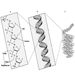
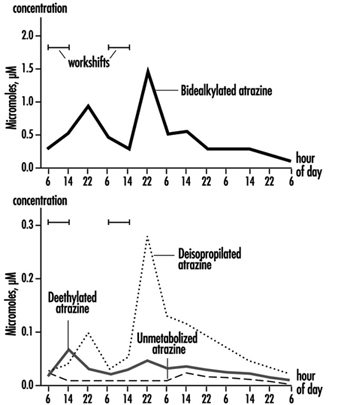
A medição da excreção urinária de metabólitos triazínicos e do composto original não modificado foi aplicada a indivíduos expostos à atrazina em estudos limitados. A Figura 2 mostra os perfis de excreção urinária de metabólitos de atrazina de um trabalhador industrial com exposição dérmica à atrazina variando de 174 a 275 μmol/turno de trabalho (Catenacci et al. 1993). Uma vez que outras clorotriazinas (simazina, propazina, terbutilazina) seguem a mesma via de biotransformação da atrazina, os níveis de metabólitos triazínicos desalquilados podem ser determinados para monitorar a exposição a todos os herbicidas de clorotriazina.
Figura 2. Perfis de excreção urinária de metabólitos de atrazina
A determinação de compostos não modificados na urina pode ser útil como confirmação qualitativa da natureza do composto que gerou a exposição. Um período de coleta de urina de 24 horas iniciado no início da exposição é recomendado para a determinação do metabólito.
Recentemente, usando um ensaio imunossorvente ligado a enzima (teste ELISA), um conjugado de ácido mercaptúrico de atrazina foi identificado como seu principal metabólito urinário em trabalhadores expostos. Este composto foi encontrado em concentrações pelo menos 10 vezes maiores que as de qualquer produto desalquilado. Foi observada uma relação entre a exposição cumulativa dérmica e por inalação e a quantidade total de conjugado de ácido mercaptúrico excretado durante um período de 10 dias (Lucas et al. 1993).
Derivados de Cumarina
Indicadores biológicos de efeito.
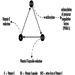
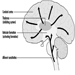
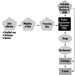
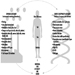
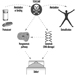
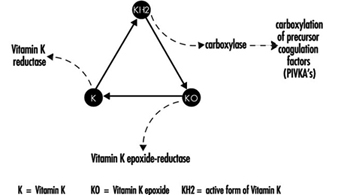
Os rodenticidas cumarínicos inibem a atividade das enzimas do ciclo da vitamina K no fígado de mamíferos, incluindo humanos (figura 3), causando assim uma redução dose-dependente da síntese de fatores de coagulação dependentes da vitamina K, nomeadamente o fator II (protrombina) , VII, IX e X. Os efeitos anticoagulantes aparecem quando os níveis plasmáticos dos fatores de coagulação caem abaixo de aproximadamente 20% do normal.
Figura 3. Ciclo da vitamina K
Esses antagonistas da vitamina K foram agrupados nos chamados compostos de “primeira geração” (por exemplo, varfarina) e compostos de “segunda geração” (por exemplo, brodifacume, difenacume), os últimos caracterizados por uma meia-vida biológica muito longa (100 a 200 dias ).
A determinação do tempo de protrombina é amplamente utilizada no monitoramento da exposição a cumarinas. No entanto, este teste é sensível apenas a uma diminuição do fator de coagulação de aproximadamente 20% dos níveis plasmáticos normais. O teste não é adequado para detecção de efeitos precoces de exposição. Para tanto, recomenda-se a determinação da concentração plasmática de protrombina.
No futuro, esses testes podem ser substituídos pela determinação dos precursores do fator de coagulação (PIVKA), que são substâncias detectáveis no sangue apenas no caso de bloqueio do ciclo da vitamina K por cumarinas.
Com condições de exposição prolongada, o tempo de coleta de sangue não é crítico. Em casos de superexposição aguda, o monitoramento biológico deve ser feito por pelo menos cinco dias após o evento, tendo em vista a latência do efeito anticoagulante. Para aumentar a sensibilidade desses testes, recomenda-se a medição dos valores basais antes da exposição.
Indicadores biológicos de exposição.
A medição de cumarinas não modificadas no sangue foi proposta como um teste para monitorar a exposição humana. No entanto, a experiência na aplicação desses índices é muito limitada principalmente porque as técnicas analíticas são muito mais complexas (e menos padronizadas) em comparação com as necessárias para monitorar os efeitos no sistema de coagulação (Chalermchaikit, Felice e Murphy 1993).
Herbicidas Fenoxi
Indicadores biológicos de exposição.
Os herbicidas fenoxi dificilmente são biotransformados em mamíferos. Em humanos, mais de 95% de uma dose de ácido 2,4-diclorofenoxiacético (2,4-D) é excretada inalterada na urina em cinco dias, e o ácido 2,4,5-triclorofenoxiacético (2,4,5-T) e ácido 4-cloro-2-metilfenoxiacético (MCPA) também são excretados na maior parte inalterados pela urina dentro de alguns dias após a absorção oral. A medição de compostos inalterados na urina tem sido aplicada no monitoramento da exposição ocupacional a esses herbicidas. Em estudos de campo, os níveis urinários de trabalhadores expostos variaram de 0.10 a 8 μg/l para 2,4-D, de 0.05 a 4.5 μg/l para 2,4,5-T e abaixo de 0.1 μg/l a 15 μg/l para MCPA. Recomenda-se um período de 24 horas de coleta de urina a partir do final da exposição para a determinação de compostos inalterados. Métodos analíticos para as medições de herbicidas fenoxi na urina foram relatados por Draper (1982).
Compostos de amônio quaternário
Indicadores biológicos de exposição.
Diquat e paraquat são herbicidas pouco biotransformados pelo organismo humano. Devido à sua elevada solubilidade em água, são facilmente excretados inalterados na urina. Concentrações de urina abaixo do limite de detecção analítica (0.01 μg/l) foram frequentemente observadas em trabalhadores expostos ao paraquat; enquanto em países tropicais, concentrações de até 0.73 μg/l foram medidas após o manuseio incorreto do paraquat. Concentrações urinárias de diquat inferiores ao limite de detecção analítica (0.047 μg/l) foram relatadas para indivíduos com exposições dérmicas de 0.17 a 1.82 μg/he exposições por inalação inferiores a 0.01 μg/h. Idealmente, amostras de 24 horas de urina coletadas no final da exposição devem ser usadas para análise. Quando isso não for prático, uma amostra pontual no final do dia de trabalho pode ser usada.
A determinação dos níveis de paraquat no soro é útil para fins de prognóstico em caso de intoxicação aguda: pacientes com níveis de paraquat no soro de até 0.1 μg/l vinte e quatro horas após a ingestão provavelmente sobreviverão.
Os métodos analíticos para determinação de paraquat e diquat foram revisados por Summers (1980).
Pesticidas diversos
4,6-Dinitro-o-cresol (DNOC).
O DNOC é um herbicida introduzido em 1925, mas o uso desse composto vem diminuindo progressivamente devido à sua alta toxicidade para as plantas e para o homem. Uma vez que as concentrações de DNOC no sangue se correlacionam até certo ponto com a gravidade dos efeitos adversos à saúde, a medida de DNOC inalterado no sangue foi proposta para monitorar exposições ocupacionais e para avaliação do curso clínico de envenenamentos.
Pentaclorofenol.
O pentaclorofenol (PCP) é um biocida de amplo espectro com ação pesticida contra ervas daninhas, insetos e fungos. As medições de PCP inalterado no sangue ou na urina foram recomendadas como índices adequados no monitoramento de exposições ocupacionais (Colosio et al. 1993), porque esses parâmetros estão significativamente correlacionados com a carga corporal de PCP. Em trabalhadores com exposição prolongada ao PCP o horário da coleta de sangue não é crítico, enquanto as amostras de urina devem ser coletadas na manhã seguinte à exposição.
Um método de múltiplos resíduos para a medição de pesticidas halogenados e nitrofenólicos foi descrito por Shafik et al. (1973b).
Outros testes propostos para o monitoramento biológico da exposição a pesticidas estão listados na tabela 9.
Tabela 9. Outros índices propostos na literatura para o monitoramento biológico da exposição a agrotóxicos
|
Compound |
índice biológico |
|
|
Urina |
Sangue |
|
|
Bromofos |
Bromofos |
Bromofos |
|
Captan |
Tetrahidroftalimida |
|
|
Carbofurano |
3-Hidroxicarbofurano |
|
|
Clordimeforme |
4-cloro-o-derivados de toluidina |
|
|
Clorobenzilato |
p,p-1-Diclorobenzofenona |
|
|
Dicloropropeno |
Metabólitos do ácido mercaptúrico |
|
|
Fenitrotion |
p-Nitrocresol |
|
|
ferbam |
Tiram |
|
|
Fluazifop-Butil |
Fluazifope |
|
|
Flufenoxurão |
Flufenoxurão |
|
|
glifosato |
glifosato |
|
|
Malatião |
Malatião |
Malatião |
|
compostos organoestânicos |
Estanho |
Estanho |
|
Trifenomorfo |
Morfolina, trifenilcarbinol |
|
|
Ziram |
Tiram |
|
Conclusões
Indicadores biológicos para monitorar a exposição a pesticidas têm sido aplicados em vários estudos experimentais e de campo.
Alguns testes, como aqueles para colinesterase no sangue ou para pesticidas não modificados selecionados na urina ou no sangue, foram validados por ampla experiência. Limites de exposição biológica foram propostos para esses testes (tabela 10). Outros testes, em particular os de metabólitos sanguíneos ou urinários, sofrem maiores limitações por dificuldades analíticas ou por limitações na interpretação dos resultados.
Tabela 10. Valores-limite biológicos recomendados (a partir de 1996)
|
Compound |
índice biológico |
NO1 |
BAT2 |
HBBL3 |
BLV4 |
|
inibidores de ACHE |
DOR no sangue |
70% |
70% |
% 70 |
|
|
DNO |
DNOC no sangue |
20 mg/l, |
|||
|
Lindano |
Lindano no sangue |
0.02mg / l |
0.02mg / l |
||
|
Paratião |
PNP na urina |
0.5mg / l |
0.5mg / l |
||
|
Pentaclorofenol (PCP) |
PCP na urina PCP no plasma |
2 mg / l 5 mg / l |
0.3mg / l 1 mg / l |
||
|
Dieldrin/Aldrin |
Dieldrin no sangue |
100 mg / l |
|||
|
endrin |
Anti-12-hidroxiendrina na urina |
130 mg / l |
|||
|
DDT |
DDT e DDE no soro |
250 mg / l |
|||
|
Cumarinas |
Tempo de protrombina no plasma Concentração de protrombina no plasma |
10% acima da linha de base 60% da linha de base |
|||
|
MCPA |
MCPA na urina |
0.5 mg / l |
|||
|
2,4-D |
2,4-D na urina |
0.5 mg / l |
1 Os índices de exposição biológica (BEIs) são recomendados pela Conferência Americana de Higienistas Industriais Governamentais (ACGIH 1995).
2 Os valores de tolerância biológica (BATs) são recomendados pela Comissão Alemã para a Investigação de Riscos à Saúde de Compostos Químicos na Área de Trabalho (DFG 1992).
3 Os limites biológicos baseados na saúde (HBBLs) são recomendados por um Grupo de Estudo da OMS (OMS 1982a).
4 Os valores-limite biológicos (BLVs) são propostos por um Grupo de Estudos do Comitê Científico de Pesticidas da Comissão Internacional de Saúde Ocupacional (Tordoir et al. 1994). A avaliação das condições de trabalho é necessária se este valor for excedido.
Este campo está em rápido desenvolvimento e, dada a enorme importância da utilização de indicadores biológicos para avaliar a exposição a estas substâncias, novos testes serão continuamente desenvolvidos e validados.
Método Epidemiológico Aplicado à Saúde e Segurança Ocupacional
Epidemiologia
A epidemiologia é reconhecida tanto como a ciência básica da medicina preventiva quanto aquela que informa o processo de política de saúde pública. Várias definições operacionais de epidemiologia têm sido sugeridas. A mais simples é que a epidemiologia é o estudo da ocorrência de doenças ou outras características relacionadas à saúde em populações humanas e animais. Os epidemiologistas estudam não apenas a frequência da doença, mas também se a frequência difere entre os grupos de pessoas; ou seja, eles estudam a relação de causa e efeito entre a exposição e a doença. As doenças não ocorrem ao acaso; eles têm causas - muitas vezes causadas pelo homem - que são evitáveis. Assim, muitas doenças poderiam ser evitadas se as causas fossem conhecidas. Os métodos da epidemiologia têm sido cruciais para identificar muitos fatores causais que, por sua vez, levaram a políticas de saúde destinadas a prevenir doenças, lesões e morte prematura.
Qual é a tarefa da epidemiologia e quais são seus pontos fortes e fracos quando as definições e conceitos de epidemiologia são aplicados à saúde ocupacional? Este capítulo aborda essas questões e as formas pelas quais os riscos à saúde ocupacional podem ser investigados usando técnicas epidemiológicas. Este artigo apresenta as idéias encontradas em artigos sucessivos neste capítulo.
Epidemiologia Ocupacional
A epidemiologia ocupacional tem sido definida como o estudo dos efeitos das exposições no local de trabalho na frequência e distribuição de doenças e lesões na população. Portanto, é uma disciplina orientada para a exposição com vínculos tanto com a epidemiologia quanto com a saúde ocupacional (Checkoway et al. 1989). Para tanto, utiliza métodos semelhantes aos empregados pela epidemiologia em geral.
O principal objetivo da epidemiologia ocupacional é a prevenção através da identificação das consequências das exposições no local de trabalho para a saúde. Isso reforça o foco preventivo da epidemiologia ocupacional. Com efeito, toda a investigação no domínio da saúde e segurança no trabalho deve ter fins preventivos. Assim, o conhecimento epidemiológico pode e deve ser prontamente implementável. Embora o interesse da saúde pública sempre deva ser a principal preocupação da pesquisa epidemiológica, os interesses escusos podem exercer influência, e deve-se tomar cuidado para minimizar essa influência na formulação, condução e/ou interpretação dos estudos (Soskolne 1985; Soskolne 1989).
Um segundo objetivo da epidemiologia ocupacional é usar resultados de ambientes específicos para reduzir ou eliminar riscos na população em geral. Assim, além de fornecer informações sobre os efeitos sobre a saúde das exposições no local de trabalho, os resultados dos estudos de epidemiologia ocupacional também desempenham um papel na estimativa do risco associado às mesmas exposições, mas em níveis mais baixos geralmente experimentados pela população em geral. A contaminação ambiental de processos e produtos industriais geralmente resultaria em níveis mais baixos de exposição do que aqueles experimentados no local de trabalho.
Os níveis de aplicação da epidemiologia ocupacional são:
- vigilância para descrever a ocorrência de doenças em diferentes categorias de trabalhadores e, assim, fornecer sinais de alerta precoce de riscos ocupacionais não reconhecidos
- geração e teste de uma hipótese de que uma dada exposição pode ser prejudicial, e a quantificação de um efeito
- avaliação de uma intervenção (por exemplo, uma ação preventiva como a redução dos níveis de exposição) medindo as mudanças no estado de saúde de uma população ao longo do tempo.
O papel causal que as exposições ocupacionais podem desempenhar no desenvolvimento de doenças, lesões e mortes prematuras foi identificado há muito tempo e faz parte da história da epidemiologia. Referência deve ser feita a Bernardino Ramazzini, fundador da medicina ocupacional e um dos primeiros a reviver e acrescentar à tradição hipocrática da dependência da saúde de fatores externos naturais identificáveis. No ano de 1700, ele escreveu em seu “De Morbis Artificum Diatriba” (Ramazzini 1705; Saracci 1995):
O médico tem que fazer muitas perguntas aos pacientes. Hipócrates afirma em De Affectionibus: “Quando você se depara com uma pessoa doente, você deve perguntar a ela do que ela está sofrendo, por que motivo, por quantos dias, o que ela come e quais são seus movimentos intestinais. A todas essas perguntas deve-se acrescentar: 'Que trabalho ele faz?'”.
Esse despertar da observação clínica e da atenção às circunstâncias que cercam a ocorrência da doença, levou Ramazzini a identificar e descrever muitas das doenças ocupacionais que foram posteriormente estudadas por médicos do trabalho e epidemiologistas.
Usando essa abordagem, Pott foi o primeiro a relatar em 1775 (Pott 1775) a possível conexão entre câncer e ocupação (Clayson 1962). Suas observações sobre o câncer de escroto entre limpadores de chaminés começaram com uma descrição da doença e continuaram:
O destino dessas pessoas parece singularmente difícil: na primeira infância, elas são frequentemente tratadas com grande brutalidade e quase passam fome de frio e fome; eles são lançados em chaminés estreitas e às vezes quentes, onde são machucados, queimados e quase sufocados; e quando chegam à puberdade, tornam-se particularmente sujeitos a uma doença muito nociva, dolorosa e fatal.
Desta última circunstância não há a menor dúvida, embora talvez não tenha sido suficientemente atendida, para torná-la geralmente conhecida. Outras pessoas têm câncer nas mesmas partes; e também outros, além dos trabalhadores de chumbo, a cólica de Poitou e a consequente paralisia; mas, não obstante, é uma doença à qual eles estão particularmente sujeitos; e também os limpadores de chaminés para o câncer do escroto e dos testículos.
A doença, nestas pessoas, parece derivar de um depósito de fuligem nas rugas do escroto, e a princípio não ser uma doença do hábito... inicialmente; a doença provocada por sua ocupação e, com toda probabilidade, local; qual última circunstância pode, penso eu, ser razoavelmente presumida por sempre apreender as mesmas partes; tudo isso o torna (a princípio) um caso muito diferente de um câncer que aparece em um homem idoso.
Este primeiro relato de um câncer ocupacional ainda permanece um modelo de lucidez. A natureza da doença, a ocupação em questão e o provável agente causal estão claramente definidos. Observa-se um aumento da incidência de câncer escrotal entre os limpadores de chaminés, embora nenhum dado quantitativo seja fornecido para substanciar a alegação.
Outros cinquenta anos se passaram antes que Ayrton-Paris percebesse em 1822 (Ayrton-Paris 1822) o desenvolvimento frequente de cânceres escrotais entre as fundições de cobre e estanho da Cornualha, e supôs que os vapores de arsênico poderiam ser o agente causal. Von Volkmann relatou em 1874 tumores de pele em trabalhadores de parafina na Saxônia e, pouco depois, Bell sugeriu em 1876 que o óleo de xisto era responsável pelo câncer cutâneo (Von Volkmann 1874; Bell 1876). Relatos sobre a origem ocupacional do câncer tornaram-se então relativamente mais frequentes (Clayson 1962).
Entre as primeiras observações de doenças ocupacionais estava o aumento da ocorrência de câncer de pulmão entre os mineiros de Schneeberg (Harting e Hesse 1879). É digno de nota (e trágico) que um estudo de caso recente mostre que a epidemia de câncer de pulmão em Schneeberg ainda é um grande problema de saúde pública, mais de um século após a primeira observação em 1879. Uma abordagem para identificar um “aumento” da doença e até quantificá-la esteve presente na história da medicina do trabalho. Por exemplo, como Axelson (1994) apontou, WA Guy em 1843 estudou “consumo pulmonar” em impressores de letras e encontrou um risco maior entre os tipógrafos do que entre os impressores; isso foi feito aplicando um projeto semelhante à abordagem de controle de caso (Lilienfeld e Lilienfeld 1979). No entanto, foi somente no início da década de 1950 que a epidemiologia ocupacional moderna e sua metodologia começaram a se desenvolver. As principais contribuições que marcaram esse desenvolvimento foram os estudos sobre câncer de bexiga em trabalhadores de tinturaria (Case e Hosker 1954) e câncer de pulmão entre trabalhadores de gás (Doll 1952).
Questões em Epidemiologia Ocupacional
Os artigos deste capítulo apresentam tanto a filosofia quanto as ferramentas da investigação epidemiológica. Eles se concentram em avaliar a experiência de exposição dos trabalhadores e nas doenças que surgem nessas populações. Neste capítulo, abordam-se questões relacionadas com a obtenção de conclusões válidas sobre possíveis ligações causais no caminho desde a exposição a substâncias perigosas até ao desenvolvimento de doenças.
A determinação da experiência de exposição na vida profissional de um indivíduo constitui o núcleo da epidemiologia ocupacional. A informatividade de um estudo epidemiológico depende, em primeiro lugar, da qualidade e extensão dos dados de exposição disponíveis. Em segundo lugar, os efeitos na saúde (ou as doenças) que preocupam o epidemiologista ocupacional devem ser determinados com precisão entre um grupo de trabalhadores bem definido e acessível. Finalmente, dados sobre outras influências potenciais na doença de interesse devem estar disponíveis para o epidemiologista, de modo que quaisquer efeitos de exposição ocupacional estabelecidos a partir do estudo possam ser atribuídos à exposição ocupacional per se em vez de outras causas conhecidas da doença em questão. Por exemplo, em um grupo de trabalhadores que podem trabalhar com um produto químico suspeito de causar câncer de pulmão, alguns trabalhadores também podem ter um histórico de tabagismo, outra causa de câncer de pulmão. Nesta última situação, os epidemiologistas ocupacionais devem determinar qual exposição (ou qual fator de risco - o produto químico ou o tabaco, ou, na verdade, os dois em combinação) é responsável por qualquer aumento no risco de câncer de pulmão no grupo de trabalhadores sendo estudado.
Avaliação da exposição
Se um estudo tiver acesso apenas ao fato de que um trabalhador foi empregado em uma determinada indústria, então os resultados de tal estudo podem vincular os efeitos na saúde apenas a essa indústria. Da mesma forma, se existe conhecimento sobre a exposição para as ocupações dos trabalhadores, as conclusões podem ser tiradas diretamente apenas no que diz respeito às ocupações. Inferências indiretas sobre exposições a produtos químicos podem ser feitas, mas sua confiabilidade deve ser avaliada situação a situação. Se um estudo tiver acesso, no entanto, a informações sobre o departamento e/ou o cargo de cada trabalhador, as conclusões poderão ser feitas nesse nível mais refinado de experiência no local de trabalho. Quando as informações sobre as substâncias reais com as quais uma pessoa trabalha são conhecidas do epidemiologista (em colaboração com um higienista industrial), esse seria o melhor nível de informações de exposição disponíveis na ausência de dosimetria raramente disponível. Além disso, os resultados desses estudos podem fornecer informações mais úteis para a indústria criar locais de trabalho mais seguros.
A epidemiologia tem sido uma espécie de disciplina de “caixa preta” até agora, porque estudou a relação entre exposição e doença (os dois extremos da cadeia causal), sem considerar as etapas mecanicistas intermediárias. Essa abordagem, apesar de sua aparente falta de refinamento, tem sido extremamente útil: na verdade, todas as causas conhecidas de câncer em humanos, por exemplo, foram descobertas com as ferramentas da epidemiologia.
O método epidemiológico é baseado em registros disponíveis — questionários, cargos ou outros “proxies” de exposição; isso torna a condução de estudos epidemiológicos e a interpretação de seus achados relativamente simples.
As limitações da abordagem mais grosseira da avaliação da exposição, no entanto, tornaram-se evidentes nos últimos anos, com os epidemiologistas enfrentando problemas mais complexos. Limitando nossa consideração à epidemiologia do câncer ocupacional, os fatores de risco mais conhecidos foram descobertos devido a altos níveis de exposição no passado; um número limitado de exposições para cada trabalho; grandes populações de trabalhadores expostos; e uma correspondência clara entre informações “proxy” e exposições químicas (por exemplo, trabalhadores de calçados e benzeno, estaleiros navais e amianto, e assim por diante). Hoje em dia, a situação é substancialmente diferente: os níveis de exposição são consideravelmente mais baixos nos países ocidentais (esta ressalva deve ser sempre enfatizada); os trabalhadores estão expostos a muitos produtos químicos e misturas diferentes no mesmo cargo (por exemplo, trabalhadores agrícolas); populações homogêneas de trabalhadores expostos são mais difíceis de encontrar e geralmente são em pequeno número; e, a correspondência entre informações “proxy” e exposição real torna-se progressivamente mais fraca. Nesse contexto, as ferramentas da epidemiologia têm sensibilidade reduzida devido à classificação errônea da exposição.
Além disso, a epidemiologia se baseou em pontos finais “difíceis”, como a morte na maioria dos estudos de coorte. No entanto, os trabalhadores podem preferir ver algo diferente de “contagem de corpos” quando os efeitos potenciais de exposição ocupacional à saúde são estudados. Portanto, o uso de indicadores mais diretos de exposição e resposta precoce teria algumas vantagens. Marcadores biológicos podem fornecer apenas uma ferramenta.
marcadores biológicos
O uso de marcadores biológicos, como níveis de chumbo em exames de sangue ou de função hepática, não é novidade na epidemiologia ocupacional. No entanto, a utilização de técnicas moleculares em estudos epidemiológicos tornou possível o uso de biomarcadores para avaliar a exposição de órgãos-alvo, determinar a suscetibilidade e estabelecer doenças precocemente.
Os usos potenciais de biomarcadores no contexto da epidemiologia ocupacional são:
- avaliação da exposição nos casos em que as ferramentas epidemiológicas tradicionais são insuficientes (particularmente para doses baixas e riscos baixos)
- para desvendar o papel causador de agentes ou substâncias químicas individuais em múltiplas exposições ou misturas
- estimativa da carga total de exposição a produtos químicos com o mesmo alvo mecanístico
- investigação de mecanismos patogenéticos
- estudo da suscetibilidade individual (por exemplo, polimorfismos metabólicos, reparo do DNA) (Vineis 1992)
- para classificar a exposição e/ou doença com mais precisão, aumentando assim o poder estatístico.
Grande entusiasmo surgiu na comunidade científica sobre esses usos, mas, como observado acima, a complexidade metodológica do uso dessas novas “ferramentas moleculares” deve servir para alertar contra o otimismo excessivo. Biomarcadores de exposições químicas (como adutos de DNA) têm várias deficiências:
- Eles geralmente refletem exposições recentes e, portanto, são de uso limitado em estudos de caso-controle, ao passo que requerem amostragens repetidas por períodos prolongados para utilização em investigações de coorte.
- Embora possam ser altamente específicos e, assim, melhorar a classificação incorreta da exposição, os resultados geralmente permanecem difíceis de interpretar.
- Quando exposições químicas complexas são investigadas (por exemplo, poluição do ar ou fumaça ambiental de tabaco), é possível que o biomarcador reflita um componente específico da mistura, enquanto o efeito biológico pode ser devido a outro.
- Em muitas situações, não está claro se um biomarcador reflete uma exposição relevante, um correlato da exposição relevante, a suscetibilidade individual ou um estágio inicial da doença, limitando assim a inferência causal.
- A determinação da maioria dos biomarcadores requer um teste caro ou um procedimento invasivo ou ambos, criando assim restrições para o tamanho adequado do estudo e poder estatístico.
- Um biomarcador de exposição nada mais é do que um proxy para o real objetivo de uma investigação epidemiológica, que, via de regra, se concentra em uma exposição ambiental evitável (Trichopoulos 1995; Pearce et al. 1995).
Ainda mais importante do que as deficiências metodológicas é a consideração de que as técnicas moleculares podem nos levar a redirecionar nosso foco da identificação de riscos no ambiente exógeno para a identificação de indivíduos de alto risco e, em seguida, fazer avaliações de risco personalizadas medindo fenótipo, carga de adução e mutações adquiridas. Isso direcionaria nosso foco, conforme observado por McMichael, para uma forma de avaliação clínica, em vez de uma epidemiologia de saúde pública. Concentrar-se nos indivíduos pode nos distrair do importante objetivo de saúde pública de criar um ambiente menos perigoso (McMichael 1994).
Duas outras questões importantes surgem em relação ao uso de biomarcadores:
- O uso de biomarcadores em epidemiologia ocupacional deve ser acompanhado por uma política clara no que diz respeito ao consentimento informado. O trabalhador pode ter vários motivos para recusar a cooperação. Uma razão muito prática é que a identificação de, digamos, uma alteração em um marcador de resposta precoce, como a troca de cromátides irmãs, implica a possibilidade de discriminação por seguradoras de saúde e vida e por empregadores que podem evitar o trabalhador porque ele ou ela pode ser mais propenso à doença. Uma segunda razão diz respeito à triagem genética: uma vez que as distribuições de genótipos e fenótipos variam de acordo com o grupo étnico, as oportunidades ocupacionais para minorias podem ser prejudicadas pela triagem genética. Em terceiro lugar, podem ser levantadas dúvidas sobre a previsibilidade dos testes genéticos: como o valor preditivo depende da prevalência da condição que o teste visa identificar, se esta for rara, o valor preditivo será baixo e o uso prático do rastreamento teste será questionável. Até agora, nenhum dos testes de triagem genética foi julgado aplicável no campo (Ashford et al. 1990).
- Princípios éticos devem ser aplicados antes do uso de biomarcadores. Esses princípios foram avaliados para biomarcadores usados para identificar a suscetibilidade individual a doenças por um Grupo de Trabalho interdisciplinar do Escritório Técnico dos Sindicatos Europeus, com o apoio da Comissão das Comunidades Européias (Van Damme et al. 1995); seu relatório reforçou a visão de que os testes só podem ser realizados com o objetivo de prevenir doenças na força de trabalho. Entre outras considerações, o uso de testes deve nunca.
- servir como um meio para “seleção do mais apto”
- ser usado para evitar a implementação de medidas preventivas eficazes, como a identificação e substituição de fatores de risco ou melhorias nas condições no local de trabalho
- criar, confirmar ou reforçar a desigualdade social
- criar uma lacuna entre os princípios éticos seguidos no local de trabalho e os princípios éticos que devem ser respeitados em uma sociedade democrática
- obrigar o candidato a emprego a revelar dados pessoais que não sejam estritamente necessários para a obtenção do emprego.
Finalmente, acumulam-se evidências de que a ativação ou inativação metabólica de substâncias perigosas (e de carcinógenos em particular) varia consideravelmente nas populações humanas e é parcialmente determinada geneticamente. Além disso, a variabilidade interindividual na suscetibilidade a carcinógenos pode ser particularmente importante em baixos níveis de exposição ocupacional e ambiental (Vineis et al. 1994). Tais descobertas podem afetar fortemente as decisões regulatórias que focam o processo de avaliação de risco nos mais suscetíveis (Vineis e Martone 1995).
Desenho e validade do estudo
O artigo de Hernberg sobre desenhos de estudos epidemiológicos e suas aplicações em medicina ocupacional concentra-se no conceito de “base de estudo”, definida como a experiência de morbidade (em relação a alguma exposição) de uma população enquanto ela é acompanhada ao longo do tempo. Assim, a base do estudo não é apenas uma população (ou seja, um grupo de pessoas), mas a experiência de ocorrência de doenças dessa população durante um determinado período de tempo (Miettinen 1985, Hernberg 1992). Se esse conceito unificador de uma base de estudo for adotado, é importante reconhecer que os diferentes desenhos de estudo (por exemplo, projetos de caso-controle e de coorte) são simplesmente maneiras diferentes de “coletar” informações sobre a exposição e a doença do mesmo estudo. base; não são abordagens diametralmente diferentes.
O artigo sobre validade no desenho do estudo da Sasco aborda as definições e a importância da confusão. Os investigadores do estudo devem sempre considerar a possibilidade de confusão em estudos ocupacionais, e nunca pode ser suficientemente enfatizado que a identificação de variáveis potencialmente confusas é parte integrante de qualquer desenho e análise de estudo. Dois aspectos da confusão devem ser abordados na epidemiologia ocupacional:
- A confusão negativa deve ser explorada: por exemplo, algumas populações industriais têm baixa exposição a fatores de risco associados ao estilo de vida por causa de um local de trabalho sem fumo; sopradores de vidro tendem a fumar menos do que a população em geral.
- Quando a confusão é considerada, uma estimativa de sua direção e seu impacto potencial deve ser avaliada. Isso é particularmente verdadeiro quando os dados para controlar a confusão são escassos. Por exemplo, fumar é um importante fator de confusão na epidemiologia ocupacional e sempre deve ser considerado. No entanto, quando os dados sobre tabagismo não estão disponíveis (como é frequentemente o caso em estudos de coorte), é improvável que o tabagismo possa explicar um grande excesso de risco encontrado em um grupo ocupacional. Isso é bem descrito em um artigo de Axelson (1978) e discutido posteriormente por Greenland (1987). Quando dados detalhados sobre ocupação e tabagismo estão disponíveis na literatura, a confusão não parece distorcer fortemente as estimativas relativas à associação entre câncer de pulmão e ocupação (Vineis e Simonato, 1991). Além disso, a suspeita de confusão nem sempre introduz associações não válidas. Uma vez que os investigadores também correm o risco de serem desviados por outros vieses de observação e seleção não detectados, eles devem receber tanta ênfase quanto a questão da confusão no planejamento de um estudo (Stellman 1987).
Tempo e variáveis relacionadas ao tempo, como idade de risco, período do calendário, tempo desde a contratação, tempo desde a primeira exposição, duração da exposição e seu tratamento na fase de análise, estão entre as questões metodológicas mais complexas da epidemiologia ocupacional. Eles não são abordados neste capítulo, mas duas referências metodológicas recentes e relevantes são observadas (Pearce 1992; Robins et al. 1992).
Estatísticas
O artigo sobre estatística de Biggeri e Braga, assim como o título deste capítulo, indicam que os métodos estatísticos não podem ser separados da pesquisa epidemiológica. Isso ocorre porque: (a) uma compreensão sólida das estatísticas pode fornecer informações valiosas sobre o desenho adequado de uma investigação e (b) estatísticas e epidemiologia compartilham uma herança comum, e toda a base quantitativa da epidemiologia é fundamentada na noção de probabilidade ( Clayton 1992; Clayton e Hills 1993). Em muitos dos artigos que se seguem, a evidência empírica e a prova de relações causais hipotéticas são avaliadas usando argumentos probabilísticos e desenhos de estudo apropriados. Por exemplo, a ênfase é colocada na estimativa da medida de risco de juros, como taxas ou riscos relativos, e na construção de intervalos de confiança em torno dessas estimativas, em vez da execução de testes estatísticos de probabilidade (Poole 1987; Gardner e Altman 1989; Greenland 1990 ). Uma breve introdução ao raciocínio estatístico usando a distribuição binomial é fornecida. A estatística deve ser uma companheira do raciocínio científico. Mas é inútil na ausência de pesquisas adequadamente planejadas e conduzidas. Os estatísticos e epidemiologistas estão cientes de que a escolha dos métodos determina o que e até que ponto fazemos observações. A escolha criteriosa das opções de projeto é, portanto, de fundamental importância para garantir observações válidas.
Ética
O último artigo, de Vineis, aborda questões éticas em pesquisas epidemiológicas. Pontos a serem mencionados nesta introdução referem-se à epidemiologia como uma disciplina que implica ação preventiva por definição. Aspectos éticos específicos relativos à proteção dos trabalhadores e da população em geral exigem o reconhecimento de que:
- Os estudos epidemiológicos em ambientes ocupacionais não devem, de forma alguma, atrasar as medidas preventivas no local de trabalho.
- A epidemiologia ocupacional não se refere a fatores de estilo de vida, mas a situações em que geralmente pouco ou nenhum papel pessoal é desempenhado na escolha da exposição. Isto implica uma aposta particular na prevenção eficaz e na transmissão imediata de informação aos trabalhadores e ao público.
- A pesquisa revela os perigos para a saúde e fornece o conhecimento para a ação preventiva. Os problemas éticos de não realizar pesquisas, quando factíveis, devem ser considerados.
- A notificação aos trabalhadores dos resultados dos estudos epidemiológicos é uma questão ética e metodológica na comunicação de risco. A pesquisa para avaliar o impacto potencial e a eficácia da notificação deve receber alta prioridade (Schulte et al. 1993).
Formação em Epidemiologia Ocupacional
Pessoas com diversas origens podem encontrar seu caminho para a especialização em epidemiologia ocupacional. Medicina, enfermagem e estatística são algumas das formações mais prováveis entre os especialistas nessa área. Na América do Norte, cerca de metade de todos os epidemiologistas treinados têm formação científica, enquanto a outra metade terá seguido o caminho do doutor em medicina. Em países fora da América do Norte, a maioria dos especialistas em epidemiologia ocupacional terá avançado nas categorias de doutor em medicina. Na América do Norte, aqueles com treinamento médico tendem a ser considerados “especialistas em conteúdo”, enquanto aqueles que são treinados pela via científica são considerados “especialistas metodológicos”. Muitas vezes, é vantajoso para um especialista em conteúdo se unir a um especialista em metodologia para projetar e conduzir o melhor estudo possível.
Não só é necessário conhecimento de métodos epidemiológicos, estatísticas e computadores para a especialidade de epidemiologia ocupacional, mas também conhecimento de toxicologia, higiene industrial e registros de doenças (Merletti e Comba 1992). Como grandes estudos podem exigir a vinculação a registros de doenças, o conhecimento das fontes de dados populacionais é útil. Conhecimento de trabalho e organização corporativa também é importante. Teses em nível de mestrado e dissertações em nível de doutorado de formação equipam os alunos com os conhecimentos necessários para a realização de grandes estudos baseados em registros e entrevistas com trabalhadores.
Proporção de doenças atribuíveis à ocupação
A proporção de doenças atribuíveis a exposições ocupacionais em um grupo de trabalhadores expostos ou na população em geral é coberta pelo menos com relação ao câncer em outra parte deste enciclopédia. Aqui devemos lembrar que se uma estimativa for computada, ela deve ser para uma doença específica (e um local específico no caso do câncer), um período de tempo específico e uma área geográfica específica. Além disso, deve basear-se em medidas precisas da proporção de pessoas expostas e do grau de exposição. Isso implica que a proporção de doenças atribuíveis à ocupação pode variar de muito baixa ou zero em certas populações a muito alta em outras localizadas em áreas industriais onde, por exemplo, até 40% dos cânceres de pulmão podem ser atribuídos a exposições ocupacionais (Vineis e Simonato 1991). As estimativas que não são baseadas em uma revisão detalhada de estudos epidemiológicos bem desenhados podem, na melhor das hipóteses, ser consideradas como suposições informadas e têm valor limitado.
Transferência de indústrias perigosas
A maioria das pesquisas epidemiológicas é realizada no mundo desenvolvido, onde a regulamentação e o controle de riscos ocupacionais conhecidos reduziram o risco de doenças nas últimas décadas. Ao mesmo tempo, porém, houve uma grande transferência de indústrias perigosas para o mundo em desenvolvimento (Jeyaratnam 1994). Produtos químicos anteriormente proibidos nos Estados Unidos ou na Europa agora são produzidos em países em desenvolvimento. Por exemplo, a moagem de amianto foi transferida dos Estados Unidos para o México, e a produção de benzidina de países europeus para a ex-Iugoslávia e Coréia (Simonato 1986; LaDou 1991; Pearce et al. 1994).
Um sinal indireto do nível de risco ocupacional e das condições de trabalho no mundo em desenvolvimento é a epidemia de intoxicação aguda que ocorre em alguns desses países. De acordo com uma avaliação, há cerca de 20,000 mortes a cada ano no mundo devido à intoxicação aguda por pesticidas, mas isso provavelmente é uma subestimação substancial (Kogevinas et al. 1994). Estima-se que 99% de todas as mortes por envenenamento agudo por pesticidas ocorrem em países em desenvolvimento, onde apenas 20% dos agroquímicos do mundo são usados (Kogevinas et al. 1994). Isso quer dizer que, mesmo que a pesquisa epidemiológica pareça apontar para uma redução dos riscos ocupacionais, isso pode ser simplesmente devido ao fato de que a maior parte dessa pesquisa está sendo realizada no mundo desenvolvido. Os riscos ocupacionais podem simplesmente ter sido transferidos para o mundo em desenvolvimento e a carga total de exposição ocupacional mundial pode ter aumentado (Vineis et al. 1995).
Epidemiologia Veterinária
Por razões óbvias, a epidemiologia veterinária não é diretamente pertinente à saúde ocupacional e à epidemiologia ocupacional. No entanto, pistas para causas ambientais e ocupacionais de doenças podem vir de estudos epidemiológicos em animais por várias razões:
- O tempo de vida dos animais é relativamente curto em comparação com o dos humanos, e o período de latência para doenças (por exemplo, a maioria dos cânceres) é mais curto em animais do que em humanos. Isso implica que uma doença que ocorre em um animal selvagem ou de estimação pode servir como um evento sentinela para nos alertar sobre a presença de um potencial tóxico ambiental ou carcinógeno para humanos antes que ele fosse identificado por outros meios (Glickman 1993).
- Marcadores de exposições, como adutos de hemoglobina ou níveis de absorção e excreção de toxinas, podem ser medidos em animais selvagens e de estimação para avaliar a contaminação ambiental de fontes industriais (Blondin e Viau 1992; Reynolds et al. 1994; Hungerford et al. 1995) .
- Os animais não são expostos a alguns fatores que podem atuar como fatores de confusão em estudos humanos e, portanto, as investigações em populações de animais podem ser conduzidas sem considerar esses fatores de confusão em potencial. Por exemplo, um estudo de câncer de pulmão em cães de estimação pode detectar associações significativas entre a doença e a exposição ao amianto (por exemplo, por meio de ocupações relacionadas ao amianto dos proprietários e proximidade de fontes industriais de amianto). Claramente, tal estudo removeria o efeito do tabagismo ativo como um fator de confusão.
Veterinários falam sobre uma revolução epidemiológica na medicina veterinária (Schwabe 1993) e surgiram livros sobre a disciplina (Thrusfield 1986; Martin et al. 1987). Certamente, pistas para riscos ambientais e ocupacionais vieram dos esforços conjuntos de epidemiologistas humanos e animais. Entre outros, o efeito de fenoxi-herbicidas em ovelhas e cães (Newell et al. 1984; Hayes et al. 1990), de campos magnéticos (Reif et al. 1995) e pesticidas (especialmente preparações contra pulgas) contaminados com compostos semelhantes ao amianto em cães (Glickman et al. 1983) são contribuições notáveis.
Pesquisa participativa, comunicação de resultados e prevenção
É importante reconhecer que muitos estudos epidemiológicos no campo da saúde ocupacional são iniciados por meio da experiência e preocupação dos próprios trabalhadores (Olsen et al. 1991). Freqüentemente, os trabalhadores - aqueles expostos histórica e/ou presentemente - acreditavam que algo estava errado muito antes de isso ser confirmado pela pesquisa. A epidemiologia ocupacional pode ser pensada como uma forma de “dar sentido” à experiência dos trabalhadores, de coletar e agrupar os dados de forma sistemática e permitir inferir sobre as causas ocupacionais de seus adoecimentos. Além disso, os próprios trabalhadores, seus representantes e os responsáveis pela saúde dos trabalhadores são as pessoas mais adequadas para interpretar os dados coletados. Eles, portanto, devem sempre ser participantes ativos em qualquer investigação realizada no local de trabalho. Somente seu envolvimento direto garantirá que o local de trabalho permanecerá seguro após a saída dos pesquisadores. O objetivo de qualquer estudo é o uso dos resultados na prevenção de doenças e incapacidades, e o sucesso disso depende em grande parte da garantia de que os expostos participem da obtenção e interpretação dos resultados do estudo. O papel e o uso dos resultados da pesquisa no processo de litígio, à medida que os trabalhadores buscam indenização por danos causados pela exposição no local de trabalho, está além do escopo deste capítulo. Para alguma compreensão sobre isso, o leitor é encaminhado para outro lugar (Soskolne, Lilienfeld e Black 1994).
Abordagens participativas para garantir a condução da pesquisa epidemiológica ocupacional tornaram-se, em alguns lugares, uma prática padrão na forma de comitês diretores estabelecidos para supervisionar a iniciativa de pesquisa desde o início até a conclusão. Esses comitês são multipartidos em sua estrutura, incluindo trabalho, ciência, gestão e/ou governo. Com representantes de todos os grupos de partes interessadas no processo de pesquisa, a comunicação dos resultados será mais eficaz em virtude de sua maior credibilidade, porque “um deles” supervisionaria a pesquisa e comunicaria os resultados aos seus respectivos eleitorado. Desta forma, o maior nível de prevenção eficaz é provável.
Essas e outras abordagens participativas na pesquisa em saúde ocupacional são realizadas com o envolvimento daqueles que vivenciam ou são afetados pelo problema relacionado à exposição. Isso deve ser visto mais comumente em todas as pesquisas epidemiológicas (Laurell et al. 1992). É relevante lembrar que enquanto no trabalho epidemiológico o objetivo da análise é a estimativa da magnitude e distribuição do risco, na pesquisa participativa, a evitabilidade do risco também é um objetivo (Loewenson e Biocca 1995). Essa complementaridade entre epidemiologia e prevenção efetiva faz parte da mensagem deste enciclopédia e deste capítulo.
Mantendo a relevância da saúde pública
Embora novos desenvolvimentos na metodologia epidemiológica, na análise de dados e na avaliação e medição da exposição (como novas técnicas de biologia molecular) sejam bem-vindos e importantes, eles também podem contribuir para uma abordagem reducionista com foco em indivíduos, e não em populações. Já foi dito que:
… a epidemiologia deixou de funcionar como parte de uma abordagem multidisciplinar para entender a causa da doença nas populações e tornou-se um conjunto de métodos genéricos para medir associações de exposição e doença em indivíduos. , históricos, políticos e outros fatores populacionais como principais causas de doenças.... A epidemiologia deve se reintegrar à saúde pública e deve redescobrir a perspectiva populacional (Pearce 1996).
Os epidemiologistas ocupacionais e ambientais têm um papel importante a desempenhar, não apenas no desenvolvimento de novos métodos epidemiológicos e aplicações para esses métodos, mas também na garantia de que esses métodos sejam sempre integrados na perspectiva populacional adequada.
Antropometria
Este artigo é uma adaptação da 3ª edição da Enciclopédia de Saúde e Segurança Ocupacional.
A antropometria é um ramo fundamental da antropologia física. Representa o aspecto quantitativo. Um amplo sistema de teorias e práticas é dedicado à definição de métodos e variáveis para relacionar os objetivos nos diferentes campos de aplicação. Nos campos da saúde ocupacional, segurança e ergonomia, os sistemas antropométricos estão preocupados principalmente com a construção, composição e constituição do corpo e com as dimensões da inter-relação do corpo humano com as dimensões do local de trabalho, máquinas, ambiente industrial e roupas.
variáveis antropométricas
Uma variável antropométrica é uma característica mensurável do corpo que pode ser definida, padronizada e referida a uma unidade de medida. As variáveis lineares são geralmente definidas por pontos de referência que podem ser rastreados com precisão até o corpo. Os pontos de referência são geralmente de dois tipos: os anatômicos esqueléticos, que podem ser encontrados e rastreados sentindo as proeminências ósseas através da pele, e os pontos de referência virtuais que são simplesmente encontrados como distâncias máximas ou mínimas usando os ramos de um paquímetro.
As variáveis antropométricas têm componentes genéticos e ambientais e podem ser usadas para definir a variabilidade individual e populacional. A escolha das variáveis deve estar relacionada ao objetivo específico da pesquisa e padronizada com outras pesquisas da mesma área, pois o número de variáveis descritas na literatura é extremamente grande, tendo sido descritas até 2,200 para o corpo humano.
As variáveis antropométricas são principalmente linear medidas, como alturas, distâncias de pontos de referência com o sujeito em pé ou sentado em postura padronizada; diâmetros, como distâncias entre marcos bilaterais; comprimentos, como distâncias entre dois marcos diferentes; medidas curvas, ou seja, arcos, como distâncias na superfície do corpo entre dois pontos de referência; e circunferências, como medidas circulares fechadas em superfícies corporais, geralmente posicionadas em pelo menos um ponto de referência ou em uma altura definida.
Outras variáveis podem exigir métodos e instrumentos especiais. Por exemplo, a espessura das dobras cutâneas é medida por meio de calibradores especiais de pressão constante. Os volumes são medidos por cálculo ou por imersão em água. Para obter informações completas sobre as características da superfície do corpo, uma matriz de computador de pontos de superfície pode ser plotada usando técnicas bioestereométricas.
Instrumentos
Embora instrumentos antropométricos sofisticados tenham sido descritos e utilizados com vistas à coleta automatizada de dados, os instrumentos antropométricos básicos são bastante simples e fáceis de usar. Muito cuidado deve ser tomado para evitar erros comuns resultantes de má interpretação de pontos de referência e posturas incorretas dos sujeitos.
O instrumento antropométrico padrão é o antropômetro - uma haste rígida de 2 metros de comprimento, com duas escalas de leitura, com as quais as dimensões verticais do corpo, como alturas de pontos de referência do chão ou do assento, e dimensões transversais, como diâmetros, podem ser medidas.
Normalmente, a haste pode ser dividida em 3 ou 4 seções que se encaixam uma na outra. Um ramal deslizante com garra reta ou curva permite medir distâncias do chão para alturas, ou de um ramal fixo para diâmetros. Antropômetros mais elaborados possuem uma única escala de alturas e diâmetros para evitar erros de escala, ou são equipados com dispositivos de leitura mecânicos ou eletrônicos digitais (figura 1).
Um estadiômetro é um antropômetro fixo, geralmente usado apenas para estatura e freqüentemente associado a uma balança de feixe de peso.
Para diâmetros transversais pode-se utilizar uma série de paquímetros: o pelvímetro para medidas até 600 mm e o cefalômetro até 300 mm. Este último é particularmente adequado para medições de cabeça quando usado em conjunto com uma bússola (figura 2).
Figura 2. Um cefalômetro junto com uma bússola
O estribo é usado para medir os pés e a cabeceira fornece coordenadas cartesianas da cabeça quando orientada no “plano de Frankfort” (um plano horizontal que passa por porção e orbital pontos de referência da cabeça). A mão pode ser medida com um paquímetro ou com um dispositivo especial composto por cinco réguas deslizantes.
A espessura da dobra cutânea é medida com um paquímetro de pressão constante, geralmente com uma pressão de 9.81 x 104 Pa (a pressão imposta por um peso de 10 g em uma área de 1 mm2).
Para arcos e perímetros, é usada uma fita de aço flexível e estreita com seção plana. As fitas de aço auto-alisantes devem ser evitadas.
Sistemas de variáveis
Um sistema de variáveis antropométricas é um conjunto coerente de medidas corporais para resolver alguns problemas específicos.
No campo da ergonomia e segurança, o principal problema é adequar os equipamentos e o espaço de trabalho aos humanos e adequar as roupas ao tamanho certo.
O equipamento e o espaço de trabalho requerem principalmente medidas lineares de membros e segmentos corporais que podem ser facilmente calculadas a partir de alturas e diâmetros de referência, enquanto os tamanhos de alfaiataria são baseados principalmente em arcos, circunferências e comprimentos de fitas flexíveis. Ambos os sistemas podem ser combinados de acordo com a necessidade.
Em qualquer caso, é absolutamente necessário ter uma referência espacial precisa para cada medição. Os pontos de referência devem, portanto, estar ligados por alturas e diâmetros e cada arco ou circunferência deve ter uma referência de ponto de referência definida. Alturas e declives devem ser indicados.
Em uma pesquisa específica, o número de variáveis deve ser limitado ao mínimo para evitar estresse indevido no sujeito e no operador.
Um conjunto básico de variáveis para o espaço de trabalho foi reduzido para 33 variáveis medidas (figura 3) mais 20 derivadas de um cálculo simples. Para uma pesquisa militar de uso geral, Hertzberg e colaboradores usam 146 variáveis. Para roupas e propósitos biológicos em geral, o Conselho de Moda Italiano (Ente Italiano della Moda) usa um conjunto de 32 variáveis de propósito geral e 28 técnicas. A norma alemã (DIN 61 516) de controle de dimensões corporais para roupas inclui 12 variáveis. A recomendação da Organização Internacional de Padronização (ISO) para antropometria inclui uma lista central de 36 variáveis (ver tabela 1). As tabelas International Data on Anthropometry publicadas pela OIT listam 19 dimensões corporais para as populações de 20 diferentes regiões do mundo (Jürgens, Aune e Pieper 1990).
Figura 3. Conjunto básico de variáveis antropométricas
Tabela 1. Lista central antropométrica básica
1.1 Alcance para frente (agarrar a mão com o sujeito em pé contra a parede)
1.2 Estatura (distância vertical do chão ao vértice da cabeça)
1.3 Altura dos olhos (do chão ao canto interno dos olhos)
1.4 Altura do ombro (do chão ao acrômio)
1.5 Altura do cotovelo (do chão à depressão radial do cotovelo)
1.6 Altura da virilha (do chão ao osso púbico)
1.7 Altura da ponta do dedo (do chão ao eixo do punho)
1.8 Largura do ombro (diâmetro biacromial)
1.9 Largura do quadril, em pé (a distância máxima entre os quadris)
2.1 Altura sentada (do assento ao vértice da cabeça)
2.2 Altura dos olhos, sentado (do assento ao canto interno do olho)
2.3 Altura do ombro, sentado (do assento ao acrômio)
2.4 Altura do cotovelo, sentado (do assento ao ponto mais baixo do cotovelo dobrado)
2.5 Altura do joelho (do apoio para os pés até a superfície superior da coxa)
2.6 Comprimento da perna (altura da superfície sentada)
2.7 Comprimento antebraço-mão (da parte de trás do cotovelo dobrado até o eixo da pegada)
2.8 Profundidade do corpo, sentado (profundidade do assento)
2.9 Comprimento nádega-joelho (da rótula até o ponto mais traseiro da nádega)
2.10 Cotovelo à largura do cotovelo (distância entre as superfícies laterais dos cotovelos)
2.11 Largura do quadril, sentado (largura do assento)
3.1 Largura do dedo indicador, proximal (na articulação entre as falanges medial e proximal)
3.2 Largura do dedo indicador, distal (na articulação entre as falanges distal e medial)
3.3 Comprimento do dedo indicador
3.4 Comprimento da mão (da ponta do dedo médio ao estiloide)
3.5 Largura da mão (nos metacarpos)
3.6 Circunferência do pulso
4.1 Largura do pé
4.2 Comprimento do pé
5.1 Circunferência térmica (na glabela)
5.2 Arco sagital (da glabela ao ínion)
5.3 Comprimento da cabeça (da glabela ao opistocrânio)
5.4 Largura da cabeça (máximo acima da orelha)
5.5 Arco Bitragion (sobre a cabeça entre as orelhas)
6.1 Circunferência da cintura (no umbigo)
6.2 Altura da tíbia (do chão ao ponto mais alto da margem ântero-medial da glenoide da tíbia)
6.3 Altura cervical sentado (até a ponta do processo espinhoso da 7ª vértebra cervical).
Fonte: Adaptado de ISO/DP 7250 1980).
Precisão e erros
A precisão das dimensões do corpo vivo deve ser considerada de maneira estocástica porque o corpo humano é altamente imprevisível, tanto como estrutura estática quanto dinâmica.
Um único indivíduo pode crescer ou mudar em musculatura e gordura; sofrem alterações esqueléticas como consequência do envelhecimento, doenças ou acidentes; ou modificar o comportamento ou a postura. Assuntos diferentes diferem por proporções, não apenas por dimensões gerais. Sujeitos de alta estatura não são meras ampliações de outros baixos; os tipos constitucionais e somatotipos provavelmente variam mais do que as dimensões gerais.
O uso de manequins, particularmente aqueles que representam os percentis padrão 5, 50 e 95 para testes de adaptação, pode ser altamente enganoso, se as variações corporais nas proporções corporais não forem levadas em consideração.
Erros resultam de má interpretação de pontos de referência e uso incorreto de instrumentos (erro pessoal), instrumentos imprecisos ou inexatos (erro instrumental) ou mudanças na postura do sujeito (erro do sujeito - este último pode ser devido a dificuldades de comunicação se o contexto cultural ou linguístico do o assunto difere daquele do operador).
tratamento estatístico
Os dados antropométricos devem ser tratados por procedimentos estatísticos, principalmente no campo dos métodos de inferência aplicando métodos univariados (média, moda, percentis, histogramas, análise de variância, etc.), bivariados (correlação, regressão) e multivariados (correlação e regressão múltiplas, análise fatorial , etc.) métodos. Vários métodos gráficos baseados em aplicações estatísticas foram concebidos para classificar os tipos humanos (antropometrogramas, morfossomatogramas).
Amostragem e pesquisa
Como os dados antropométricos não podem ser coletados para toda a população (exceto no caso raro de uma população particularmente pequena), a amostragem geralmente é necessária. Uma amostra basicamente aleatória deve ser o ponto de partida de qualquer levantamento antropométrico. Para manter o número de indivíduos medidos em um nível razoável, geralmente é necessário recorrer à amostragem estratificada em vários estágios. Isso permite a subdivisão mais homogênea da população em várias classes ou estratos.
A população pode ser subdividida por sexo, faixa etária, área geográfica, variáveis sociais, atividade física e assim por diante.
Os formulários de pesquisa devem ser projetados tendo em mente o procedimento de medição e o tratamento de dados. Um estudo ergonômico preciso do procedimento de medição deve ser feito para reduzir a fadiga do operador e possíveis erros. Por este motivo, as variáveis devem ser agrupadas de acordo com o instrumento utilizado e ordenadas em sequência de forma a reduzir o número de flexões do corpo que o operador deve realizar.
Para reduzir o efeito de erro pessoal, a pesquisa deve ser realizada por um operador. Caso seja necessário utilizar mais de um operador, é necessário treinamento para garantir a replicabilidade das medições.
Antropometria populacional
Desconsiderando o conceito altamente criticado de “raça”, as populações humanas são, no entanto, altamente variáveis em tamanho de indivíduos e em distribuição de tamanho. Geralmente as populações humanas não são estritamente mendelianas; eles são comumente o resultado da mistura. Às vezes, duas ou mais populações, com origens e adaptações diferentes, convivem na mesma área sem cruzar. Isso complica a distribuição teórica dos traços. Do ponto de vista antropométrico, os sexos são populações diferentes. Populações de empregados podem não corresponder exatamente à população biológica da mesma área em consequência de possível seleção aptitudinal ou auto-seleção por opção de trabalho.
Populações de diferentes áreas podem diferir em consequência de diferentes condições de adaptação ou estruturas biológicas e genéticas.
Quando o ajuste perfeito é importante, é necessário um levantamento em uma amostra aleatória.
Ensaios de montagem e regulamentação
A adaptação do espaço de trabalho ou equipamento ao usuário pode depender não apenas das dimensões corporais, mas também de variáveis como tolerância ao desconforto e natureza das atividades, vestimentas, ferramentas e condições ambientais. Pode ser usada uma combinação de uma lista de verificação de fatores relevantes, um simulador e uma série de testes de ajuste usando uma amostra de indivíduos escolhidos para representar a faixa de tamanhos corporais da população de usuários esperada.
O objetivo é encontrar intervalos de tolerância para todos os assuntos. Se os intervalos se sobrepõem, é possível selecionar um intervalo final mais estreito que não esteja fora dos limites de tolerância de qualquer assunto. Se não houver sobreposição, será necessário tornar a estrutura ajustável ou fornecê-la em tamanhos diferentes. Se mais de duas dimensões forem ajustáveis, um sujeito pode não ser capaz de decidir qual dos ajustes possíveis se ajustará melhor a ele.
A capacidade de ajuste pode ser uma questão complicada, especialmente quando posturas desconfortáveis resultam em fadiga. Indicações precisas devem, portanto, ser dadas ao usuário que frequentemente sabe pouco ou nada sobre suas próprias características antropométricas. Em geral, um projeto preciso deve reduzir ao mínimo a necessidade de ajuste. De qualquer forma, deve-se ter sempre em mente que se trata de antropometria, não apenas de engenharia.
antropometria dinâmica
A antropometria estática pode fornecer informações amplas sobre o movimento se um conjunto adequado de variáveis for escolhido. No entanto, quando os movimentos são complicados e um ajuste próximo ao ambiente industrial é desejável, como na maioria das interfaces usuário-máquina e homem-veículo, é necessário um levantamento exato das posturas e movimentos. Isso pode ser feito com maquetes adequadas que permitem traçar linhas de alcance ou por fotografia. Nesse caso, uma câmera equipada com uma teleobjetiva e uma haste antropométrica, posicionada no plano sagital do sujeito, permite fotografias padronizadas com pouca distorção da imagem. Pequenos rótulos nas articulações dos sujeitos possibilitam o traçado exato dos movimentos.
Outra forma de estudar os movimentos é formalizar as mudanças posturais de acordo com uma série de planos horizontais e verticais que passam pelas articulações. Novamente, o uso de modelos humanos computadorizados com sistemas de desenho assistido por computador (CAD) é uma maneira viável de incluir a antropometria dinâmica no projeto ergonômico do local de trabalho.
Introdução e Conceitos
A toxicologia mecanicista é o estudo de como agentes químicos ou físicos interagem com organismos vivos para causar toxicidade. O conhecimento do mecanismo de toxicidade de uma substância aumenta a capacidade de prevenir a toxicidade e projetar produtos químicos mais desejáveis; constitui a base para a terapia de superexposição e freqüentemente permite uma maior compreensão dos processos biológicos fundamentais. Para fins deste enciclopédia a ênfase será colocada em animais para prever a toxicidade humana. Diferentes áreas da toxicologia incluem toxicologia mecanicista, descritiva, regulatória, forense e ambiental (Klaassen, Amdur e Doull 1991). Todos eles se beneficiam da compreensão dos mecanismos fundamentais da toxicidade.
Por que entender os mecanismos de toxicidade?
Compreender o mecanismo pelo qual uma substância causa toxicidade aprimora diferentes áreas da toxicologia de maneiras diferentes. A compreensão mecanicista ajuda o regulador governamental a estabelecer limites seguros legalmente obrigatórios para a exposição humana. Ele ajuda os toxicologistas a recomendar cursos de ação em relação à limpeza ou remediação de locais contaminados e, juntamente com as propriedades físicas e químicas da substância ou mistura, pode ser usado para selecionar o grau de equipamento de proteção necessário. O conhecimento mecanicista também é útil para formar a base da terapia e o projeto de novos medicamentos para o tratamento de doenças humanas. Para o toxicologista forense, o mecanismo de toxicidade geralmente fornece informações sobre como um agente químico ou físico pode causar morte ou incapacitação.
Se o mecanismo de toxicidade for compreendido, a toxicologia descritiva torna-se útil para prever os efeitos tóxicos de produtos químicos relacionados. É importante entender, no entanto, que a falta de informações mecanísticas não impede os profissionais de saúde de proteger a saúde humana. Decisões prudentes baseadas em estudos com animais e na experiência humana são usadas para estabelecer níveis seguros de exposição. Tradicionalmente, uma margem de segurança foi estabelecida usando o “nível de nenhum efeito adverso” ou um “nível de efeito adverso mais baixo” de estudos em animais (usando projetos de exposição repetida) e dividindo esse nível por um fator de 100 para exposição ocupacional ou 1,000 para exposição ocupacional. outra exposição ambiental humana. O sucesso desse processo é evidente a partir dos poucos incidentes de efeitos adversos à saúde atribuídos à exposição a produtos químicos em trabalhadores onde os limites de exposição apropriados foram estabelecidos e respeitados no passado. Além disso, o tempo de vida humano continua a aumentar, assim como a qualidade de vida. Em geral, o uso de dados de toxicidade levou a um controle regulamentar e voluntário eficaz. O conhecimento detalhado dos mecanismos tóxicos aumentará a previsibilidade dos novos modelos de risco atualmente em desenvolvimento e resultará em melhoria contínua.
A compreensão dos mecanismos ambientais é complexa e pressupõe o conhecimento da perturbação e homeostase (equilíbrio) do ecossistema. Embora não discutido neste artigo, uma compreensão aprimorada dos mecanismos tóxicos e suas consequências finais em um ecossistema ajudaria os cientistas a tomar decisões prudentes sobre o manuseio de resíduos municipais e industriais. A gestão de resíduos é uma área de pesquisa em crescimento e continuará a ser muito importante no futuro.
Técnicas para estudar mecanismos de toxicidade
A maioria dos estudos mecanísticos começa com um estudo toxicológico descritivo em animais ou observações clínicas em humanos. Idealmente, os estudos em animais incluem observações comportamentais e clínicas cuidadosas, exame bioquímico cuidadoso de elementos do sangue e da urina para sinais de função adversa dos principais sistemas biológicos do corpo e uma avaliação post-mortem de todos os sistemas de órgãos por exame microscópico para verificar se há lesões (consulte as diretrizes de teste da OCDE; diretivas da CE sobre avaliação química; regras de teste da EPA dos EUA; regulamentos de produtos químicos do Japão). Isso é análogo a um exame físico humano completo que ocorreria em um hospital durante um período de dois a três dias, exceto para o exame post-mortem.
Compreender os mecanismos de toxicidade é a arte e a ciência da observação, criatividade na seleção de técnicas para testar várias hipóteses e integração inovadora de sinais e sintomas em uma relação causal. Os estudos mecanísticos começam com a exposição, seguem a distribuição relacionada ao tempo e o destino no corpo (farmacocinética) e medem o efeito tóxico resultante em algum nível do sistema e em algum nível de dose. Diferentes substâncias podem atuar em diferentes níveis do sistema biológico causando toxicidade.
Exposição
A rota de exposição em estudos mecanísticos é geralmente a mesma da exposição humana. A rota é importante porque pode haver efeitos que ocorrem localmente no local da exposição, além de efeitos sistêmicos após a substância química ter sido absorvida pelo sangue e distribuída por todo o corpo. Um exemplo simples, mas convincente, de um efeito local seria a irritação e eventual corrosão da pele após a aplicação de soluções ácidas ou alcalinas fortes projetadas para limpar superfícies duras. Da mesma forma, irritação e morte celular podem ocorrer nas células que revestem o nariz e/ou os pulmões após a exposição a vapores ou gases irritantes, como óxidos de nitrogênio ou ozônio. (Ambos são constituintes da poluição do ar, ou smog). Após a absorção de um produto químico no sangue através da pele, pulmões ou trato gastrointestinal, a concentração em qualquer órgão ou tecido é controlada por muitos fatores que determinam a farmacocinética do produto químico no corpo. O corpo tem a capacidade de ativar e desintoxicar vários produtos químicos, conforme observado abaixo.
Papel da Farmacocinética na Toxicidade
A farmacocinética descreve as relações de tempo para absorção química, distribuição, metabolismo (alterações bioquímicas no corpo) e eliminação ou excreção do corpo. Em relação aos mecanismos de toxicidade, essas variáveis farmacocinéticas podem ser muito importantes e, em alguns casos, determinar se a toxicidade ocorrerá ou não. Por exemplo, se um material não for absorvido em quantidade suficiente, não ocorrerá toxicidade sistêmica (dentro do corpo). Por outro lado, um produto químico altamente reativo que é desintoxicado rapidamente (segundos ou minutos) por enzimas digestivas ou hepáticas pode não ter tempo para causar toxicidade. Algumas substâncias e misturas halogenadas policíclicas, bem como certos metais como o chumbo, não causariam toxicidade significativa se a excreção fosse rápida; mas o acúmulo em níveis suficientemente altos determina sua toxicidade, uma vez que a excreção não é rápida (às vezes medida em anos). Felizmente, a maioria dos produtos químicos não tem uma retenção tão longa no corpo. A acumulação de um material inócuo ainda não induziria toxicidade. A taxa de eliminação do corpo e desintoxicação é frequentemente referida como a meia-vida do produto químico, que é o tempo para 50% do produto químico ser excretado ou alterado para uma forma não tóxica.
No entanto, se um produto químico se acumula em uma determinada célula ou órgão, isso pode sinalizar um motivo para examinar mais detalhadamente sua potencial toxicidade nesse órgão. Mais recentemente, modelos matemáticos foram desenvolvidos para extrapolar variáveis farmacocinéticas de animais para humanos. Esses modelos farmacocinéticos são extremamente úteis para gerar hipóteses e testar se o animal experimental pode ser uma boa representação para humanos. Numerosos capítulos e textos foram escritos sobre este assunto (Gehring et al. 1976; Reitz et al. 1987; Nolan et al. 1995). Um exemplo simplificado de um modelo fisiológico é representado na figura 1.
Figura 1. Um modelo farmacocinético simplificado
Diferentes níveis e sistemas podem ser afetados adversamente
A toxicidade pode ser descrita em diferentes níveis biológicos. A lesão pode ser avaliada na pessoa como um todo (ou animal), no sistema orgânico, na célula ou na molécula. Os sistemas de órgãos incluem os sistemas imunológico, respiratório, cardiovascular, renal, endócrino, digestivo, musculoesquelético, sanguíneo, reprodutivo e nervoso central. Alguns órgãos-chave incluem o fígado, rim, pulmão, cérebro, pele, olhos, coração, testículos ou ovários e outros órgãos importantes. No nível celular/bioquímico, os efeitos adversos incluem interferência com a função normal da proteína, função do receptor endócrino, inibição da energia metabólica ou inibição ou indução de enzimas xenobióticas (substâncias estranhas). Os efeitos adversos no nível molecular incluem alteração da função normal da transcrição do DNA-RNA, da ligação específica do receptor citoplasmático e nuclear e dos genes ou produtos gênicos. Em última análise, a disfunção em um sistema de órgão principal é provavelmente causada por uma alteração molecular em uma célula-alvo específica dentro desse órgão. No entanto, nem sempre é possível rastrear um mecanismo de volta a uma origem molecular de causalidade, nem é necessário. A intervenção e a terapia podem ser planejadas sem uma compreensão completa do alvo molecular. No entanto, o conhecimento sobre o mecanismo específico de toxicidade aumenta o valor preditivo e a precisão da extrapolação para outros produtos químicos. A Figura 2 é uma representação esquemática dos vários níveis onde a interferência de processos fisiológicos normais pode ser detectada. As setas indicam que as consequências para um indivíduo podem ser determinadas de cima para baixo (exposição, farmacocinética à toxicidade do sistema/órgão) ou de baixo para cima (alteração molecular, efeito celular/bioquímico para toxicidade do sistema/órgão).
Figura 2. Representação dos mecanismos de toxicidade
Exemplos de Mecanismos de Toxicidade
Os mecanismos de toxicidade podem ser diretos ou muito complexos. Freqüentemente, há uma diferença entre o tipo de toxicidade, o mecanismo de toxicidade e o nível do efeito, relacionado a se os efeitos adversos são devidos a uma única dose aguda alta (como um envenenamento acidental) ou a uma dose mais baixa exposição repetida (de exposição ocupacional ou ambiental). Classicamente, para fins de teste, uma dose única alta aguda é administrada por intubação direta no estômago de um roedor ou exposição a uma atmosfera de gás ou vapor por duas a quatro horas, o que melhor se assemelhar à exposição humana. Os animais são observados durante um período de duas semanas após a exposição e, em seguida, os principais órgãos externos e internos são examinados quanto a lesões. O teste de dose repetida varia de meses a anos. Para espécies de roedores, dois anos é considerado um estudo crônico (durante toda a vida) suficiente para avaliar toxicidade e carcinogenicidade, enquanto para primatas não humanos, dois anos seriam considerados um estudo subcrônico (menos que uma vida inteira) para avaliar toxicidade de dose repetida. Após a exposição, é realizado um exame completo de todos os tecidos, órgãos e fluidos para determinar quaisquer efeitos adversos.
Mecanismos de Toxicidade Aguda
Os exemplos a seguir são específicos para efeitos agudos de altas doses que podem levar à morte ou incapacitação grave. No entanto, em alguns casos, a intervenção resultará em efeitos transitórios e totalmente reversíveis. A dose ou gravidade da exposição determinará o resultado.
Asfixiantes simples. O mecanismo de toxicidade para gases inertes e algumas outras substâncias não reativas é a falta de oxigênio (anoxia). Esses produtos químicos, que causam privação de oxigênio no sistema nervoso central (SNC), são denominados asfixiantes simples. Se uma pessoa entra em um espaço fechado que contém nitrogênio sem oxigênio suficiente, ocorre uma depleção imediata de oxigênio no cérebro e leva à inconsciência e eventual morte se a pessoa não for removida rapidamente. Em casos extremos (próximo de oxigênio zero), a inconsciência pode ocorrer em poucos segundos. O resgate depende da rápida remoção para um ambiente oxigenado. A sobrevida com dano cerebral irreversível pode ocorrer a partir do resgate tardio, devido à morte de neurônios, que não conseguem se regenerar.
Asfixiantes químicos. O monóxido de carbono (CO) compete com o oxigênio pela ligação à hemoglobina (nos glóbulos vermelhos) e, portanto, priva os tecidos de oxigênio para o metabolismo energético; morte celular pode resultar. A intervenção inclui a remoção da fonte de CO e o tratamento com oxigênio. O uso direto do oxigênio é baseado na ação tóxica do CO. Outro potente asfixiante químico é o cianeto. O íon cianeto interfere no metabolismo celular e na utilização de oxigênio para energia. O tratamento com nitrito de sódio provoca uma alteração da hemoglobina nos glóbulos vermelhos para metahemoglobina. A metahemoglobina tem maior afinidade de ligação com o íon cianeto do que o alvo celular do cianeto. Consequentemente, a metahemoglobina se liga ao cianeto e mantém o cianeto longe das células-alvo. Isso forma a base para a terapia antídoto.
Depressores do sistema nervoso central (SNC). A toxicidade aguda é caracterizada por sedação ou inconsciência para uma série de materiais como solventes que não são reativos ou que são transformados em intermediários reativos. Supõe-se que a sedação/anestesia se deva a uma interação do solvente com as membranas das células do SNC, o que prejudica sua capacidade de transmitir sinais elétricos e químicos. Embora a sedação possa parecer uma forma leve de toxicidade e tenha sido a base para o desenvolvimento dos primeiros anestésicos, “a dose ainda faz o veneno”. Se uma dose suficiente for administrada por ingestão ou inalação, o animal pode morrer devido a parada respiratória. Se a morte anestésica não ocorrer, esse tipo de toxicidade geralmente é prontamente reversível quando o indivíduo é removido do ambiente ou o produto químico é redistribuído ou eliminado do corpo.
Efeitos de pele. Os efeitos adversos na pele podem variar de irritação a corrosão, dependendo da substância encontrada. Ácidos fortes e soluções alcalinas são incompatíveis com tecidos vivos e são corrosivos, causando queimaduras químicas e possíveis cicatrizes. A cicatrização ocorre devido à morte das células dérmicas profundas da pele, responsáveis pela regeneração. Concentrações mais baixas podem apenas causar irritação da primeira camada da pele.
Outro mecanismo tóxico específico da pele é o da sensibilização química. Por exemplo, a sensibilização ocorre quando o 2,4-dinitroclorobenzeno se liga a proteínas naturais da pele e o sistema imunológico reconhece o complexo ligado à proteína alterado como um material estranho. Ao responder a esse material estranho, o sistema imunológico ativa células especiais para eliminar a substância estranha por meio da liberação de mediadores (citocinas) que causam erupção cutânea ou dermatite (consulte “Imunotoxicologia”). Esta é a mesma reação do sistema imunológico quando ocorre a exposição à hera venenosa. A sensibilização imune é muito específica para o produto químico em particular e leva pelo menos duas exposições antes que uma resposta seja eliciada. A primeira exposição sensibiliza (configura as células para reconhecer o produto químico) e as exposições subsequentes desencadeiam a resposta do sistema imunológico. A remoção do contato e a terapia sintomática com cremes anti-inflamatórios contendo esteróides geralmente são eficazes no tratamento de indivíduos sensibilizados. Em casos graves ou refratários, um imunossupressor de ação sistêmica, como a prednisona, é usado em conjunto com o tratamento tópico.
Sensibilização pulmonar. Uma resposta de sensibilização imune é provocada por diisocianato de tolueno (TDI), mas o local-alvo são os pulmões. A superexposição ao TDI em indivíduos suscetíveis causa edema pulmonar (acúmulo de líquido), constrição brônquica e respiração prejudicada. Esta é uma condição séria e requer a remoção do indivíduo de possíveis exposições subsequentes. O tratamento é principalmente sintomático. A sensibilização da pele e dos pulmões segue uma resposta à dose. Exceder o nível estabelecido para exposição ocupacional pode causar efeitos adversos.
Efeitos oculares. As lesões oculares variam desde o avermelhamento da camada externa (vermelhidão da piscina) até a formação de catarata da córnea e danos à íris (parte colorida do olho). Os testes de irritação ocular são realizados quando se acredita que não ocorrerão ferimentos graves. Muitos dos mecanismos que causam a corrosão da pele também podem causar lesões nos olhos. Materiais corrosivos à pele, como ácidos fortes (pH menor que 2) e álcalis (pH maior que 11.5), não são testados nos olhos de animais porque a maioria causará corrosão e cegueira devido a um mecanismo semelhante ao que causa a corrosão da pele . Além disso, agentes ativos de superfície, como detergentes e surfactantes, podem causar lesões oculares, desde irritação até corrosão. Um grupo de materiais que requer cautela são os surfactantes carregados positivamente (catiônicos), que podem causar queimaduras, opacidade permanente da córnea e vascularização (formação de vasos sanguíneos). Outra substância química, o dinitrofenol, tem um efeito específico na formação de catarata. Isso parece estar relacionado à concentração dessa substância química no olho, que é um exemplo de especificidade de distribuição farmacocinética.
Embora a lista acima esteja longe de ser exaustiva, ela é projetada para dar ao leitor uma apreciação de vários mecanismos de toxicidade aguda.
Mecanismos de Toxicidade Subcrônica e Crônica
Quando administrados em dose alta única, alguns produtos químicos não apresentam o mesmo mecanismo de toxicidade de quando administrados repetidamente em doses menores, mas ainda tóxicas. Quando uma única dose alta é administrada, há sempre a possibilidade de exceder a capacidade da pessoa de desintoxicar ou excretar o produto químico, e isso pode levar a uma resposta tóxica diferente do que quando doses repetidas mais baixas são administradas. O álcool é um bom exemplo. Altas doses de álcool levam a efeitos primários no sistema nervoso central, enquanto baixas doses repetitivas resultam em lesão hepática.
Inibição da anticolinesterase. A maioria dos pesticidas organofosforados, por exemplo, tem pouca toxicidade para mamíferos até que sejam metabolicamente ativados, principalmente no fígado. O principal mecanismo de ação dos organofosforados é a inibição da acetilcolinesterase (AChE) no cérebro e no sistema nervoso periférico. AChE é a enzima normal que termina a estimulação do neurotransmissor acetilcolina. A leve inibição da AChE por um período prolongado não foi associada a efeitos adversos. Em altos níveis de exposição, a incapacidade de terminar esta estimulação neuronal resulta em superestimulação do sistema nervoso colinérgico. A superestimulação colinérgica acaba resultando em uma série de sintomas, incluindo parada respiratória, seguida de morte se não for tratada. O tratamento primário é a administração de atropina, que bloqueia os efeitos da acetilcolina, e a administração de cloreto de pralidoxima, que reativa a AChE inibida. Portanto, tanto a causa quanto o tratamento da toxicidade do organofosforado são abordados pela compreensão da base bioquímica da toxicidade.
ativação metabólica. Muitos produtos químicos, incluindo tetracloreto de carbono, clorofórmio, acetilaminofluoreno, nitrosaminas e paraquat são metabolicamente ativados em radicais livres ou outros intermediários reativos que inibem e interferem na função celular normal. Em altos níveis de exposição, isso resulta em morte celular (consulte “Lesão celular e morte celular”). Embora as interações específicas e os alvos celulares permaneçam desconhecidos, os sistemas de órgãos que têm a capacidade de ativar essas substâncias químicas, como fígado, rim e pulmão, são todos alvos potenciais para lesões. Especificamente, determinadas células dentro de um órgão têm uma capacidade maior ou menor de ativar ou desintoxicar esses intermediários, e essa capacidade determina a suscetibilidade intracelular dentro de um órgão. O metabolismo é uma das razões pelas quais a compreensão da farmacocinética, que descreve esses tipos de transformações e a distribuição e eliminação desses intermediários, é importante para reconhecer o mecanismo de ação desses produtos químicos.
Mecanismos do câncer. O câncer é uma multiplicidade de doenças e, embora a compreensão de certos tipos de câncer esteja aumentando rapidamente devido às muitas técnicas de biologia molecular desenvolvidas desde 1980, ainda há muito a aprender. No entanto, está claro que o desenvolvimento do câncer é um processo de vários estágios, e genes críticos são a chave para diferentes tipos de câncer. Alterações no DNA (mutações somáticas) em vários desses genes críticos podem causar aumento da suscetibilidade ou lesões cancerígenas (consulte “Toxicologia genética”). A exposição a produtos químicos naturais (em alimentos cozidos como carne e peixe) ou produtos químicos sintéticos (como benzidina, usada como corante) ou agentes físicos (luz ultravioleta do sol, radônio do solo, radiação gama de procedimentos médicos ou atividades industriais) são todos contribuintes para mutações genéticas somáticas. No entanto, existem substâncias naturais e sintéticas (como antioxidantes) e processos de reparo do DNA que são protetores e mantêm a homeostase. É claro que a genética é um fator importante no câncer, uma vez que síndromes de doenças genéticas como xeroderma pigmentoso, onde há uma falta de reparo normal do DNA, aumentam dramaticamente a suscetibilidade ao câncer de pele devido à exposição à luz ultravioleta do sol.
Mecanismos reprodutivos. Semelhante ao câncer, muitos mecanismos de toxicidade reprodutiva e/ou de desenvolvimento são conhecidos, mas há muito a ser aprendido. Sabe-se que certos vírus (como a rubéola), infecções bacterianas e medicamentos (como a talidomida e a vitamina A) afetarão adversamente o desenvolvimento. Recentemente, o trabalho de Khera (1991), revisado por Carney (1994), mostra boas evidências de que os efeitos anormais no desenvolvimento em testes com animais com etileno glicol são atribuíveis a metabólitos ácidos metabólicos maternos. Isso ocorre quando o etileno glicol é metabolizado em metabólitos ácidos, incluindo ácido glicólico e oxálico. Os efeitos subsequentes na placenta e no feto parecem ser devidos a este processo de intoxicação metabólica.
Conclusão
A intenção deste artigo é dar uma perspectiva sobre vários mecanismos conhecidos de toxicidade e a necessidade de estudos futuros. É importante entender que o conhecimento mecanicista não é absolutamente necessário para proteger a saúde humana ou ambiental. Esse conhecimento aumentará a capacidade do profissional de prever e gerenciar melhor a toxicidade. As técnicas reais usadas na elucidação de qualquer mecanismo particular dependem do conhecimento coletivo dos cientistas e do pensamento daqueles que tomam decisões sobre a saúde humana.
Avaliação de exposição
A avaliação das exposições é uma etapa crítica na identificação de riscos no local de trabalho por meio de investigação epidemiológica. O processo de avaliação da exposição pode ser subdividido em uma série de atividades. Esses incluem:
- compilar um inventário de agentes e misturas potencialmente tóxicos presentes no ambiente de trabalho visado
- determinar como as exposições ocorrem e qual a probabilidade de elas variarem entre os funcionários
- selecionar medidas ou índices apropriados para quantificar as exposições
- coletar dados que permitirão que os participantes do estudo recebam valores de exposição qualitativos ou quantitativos para cada medida. Sempre que possível, essas atividades devem ser realizadas sob a orientação de um higienista industrial qualificado.
Estudos de saúde ocupacional são frequentemente criticados por causa de inadequações na avaliação de exposições. As inadequações podem levar a uma classificação incorreta diferencial ou não diferencial da exposição e subsequente viés ou perda de precisão nas análises do efeito da exposição. Esforços para melhorar a situação são evidenciados por várias conferências internacionais recentes e textos dedicados a este tópico (ACGIH 1991; Armstrong et al. 1992; Proceedings of the Conference on Retrospective Assessment of Occupational Exposures in Epidemiology 1995). Claramente, os desenvolvimentos técnicos estão oferecendo novas oportunidades para o avanço da avaliação da exposição. Esses desenvolvimentos incluem melhorias na instrumentação analítica, uma melhor compreensão dos processos farmacocinéticos e a descoberta de novos biomarcadores de exposição. Como os estudos de saúde ocupacional geralmente dependem de informações históricas de exposição para as quais nenhum monitoramento específico teria sido realizado, a necessidade de avaliação retrospectiva da exposição acrescenta uma dimensão adicional de complexidade a esses estudos. No entanto, padrões aprimorados para avaliação e para garantir a confiabilidade de tais avaliações continuam a ser desenvolvidos (Siemiatycki et al. 1986). As avaliações de exposição prospectiva, é claro, podem ser mais facilmente validadas.
O termo exposição refere-se à concentração de um agente na fronteira entre o indivíduo e o ambiente. A exposição é normalmente presumida quando se sabe que um agente está presente em um ambiente de trabalho e há uma expectativa razoável de contato do funcionário com esse agente. As exposições podem ser expressas como uma concentração média ponderada no tempo (TWA) de 8 horas, que é uma medida da intensidade da exposição calculada em média durante um turno de trabalho de 8 horas. As concentrações máximas são intensidades médias em períodos de tempo mais curtos, como 15 minutos. A exposição cumulativa é uma medida do produto da intensidade e duração médias (por exemplo, uma concentração média de TWA de 8 horas multiplicada pelos anos trabalhados nessa concentração média). Dependendo da natureza do estudo e dos resultados de saúde de interesse, a avaliação do pico, intensidade média, exposições cumulativas ou retardadas pode ser desejável.
Em contraste, dosar refere-se à deposição ou absorção de um agente por unidade de tempo. A dose ou ingestão diária de um agente pode ser estimada combinando dados de medição ambiental com suposições padrão relacionadas, entre outros fatores, taxas de respiração e penetração dérmica. Alternativamente, a ingestão pode ser estimada com base em dados de biomonitoramento. A dose idealmente seria medida no órgão alvo de interesse.
Fatores importantes de avaliação da exposição incluem:
- identificação dos agentes relevantes
- determinação de sua presença e concentrações em meios ambientais apropriados (por exemplo, ar, superfícies de contato)
- avaliação das vias de entrada prováveis (inalação, absorção cutânea, ingestão), duração da exposição (variação diária) e duração cumulativa da exposição expressa em semanas, meses ou anos
- avaliação da eficácia dos controles de engenharia e pessoais (por exemplo, o uso de roupas de proteção e proteção respiratória pode mediar as exposições) e, finalmente
- hospedeiro e outras considerações que podem modular as concentrações de órgãos-alvo.
Estes incluem o nível físico da atividade de trabalho e o estado de saúde anterior dos indivíduos. Cuidados especiais devem ser tomados na avaliação da exposição a agentes que são persistentes ou tendem a bioacumular (por exemplo, certos metais, radionuclídeos ou compostos orgânicos estáveis). Com esses materiais, as cargas corporais internas podem aumentar insidiosamente mesmo quando as concentrações ambientais parecem ser baixas.
Embora a situação possa ser bastante complexa, muitas vezes não é. Certamente, muitas contribuições valiosas para a identificação de riscos ocupacionais vieram de estudos que usam abordagens de bom senso para avaliação de exposição. Fontes de informação que podem ser úteis na identificação e categorização de exposições incluem:
- entrevistas com funcionários
- pessoal do empregador e registros de produção (incluem registros de trabalho, descrições de trabalho, histórico de instalações e processos e inventários de produtos químicos)
- Julgamento perito
- registros de higiene industrial (monitoramento de área, pessoal e conformidade e amostras de limpeza de superfície, juntamente com riscos à saúde ou relatórios de pesquisa abrangentes)
- entrevistas com funcionários antigos ou aposentados e
- dados de biomonitoramento.
Existem várias vantagens em categorizar as exposições individuais com o máximo de detalhes possível. Claramente, a informatividade de um estudo será aprimorada na medida em que as exposições relevantes forem adequadamente descritas. Em segundo lugar, a credibilidade dos resultados pode ser aumentada porque o potencial de confusão pode ser abordado de forma mais satisfatória. Por exemplo, referentes e indivíduos expostos irão diferir quanto ao status de exposição, mas também podem diferir em relação a outros fatores explicativos medidos e não medidos para a doença de interesse. No entanto, se um gradiente de exposição puder ser estabelecido na população do estudo, é menos provável que o mesmo grau de confusão persista nos subgrupos de exposição, fortalecendo assim os achados gerais do estudo.
Matrizes de Exposição de Trabalho
Uma das abordagens mais práticas e frequentemente usadas para avaliar a exposição tem sido estimar as exposições indiretamente com base nos cargos. O uso de matrizes de exposição de trabalho pode ser eficaz quando históricos de trabalho completos estão disponíveis e há uma constância razoável tanto nas tarefas quanto nas exposições associadas aos trabalhos em estudo. Em uma escala mais ampla, os agrupamentos padrão de cargos e setores foram elaborados a partir de dados de censos coletados rotineiramente ou dados ocupacionais fornecidos em atestados de óbito. Infelizmente, as informações mantidas nesses grandes sistemas de registro geralmente se limitam à ocupação “atual” ou “normal”. Além disso, como os agrupamentos padrão não levam em consideração as condições presentes em locais de trabalho específicos, eles geralmente devem ser considerados como substitutos brutos da exposição.
Para estudos de caso-controle baseados na comunidade e em registros, uma avaliação de exposição mais detalhada foi obtida utilizando a opinião de especialistas para traduzir os dados do histórico de trabalho obtidos por meio de entrevistas pessoais em avaliações semiquantitativas de prováveis exposições a agentes específicos (Siemiatycki et al. 1986 ). Especialistas, como químicos e higienistas industriais, são escolhidos para auxiliar na avaliação da exposição devido ao seu conhecimento e familiaridade com vários processos industriais. Ao combinar os dados detalhados do questionário com o conhecimento dos processos industriais, esta abordagem tem sido útil para caracterizar as diferenças de exposição nas instalações de trabalho.
A abordagem da matriz de exposição ao trabalho também foi empregada com sucesso em estudos específicos da indústria e da empresa (Gamble e Spirtas 1976). Históricos de cargos individuais (uma lista cronológica de departamentos anteriores e atribuições de cargos para cada funcionário) geralmente são mantidos nos arquivos pessoais da empresa e, quando disponíveis, fornecem um histórico completo de cargos para os funcionários enquanto eles trabalham naquela instalação. Esses dados podem ser ampliados por meio de entrevistas pessoais com os participantes do estudo. O próximo passo é inventariar todos os cargos e designações de departamento ou área de trabalho usados durante o período de estudo. Estes podem facilmente chegar a centenas ou mesmo milhares dentro de grandes instalações de multiprocessos ou entre empresas dentro de uma indústria, quando produção, manutenção, pesquisa, engenharia, serviços de suporte de fábrica e trabalhos administrativos são considerados ao longo do tempo (muitas vezes várias décadas), permitindo mudanças nos processos industriais. A consolidação de dados pode ser facilitada criando um arquivo de computador com todos os registros do histórico de trabalho e, em seguida, usando rotinas de edição para padronizar a terminologia do cargo. Esses trabalhos que envolvem exposições relativamente homogêneas podem ser combinados para simplificar o processo de vinculação de exposições a trabalhos individuais. No entanto, o agrupamento de empregos e locais de trabalho deve ser apoiado, sempre que possível, por dados de medição coletados de acordo com uma estratégia de amostragem sólida.
Mesmo com históricos de trabalho computadorizados, a ligação retrospectiva de dados de exposição a indivíduos pode ser uma tarefa difícil. Certamente, as condições do local de trabalho serão alteradas à medida que as tecnologias mudarem, a demanda do produto mudar e novas regulamentações forem implementadas. Também pode haver mudanças nas formulações de produtos e padrões sazonais de produção em muitas indústrias. Registros permanentes podem ser mantidos em relação a algumas mudanças. No entanto, é menos provável que os registros sejam retidos em relação a processos sazonais e outros processos marginais e mudanças na produção. Os funcionários também podem ser treinados para executar vários trabalhos e, em seguida, alternar entre os trabalhos à medida que as demandas da produção mudam. Todas essas circunstâncias adicionam complexidade aos perfis de exposição dos funcionários. No entanto, também existem configurações de trabalho que permaneceram relativamente inalteradas por muitos anos. Em última análise, cada ambiente de trabalho deve ser avaliado por si só.
Em última análise, será necessário resumir o histórico de exposição da vida profissional de cada pessoa em um estudo. Foi demonstrada uma influência considerável nas medidas finais de exposição-efeito de risco (Suarez-Almazor et al. 1992), e, portanto, deve-se ter muito cuidado ao selecionar a medida resumida de exposição mais apropriada.
Higiene Industrial - Medição Ambiental
O monitoramento das exposições no trabalho é uma atividade contínua fundamental na proteção da saúde dos funcionários. Assim, os registros de higiene industrial podem já existir no momento em que um estudo epidemiológico está sendo planejado. Nesse caso, esses dados devem ser revisados para determinar o quão bem a população-alvo foi coberta, quantos anos de dados estão representados nos arquivos e com que facilidade as medições podem ser vinculadas a empregos, áreas de trabalho e indivíduos. Essas determinações serão úteis tanto na avaliação da viabilidade do estudo epidemiológico quanto na identificação de lacunas de dados que podem ser remediadas com amostragem de exposição adicional.
A questão da melhor forma de vincular os dados de medição a trabalhos e indivíduos específicos é particularmente importante. A amostragem de área e zona respiratória pode ser útil para higienistas industriais na identificação de fontes de emissão para ações corretivas, mas pode ser menos útil na caracterização de exposições reais de funcionários, a menos que estudos cuidadosos de tempo das atividades de trabalho dos funcionários tenham sido realizados. Por exemplo, o monitoramento contínuo da área pode identificar exposições a excursões em determinados momentos do dia, mas permanece a dúvida se os funcionários estavam ou não na área de trabalho naquele momento.
Os dados de amostragem pessoal geralmente fornecem estimativas mais precisas da exposição do funcionário, desde que a amostragem seja realizada em condições representativas, o uso de equipamentos de proteção individual seja devidamente levado em consideração e as tarefas de trabalho e as condições do processo sejam relativamente constantes no dia a dia. Amostras pessoais podem ser prontamente vinculadas ao funcionário individual por meio do uso de identificadores pessoais. Esses dados podem ser generalizados para outros funcionários nas mesmas funções e para outros períodos de tempo, conforme justificado. No entanto, com base em sua própria experiência, Rappaport et al. (1993) advertiram que as concentrações de exposição podem ser altamente variáveis, mesmo entre funcionários designados para o que são considerados grupos de exposição homogêneos. Mais uma vez, o julgamento de especialistas é necessário para decidir se grupos de exposição homogêneos podem ou não ser presumidos.
Os pesquisadores combinaram com sucesso uma abordagem de matriz de exposição de trabalho com a utilização de dados de medição ambiental para estimar as exposições dentro das células da matriz. Quando faltam dados de medição, pode ser possível preencher as lacunas de dados por meio do uso de modelagem de exposição. Geralmente, isso envolve o desenvolvimento de um modelo para relacionar concentrações ambientais a determinantes mais facilmente avaliados de concentrações de exposição (por exemplo, volumes de produção, características físicas da instalação, incluindo o uso de sistemas de ventilação de exaustão, volatilidade do agente e natureza da atividade de trabalho). O modelo é construído para ambientes de trabalho com concentrações ambientais conhecidas e, em seguida, usado para estimar concentrações em ambientes de trabalho semelhantes sem dados de medição, mas com informações sobre parâmetros como ingredientes constituintes e volumes de produção. Esta abordagem pode ser particularmente útil para a estimativa retrospectiva de exposições.
Outra questão importante de avaliação é o tratamento da exposição a misturas. Primeiro, do ponto de vista analítico, a detecção separada de compostos quimicamente relacionados e a eliminação de interferências de outras substâncias presentes na amostra podem não estar dentro da capacidade do procedimento analítico. As várias limitações nos procedimentos analíticos usados para fornecer dados de medição precisam ser avaliadas e os objetivos do estudo modificados de acordo. Em segundo lugar, pode ser que certos agentes sejam quase sempre usados em conjunto e, portanto, ocorram aproximadamente nas mesmas proporções relativas em todo o ambiente de trabalho em estudo. Nesta situação, as análises estatísticas internas per se não será útil para distinguir se os efeitos são ou não devidos a um ou a outros agentes ou devido a uma combinação dos agentes. Tais julgamentos só seriam possíveis com base na revisão de estudos externos nos quais as mesmas combinações de agentes não tivessem ocorrido. Finalmente, em situações em que diferentes materiais são usados de forma intercambiável dependendo das especificações do produto (por exemplo, o uso de diferentes corantes para obter contrastes de cores desejados), pode ser impossível atribuir efeitos a qualquer agente específico.
Monitoramento Biológico
Biomarcadores são alterações moleculares, bioquímicas ou celulares que podem ser medidas em meios biológicos como tecidos, células ou fluidos humanos. A principal razão para o desenvolvimento de biomarcadores de exposição é fornecer uma estimativa da dose interna para um determinado agente. Essa abordagem é especialmente útil quando são prováveis várias vias de exposição (por exemplo, inalação e absorção pela pele), quando o equipamento de proteção é usado de forma intermitente ou quando as condições de exposição são imprevisíveis. O biomonitoramento pode ser especialmente vantajoso quando se sabe que os agentes de interesse têm meias-vidas biológicas relativamente longas. De uma perspectiva estatística, uma vantagem do monitoramento biológico sobre o monitoramento do ar pode ser vista com agentes tendo uma meia-vida tão curta quanto dez horas, dependendo do grau de variabilidade ambiental (Droz e Wu 1991). As meias-vidas extremamente longas de materiais como dioxinas cloradas (medidas em anos) tornam esses compostos candidatos ideais para monitoramento biológico. Tal como acontece com os métodos analíticos para medir as concentrações de ar, deve-se estar ciente de possíveis interferências. Por exemplo, antes de utilizar um determinado metabólito como biomarcador, deve-se determinar se outras substâncias comuns, como as contidas em certos medicamentos e na fumaça do cigarro, podem ou não ser metabolizadas até o mesmo ponto final. Em geral, o conhecimento básico da farmacocinética de um agente é necessário antes que o monitoramento biológico seja utilizado como base para a avaliação da exposição.
Os pontos de medição mais frequentes incluem ar alveolar, urina e sangue. Amostras de ar alveolar podem ser úteis na caracterização de altas exposições a solventes de curto prazo que ocorreram dentro de minutos ou horas após a coleta da amostra. Amostras urinárias são normalmente coletadas para determinar as taxas de excreção de metabólitos do composto de interesse. Amostras de sangue podem ser coletadas para medição direta do composto, para medição de metabólitos ou para determinação de proteínas ou adutos de DNA (por exemplo, adutos de albumina ou hemoglobina e adutos de DNA em linfócitos circulantes). Células de tecidos acessíveis, como células epiteliais da área bucal da boca, também podem ser amostradas para identificação de adutos de DNA.
A determinação da atividade da colinesterase nas hemácias e no plasma exemplifica o uso de alterações bioquímicas como medida de exposição. Os pesticidas organofosforados inibem a atividade da colinesterase e, portanto, a medição dessa atividade antes e depois da provável exposição a esses compostos pode ser um indicador útil da intensidade da exposição. No entanto, à medida que se avança no espectro das alterações biológicas, torna-se mais difícil distinguir entre os biomarcadores de exposição e os de efeito. Em geral, as medidas de efeito tendem a ser inespecíficas para a substância de interesse e, portanto, outras possíveis explicações do efeito podem precisar ser avaliadas para apoiar o uso desse parâmetro como uma medida de exposição. As medidas de exposição devem estar diretamente vinculadas ao agente de interesse ou deve haver uma base sólida para vincular qualquer medida indireta ao agente. Apesar dessas qualificações, o monitoramento biológico é muito promissor como meio de melhorar a avaliação da exposição em apoio a estudos epidemiológicos.
Conclusões
Ao fazer comparações em estudos de epidemiologia ocupacional, a necessidade é ter um grupo de trabalhadores com exposição para comparar com um grupo de trabalhadores sem exposição. Essas distinções são grosseiras, mas podem ser úteis na identificação de áreas problemáticas. Claramente, no entanto, quanto mais refinada a medida de exposição, mais útil será o estudo, especificamente em termos de sua capacidade de identificar e desenvolver programas de intervenção direcionados adequadamente.
trabalho muscular
Trabalho Muscular em Atividades Ocupacionais
Nos países industrializados, cerca de 20% dos trabalhadores ainda estão empregados em empregos que exigem esforço muscular (Rutenfranz et al. 1990). O número de trabalhos físicos pesados convencionais diminuiu, mas, por outro lado, muitos trabalhos tornaram-se mais estáticos, assimétricos e estacionários. Nos países em desenvolvimento, o trabalho muscular de todas as formas ainda é muito comum.
O trabalho muscular em atividades ocupacionais pode ser dividido em quatro grupos: trabalho muscular dinâmico pesado, manuseio manual de materiais, trabalho estático e trabalho repetitivo. Tarefas de trabalho dinâmicas pesadas são encontradas na silvicultura, agricultura e indústria da construção, por exemplo. O manuseio de materiais é comum, por exemplo, em enfermagem, transporte e armazenamento, enquanto as cargas estáticas existem no trabalho de escritório, na indústria eletrônica e nas tarefas de reparo e manutenção. Tarefas de trabalho repetitivas podem ser encontradas nas indústrias alimentícia e de processamento de madeira, por exemplo.
É importante notar que o manuseio manual de materiais e o trabalho repetitivo são basicamente trabalhos musculares dinâmicos ou estáticos, ou uma combinação dos dois.
Fisiologia do Trabalho Muscular
Trabalho muscular dinâmico
No trabalho dinâmico, os músculos esqueléticos ativos se contraem e relaxam ritmicamente. O fluxo sanguíneo para os músculos é aumentado para corresponder às necessidades metabólicas. O aumento do fluxo sanguíneo é obtido através do aumento do bombeamento do coração (débito cardíaco), diminuição do fluxo sanguíneo para áreas inativas, como rins e fígado, e aumento do número de vasos sanguíneos abertos na musculatura em trabalho. A frequência cardíaca, a pressão arterial e a extração de oxigênio nos músculos aumentam linearmente em relação à intensidade do trabalho. Além disso, a ventilação pulmonar é aumentada devido à respiração mais profunda e ao aumento da frequência respiratória. O objetivo de ativar todo o sistema cardiorrespiratório é aumentar o fornecimento de oxigênio aos músculos ativos. O nível de consumo de oxigênio medido durante o trabalho muscular dinâmico pesado indica a intensidade do trabalho. O consumo máximo de oxigênio (VO2max) indica a capacidade máxima da pessoa para o trabalho aeróbico. Os valores de consumo de oxigênio podem ser traduzidos em gasto energético (1 litro de consumo de oxigênio por minuto corresponde a aproximadamente 5 kcal/min ou 21 kJ/min).
No caso do trabalho dinâmico, quando a massa muscular ativa é menor (como nos braços), a capacidade máxima de trabalho e o consumo máximo de oxigênio são menores do que no trabalho dinâmico com grandes músculos. Com a mesma produção de trabalho externo, o trabalho dinâmico com músculos pequenos provoca respostas cardiorrespiratórias mais altas (por exemplo, frequência cardíaca, pressão arterial) do que o trabalho com músculos grandes (figura 1).
Figura 1. Trabalho estático versus dinâmico
Trabalho muscular estático
No trabalho estático, a contração muscular não produz movimento visível, como, por exemplo, em um membro. O trabalho estático aumenta a pressão dentro do músculo, que junto com a compressão mecânica oclui parcial ou totalmente a circulação sanguínea. A entrega de nutrientes e oxigênio para o músculo e a remoção de produtos metabólicos finais do músculo são prejudicadas. Assim, no trabalho estático, os músculos se cansam mais facilmente do que no trabalho dinâmico.
A característica circulatória mais proeminente do trabalho estático é o aumento da pressão arterial. A frequência cardíaca e o débito cardíaco não mudam muito. Acima de certa intensidade de esforço, a pressão arterial aumenta em relação direta com a intensidade e a duração do esforço. Além disso, na mesma intensidade relativa de esforço, o trabalho estático com grandes grupos musculares produz uma maior resposta da pressão arterial do que o trabalho com músculos menores. (Veja a figura 2)
Figura 2. O modelo tensão-deformação expandido modificado de Rohmert (1984)
Em princípio, a regulação da ventilação e circulação no trabalho estático é semelhante à do trabalho dinâmico, mas os sinais metabólicos dos músculos são mais fortes e induzem um padrão de resposta diferente.
Consequências da Sobrecarga Muscular nas Atividades Ocupacionais
O grau de esforço físico que um trabalhador experimenta no trabalho muscular depende do tamanho da massa muscular de trabalho, do tipo de contrações musculares (estáticas, dinâmicas), da intensidade das contrações e das características individuais.
Quando a carga muscular não ultrapassa as capacidades físicas do trabalhador, o corpo se adapta à carga e a recuperação é rápida quando o trabalho é interrompido. Se a carga muscular for muito alta, ocorrerá fadiga, a capacidade de trabalho será reduzida e a recuperação será mais lenta. Cargas de pico ou sobrecarga prolongada podem resultar em danos aos órgãos (na forma de doenças ocupacionais ou relacionadas ao trabalho). Por outro lado, trabalhos musculares de certa intensidade, frequência e duração também podem resultar em efeitos de treinamento, já, por outro lado, demandas musculares excessivamente baixas podem causar efeitos de destreinamento. Essas relações são representadas pelos chamados conceito de tensão-deformação expandida desenvolvido por Rohmert (1984) (figura 3).
Figura 3. Análise de cargas de trabalho aceitáveis
Em geral, há poucas evidências epidemiológicas de que a sobrecarga muscular seja um fator de risco para doenças. No entanto, problemas de saúde, incapacidade e sobrecarga subjetiva no trabalho convergem em trabalhos fisicamente exigentes, especialmente com trabalhadores mais velhos. Além disso, muitos fatores de risco para doenças musculoesqueléticas relacionadas ao trabalho estão ligados a diferentes aspectos da carga de trabalho muscular, como o esforço de força, más posturas de trabalho, elevação e picos súbitos de cargas.
Um dos objetivos da ergonomia tem sido determinar limites aceitáveis para cargas musculares que possam ser aplicadas para a prevenção de fadiga e distúrbios. Enquanto a prevenção de efeitos crônicos é o foco da epidemiologia, a fisiologia do trabalho lida principalmente com efeitos de curto prazo, ou seja, fadiga em tarefas de trabalho ou durante um dia de trabalho.
Carga de Trabalho Aceitável em Trabalho Muscular Dinâmico Pesado
A avaliação da carga de trabalho aceitável em tarefas dinâmicas de trabalho tem sido tradicionalmente baseada em medições de consumo de oxigênio (ou, correspondentemente, gasto de energia). O consumo de oxigênio pode ser medido com relativa facilidade no campo com dispositivos portáteis (p. , com o dispositivo SportTester. O uso da frequência cardíaca na estimativa do consumo de oxigênio requer que seja calibrado individualmente contra o consumo de oxigênio medido em um modo de trabalho padrão no laboratório, ou seja, o investigador deve conhecer o consumo de oxigênio do sujeito individual em uma determinada frequência cardíaca. As gravações da frequência cardíaca devem ser tratadas com cautela porque também são afetadas por fatores como condicionamento físico, temperatura ambiente, fatores psicológicos e tamanho da massa muscular ativa. Assim, as medições da frequência cardíaca podem levar a superestimativas do consumo de oxigênio, da mesma forma que os valores de consumo de oxigênio podem dar origem a subestimativas da tensão fisiológica global, refletindo apenas as necessidades de energia.
Tensão aeróbica relativa (RAS) é definido como a fração (expressa em porcentagem) do consumo de oxigênio de um trabalhador medido no trabalho em relação ao seu VO2max medida em laboratório. Se apenas as medições da frequência cardíaca estiverem disponíveis, uma aproximação aproximada do RAS pode ser feita calculando um valor para a faixa percentual da frequência cardíaca (% da faixa de FC) com a chamada fórmula de Karvonen, conforme a figura 3.
VO2max geralmente é medido em uma bicicleta ergométrica ou esteira, para a qual a eficiência mecânica é alta (20-25%). Quando a massa muscular ativa é menor ou o componente estático é maior, o VO2max e a eficiência mecânica será menor do que no caso de exercícios com grandes grupos musculares. Por exemplo, verificou-se que na triagem de encomendas postais o VO2max dos trabalhadores foi de apenas 65% do máximo medido em bicicleta ergométrica, e a eficiência mecânica da tarefa foi inferior a 1%. Quando as diretrizes são baseadas no consumo de oxigênio, o modo de teste no teste máximo deve ser o mais próximo possível da tarefa real. Esse objetivo, no entanto, é difícil de ser alcançado.
Segundo o estudo clássico de Åstrand (1960), a RAS não deve ultrapassar 50% durante uma jornada de trabalho de oito horas. Em seus experimentos, com uma carga de trabalho de 50%, o peso corporal diminuiu, a frequência cardíaca não atingiu o estado estacionário e o desconforto subjetivo aumentou durante o dia. Ela recomendou um limite de RAS de 50% para homens e mulheres. Mais tarde, ela descobriu que os trabalhadores da construção escolhiam espontaneamente um nível médio de RAS de 40% (intervalo de 25-55%) durante um dia de trabalho. Vários estudos mais recentes indicaram que o RAS aceitável é inferior a 50%. A maioria dos autores recomenda 30-35% como nível aceitável de RAS para toda a jornada de trabalho.
Originalmente, os níveis aceitáveis de RAS foram desenvolvidos para trabalho muscular dinâmico puro, que raramente ocorre na vida real de trabalho. Pode acontecer que os níveis aceitáveis de RAS não sejam excedidos, por exemplo, em uma tarefa de elevação, mas a carga local nas costas pode exceder muito os níveis aceitáveis. Apesar de suas limitações, a determinação do RAS tem sido amplamente utilizada na avaliação do esforço físico em diferentes trabalhos.
Além da medição ou estimativa do consumo de oxigênio, outros métodos de campo fisiológico úteis também estão disponíveis para a quantificação do estresse físico ou tensão em trabalhos dinâmicos pesados. Técnicas observacionais podem ser usadas na estimativa do gasto energético (por exemplo, com o auxílio do escala Edholm) (Edholm 1966). Avaliação do esforço percebido (RPE) indica o acúmulo subjetivo de fadiga. Novos sistemas de monitoramento ambulatorial da pressão arterial permitem análises mais detalhadas das respostas circulatórias.
Carga de Trabalho Aceitável no Manuseio Manual de Materiais
O manuseio manual de materiais inclui tarefas de trabalho como levantar, carregar, empurrar e puxar várias cargas externas. A maior parte da pesquisa nesta área se concentrou em problemas lombares em tarefas de levantamento, especialmente do ponto de vista biomecânico.
Um nível de RAS de 20-35% tem sido recomendado para tarefas de levantamento, quando a tarefa é comparada a um consumo máximo individual de oxigênio obtido em um teste de bicicleta ergométrica.
As recomendações para uma frequência cardíaca máxima permitida são absolutas ou relacionadas à frequência cardíaca em repouso. Os valores absolutos para homens e mulheres são 90-112 batimentos por minuto no manuseio manual contínuo de materiais. Esses valores são aproximadamente os mesmos que os valores recomendados para o aumento da frequência cardíaca acima dos níveis de repouso, ou seja, 30 a 35 batimentos por minuto. Estas recomendações também são válidas para trabalho muscular dinâmico pesado para homens e mulheres jovens e saudáveis. No entanto, como mencionado anteriormente, os dados da frequência cardíaca devem ser tratados com cautela, porque também são afetados por outros fatores além do trabalho muscular.
As diretrizes de carga de trabalho aceitável para movimentação manual de materiais com base em análises biomecânicas compreendem vários fatores, como peso da carga, frequência de movimentação, altura de levantamento, distância da carga do corpo e características físicas da pessoa.
Em um estudo de campo em grande escala (Louhevaara, Hakola e Ollila 1990), descobriu-se que trabalhadores saudáveis do sexo masculino podiam manusear encomendas postais pesando de 4 a 5 quilos durante um turno sem quaisquer sinais de fadiga objetiva ou subjetiva. A maior parte do manuseio ocorreu abaixo do nível do ombro, a frequência média de manuseio foi inferior a 8 pacotes por minuto e o número total de pacotes foi inferior a 1,500 por turno. A frequência cardíaca média dos trabalhadores foi de 101 batimentos por minuto e o consumo médio de oxigênio de 1.0 l/min, o que correspondeu a 31% da RAS em relação ao máximo da bicicleta.
Observações de posturas de trabalho e uso de força realizadas, por exemplo, de acordo com o método OWAS (Karhu, Kansi e Kuorinka 1977), avaliações de esforço percebido e registros ambulatoriais da pressão arterial também são métodos adequados para avaliações de estresse e tensão no manuseio manual de materiais. A eletromiografia pode ser usada para avaliar as respostas de tensão local, por exemplo, nos músculos do braço e das costas.
Carga de Trabalho Aceitável para Trabalho Muscular Estático
O trabalho muscular estático é necessário principalmente para manter as posturas de trabalho. O tempo de resistência da contração estática é exponencialmente dependente da força relativa da contração. Isso significa, por exemplo, que quando a contração estática requer 20% da força máxima, o tempo de resistência é de 5 a 7 minutos, e quando a força relativa é de 50%, o tempo de resistência é de cerca de 1 minuto.
Estudos mais antigos indicaram que nenhuma fadiga será desenvolvida quando a força relativa estiver abaixo de 15% da força máxima. No entanto, estudos mais recentes indicam que a força relativa aceitável é específica para o músculo ou grupo muscular, e é de 2 a 5% da força estática máxima. Esses limites de força são, no entanto, difíceis de usar em situações práticas de trabalho porque requerem registros eletromiográficos.
Para o praticante, menos métodos de campo estão disponíveis para a quantificação da tensão no trabalho estático. Existem alguns métodos observacionais (por exemplo, o método OWAS) para analisar a proporção de más posturas de trabalho, ou seja, posturas que se desviam das posições intermediárias normais das articulações principais. Medições de pressão arterial e avaliações de esforço percebido podem ser úteis, enquanto a freqüência cardíaca não é tão aplicável.
Carga de Trabalho Aceitável em Trabalho Repetitivo
O trabalho repetitivo com pequenos grupos musculares se assemelha ao trabalho muscular estático do ponto de vista das respostas circulatórias e metabólicas. Normalmente, no trabalho repetitivo, os músculos se contraem mais de 30 vezes por minuto. Quando a força relativa de contração excede 10% da força máxima, o tempo de resistência e a força muscular começam a diminuir. No entanto, há uma grande variação individual nos tempos de resistência. Por exemplo, o tempo de resistência varia entre dois a cinquenta minutos quando o músculo se contrai de 90 a 110 vezes por minuto em um nível de força relativa de 10 a 20% (Laurig 1974).
É muito difícil estabelecer critérios definitivos para o trabalho repetitivo, porque mesmo níveis muito leves de trabalho (como com o uso de um mouse de microcomputador) podem causar aumentos na pressão intramuscular, o que às vezes pode levar ao inchaço das fibras musculares, dor e redução na força muscular.
O trabalho muscular repetitivo e estático causará fadiga e capacidade de trabalho reduzida em níveis de força relativa muito baixos. Portanto, as intervenções ergonômicas devem ter como objetivo minimizar ao máximo o número de movimentos repetitivos e contrações estáticas. Muito poucos métodos de campo estão disponíveis para avaliação de tensão em trabalho repetitivo.
Prevenção da Sobrecarga Muscular
Existe relativamente pouca evidência epidemiológica para mostrar que a carga muscular é prejudicial à saúde. No entanto, estudos fisiológicos e ergonômicos do trabalho indicam que a sobrecarga muscular resulta em fadiga (isto é, diminuição da capacidade de trabalho) e pode reduzir a produtividade e a qualidade do trabalho.
A prevenção da sobrecarga muscular pode ser direcionada ao conteúdo do trabalho, ao ambiente de trabalho e ao trabalhador. A carga pode ser ajustada por meios técnicos, que incidem sobre o ambiente de trabalho, ferramentas e/ou métodos de trabalho. A maneira mais rápida de regular a carga de trabalho muscular é aumentar a flexibilidade do tempo de trabalho individualmente. Isso significa projetar regimes de trabalho e descanso que levem em consideração a carga de trabalho e as necessidades e capacidades de cada trabalhador.
O trabalho muscular estático e repetitivo deve ser mínimo. Fases ocasionais de trabalho dinâmico pesado podem ser úteis para a manutenção da aptidão física do tipo resistência. Provavelmente, a forma mais útil de atividade física que pode ser incorporada a um dia de trabalho é uma caminhada rápida ou subir escadas.
A prevenção da sobrecarga muscular, no entanto, é muito difícil se a aptidão física ou as habilidades de trabalho de um trabalhador forem deficientes. O treinamento adequado melhorará as habilidades de trabalho e poderá reduzir as cargas musculares no trabalho. Além disso, o exercício físico regular durante o trabalho ou lazer aumentará as capacidades musculares e cardiorrespiratórias do trabalhador.
Lesão Celular e Morte Celular
Praticamente toda a medicina é dedicada a prevenir a morte celular, em doenças como infarto do miocárdio, acidente vascular cerebral, trauma e choque, ou causá-la, como no caso de doenças infecciosas e câncer. É, portanto, essencial entender a natureza e os mecanismos envolvidos. A morte celular tem sido classificada como “acidental”, isto é, causada por agentes tóxicos, isquemia e outros, ou “programada”, como ocorre durante o desenvolvimento embriológico, incluindo formação de dígitos e reabsorção da cauda do girino.
A lesão celular e a morte celular são, portanto, importantes tanto na fisiologia quanto na fisiopatologia. A morte celular fisiológica é extremamente importante durante a embriogênese e o desenvolvimento embrionário. O estudo da morte celular durante o desenvolvimento trouxe importantes e novas informações sobre a genética molecular envolvida, especialmente através do estudo do desenvolvimento em animais invertebrados. Nesses animais, a localização precisa e o significado das células destinadas à morte celular foram cuidadosamente estudados e, com o uso de técnicas clássicas de mutagênese, vários genes envolvidos já foram identificados. Nos órgãos adultos, o equilíbrio entre a morte celular e a proliferação celular controla o tamanho do órgão. Em alguns órgãos, como a pele e o intestino, há uma renovação contínua das células. Na pele, por exemplo, as células se diferenciam à medida que atingem a superfície e, finalmente, sofrem diferenciação terminal e morte celular à medida que a queratinização prossegue com a formação de envelopes reticulados.
Muitas classes de produtos químicos tóxicos são capazes de induzir lesão celular aguda seguida de morte. Estes incluem anóxia e isquemia e seus análogos químicos, como cianeto de potássio; carcinógenos químicos, que formam eletrófilos que se ligam covalentemente a proteínas em ácidos nucléicos; produtos químicos oxidantes, resultando na formação de radicais livres e danos oxidantes; ativação do complemento; e uma variedade de ionóforos de cálcio. A morte celular também é um componente importante da carcinogênese química; muitos carcinógenos químicos completos, em doses carcinogênicas, produzem necrose aguda e inflamação seguida de regeneração e pré-neoplasia.
Definições
lesão celular
A lesão celular é definida como um evento ou estímulo, como um produto químico tóxico, que perturba a homeostase normal da célula, causando assim a ocorrência de vários eventos (figura 1). Os principais alvos de lesão letal ilustrados são a inibição da síntese de ATP, a ruptura da integridade da membrana plasmática ou a retirada de fatores de crescimento essenciais.
Lesões letais resultam na morte de uma célula após um período de tempo variável, dependendo da temperatura, do tipo de célula e do estímulo; ou podem ser subletais ou crônicos - isto é, a lesão resulta em um estado homeostático alterado que, embora anormal, não resulta em morte celular (Trump e Arstila 1971; Trump e Berezesky 1992; Trump e Berezesky 1995; Trump, Berezesky e Osórnio-Vargas 1981). No caso de uma lesão letal, há uma fase anterior ao momento da morte celular
durante esse tempo, a célula se recuperará; entretanto, após um determinado ponto no tempo (o “ponto sem retorno” ou ponto de morte celular), a remoção da lesão não resulta em recuperação, mas a célula sofre degradação e hidrólise, atingindo finalmente o equilíbrio físico-químico com o meio Ambiente. Esta é a fase conhecida como necrose. Durante a fase pré-letal, vários tipos principais de mudança ocorrem, dependendo da célula e do tipo de lesão. Estes são conhecidos como apoptose e oncose.
Apoptosis
Apoptose é derivado das palavras gregas apo, significando longe de, e ptose, significando cair. O termo caindo longe de deriva do fato de que, durante esse tipo de alteração pré-letal, as células encolhem e sofrem bolhas acentuadas na periferia. As bolhas então se desprendem e flutuam. A apoptose ocorre em uma variedade de tipos de células após vários tipos de lesão tóxica (Wyllie, Kerr e Currie 1980). É especialmente proeminente nos linfócitos, onde é o mecanismo predominante para renovação de clones de linfócitos. Os fragmentos resultantes resultam nos corpos basofílicos vistos dentro dos macrófagos nos gânglios linfáticos. Em outros órgãos, a apoptose ocorre tipicamente em células únicas que são rapidamente eliminadas antes e após a morte por fagocitose dos fragmentos por células parenquimatosas adjacentes ou por macrófagos. A apoptose que ocorre em células únicas com subsequente fagocitose normalmente não resulta em inflamação. Antes da morte, as células apoptóticas apresentam um citosol muito denso com mitocôndrias normais ou condensadas. O retículo endoplasmático (ER) é normal ou apenas ligeiramente dilatado. A cromatina nuclear é marcadamente agrupada ao longo do envelope nuclear e ao redor do nucléolo. O contorno nuclear também é irregular e ocorre fragmentação nuclear. A condensação da cromatina está associada à fragmentação do DNA que, em muitos casos, ocorre entre os nucleossomos, dando uma aparência característica de escada na eletroforese.
Na apoptose, aumentou [Ca2+]i pode estimular K+ efluxo resultando em encolhimento celular, o que provavelmente requer ATP. Lesões que inibem totalmente a síntese de ATP, portanto, têm maior probabilidade de resultar em apoptose. Um aumento sustentado de [Ca2+]i tem uma série de efeitos deletérios, incluindo a ativação de proteases, endonucleases e fosfolipases. A ativação da endonuclease resulta em quebras simples e duplas de DNA que, por sua vez, estimulam níveis aumentados de p53 e na poli-ADP ribosilação, e de proteínas nucleares essenciais no reparo do DNA. A ativação de proteases modifica uma série de substratos, incluindo actina e proteínas relacionadas, levando à formação de bolhas. Outro substrato importante é a poli(ADP-ribose) polimerase (PARP), que inibe o reparo do DNA. Aumentou [Ca2+]i também está associada à ativação de várias proteínas quinases, como MAP quinase, calmodulina quinase e outras. Essas quinases estão envolvidas na ativação de fatores de transcrição que iniciam a transcrição de genes precoces imediatos, por exemplo, c-fos, c-jun e c-myc, e na ativação da fosfolipase A2 que resulta na permeabilização da membrana plasmática e das membranas intracelulares, como a membrana interna da mitocôndria.
oncose
Oncose, derivado da palavra grega É s, inchar, é assim chamado porque neste tipo de alteração pré-letal a célula começa a inchar quase imediatamente após a lesão (Majno e Joris 1995). A razão para o inchaço é um aumento de cátions na água dentro da célula. O principal cátion responsável é o sódio, que normalmente é regulado para manter o volume celular. No entanto, na ausência de ATP ou se a Na-ATPase do plasmalema for inibida, o controle do volume é perdido devido à proteína intracelular e o sódio na água continua a aumentar. Entre os eventos precoces na oncose estão, portanto, o aumento da [Na+]i que leva ao inchaço celular e aumento da [Ca2+]i resultante do influxo do espaço extracelular ou da liberação dos estoques intracelulares. Isso resulta em inchaço do citosol, inchaço do retículo endoplasmático e do aparelho de Golgi e na formação de bolhas aquosas ao redor da superfície celular. As mitocôndrias inicialmente sofrem condensação, mas depois elas também mostram um inchaço de alta amplitude devido a danos na membrana mitocondrial interna. Nesse tipo de alteração pré-letal, a cromatina sofre condensação e, por fim, degradação; no entanto, o padrão de escada característico da apoptose não é observado.
Necrose
Necrose refere-se à série de alterações que ocorrem após a morte celular, quando a célula é convertida em detritos que normalmente são removidos pela resposta inflamatória. Dois tipos podem ser distinguidos: necrose oncótica e necrose apoptótica. A necrose oncótica geralmente ocorre em grandes zonas, por exemplo, em um infarto do miocárdio ou regionalmente em um órgão após toxicidade química, como o túbulo renal proximal após a administração de HgCl2. Amplas zonas de um órgão estão envolvidas e as células necróticas rapidamente incitam uma reação inflamatória, primeiro aguda e depois crônica. No caso de o organismo sobreviver, em muitos órgãos a necrose é seguida pela eliminação das células mortas e regeneração, por exemplo, no fígado ou rim após toxicidade química. Em contraste, a necrose apoptótica ocorre tipicamente em uma única célula e os detritos necróticos são formados dentro dos fagócitos de macrófagos ou células parenquimatosas adjacentes. As primeiras características das células necróticas incluem interrupções na continuidade da membrana plasmática e o aparecimento de densidades floculentas, representando proteínas desnaturadas dentro da matriz mitocondrial. Em algumas formas de lesão que inicialmente não interferem no acúmulo mitocondrial de cálcio, depósitos de fosfato de cálcio podem ser vistos dentro da mitocôndria. Outros sistemas de membrana são fragmentados de forma semelhante, como o RE, os lisossomos e o aparelho de Golgi. Por fim, a cromatina nuclear sofre lise, resultante do ataque das hidrolases lisossômicas. Após a morte celular, as hidrolases lisossômicas desempenham um papel importante na remoção de detritos com catepsinas, nucleolases e lipases, uma vez que estas têm um pH ácido ótimo e podem sobreviver ao baixo pH das células necróticas, enquanto outras enzimas celulares são desnaturadas e inativadas.
Mecanismos
estímulo inicial
No caso de lesões letais, as interações iniciais mais comuns que resultam em lesões que levam à morte celular são a interferência no metabolismo energético, como anoxia, isquemia ou inibidores da respiração, e glicólise, como cianeto de potássio, monóxido de carbono, iodo-acetato e em breve. Como mencionado acima, altas doses de compostos que inibem o metabolismo energético normalmente resultam em oncose. O outro tipo comum de lesão inicial que resulta em morte celular aguda é a modificação da função da membrana plasmática (Trump e Arstila 1971; Trump, Berezesky e Osornio-Vargas 1981). Isso pode ser dano direto e permeabilização, como no caso de trauma ou ativação do complexo C5b-C9 do complemento, dano mecânico à membrana celular ou inibição do sódio-potássio (Na+-K+) bomba com glicosídeos como ouabaína. Ionóforos de cálcio, como ionomicina ou A23187, que transportam rapidamente [Ca2+] descendo o gradiente para dentro da célula, também causam lesões letais agudas. Em alguns casos, o padrão na alteração pré-letal é a apoptose; em outros, é oncose.
Vias de sinalização
Com muitos tipos de lesão, a respiração mitocondrial e a fosforilação oxidativa são rapidamente afetadas. Em algumas células, isso estimula a glicólise anaeróbia, que é capaz de manter o ATP, mas em muitas lesões isso é inibido. A falta de ATP resulta na incapacidade de energizar vários processos homeostáticos importantes, em particular, o controle da homeostase iônica intracelular (Trump e Berezesky 1992; Trump, Berezesky e Osornio-Vargas 1981). Isso resulta em aumentos rápidos de [Ca2+]i, e aumentou [Na+] e [Cl-] resulta em inchaço celular. Aumentos em [Ca2+]i resultam na ativação de vários outros mecanismos de sinalização discutidos abaixo, incluindo uma série de quinases, que podem resultar em aumento imediato da transcrição precoce de genes. Aumentou [Ca2+]i também modifica a função do citoesqueleto, resultando em parte na formação de bolhas e na ativação de endonucleases, proteases e fosfolipases. Estes parecem desencadear muitos dos efeitos importantes discutidos acima, como danos à membrana através da ativação de protease e lipase, degradação direta do DNA pela ativação de endonuclease e ativação de quinases como MAP quinase e calmodulina quinase, que atuam como fatores de transcrição.
Através de um extenso trabalho de desenvolvimento em invertebrados C. elegans e Drosophila, assim como células humanas e animais, uma série de genes pró-morte foram identificados. Descobriu-se que alguns desses genes de invertebrados têm contrapartes de mamíferos. Por exemplo, o gene ced-3, essencial para a morte celular programada em C. elegans, tem atividade de protease e uma forte homologia com a enzima de conversão de interleucina (ICE) de mamíferos. Um gene intimamente relacionado chamado apopaína ou prICE foi recentemente identificado com uma homologia ainda mais estreita (Nicholson et al. 1995). No Drosophila, o gene reaper parece estar envolvido em um sinal que leva à morte celular programada. Outros genes pró-morte incluem a proteína de membrana Fas e o importante gene supressor de tumor, p53, que é amplamente conservado. A p53 é induzida no nível da proteína após o dano ao DNA e quando fosforilada atua como um fator de transcrição para outros genes, como gadd45 e waf-1, que estão envolvidos na sinalização da morte celular. Outros genes precoces imediatos, como c-fos, c-jun e c-myc, também parecem estar envolvidos em alguns sistemas.
Ao mesmo tempo, existem genes anti-morte que parecem neutralizar os genes pró-morte. O primeiro deles a ser identificado foi o ced-9 de C. elegans, que é homólogo ao bcl-2 em humanos. Esses genes agem de uma maneira ainda desconhecida para impedir a morte celular por toxinas genéticas ou químicas. Algumas evidências recentes indicam que o bcl-2 pode atuar como um antioxidante. Atualmente, há muito esforço em andamento para entender os genes envolvidos e desenvolver maneiras de ativar ou inibir esses genes, dependendo da situação.
Medidas resumidas de exposição na vida profissional
Os pesquisadores têm sorte quando têm à sua disposição uma cronologia detalhada da experiência de vida profissional dos trabalhadores, que fornece uma revisão histórica dos empregos que ocuparam ao longo do tempo. Para esses trabalhadores um matriz de exposição de trabalho pode então ser configurado para permitir que cada mudança de trabalho pela qual um trabalhador tenha passado seja associada a informações de exposição específicas.
Os históricos detalhados de exposição devem ser resumidos para fins de análise, a fim de determinar se os padrões são evidentes e podem estar relacionados a questões de saúde e segurança no local de trabalho. Podemos visualizar uma lista de, digamos, 20 mudanças de emprego que um trabalhador experimentou em sua vida profissional. Existem várias maneiras alternativas de resumir os detalhes da exposição (para cada uma das 20 mudanças de emprego neste exemplo), levando em consideração a duração e/ou concentração/dose/grau de exposição.
É importante notar, no entanto, que conclusões diferentes de um estudo podem ser alcançadas dependendo do método selecionado (Suarez-Almazor et al. 1992). Um exemplo de cinco medidas resumidas de exposição na vida profissional é mostrado na tabela 1.
Tabela 1. Fórmulas e dimensões ou unidades das cinco medidas resumidas selecionadas de exposição na vida profissional
|
Medida de exposição |
Fórmula |
Dimensões/Unidades |
|
Índice de exposição cumulativa (CEI) |
Σ (grau x tempo de exposição) |
série e tempo |
|
Nota média (MG) |
Σ (grau x tempo de exposição)/tempo total de exposição |
grau |
|
Nota mais alta de sempre (HG) |
grau mais alto ao qual exposto por ≥ 7 dias |
grau |
|
Nota média ponderada pelo tempo (TWA) |
Σ (grau x tempo de exposição)/tempo total empregado |
grau |
|
Tempo total exposto (TTE) |
Σ tempo exposto |
tempo |
Adaptado de Suarez-Almazor et al. 1992.
Índice de exposição cumulativa. O índice de exposição cumulativa (CEI) equivale a “dose” em estudos toxicológicos e representa a soma, ao longo da vida útil, dos produtos de grau de exposição e duração da exposição para cada cargo sucessivo. Inclui o tempo em suas unidades.
Nota média. A nota média (MG) acumula os produtos do grau de exposição e duração da exposição para cada cargo sucessivo (ou seja, o CEI) e divide pelo tempo total exposto em qualquer grau maior que zero. MG é independente do tempo em suas unidades; a medida sumária para uma pessoa exposta por um longo período a uma alta concentração será semelhante à de uma pessoa exposta por um curto período a uma alta concentração. Dentro de qualquer conjunto correspondente em um projeto de controle de caso, MG é um grau médio de exposição por unidade de tempo exposto. É uma nota média para o tempo efetivamente exposto ao agente em questão.
Grau mais alto de todos os tempos. O grau mais alto de todos os tempos (HG) é determinado a partir da verificação do histórico de trabalho para a atribuição de grau mais alto no período de observação ao qual o trabalhador foi exposto por pelo menos sete dias. O HG pode deturpar a exposição da vida profissional de uma pessoa porque, por sua própria formulação, é baseado em um procedimento de maximização em vez de uma média e, portanto, é independente da duração da exposição em suas unidades.
Nota média ponderada pelo tempo. O grau de média ponderada pelo tempo (TWA) é o índice de exposição cumulativa (CEI) dividido pelo tempo total empregado. Dentro de qualquer conjunto correspondente em um projeto de caso-controle, a média do grau TWA sobre o tempo total empregado. Difere do MG, que calcula a média apenas sobre o tempo total efetivamente exposto. Assim, o grau TWA pode ser visto como uma exposição média por unidade de tempo durante todo o período de emprego, independentemente da exposição per se.
Tempo total exposto. O tempo total exposto (TTE) acumula todos os períodos de tempo associados à exposição em unidades de tempo. TTE tem apelo por sua simplicidade. No entanto, é bem aceito que os efeitos na saúde devem estar relacionados não apenas à duração da exposição química, mas também à intensidade dessa exposição (ou seja, a concentração ou grau).
Claramente, a utilidade de uma medida sumária da exposição é determinada pelo respectivo peso que atribui à duração ou à concentração da exposição ou a ambas. Assim, medidas diferentes podem produzir resultados diferentes (Walker e Blettner 1985). Idealmente, a medida resumida selecionada deve ser baseada em um conjunto de suposições defensáveis em relação ao mecanismo biológico postulado para o agente ou associação de doença em estudo (Smith 1987). No entanto, este procedimento nem sempre é possível. Muitas vezes, o efeito biológico da duração da exposição ou da concentração do agente em estudo é desconhecido. Nesse contexto, o uso de diferentes medidas de exposição pode ser útil para sugerir um mecanismo pelo qual a exposição exerce seu efeito.
Recomenda-se que, na ausência de modelos comprovados para avaliar a exposição, uma variedade de medidas resumidas de exposição da vida profissional seja usada para estimar o risco. Essa abordagem facilitaria a comparação dos achados entre os estudos.
Posturas no Trabalho
A postura de uma pessoa no trabalho – a organização mútua do tronco, cabeça e extremidades – pode ser analisada e compreendida sob vários pontos de vista. As posturas visam o avanço do trabalho; assim, eles têm uma finalidade que influencia sua natureza, sua relação temporal e seu custo (fisiológico ou não) para a pessoa em questão. Existe uma estreita interação entre as capacidades e características fisiológicas do corpo e a exigência do trabalho.
A carga musculoesquelética é um elemento necessário nas funções corporais e indispensável no bem-estar. Do ponto de vista do desenho da obra, a questão é encontrar o equilíbrio ideal entre o necessário e o excessivo.
As posturas têm interessado pesquisadores e profissionais pelo menos pelas seguintes razões:
- Uma postura é a fonte de carga musculoesquelética. Exceto para ficar em pé relaxado, sentar e deitar horizontalmente, os músculos precisam criar forças para equilibrar a postura e/ou controlar os movimentos. Em tarefas pesadas clássicas, por exemplo na indústria da construção ou no manuseio manual de materiais pesados, as forças externas, tanto dinâmicas quanto estáticas, somam-se às forças internas do corpo, às vezes criando altas cargas que podem exceder a capacidade dos tecidos. (Ver figura 1) Mesmo em posturas relaxadas, quando o trabalho muscular se aproxima de zero, os tendões e as articulações podem estar sobrecarregados e mostrar sinais de fadiga. Um trabalho com carga aparente baixa - um exemplo é o de um microscopista - pode se tornar tedioso e extenuante quando executado por um longo período de tempo.
- A postura está intimamente relacionada com o equilíbrio e a estabilidade. Na verdade, a postura é controlada por vários reflexos neurais, onde a entrada de sensações táteis e pistas visuais do ambiente desempenham um papel importante. Algumas posturas, como alcançar objetos à distância, são inerentemente instáveis. A perda de equilíbrio é uma causa imediata comum de acidentes de trabalho. Algumas tarefas de trabalho são executadas em um ambiente onde a estabilidade nem sempre pode ser garantida, por exemplo, na indústria da construção.
- A postura é a base dos movimentos habilidosos e da observação visual. Muitas tarefas exigem movimentos finos e habilidosos das mãos e observação atenta do objeto do trabalho. Nesses casos, a postura se torna a plataforma dessas ações. A atenção é direcionada para a tarefa, e os elementos posturais são alistados para apoiar as tarefas: a postura torna-se imóvel, a carga muscular aumenta e torna-se mais estática. Um grupo de pesquisa francês mostrou em seu estudo clássico que a imobilidade e a carga musculoesquelética aumentavam quando a taxa de trabalho aumentava (Teiger, Laville e Duraffourg 1974).
- A postura é uma fonte de informação sobre os eventos que ocorrem no trabalho. A observação da postura pode ser intencional ou inconsciente. Sabe-se que supervisores e trabalhadores hábeis usam observações posturais como indicadores do processo de trabalho. Muitas vezes, observar informações posturais não é consciente. Por exemplo, em uma torre de perfuração de petróleo, dicas posturais foram usadas para comunicar mensagens entre os membros da equipe durante diferentes fases de uma tarefa. Isso ocorre em condições em que outros meios de comunicação não são possíveis.
Figura 1. Posições de mão muito altas ou flexão para frente estão entre as formas mais comuns de criar carga "estática"
Segurança, Saúde e Posturas de Trabalho
Do ponto de vista da segurança e saúde, todos os aspectos da postura descritos acima podem ser importantes. No entanto, as posturas como fonte de doenças músculo-esqueléticas, como as doenças lombares, têm atraído mais atenção. Problemas musculoesqueléticos relacionados ao trabalho repetitivo também estão ligados às posturas.
Dor lombar (LBP) é um termo genérico para várias doenças lombares. Tem muitas causas e a postura é um possível elemento causal. Estudos epidemiológicos mostraram que o trabalho fisicamente pesado leva à lombalgia e que as posturas são um elemento desse processo. Existem vários mecanismos possíveis que explicam por que certas posturas podem causar lombalgia. As posturas de flexão para a frente aumentam a carga na coluna e nos ligamentos, que são especialmente vulneráveis a cargas em uma postura torcida. As cargas externas, especialmente as dinâmicas, como as impostas por solavancos e deslizamentos, podem aumentar muito as cargas nas costas.
Do ponto de vista da segurança e saúde, é importante identificar más posturas e outros elementos posturais no âmbito da análise de segurança e saúde do trabalho em geral.
Registrando e medindo posturas de trabalho
As posturas podem ser registradas e medidas objetivamente pelo uso de observação visual ou técnicas de medição mais ou menos sofisticadas. Eles também podem ser registrados usando esquemas de autoavaliação. A maioria dos métodos considera a postura como um dos elementos em um contexto mais amplo, por exemplo, como parte do conteúdo do trabalho - como fazem a AET e a Renault. Os perfis das postagens (Landau e Rohmert 1981; RNUR 1976) - ou como ponto de partida para cálculos biomecânicos que também levam em consideração outros componentes.
Apesar dos avanços na tecnologia de medição, a observação visual permanece, em condições de campo, o único meio praticável de registro sistemático de posturas. No entanto, a precisão de tais medições permanece baixa. Apesar disso, as observações posturais podem ser uma rica fonte de informações sobre o trabalho em geral.
A seguinte lista curta de métodos e técnicas de medição apresenta exemplos selecionados:
- Questionários e diários de autorrelato. Questionários e diários de autorrelato são um meio econômico de coletar informações posturais. O autorrelato é baseado na percepção do sujeito e geralmente se desvia muito das posturas observadas “objetivamente”, mas ainda pode transmitir informações importantes sobre o tédio do trabalho.
- Observação de posturas. A observação das posturas inclui o registro puramente visual das posturas e seus componentes, bem como métodos nos quais uma entrevista completa a informação. Suporte de computador geralmente está disponível para esses métodos. Muitos métodos estão disponíveis para observações visuais. O método pode simplesmente conter um catálogo de ações, incluindo posturas do tronco e membros (por exemplo, Keyserling 1986; Van der Beek, Van Gaalen e Frings-Dresen 1992). O método OWAS propõe um esquema estruturado para a análise, classificação e avaliação de posturas de tronco e membros projetadas para condições de campo (Karhu, Kansi e Kuorinka 1977). O método de registro e análise pode conter esquemas de notação, alguns deles bastante detalhados (como no método de segmentação postural, de Corlett e Bishop 1976), e podem fornecer uma notação para a posição de muitos elementos anatômicos para cada elemento da tarefa ( Dry 1987).
- Análise postural assistida por computador. Os computadores têm auxiliado as análises posturais de várias maneiras. Computadores portáteis e programas especiais permitem fácil registro e rápida análise das posturas. Persson e Kilbom (1983) desenvolveram o programa VIRA para estudo dos membros superiores; Kerguelen (1986) produziu um pacote completo de registro e análise para tarefas de trabalho; Kivi e Mattila (1991) projetaram uma versão computadorizada do OWAS para gravação e análise.
O vídeo geralmente é parte integrante do processo de gravação e análise. O Instituto Nacional de Saúde e Segurança Ocupacional dos Estados Unidos (NIOSH) apresentou diretrizes para o uso de métodos de vídeo na análise de riscos (NIOSH 1990).
Programas de computador biomecânicos e antropométricos oferecem ferramentas especializadas para analisar alguns elementos posturais na atividade de trabalho e no laboratório (por exemplo, Chaffin 1969).
Fatores que afetam as posturas de trabalho
As posturas de trabalho servem a um objetivo, a uma finalidade fora de si mesmas. É por isso que estão relacionados com as condições externas de trabalho. A análise postural que não leva em consideração o ambiente de trabalho e a tarefa em si é de interesse limitado para os ergonomistas.
As características dimensionais do local de trabalho definem amplamente as posturas (como no caso de uma tarefa sentada), mesmo para tarefas dinâmicas (por exemplo, o manuseio de materiais em um espaço confinado). As cargas a serem manuseadas forçam o corpo a uma determinada postura, assim como o peso e a natureza da ferramenta de trabalho. Algumas tarefas exigem que o peso do corpo seja usado para apoiar uma ferramenta ou para aplicar força no objeto do trabalho, conforme mostrado, por exemplo, na figura 2.
Figura 2. Aspectos ergonômicos da postura em pé
Diferenças individuais, idade e sexo influenciam as posturas. De fato, descobriu-se que uma postura “típica” ou “melhor”, por exemplo no manejo manual, é em grande parte ficção. Para cada indivíduo e cada situação de trabalho, há uma série de “melhores” posturas alternativas do ponto de vista de diferentes critérios.
Auxiliares de trabalho e suportes para posturas de trabalho
Cintos, suportes lombares e órteses têm sido recomendados para tarefas com risco de dor lombar ou lesões musculoesqueléticas nos membros superiores. Supõe-se que esses dispositivos dão suporte aos músculos, por exemplo, controlando a pressão intra-abdominal ou os movimentos das mãos. Espera-se também que limitem a amplitude de movimento do cotovelo, punho ou dedos. Não há evidências de que modificar elementos posturais com esses dispositivos ajudaria a evitar problemas musculoesqueléticos.
Suportes posturais no local de trabalho e em máquinas, como alças, almofadas de apoio para ajoelhar-se e auxiliares de assento, podem ser úteis para aliviar as cargas posturais e a dor.
Regulamentos de Segurança e Saúde relativos aos Elementos Posturais
Posturas ou elementos posturais não foram sujeitos a atividades regulatórias per se. No entanto, vários documentos contêm declarações que dizem respeito às posturas ou incluem a questão das posturas como elemento integrante de um regulamento. Uma imagem completa do material regulamentar existente não está disponível. As referências a seguir são apresentadas como exemplos.
- A Organização Internacional do Trabalho publicou uma Recomendação em 1967 sobre cargas máximas a serem movimentadas. Embora a Recomendação não regule os elementos posturais como tais, ela tem uma influência significativa na tensão postural. A Recomendação está desatualizada, mas serviu a um importante propósito de chamar a atenção para os problemas no manuseio manual de materiais.
- As diretrizes de elevação do NIOSH (NIOSH 1981), como tal, também não são regulamentos, mas alcançaram esse status. As diretrizes determinam limites de peso para cargas usando a localização da carga – um elemento postural – como base.
- Tanto na Organização Internacional de Normalização como na Comunidade Europeia existem normas e directivas de ergonomia que contêm matéria relativa aos elementos posturais (CEN 1990 e 1991).
Toxicologia Genética
A toxicologia genética, por definição, é o estudo de como os agentes químicos ou físicos afetam o intrincado processo da hereditariedade. Os produtos químicos genotóxicos são definidos como compostos capazes de modificar o material hereditário das células vivas. A probabilidade de um determinado produto químico causar danos genéticos inevitavelmente depende de várias variáveis, incluindo o nível de exposição do organismo ao produto químico, a distribuição e retenção do produto químico uma vez que entra no corpo, a eficiência da ativação metabólica e/ou sistemas de desintoxicação em tecidos-alvo e a reatividade do produto químico ou de seus metabólitos com macromoléculas críticas dentro das células. A probabilidade de que o dano genético cause doença depende, em última análise, da natureza do dano, da capacidade da célula de reparar ou amplificar o dano genético, da oportunidade de expressar qualquer alteração induzida e da capacidade do corpo de reconhecer e suprimir a multiplicação de células aberrantes.
Em organismos superiores, a informação hereditária é organizada em cromossomos. Os cromossomos consistem em filamentos fortemente condensados de DNA associado a proteínas. Dentro de um único cromossomo, cada molécula de DNA existe como um par de cadeias longas e não ramificadas de subunidades de nucleotídeos ligadas entre si por ligações fosfodiéster que unem o carbono 5 de uma porção de desoxirribose ao carbono 3 da próxima (figura 1). Além disso, uma das quatro bases nucleotídicas diferentes (adenina, citosina, guanina ou timina) está ligada a cada subunidade de desoxirribose como contas em um cordão. Tridimensionalmente, cada par de fitas de DNA forma uma dupla hélice com todas as bases voltadas para o interior da espiral. Dentro da hélice, cada base está associada à sua base complementar na fita de DNA oposta; a ligação de hidrogênio dita o emparelhamento forte e não covalente de adenina com timina e guanina com citosina (figura 1). Como a sequência de bases nucleotídicas é complementar em todo o comprimento da molécula de DNA duplex, ambas as fitas carregam essencialmente a mesma informação genética. De fato, durante a replicação do DNA, cada fita serve como modelo para a produção de uma nova fita parceira.
Figura 1. A organização (a) primária, (b) secundária e (c) terciária da informação hereditária humana
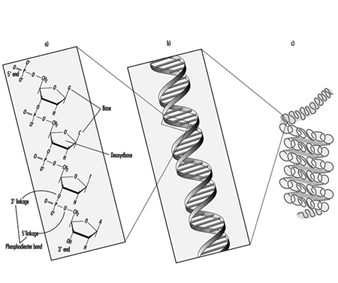 Usando o RNA e uma série de proteínas diferentes, a célula decifra a informação codificada pela sequência linear de bases dentro de regiões específicas do DNA (genes) e produz proteínas que são essenciais para a sobrevivência celular básica, bem como para o crescimento e diferenciação normais. Em essência, os nucleotídeos funcionam como um alfabeto biológico usado para codificar os aminoácidos, os blocos de construção das proteínas.
Usando o RNA e uma série de proteínas diferentes, a célula decifra a informação codificada pela sequência linear de bases dentro de regiões específicas do DNA (genes) e produz proteínas que são essenciais para a sobrevivência celular básica, bem como para o crescimento e diferenciação normais. Em essência, os nucleotídeos funcionam como um alfabeto biológico usado para codificar os aminoácidos, os blocos de construção das proteínas.
Quando nucleotídeos incorretos são inseridos ou nucleotídeos são perdidos, ou quando nucleotídeos desnecessários são adicionados durante a síntese de DNA, o erro é chamado de mutação. Estima-se que ocorra menos de uma mutação para cada 109 nucleotídeos incorporados durante a replicação normal das células. Embora as mutações não sejam necessariamente prejudiciais, as alterações que causam inativação ou superexpressão de genes importantes podem resultar em uma variedade de distúrbios, incluindo câncer, doenças hereditárias, anormalidades do desenvolvimento, infertilidade e morte embrionária ou perinatal. Muito raramente, uma mutação pode levar a uma maior sobrevida; tais ocorrências são a base da seleção natural.
Embora alguns produtos químicos reajam diretamente com o DNA, a maioria requer ativação metabólica. No último caso, intermediários eletrofílicos, como epóxidos ou íons de carbono, são responsáveis por induzir lesões em uma variedade de sítios nucleofílicos dentro do material genético (figura 2). Em outros casos, a genotoxicidade é mediada por subprodutos da interação do composto com lipídios intracelulares, proteínas ou oxigênio.
Figura 2. Bioativação de: a) benzo(a)pireno; e b) N-nitrosodimetilamina
Devido à sua relativa abundância nas células, as proteínas são o alvo mais frequente da interação tóxica. No entanto, a modificação do DNA é de maior preocupação devido ao papel central desta molécula na regulação do crescimento e diferenciação através de múltiplas gerações de células.
No nível molecular, os compostos eletrofílicos tendem a atacar o oxigênio e o nitrogênio no DNA. Os locais mais propensos à modificação estão ilustrados na figura 3. Embora os oxigênios dentro dos grupos fosfato no esqueleto do DNA também sejam alvos para modificação química, acredita-se que o dano às bases seja biologicamente mais relevante, uma vez que esses grupos são considerados os principais elementos na molécula de DNA.
Figura 3. Locais primários de danos ao DNA induzidos quimicamente
Os compostos que contêm uma porção eletrofílica normalmente exercem genotoxicidade pela produção de mono-adutos no DNA. Da mesma forma, os compostos que contêm duas ou mais porções reativas podem reagir com dois centros nucleofílicos diferentes e, assim, produzir reticulações intra ou intermoleculares no material genético (figura 4). As ligações cruzadas entre fitas DNA-DNA e DNA-proteína podem ser particularmente citotóxicas, pois podem formar blocos completos para a replicação do DNA. Por razões óbvias, a morte de uma célula elimina a possibilidade de ela sofrer mutação ou transformação neoplásica. Agentes genotóxicos também podem atuar induzindo quebras no esqueleto fosfodiéster, ou entre bases e açúcares (produzindo sítios abásicos) no DNA. Essas quebras podem ser resultado direto da reatividade química no local danificado ou podem ocorrer durante o reparo de um dos tipos de lesão de DNA mencionados acima.
Figura 4. Vários tipos de dano ao complexo proteína-DNA
Nos últimos trinta a quarenta anos, várias técnicas foram desenvolvidas para monitorar o tipo de dano genético induzido por vários produtos químicos. Tais ensaios são descritos em detalhes em outras partes deste capítulo e enciclopédia.
A replicação incorreta de "microlesões", como mono-adutos, locais abásicos ou quebras de fita simples, pode resultar em substituições de pares de bases de nucleotídeos ou na inserção ou exclusão de fragmentos de polinucleotídeos curtos no DNA cromossômico. Em contraste, “macrolesões”, como adutos volumosos, ligações cruzadas ou quebras de fita dupla podem desencadear o ganho, perda ou rearranjo de pedaços relativamente grandes de cromossomos. De qualquer forma, as consequências podem ser devastadoras para o organismo, pois qualquer um desses eventos pode levar à morte celular, perda de função ou transformação maligna das células. Exatamente como o dano ao DNA causa câncer é amplamente desconhecido. Atualmente, acredita-se que o processo pode envolver ativação inadequada de proto-oncogenes, como meu c e ras, e/ou inativação de genes supressores de tumor recentemente identificados, como p53. A expressão anormal de qualquer tipo de gene anula os mecanismos celulares normais para controlar a proliferação e/ou diferenciação celular.
A preponderância da evidência experimental indica que o desenvolvimento de câncer após a exposição a compostos eletrofílicos é um evento relativamente raro. Isso pode ser explicado, em parte, pela capacidade intrínseca da célula de reconhecer e reparar o DNA danificado ou pela falha das células com DNA danificado em sobreviver. Durante o reparo, a base danificada, nucleotídeo ou trecho curto de nucleotídeos ao redor do local danificado é removido e (usando a fita oposta como modelo) um novo pedaço de DNA é sintetizado e inserido no lugar. Para ser eficaz, o reparo do DNA deve ocorrer com grande precisão antes da divisão celular, antes das oportunidades de propagação da mutação.
Estudos clínicos demonstraram que pessoas com defeitos hereditários na capacidade de reparar DNA danificado frequentemente desenvolvem câncer e/ou anormalidades de desenvolvimento em idade precoce (tabela 1). Esses exemplos fornecem fortes evidências que ligam o acúmulo de danos ao DNA a doenças humanas. Da mesma forma, os agentes que promovem a proliferação celular (como o acetato de tetradecanoilforbol) geralmente aumentam a carcinogênese. Para esses compostos, o aumento da probabilidade de transformação neoplásica pode ser consequência direta da diminuição do tempo disponível para a célula realizar o reparo adequado do DNA.
Tabela 1. Distúrbios hereditários propensos ao câncer que parecem envolver defeitos no reparo do DNA
| Síndrome | Sintomas | Fenótipo celular |
| Ataxia Telangiectasia | Deterioração neurológica Imunodeficiência Alta incidência de linfoma |
Hipersensibilidade à radiação ionizante e a certos agentes alquilantes. Replicação desregulada do DNA danificado (pode indicar tempo reduzido para o reparo do DNA) |
| síndrome de Bloom | Anormalidades de desenvolvimento Lesões na pele exposta Alta incidência de tumores do sistema imunológico e do trato gastrointestinal |
Alta frequência de aberrações cromossômicas Ligação defeituosa de quebras associadas ao reparo do DNA |
| Anemia de Fanconi | Retardo de crescimento Alta incidência de leucemia |
Hipersensibilidade a agentes de reticulação Alta frequência de aberrações cromossômicas Reparo defeituoso de ligações cruzadas no DNA |
| Câncer de cólon hereditário sem polipose | Alta incidência de câncer de cólon | Defeito no reparo do DNA incompatível (quando a inserção do nucleotídeo errado ocorre durante a replicação) |
| Xeroderma pigmentoso | Alta incidência de epitelioma em áreas expostas da pele Comprometimento neurológico (em muitos casos) |
Hipersensibilidade à luz ultravioleta e a muitos carcinógenos químicos Defeitos no reparo por excisão e/ou replicação do DNA danificado |
As primeiras teorias sobre como os produtos químicos interagem com o DNA remontam a estudos conduzidos durante o desenvolvimento do gás mostarda para uso em guerra. Uma compreensão maior surgiu dos esforços para identificar agentes anticancerígenos que interromperiam seletivamente a replicação de células tumorais que se dividem rapidamente. O aumento da preocupação pública com os perigos em nosso meio ambiente levou a pesquisas adicionais sobre os mecanismos e consequências da interação química com o material genético. Exemplos de vários tipos de produtos químicos que exercem genotoxicidade são apresentados na tabela 2.
Tabela 2. Exemplos de produtos químicos que exibem genotoxicidade em células humanas
| Classe de produto químico | Exemplo | Fonte de exposição | Provável lesão genotóxica |
| Aflatoxinas | Aflatoxina B1 | Comida contaminada | Adutos de DNA volumosos |
| Aminas aromáticas | 2-Acetilaminofluoreno | Ambiental | Adutos de DNA volumosos |
| Aziridina quinonas | Mitomicina C | quimioterapia para câncer | Mono-adutos, ligações cruzadas entre fitas e quebras de fita simples no DNA. |
| Hidrocarbonetos clorados | Cloreto de vinilo | Ambiental | Mono-adutos no DNA |
| Metais e compostos metálicos | Cisplatina | quimioterapia para câncer | Ambas as ligações cruzadas intra e intercadeias no DNA |
| compostos de níquel | Ambiental | Mono-adutos e quebras de fita simples no DNA | |
| Mostardas Nitrogenadas | Ciclofosfamida | quimioterapia para câncer | Mono-adutos e ligações cruzadas entre fitas no DNA |
| Nitrosaminas | N-nitrosodimetilamina | Comida contaminada | Mono-adutos no DNA |
| Hidrocarbonetos aromáticos policíclicos | Benzo (a) pireno | Ambiental | Adutos de DNA volumosos |
Mais...
Medindo os efeitos das exposições
A epidemiologia envolve medir a ocorrência de doenças e quantificar associações entre doenças e exposições.
Medidas de Ocorrência da Doença
A ocorrência da doença pode ser medida por frequências (conta) mas é melhor descrito por taxas, que são compostos por três elementos: o número de pessoas afetadas (numerador), o número de pessoas na população de origem ou base (ou seja, a população em risco) de onde vêm as pessoas afetadas e o período de tempo coberto. O denominador da taxa é o total de tempo-pessoa experimentado pela população de origem. As taxas permitem comparações mais informativas entre populações de tamanhos diferentes do que apenas contagens. Risco, a probabilidade de um indivíduo desenvolver uma doença dentro de um período de tempo especificado, é uma proporção, variando de 0 a 1, e não uma taxa per se. Taxa de ataque, a proporção de pessoas em uma população que são afetadas dentro de um período de tempo especificado, é tecnicamente uma medida de risco, não uma taxa.
A morbidade específica da doença inclui incidência, que se refere ao número de pessoas recém-diagnosticadas com a doença de interesse. predomínio refere-se ao número de casos existentes. Mortalidade refere-se ao número de pessoas que morrem.
Incidência é definido como o número de novos casos diagnosticados dentro de um período de tempo especificado, enquanto o taxa de incidência é esse número dividido pelo total de tempo-pessoa experimentado pela população de origem (tabela 1). Para o câncer, as taxas geralmente são expressas como taxas anuais por 100,000 pessoas. As taxas para outras doenças mais comuns podem ser expressas por um número menor de pessoas. Por exemplo, as taxas de defeitos congênitos geralmente são expressas por 1,000 nascidos vivos. Incidência cumulativa, a proporção de pessoas que se tornam casos dentro de um período de tempo especificado, é uma medida de risco médio para uma população.
Tabela 1. Medidas de ocorrência da doença: População hipotética observada por um período de cinco anos
|
Casos recém-diagnosticados |
10 |
|
Casos vivos previamente diagnosticados |
12 |
|
Mortes, todas as causas* |
5 |
|
Óbitos, doença de interesse |
3 |
|
Pessoas na população |
100 |
|
Anos observados |
5 |
|
Incidência |
Pessoas 10 |
|
Taxa de incidência anual |
|
|
Prevalência pontual (no final do 5º ano) |
(10 + 12 - 3) = 19 pessoas |
|
Prevalência do período (período de cinco anos) |
(10 + 12) = 22 pessoas |
|
taxa de mortalidade anual |
|
|
Taxa anual de mortalidade |
|
*Para simplificar os cálculos, este exemplo pressupõe que todas as mortes ocorreram no final do período de cinco anos, de modo que todas as 100 pessoas da população permaneceram vivas durante os cinco anos completos.
predomínio inclui prevalência pontual, o número de casos de doença em um ponto no tempo, e prevalência de período, o número total de casos de uma doença conhecida por ter existido em algum momento durante um período especificado.
Mortalidade, que diz respeito a óbitos e não a casos recém-diagnosticados de doenças, reflete fatores que causam doenças, bem como fatores relacionados à qualidade da assistência médica, como triagem, acesso a assistência médica e disponibilidade de tratamentos eficazes. Consequentemente, os esforços de geração de hipóteses e a pesquisa etiológica podem ser mais informativos e fáceis de interpretar quando baseados na incidência e não nos dados de mortalidade. No entanto, os dados de mortalidade geralmente estão mais prontamente disponíveis em grandes populações do que os dados de incidência.
O termo índice de mortalidade é geralmente aceito para significar a taxa de mortes por todas as causas combinadas, enquanto taxa de mortalidade é a taxa de mortalidade por uma causa específica. Para uma determinada doença, o taxa de letalidade (tecnicamente uma proporção, não uma taxa) é o número de pessoas que morreram da doença durante um período de tempo especificado dividido pelo número de pessoas com a doença. O complemento da taxa de letalidade é o taxa de sobrevivência. A taxa de sobrevivência de cinco anos é uma referência comum para doenças crônicas como o câncer.
A ocorrência de uma doença pode variar entre subgrupos da população ou ao longo do tempo. Uma medida de doença para uma população inteira, sem consideração de quaisquer subgrupos, é chamada de taxa bruta. Por exemplo, uma taxa de incidência para todas as faixas etárias combinadas é uma taxa bruta. As taxas para as faixas etárias individuais são as taxas específicas de idade. Para comparar duas ou mais populações com diferentes distribuições de idade, ajustado por idade (ou, padronizada por idade) as taxas devem ser calculadas para cada população multiplicando cada taxa específica por idade pela porcentagem da população padrão (por exemplo, uma das populações em estudo, a população dos EUA em 1970) nessa faixa etária e, em seguida, somando todas as faixas etárias para produzir uma taxa global ajustada à idade. As taxas podem ser ajustadas para outros fatores além da idade, como raça, sexo ou tabagismo, se as taxas específicas da categoria forem conhecidas.
A vigilância e avaliação de dados descritivos podem fornecer pistas sobre a etiologia da doença, identificar subgrupos de alto risco que podem ser adequados para programas de intervenção ou triagem e fornecer dados sobre a eficácia de tais programas. Fontes de informação que têm sido usadas para atividades de vigilância incluem certidões de óbito, registros médicos, registros de câncer, registros de outras doenças (por exemplo, registros de defeitos congênitos, registros de doenças renais em estágio terminal), registros de exposição ocupacional, registros de seguro de saúde ou invalidez e acidentes de trabalho registros.
Medidas de Associação
A epidemiologia tenta identificar e quantificar os fatores que influenciam a doença. Na abordagem mais simples, a ocorrência da doença entre pessoas expostas a um fator suspeito é comparada à ocorrência entre pessoas não expostas. A magnitude de uma associação entre exposição e doença pode ser expressa tanto em absoluto or relativo termos. (Veja também "Estudo de Caso: Medidas").
Os efeitos absolutos são medidos por diferenças de taxa e diferenças de risco (mesa 2). UMA diferença de taxa é uma taxa menos uma segunda taxa. Por exemplo, se a taxa de incidência de leucemia entre trabalhadores expostos ao benzeno é de 72 por 100,000 pessoas-ano e a taxa entre trabalhadores não expostos é de 12 por 100,000 pessoas-ano, então a diferença de taxa é de 60 por 100,000 pessoas-ano. UMA diferença de risco é uma diferença em riscos ou incidência cumulativa e pode variar de -1 a 1.
Tabela 2. Medidas de associação para um estudo de coorte
|
Cases |
Pessoa-anos em risco |
Taxa por 100,000 |
|
|
exposto |
100 |
20,000 |
500 |
|
Não exposto |
200 |
80,000 |
250 |
|
Total |
300 |
100,000 |
300 |
Diferença de taxa (RD) = 500/100,000 - 250/100,000
= 250/100,000 por ano
(146.06/100,000 - 353.94/100,000)*
Razão de taxa (ou risco relativo) (RR) = ![]()
Risco atribuível no exposto (ARe) = 100/20,000 - 200/80,000
= 250/100,000 por ano
Percentagem de risco atribuível nos expostos (ARe%) =![]()
Risco atribuível da população (PAR) = 300/100,000 - 200/80,000
= 50/100,000 por ano
Percentagem de risco atribuível à população (PAR%) =
![]()
* Entre parênteses, intervalos de confiança de 95% calculados usando as fórmulas nas caixas.
efeitos relativos baseiam-se em índices de taxas ou medidas de risco, em vez de diferenças. UMA razão da taxa é a razão de uma taxa em uma população para a taxa em outra. A razão de taxas também tem sido chamada de proporção de risco, risco relativo, taxa relativa e incidência (ou mortalidade) razão da taxa. A medida é adimensional e varia de 0 a infinito. Quando a taxa em dois grupos é semelhante (ou seja, não há efeito da exposição), o razão da taxa é igual à unidade (1). Uma exposição que aumentasse o risco renderia uma razão de taxas maior que a unidade, enquanto um fator de proteção renderia uma razão entre 0 e 1. O excesso de risco relativo é o risco relativo menos 1. Por exemplo, um risco relativo de 1.4 também pode ser expresso como um excesso de risco relativo de 40%.
Nos estudos de caso-controle (também chamados de estudos de caso-referente), são identificadas pessoas com doença (casos) e pessoas sem doença (controles ou referentes). Exposições passadas dos dois grupos são comparadas. As chances de ser um caso exposto são comparadas às chances de ser um controle exposto. Contagens completas das populações de origem de pessoas expostas e não expostas não estão disponíveis, portanto, as taxas de doenças não podem ser calculadas. Em vez disso, os casos expostos podem ser comparados aos controles expostos pelo cálculo de chances relativas, Ou o odds ratio (Tabela 3).
Tabela 3. Medidas de associação para estudos de caso-controle: Exposição ao pó de madeira e adenocarcinoma da cavidade nasal e seios paranasais
|
Cases |
Controles |
|
|
exposto |
18 |
55 |
|
Não exposto |
5 |
140 |
|
Total |
23 |
195 |
Probabilidades relativas (razão de chances) (OR) = ![]()
Percentagem de risco atribuível nos expostos (![]() ) =
) = ![]()
Percentagem de risco atribuível à população (PAR%) = ![]()
onde ![]() = proporção de controles expostos = 55/195 = 0.28
= proporção de controles expostos = 55/195 = 0.28
* Entre parênteses, intervalos de confiança de 95% calculados usando as fórmulas na caixa no verso.
Fonte: Adaptado de Hayes et al. 1986.
Medidas relativas de efeito são usadas com mais frequência do que medidas absolutas para relatar a força de uma associação. Medidas absolutas, no entanto, podem fornecer uma melhor indicação do impacto de uma associação na saúde pública. Um pequeno aumento relativo em uma doença comum, como doença cardíaca, pode afetar mais pessoas (grande diferença de risco) e ter mais impacto na saúde pública do que um grande aumento relativo (mas pequena diferença absoluta) em uma doença rara, como angiossarcoma do fígado.
Teste de significância
O teste de significância estatística geralmente é realizado em medidas de efeito para avaliar a probabilidade de que o efeito observado seja diferente da hipótese nula (ou seja, nenhum efeito). Embora muitos estudos, particularmente em outras áreas da pesquisa biomédica, possam expressar importância por valores p, estudos epidemiológicos geralmente apresentam intervalos de confiança (CI) (também chamado Limites de confiança). Um intervalo de confiança de 95%, por exemplo, é uma faixa de valores para a medida de efeito que inclui a medida estimada obtida a partir dos dados do estudo e aquela que tem 95% de probabilidade de incluir o valor verdadeiro. Valores fora do intervalo são considerados improváveis de incluir a verdadeira medida do efeito. Se o IC para uma razão de taxas incluir a unidade, não haverá diferença estatisticamente significativa entre os grupos que estão sendo comparados.
Os intervalos de confiança são mais informativos do que os valores-p sozinhos. O tamanho de um valor-p é determinado por um ou ambos os dois motivos. Ou a medida de associação (por exemplo, razão de taxa, diferença de risco) é grande ou as populações em estudo são grandes. Por exemplo, uma pequena diferença nas taxas de doença observadas em uma grande população pode produzir um valor-p altamente significativo. As razões para o grande valor-p não podem ser identificadas apenas pelo valor-p. Os intervalos de confiança, no entanto, nos permitem separar os dois fatores. Primeiro, a magnitude do efeito é perceptível pelos valores da medida do efeito e pelos números incluídos no intervalo. Taxas de risco maiores, por exemplo, indicam um efeito mais forte. Em segundo lugar, o tamanho da população afeta a largura do intervalo de confiança. Populações pequenas com estimativas estatisticamente instáveis geram intervalos de confiança mais amplos do que populações maiores.
O nível de confiança escolhido para expressar a variabilidade dos resultados (a “significância estatística”) é arbitrário, mas tradicionalmente tem sido de 95%, o que corresponde a um p-valor de 0.05. Um intervalo de confiança de 95% tem 95% de probabilidade de conter a verdadeira medida do efeito. Outros níveis de confiança, como 90%, são usados ocasionalmente.
As exposições podem ser dicotômicas (por exemplo, expostas e não expostas) ou podem envolver muitos níveis de exposição. As medidas de efeito (ou seja, resposta) podem variar de acordo com o nível de exposição. avaliando resposta à exposição relações é uma parte importante da interpretação dos dados epidemiológicos. O análogo à exposição-resposta em estudos com animais é “dose-resposta”. Se a resposta aumentar com o nível de exposição, é mais provável que uma associação seja causal do que se nenhuma tendência for observada. Os testes estatísticos para avaliar as relações exposição-resposta incluem o teste de extensão de Mantel e o teste de tendência qui-quadrado.
estandardização
Para levar em consideração outros fatores além da exposição primária de interesse e da doença, medidas de associação podem ser padronizado através de técnicas de estratificação ou regressão. Estratificação significa dividir as populações em grupos homogêneos com relação ao fator (por exemplo, grupos de gênero, grupos de idade, grupos de fumantes). As razões de risco ou odds ratio são calculadas para cada estrato e as médias ponderadas gerais das razões de risco ou odds ratio são calculadas. Esses valores globais refletem a associação entre a exposição primária e a doença, ajustada pelo fator de estratificação, ou seja, a associação com os efeitos do fator de estratificação removido.
A taxa de taxa padronizada (SRR) é a razão de duas taxas padronizadas. Em outras palavras, um SRR é uma média ponderada de índices de taxa específicos de estrato, onde os pesos para cada estrato são a distribuição de pessoa-tempo do grupo não exposto ou referente. SRRs para dois ou mais grupos podem ser comparados se os mesmos pesos forem usados. Intervalos de confiança podem ser construídos para SRRs como para razões de taxa.
A taxa de mortalidade padronizada (SMR) é uma média ponderada de razões de taxas específicas por idade onde os pesos (por exemplo, pessoa-tempo em risco) vêm do grupo em estudo e as taxas vêm da população de referência, o oposto da situação em um SRR. A população de referência usual é a população em geral, cujas taxas de mortalidade podem estar prontamente disponíveis e baseadas em grandes números e, portanto, são mais estáveis do que usando taxas de uma coorte não exposta ou subgrupo da população ocupacional em estudo. Usar os pesos da coorte em vez da população de referência é chamado de padronização indireta. O SMR é a razão entre o número observado de mortes na coorte e o número esperado, com base nas taxas da população de referência (a razão geralmente é multiplicada por 100 para apresentação). Se não houver associação, o SMR é igual a 100. Deve-se observar que, como as taxas vêm da população de referência e os pesos vêm do grupo de estudo, dois ou mais SMRs tendem a não ser comparáveis. Essa não comparabilidade é muitas vezes esquecida na interpretação dos dados epidemiológicos, e conclusões errôneas podem ser tiradas.
Efeito Trabalhador Saudável
É muito comum que as coortes ocupacionais tenham mortalidade total menor do que a população em geral, mesmo que os trabalhadores tenham maior risco de causas selecionadas de morte por exposições no local de trabalho. Esse fenômeno, chamado de efeito do trabalhador saudável, reflete o fato de que qualquer grupo de pessoas empregadas provavelmente é mais saudável, em média, do que a população em geral, que inclui trabalhadores e pessoas incapacitadas para o trabalho devido a doenças e deficiências. A taxa de mortalidade geral na população em geral tende a ser maior do que a taxa nos trabalhadores. O efeito varia em intensidade de acordo com a causa da morte. Por exemplo, parece ser menos importante para o câncer em geral do que para a doença pulmonar obstrutiva crônica. Uma razão para isso é que é provável que a maioria dos cânceres não tenha se desenvolvido a partir de qualquer predisposição para o câncer subjacente à seleção de emprego/carreira em uma idade mais jovem. O efeito do trabalhador saudável em um determinado grupo de trabalhadores tende a diminuir com o tempo.
Mortalidade Proporcional
Às vezes, uma tabulação completa de uma coorte (ou seja, tempo de pessoa em risco) não está disponível e há informações apenas sobre as mortes ou algum subconjunto de mortes sofridas pela coorte (por exemplo, mortes entre aposentados e empregados ativos, mas não entre trabalhadores que deixou o emprego antes de se tornar elegível para uma pensão). O cálculo de anos-pessoa requer métodos especiais para lidar com a avaliação de tempo-pessoa, incluindo métodos de tabela de vida. Sem informações totais de pessoa-tempo em todos os membros da coorte, independentemente do estado da doença, SMRs e SRRs não podem ser calculados. Em vez de, taxas de mortalidade proporcional (PMRs) podem ser usados. Um PMR é a razão entre o número de óbitos observados por uma causa específica em comparação com o número esperado, baseado na proporção do total de óbitos por causa específica na população de referência, multiplicado pelo número total de óbitos no estudo grupo, multiplicado por 100.
Como a proporção de mortes por todas as causas combinadas deve ser igual a 1 (PMR = 100), algumas PMRs podem parecer excessivas, mas na verdade são infladas artificialmente devido a déficits reais em outras causas de morte. Da mesma forma, alguns déficits aparentes podem apenas refletir excessos reais de outras causas de morte. Por exemplo, se os aplicadores aéreos de pesticidas tiverem um grande excesso real de mortes devido a acidentes, a exigência matemática de que o PMR para todas as causas combinadas seja igual a 100 pode fazer com que uma ou outra causa de morte pareça deficiente, mesmo que a mortalidade seja excessiva. Para amenizar esse problema potencial, os pesquisadores interessados principalmente no câncer podem calcular taxas de mortalidade por câncer proporcionais (PCMR). Os PCMRs comparam o número observado de mortes por câncer ao número esperado com base na proporção do total de mortes por câncer (em vez de todas as mortes) para o câncer de interesse na população de referência multiplicado pelo número total de mortes por câncer no grupo de estudo, multiplicado por 100. Assim, o PCMR não será afetado por uma aberração (excesso ou déficit) em uma causa de morte não oncológica, como acidentes, doenças cardíacas ou doenças pulmonares não malignas.
Os estudos de PMR podem ser melhor analisados usando taxas de chance de mortalidade (MORs), essencialmente analisando os dados como se fossem de um estudo de caso-controle. Os “controles” são as mortes de um subconjunto de todas as mortes que se acredita não estarem relacionadas à exposição em estudo. Por exemplo, se o principal interesse do estudo fosse o câncer, as taxas de chances de mortalidade poderiam ser calculadas comparando a exposição entre as mortes por câncer com a exposição entre as mortes cardiovasculares. Esta abordagem, como a PCMR, evita os problemas com a PMR que surgem quando uma flutuação em uma causa de morte afeta o risco aparente de outra simplesmente porque a PMR geral deve ser igual a 100. A escolha das causas de morte de controle é crítica, porém . Conforme mencionado acima, eles não devem estar relacionados à exposição, mas a possível relação entre exposição e doença pode não ser conhecida para muitas doenças de controle potenciais.
Risco Atribuível
Existem medidas disponíveis que expressam a quantidade de doença que seria atribuível a uma exposição se a associação observada entre a exposição e a doença fosse causal. o risco atribuível no exposto (A. R.e) é a taxa de doença nos expostos menos a taxa nos não expostos. Como as taxas de doença não podem ser medidas diretamente em estudos de caso-controle, o ARe é calculável apenas para estudos de coorte. Uma medida relacionada, mais intuitiva, o percentual de risco atribuível no exposto (A. R.e%), pode ser obtido a partir de qualquer projeto de estudo. O are% é a proporção de casos que surgem na população exposta que é atribuível à exposição (ver tabela 2 e tabela 3 para a fórmula). O are% é a razão de taxa (ou razão de chances) menos 1, dividido pela razão de taxa (ou razão de chances), multiplicado por 100.
A risco atribuível à população (PAR) e o porcentagem de risco atribuível da população (PAR%) ou fração etiológica, expressam a quantidade de doença na população total, que é composta por expostos e não expostos, devido à exposição se a associação observada for causal. O PAR pode ser obtido a partir de estudos de coorte (tabela 28.3) e o PAR% pode ser calculado em estudos de coorte e de caso-controle (tabela 2 e tabela 3).
Representatividade
Existem várias medidas de risco que foram descritas. Cada um assume métodos subjacentes para a contagem de eventos e nos representantes desses eventos para um grupo definido. Quando os resultados são comparados entre os estudos, uma compreensão dos métodos usados é essencial para explicar quaisquer diferenças observadas.
Biomecânica
Objetivos e Princípios
A biomecânica é uma disciplina que aborda o estudo do corpo como se fosse apenas um sistema mecânico: todas as partes do corpo são comparadas a estruturas mecânicas e são estudadas como tal. As seguintes analogias podem, por exemplo, ser feitas:
- ossos: alavancas, membros estruturais
- carne: volumes e massas
- juntas: superfícies de apoio e articulações
- revestimentos de juntas: lubrificantes
- músculos: motores, molas
- nervos: mecanismos de controle de feedback
- órgãos: fontes de alimentação
- tendões: cordas
- tecido: molas
- cavidades do corpo: balões.
O principal objetivo da biomecânica é estudar a forma como o corpo produz força e gera movimento. A disciplina baseia-se principalmente em anatomia, matemática e física; disciplinas relacionadas são antropometria (o estudo das medidas do corpo humano), fisiologia do trabalho e cinesiologia (o estudo dos princípios da mecânica e anatomia em relação ao movimento humano).
Ao considerar a saúde ocupacional do trabalhador, a biomecânica ajuda a entender por que algumas tarefas causam lesões e problemas de saúde. Alguns tipos relevantes de efeitos adversos à saúde são tensão muscular, problemas nas articulações, problemas nas costas e fadiga.
Tensões e entorses nas costas e problemas mais sérios envolvendo os discos intervertebrais são exemplos comuns de lesões no local de trabalho que podem ser evitadas. Isso geralmente ocorre devido a uma sobrecarga específica repentina, mas também pode refletir o esforço excessivo do corpo por muitos anos: os problemas podem ocorrer repentinamente ou podem levar tempo para se desenvolver. Um exemplo de problema que se desenvolve com o tempo é o “dedo de costureira”. Uma descrição recente descreve as mãos de uma mulher que, após 28 anos de trabalho em uma fábrica de roupas, além de costurar em seu tempo livre, desenvolveu uma pele endurecida e espessa e uma incapacidade de flexionar os dedos (Poole 1993). (Especificamente, ela sofria de uma deformidade de flexão do dedo indicador direito, nódulos de Heberden proeminentes no dedo indicador e no polegar da mão direita e uma calosidade proeminente no dedo médio direito devido ao atrito constante da tesoura.) Raio-X. filmes de suas mãos mostraram alterações degenerativas graves nas articulações externas dos dedos indicador e médio direitos, com perda de espaço articular, esclerose articular (endurecimento do tecido), osteófitos (crescimentos ósseos na articulação) e cistos ósseos.
A inspeção no local de trabalho mostrou que esses problemas eram devidos à hiperextensão repetida (dobrar-se) da articulação mais externa do dedo. A sobrecarga mecânica e a restrição do fluxo sanguíneo (visível como um branqueamento do dedo) seriam máximas nessas articulações. Esses problemas se desenvolveram em resposta ao esforço muscular repetido em um local diferente do músculo.
A biomecânica ajuda a sugerir maneiras de projetar tarefas para evitar esses tipos de lesões ou melhorar tarefas mal projetadas. As soluções para esses problemas específicos são redesenhar a tesoura e alterar as tarefas de costura para eliminar a necessidade das ações executadas.
Dois princípios importantes da biomecânica são:
- Os músculos vêm em pares. Os músculos só podem se contrair, portanto, para qualquer articulação, deve haver um músculo (ou grupo muscular) para movê-lo em uma direção e um músculo (ou grupo muscular) correspondente para movê-lo na direção oposta. A Figura 1 ilustra o ponto para a articulação do cotovelo.
- Os músculos se contraem com mais eficiência quando o par muscular está em equilíbrio relaxado. O músculo age de forma mais eficiente quando está na região intermediária da articulação que flexiona. Isso ocorre por dois motivos: primeiro, se o músculo tentar se contrair ao ser encurtado, ele puxará o músculo oposto alongado. Como o último é alongado, ele aplicará uma contraforça elástica que o músculo em contração deve superar. A Figura 2 mostra como a força muscular varia com o comprimento do músculo.
Figura 1. Os músculos esqueléticos ocorrem em pares para iniciar ou reverter um movimento
Figura 2. A tensão muscular varia com o comprimento do músculo
Em segundo lugar, se o músculo tentar se contrair fora da amplitude média do movimento da articulação, ele operará em desvantagem mecânica. A Figura 3 ilustra a mudança na vantagem mecânica do cotovelo em três posições diferentes.
Figura 3. Posições ideais para o movimento articular
Um critério importante para o planejamento do trabalho decorre desses princípios: o trabalho deve ser organizado de modo que ocorra com os músculos opostos de cada articulação em equilíbrio relaxado. Para a maioria das articulações, isso significa que a articulação deve estar em sua amplitude média de movimento.
Esta regra também significa que a tensão muscular será mínima enquanto uma tarefa é executada. Um exemplo de violação da regra é a síndrome de uso excessivo (LER, ou lesão por esforço repetitivo) que afeta os músculos da parte superior do antebraço em operadores de teclado que habitualmente operam com o punho flexionado para cima. Freqüentemente, esse hábito é imposto ao operador pelo design do teclado e da estação de trabalho.
Aplicações
A seguir estão alguns exemplos que ilustram a aplicação da biomecânica.
O diâmetro ideal dos cabos das ferramentas
O diâmetro de um cabo afeta a força que os músculos da mão podem aplicar a uma ferramenta. A pesquisa mostrou que o diâmetro ideal do cabo depende do uso para o qual a ferramenta é colocada. Para exercer impulso ao longo da linha do cabo, o melhor diâmetro é aquele que permite que os dedos e o polegar assumam uma pegada ligeiramente sobreposta. Isso é cerca de 40 mm. Para exercer torque, um diâmetro de cerca de 50-65 mm é ideal. (Infelizmente, para ambos os propósitos, a maioria dos identificadores é menor que esses valores.)
O uso de alicate
Como um caso especial de cabo, a capacidade de exercer força com o alicate depende da separação do cabo, conforme mostrado na figura 4.
Figura 4. Força de preensão das garras do alicate exercida por usuários masculinos e femininos em função da separação do cabo
postura sentada
A eletromiografia é uma técnica que pode ser usada para medir a tensão muscular. Em um estudo sobre a tensão no eretor da espinha músculos (das costas) de indivíduos sentados, verificou-se que inclinar-se para trás (com o encosto inclinado) reduziu a tensão nesses músculos. O efeito pode ser explicado porque o encosto suporta mais o peso da parte superior do corpo.
Estudos de raios-X de indivíduos em uma variedade de posturas mostraram que a posição de equilíbrio relaxado dos músculos que abrem e fecham a articulação do quadril corresponde a um ângulo do quadril de cerca de 135º. Isso é próximo da posição (128º) naturalmente adotada por essa junta em condições de imponderabilidade (no espaço). Na postura sentada, com um ângulo de 90º no quadril, os músculos isquiotibiais que percorrem as articulações do joelho e do quadril tendem a puxar o sacro (a parte da coluna vertebral que se conecta com a pelve) para uma posição vertical. O efeito é remover a lordose natural (curvatura) da coluna lombar; as cadeiras devem ter encostos apropriados para corrigir esse esforço.
Chave de fenda
Por que os parafusos são inseridos no sentido horário? A prática provavelmente surgiu no reconhecimento inconsciente de que os músculos que giram o braço direito no sentido horário (a maioria das pessoas são destras) são maiores (e, portanto, mais poderosos) do que os músculos que o giram no sentido anti-horário.
Observe que os canhotos estarão em desvantagem ao inserir os parafusos manualmente. Cerca de 9% da população é canhota e, portanto, precisará de ferramentas especiais em algumas situações: tesouras e abridores de latas são dois exemplos.
Um estudo de pessoas usando chaves de fenda em uma tarefa de montagem revelou uma relação mais sutil entre um movimento específico e um problema de saúde específico. Verificou-se que quanto maior o ângulo do cotovelo (mais reto o braço), mais as pessoas tinham inflamação no cotovelo. A razão para este efeito é que o músculo que gira o antebraço (o bíceps) também puxa a cabeça do rádio (osso do antebraço) para o capítulo (cabeça arredondada) do úmero (osso do braço). O aumento da força no ângulo maior do cotovelo causou maior força de atrito no cotovelo, com consequente aquecimento da articulação, levando à inflamação. No ângulo mais alto, o músculo também teve que puxar com maior força para efetuar a ação de parafuso, então uma força maior foi aplicada do que seria necessária com o cotovelo em cerca de 90º. A solução foi aproximar a tarefa dos operadores para reduzir o ângulo do cotovelo para cerca de 90º.
Os casos acima demonstram que uma compreensão adequada da anatomia é necessária para a aplicação da biomecânica no local de trabalho. Os projetistas de tarefas podem precisar consultar especialistas em anatomia funcional para antecipar os tipos de problemas discutidos. (O ergonomista de bolso (Brown e Mitchell 1986) com base na pesquisa eletromiográfica, sugere muitas maneiras de reduzir o desconforto físico no trabalho.)
Manuseio manual de materiais
O termo manuseio manual inclui levantar, abaixar, empurrar, puxar, carregar, mover, segurar e conter, e abrange uma grande parte das atividades da vida profissional.
A biomecânica tem relevância direta óbvia para o trabalho de manuseio manual, uma vez que os músculos devem se mover para realizar tarefas. A questão é: quanto trabalho físico se pode razoavelmente esperar que as pessoas façam? A resposta depende das circunstâncias; há realmente três perguntas que precisam ser feitas. Cada um tem uma resposta baseada em critérios cientificamente pesquisados:
- Quanto pode ser manuseado sem danos ao corpo (na forma, por exemplo, de tensão muscular, lesão no disco ou problemas nas articulações)? Isso é chamado de critério biomecânico.
- Quanto pode ser manuseado sem sobrecarregar os pulmões (respirar com dificuldade a ponto de ofegar)? Isso é chamado de critério fisiológico.
- Quanto as pessoas se sentem capazes de lidar confortavelmente? Isso é chamado de critério psicofísico.
Há uma necessidade desses três critérios diferentes porque há três reações amplamente diferentes que podem ocorrer nas tarefas de elevação: se o trabalho durar o dia todo, a preocupação será como a pessoa sente sobre a tarefa — o critério psicofísico; se a força a ser aplicada for grande, a preocupação seria que músculos e articulações fiquem não sobrecarregado ao ponto de dano - o critério biomecânico; e se o taxa de trabalho for muito grande, então pode muito bem ultrapassar o critério fisiológico, ou a capacidade aeróbica da pessoa.
Muitos fatores determinam a extensão da carga colocada no corpo por uma tarefa de movimentação manual. Todos eles sugerem oportunidades de controle.
Postura e Movimentos
Se a tarefa exigir que uma pessoa torça ou estenda uma carga para a frente, o risco de lesões é maior. A estação de trabalho geralmente pode ser reprojetada para evitar essas ações. Mais lesões nas costas ocorrem quando o levantamento começa no nível do solo em comparação com o nível do meio da coxa, e isso sugere medidas de controle simples. (Isso também se aplica ao levantamento de peso.)
A carga.
A própria carga pode influenciar o manuseio devido ao seu peso e localização. Outros fatores, como sua forma, sua estabilidade, seu tamanho e seu escorregadio podem afetar a facilidade de uma tarefa de manuseio.
Organização e ambiente.
A forma como o trabalho é organizado, tanto fisicamente quanto ao longo do tempo (temporalmente), também influencia o manejo. É melhor distribuir o fardo de descarregar um caminhão em uma área de entrega entre várias pessoas por uma hora, em vez de pedir a um trabalhador que passe o dia todo na tarefa. O ambiente influencia o manuseio - pouca luz, pisos bagunçados ou irregulares e manutenção inadequada podem fazer com que uma pessoa tropece.
Fatores pessoais.
As habilidades pessoais de manuseio, a idade da pessoa e as roupas usadas também podem influenciar os requisitos de manuseio. Educação para treinamento e levantamento são necessários tanto para fornecer as informações necessárias quanto para dar tempo para o desenvolvimento das habilidades físicas de manuseio. Os mais jovens correm mais riscos; por outro lado, os idosos têm menos força e menos capacidade fisiológica. Roupas apertadas podem aumentar a força muscular necessária em uma tarefa, pois as pessoas se esforçam contra o pano apertado; exemplos clássicos são o uniforme de enfermeira e o macacão justo quando as pessoas trabalham acima de suas cabeças.
Limites de peso recomendados
Os pontos mencionados acima indicam que é impossível afirmar um peso que seja “seguro” em todas as circunstâncias. (Os limites de peso tendem a variar de país para país de maneira arbitrária. Os estivadores indianos, por exemplo, já foram “autorizados” a levantar 110 kg, enquanto seus equivalentes na antiga República Democrática Popular da Alemanha foram “limitados” a 32 kg .) Os limites de peso também tendem a ser muito grandes. Os 55 kg sugeridos em muitos países agora são considerados muito grandes com base em evidências científicas recentes. O Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH) nos Estados Unidos adotou 23 kg como limite de carga em 1991 (Waters et al. 1993).
Cada tarefa de levantamento precisa ser avaliada por seus próprios méritos. Uma abordagem útil para determinar um limite de peso para uma tarefa de levantamento é a equação desenvolvida pelo NIOSH:
RWL = LC x HM x VM x DM x AM x CM x FM
Onde
RWL = limite de peso recomendado para a tarefa em questão
HM = a distância horizontal do centro de gravidade da carga até o ponto médio entre os tornozelos (mínimo 15 cm, máximo 80 cm)
VM = a distância vertical entre o centro de gravidade da carga e o piso no início da elevação (máximo 175 cm)
DM = curso vertical do elevador (mínimo 25 cm, máximo 200 cm)
AM = fator de assimetria – o ângulo em que a tarefa se desvia diretamente na frente do corpo
CM = multiplicador de acoplamento – a capacidade de obter um bom controle sobre o item a ser levantado, que é encontrado em uma tabela de referência
FM = multiplicadores de frequência – a frequência do levantamento.
Todas as variáveis de comprimento na equação são expressas em unidades de centímetros. Deve-se notar que 23 kg é o peso máximo que o NIOSH recomenda para elevação. Isso foi reduzido de 40 kg depois que a observação de muitas pessoas fazendo muitas tarefas de levantamento revelou que a distância média do corpo no início do levantamento é de 25 cm, não os 15 cm assumidos em uma versão anterior da equação (NIOSH 1981 ).
Índice de levantamento.
Comparando o peso a ser levantado na tarefa e o RWL, um índice de levantamento (LI) pode ser obtido pela relação:
LI=(peso a ser manuseado)/RWL.
Portanto, o uso particularmente valioso da equação NIOSH é a colocação de tarefas de levantamento em ordem de gravidade, usando o índice de levantamento para definir prioridades de ação. (A equação tem várias limitações, no entanto, que precisam ser compreendidas para sua aplicação mais eficaz. Veja Waters et al. 1993).
Estimando a Compressão Espinhal Imposta pela Tarefa
O software de computador está disponível para estimar a compressão espinhal produzida por uma tarefa de movimentação manual. Os Programas de Previsão de Força Estática 2D e 3D da Universidade de Michigan (“Backsoft”) estimam a compressão da coluna vertebral. As entradas necessárias para o programa são:
- a postura em que a atividade de manipulação é realizada
- a força exercida
- a direção do esforço de força
- o número de mãos que exercem a força
- o percentil da população em estudo.
Os programas 2D e 3D diferem porque o software 3D permite cálculos aplicados a posturas em três dimensões. A saída do programa fornece dados de compressão da coluna vertebral e lista a porcentagem da população selecionada que seria capaz de realizar a tarefa específica sem exceder os limites sugeridos para seis articulações: tornozelo, joelho, quadril, primeiro disco sacro lombar, ombro e cotovelo. Este método também tem uma série de limitações que precisam ser totalmente compreendidas para extrair o máximo valor do programa.
Imunotoxicologia
As funções do sistema imunológico são proteger o corpo de agentes infecciosos invasores e fornecer vigilância imunológica contra o surgimento de células tumorais. Possui uma primeira linha de defesa inespecífica e que pode iniciar ela própria as reações efetoras, e um ramo específico adquirido, no qual linfócitos e anticorpos carregam a especificidade de reconhecimento e posterior reatividade ao antígeno.
A imunotoxicologia foi definida como “a disciplina preocupada com o estudo dos eventos que podem levar a efeitos indesejados como resultado da interação de xenobióticos com o sistema imunológico. Esses eventos indesejados podem resultar como consequência de (1) um efeito direto e/ou indireto do xenobiótico (e/ou seu produto de biotransformação) no sistema imunológico, ou (2) uma resposta imunológica do hospedeiro ao composto e/ou seu(s) metabólito(s) ou antígenos do hospedeiro modificados pelo composto ou seus metabólitos” (Berlin et al. 1987).
Quando o sistema imunológico atua como um alvo passivo de insultos químicos, o resultado pode ser uma diminuição da resistência a infecções e certas formas de neoplasia, ou desregulação/estimulação imunológica que pode exacerbar alergia ou autoimunidade. No caso de o sistema imunológico responder à especificidade antigênica do xenobiótico ou do antígeno do hospedeiro modificado pelo composto, a toxicidade pode se manifestar como alergias ou doenças autoimunes.
Modelos animais para investigar a supressão imunológica induzida por produtos químicos foram desenvolvidos e vários desses métodos são validados (Burleson, Munson e Dean 1995; IPCS 1996). Para fins de teste, uma abordagem em camadas é seguida para fazer uma seleção adequada do grande número de ensaios disponíveis. Geralmente, o objetivo do primeiro nível é identificar potenciais imunotóxicos. Se for identificada potencial imunotoxicidade, uma segunda fase de testes é realizada para confirmar e caracterizar melhor as alterações observadas. As investigações de terceiro nível incluem estudos especiais sobre o mecanismo de ação do composto. Vários xenobióticos foram identificados como imunotóxicos causando imunossupressão em tais estudos com animais de laboratório.
O banco de dados sobre distúrbios da função imune em humanos por produtos químicos ambientais é limitado (Descotes 1986; NRC Subcommittee on Immunotoxicology 1992). O uso de marcadores de imunotoxicidade tem recebido pouca atenção em estudos clínicos e epidemiológicos para investigar o efeito desses produtos químicos na saúde humana. Esses estudos não têm sido realizados com frequência e sua interpretação muitas vezes não permite conclusões inequívocas, devido, por exemplo, à natureza descontrolada da exposição. Portanto, atualmente, a avaliação da imunotoxicidade em roedores, com posterior extrapolação para o homem, forma a base das decisões sobre perigo e risco.
As reações de hipersensibilidade, principalmente asma alérgica e dermatite de contato, são importantes problemas de saúde ocupacional nos países industrializados (Vos, Younes e Smith, 1995). O fenômeno da sensibilização de contato foi investigado primeiro na cobaia (Andersen e Maibach 1985). Até recentemente, esta tem sido a espécie de escolha para testes preditivos. Muitos métodos de teste de cobaia estão disponíveis, sendo os mais freqüentemente empregados o teste de maximização de cobaia e o teste de remendo ocluído de Buehler. Testes de cobaias e abordagens mais recentes desenvolvidas em camundongos, como testes de inchaço da orelha e o ensaio de linfonodo local, fornecem ao toxicologista as ferramentas para avaliar o risco de sensibilização da pele. A situação com relação à sensibilização do trato respiratório é muito diferente. Ainda não existem métodos bem validados ou amplamente aceitos disponíveis para a identificação de alérgenos respiratórios químicos, embora tenha havido progresso no desenvolvimento de modelos animais para a investigação de alergia respiratória química em cobaias e camundongos.
Dados humanos mostram que agentes químicos, em particular drogas, podem causar doenças autoimunes (Kammüller, Bloksma e Seinen 1989). Existem vários modelos animais experimentais de doenças autoimunes humanas. Tal compreende tanto patologia espontânea (por exemplo lúpus eritematoso sistêmico em camundongos New Zealand Black) quanto fenômenos autoimunes induzidos por imunização experimental com um autoantígeno de reação cruzada (por exemplo, artrite induzida pelo adjuvante H37Ra em ratos da linhagem Lewis). Esses modelos são aplicados na avaliação pré-clínica de drogas imunossupressoras. Muito poucos estudos abordaram o potencial desses modelos para avaliar se um xenobiótico exacerba a autoimunidade induzida ou congênita. Modelos animais adequados para investigar a capacidade de substâncias químicas de induzir doenças autoimunes praticamente não existem. Um modelo que é usado de forma limitada é o ensaio do linfonodo poplíteo em camundongos. Como a situação em humanos, fatores genéticos desempenham um papel crucial no desenvolvimento de doença autoimune (DA) em animais de laboratório, o que limitará o valor preditivo de tais testes.
O sistema imunológico
A principal função do sistema imunológico é a defesa contra bactérias, vírus, parasitas, fungos e células neoplásicas. Isso é alcançado pelas ações de vários tipos de células e seus mediadores solúveis em um concerto afinado. A defesa do hospedeiro pode ser dividida em resistência inespecífica ou inata e imunidade específica ou adquirida mediada por linfócitos (Roitt, Brostoff e Male 1989).
Componentes do sistema imunológico estão presentes em todo o corpo (Jones et al. 1990). O compartimento de linfócitos é encontrado dentro dos órgãos linfóides (figura 1). A medula óssea e o timo são classificados como órgãos linfoides primários ou centrais; os órgãos linfóides secundários ou periféricos incluem linfonodos, baço e tecido linfóide ao longo de superfícies secretoras, como os tratos gastrointestinal e respiratório, o chamado tecido linfóide associado à mucosa (MALT). Cerca de metade dos linfócitos do corpo estão localizados a qualquer momento no MALT. Além disso, a pele é um órgão importante para a indução de respostas imunes aos antígenos presentes na pele. Importantes neste processo são as células de Langerhans epidérmicas que possuem uma função de apresentação de antígenos.
Figura 1. Órgãos e tecidos linfoides primários e secundários
Células fagocíticas da linhagem de monócitos/macrófagos, denominadas sistema mononuclear fagocitário (MPS), ocorrem em órgãos linfóides e também em locais extranodais; os fagócitos extranodais incluem células de Kupffer no fígado, macrófagos alveolares no pulmão, macrófagos mesangiais no rim e células gliais no cérebro. Os leucócitos polimorfonucleares (PMNs) estão presentes principalmente no sangue e na medula óssea, mas se acumulam nos locais de inflamação.
Defesa não específica
Uma primeira linha de defesa aos microrganismos é executada por uma barreira física e química, como a pele, o trato respiratório e o trato alimentar. Essa barreira é auxiliada por mecanismos de proteção não específicos, incluindo células fagocíticas, como macrófagos e leucócitos polimorfonucleares, que são capazes de matar patógenos, e células assassinas naturais, que podem lisar células tumorais e células infectadas por vírus. O sistema complemento e certos inibidores microbianos (por exemplo, lisozima) também participam da resposta inespecífica.
Imunidade específica
Após o contato inicial do hospedeiro com o patógeno, respostas imunes específicas são induzidas. A marca desta segunda linha de defesa é o reconhecimento específico de determinantes, chamados de antígenos ou epítopos, dos patógenos por receptores na superfície celular de linfócitos B e T. Após a interação com o antígeno específico, a célula portadora do receptor é estimulada a sofrer proliferação e diferenciação, produzindo um clone de células descendentes que são específicas para o antígeno desencadeante. As respostas imunes específicas auxiliam na defesa inespecífica apresentada aos patógenos, estimulando a eficácia das respostas inespecíficas. Uma característica fundamental da imunidade específica é que a memória se desenvolve. O contato secundário com o mesmo antígeno provoca uma resposta mais rápida e vigorosa, mas bem regulada.
O genoma não tem a capacidade de carregar os códigos de uma matriz de receptores de antígenos suficiente para reconhecer o número de antígenos que podem ser encontrados. O repertório de especificidade se desenvolve por um processo de rearranjos de genes. Este é um processo aleatório, durante o qual várias especificidades são trazidas. Isso inclui especificidades para autocomponentes, que são indesejáveis. Um processo de seleção que ocorre no timo (células T) ou na medula óssea (células B) opera para eliminar essas especificidades indesejáveis.
A função efetora imune normal e a regulação homeostática da resposta imune dependem de uma variedade de produtos solúveis, conhecidos coletivamente como citocinas, que são sintetizados e secretados por linfócitos e por outros tipos de células. As citocinas têm efeitos pleiotrópicos nas respostas imune e inflamatória. A cooperação entre diferentes populações de células é necessária para a resposta imune – a regulação das respostas de anticorpos, o acúmulo de células e moléculas imunes em locais inflamatórios, o início de respostas de fase aguda, o controle da função citotóxica de macrófagos e muitos outros processos centrais para a resistência do hospedeiro . Estes são influenciados e, em muitos casos, dependem de citocinas agindo individualmente ou em conjunto.
Dois braços de imunidade específica são reconhecidos - imunidade humoral e mediada por células ou imunidade celular:
imunidade humoral. No braço humoral, os linfócitos B são estimulados após o reconhecimento do antígeno pelos receptores da superfície celular. Os receptores de antígenos nos linfócitos B são imunoglobulinas (Ig). Células B maduras (células plasmáticas) iniciam a produção de imunoglobulinas específicas do antígeno que atuam como anticorpos no soro ou ao longo das superfícies mucosas. Existem cinco classes principais de imunoglobulinas: (1) IgM, Ig pentamérica com ótima capacidade aglutinante, que é produzida pela primeira vez após estimulação antigênica; (2) IgG, a principal Ig em circulação, que pode atravessar a placenta; (3) IgA, Ig secretora para proteção de superfícies mucosas; (4) IgE, fixação de Ig a mastócitos ou granulócitos basofílicos envolvidos em reações de hipersensibilidade imediata e (5) IgD, cuja principal função é como receptora em linfócitos B.
Imunidade mediada por células. O braço celular do sistema imunológico específico é mediado por linfócitos T. Essas células também possuem receptores de antígenos em suas membranas. Eles reconhecem antígenos se apresentados por células apresentadoras de antígenos no contexto de antígenos de histocompatibilidade. Portanto, essas células têm uma restrição além da especificidade do antígeno. As células T funcionam como células auxiliares para várias respostas imunes (incluindo humorais), mediam o recrutamento de células inflamatórias e podem, como células T citotóxicas, matar células-alvo após o reconhecimento específico do antígeno.
Mecanismos de Imunotoxicidade
Imunossupressão
A resistência efetiva do hospedeiro depende da integridade funcional do sistema imunológico, que por sua vez requer que as células e moléculas componentes que orquestram as respostas imunes estejam disponíveis em número suficiente e de forma operacional. As imunodeficiências congênitas em humanos são frequentemente caracterizadas por defeitos em certas linhagens de células-tronco, resultando em produção prejudicada ou ausente de células imunes. Por analogia com doenças de imunodeficiência humana congênita e adquirida, a imunossupressão induzida por produtos químicos pode resultar simplesmente de um número reduzido de células funcionais (IPCS 1996). A ausência ou número reduzido de linfócitos pode ter efeitos mais ou menos profundos no estado imunológico. Alguns estados de imunodeficiência e imunossupressão grave, como podem ocorrer em transplantes ou terapia citostática, têm sido associados em particular ao aumento da incidência de infecções oportunistas e de certas doenças neoplásicas. As infecções podem ser bacterianas, virais, fúngicas ou protozoárias, e o tipo de infecção predominante depende da imunodeficiência associada. Pode-se esperar que a exposição a produtos químicos ambientais imunossupressores resulte em formas mais sutis de imunossupressão, que podem ser difíceis de detectar. Estes podem levar, por exemplo, a um aumento da incidência de infecções como gripe ou resfriado comum.
Tendo em vista a complexidade do sistema imunológico, com a grande variedade de células, mediadores e funções que formam uma rede complicada e interativa, os compostos imunotóxicos têm inúmeras oportunidades de exercer um efeito. Embora a natureza das lesões iniciais induzidas por muitos produtos químicos imunotóxicos ainda não tenha sido elucidada, há cada vez mais informações disponíveis, principalmente derivadas de estudos em animais de laboratório, sobre as alterações imunobiológicas que resultam na depressão da função imune (Dean et al. 1994). . Podem ocorrer efeitos tóxicos nas seguintes funções críticas (e são dados alguns exemplos de compostos imunotóxicos que afetam essas funções):
- desenvolvimento e expansão de diferentes populações de células-tronco (o benzeno exerce efeitos imunotóxicos no nível das células-tronco, causando linfocitopenia)
- proliferação de várias células linfóides e mielóides, bem como tecidos de suporte nos quais essas células amadurecem e funcionam (compostos de organoestanho imunotóxicos suprimem a atividade proliferativa de linfócitos no córtex tímico através de citotoxicidade direta; a ação timotóxica de 2,3,7,8-tetracloro -dibenzo-p-dioxina (TCDD) e compostos relacionados é provavelmente devido a uma função prejudicada das células epiteliais do timo, em vez de toxicidade direta para os timócitos)
- captação, processamento e apresentação do antígeno pelos macrófagos e outras células apresentadoras de antígenos (um dos alvos do 7,12-dimetilbenz(a)antraceno (DMBA) e do chumbo é a apresentação do antígeno pelos macrófagos; um alvo da radiação ultravioleta é o antígeno- apresentando células de Langerhans)
- função reguladora das células T-helper e T-supressoras (a função das células T-helper é prejudicada por organoestanhos, aldicarb, bifenilos policlorados (PCBs), TCDD e DMBA; a função das células T-supressoras é reduzida pelo tratamento com baixa dose de ciclofosfamida)
- produção de várias citocinas ou interleucinas (benzo(a)pireno (BP) suprime a produção de interleucina-1; a radiação ultravioleta altera a produção de citocinas pelos queratinócitos)
- a síntese de várias classes de imunoglobulinas IgM e IgG é suprimida após o tratamento com PCB e óxido de tributilestanho (TBT) e aumentada após a exposição ao hexaclorobenzeno (HCB).
- regulação e ativação do complemento (afetada pelo TCDD)
- função das células T citotóxicas (3-metilcolantreno (3-MC), DMBA e TCDD suprimem a atividade das células T citotóxicas)
- função das células assassinas naturais (NK) (a atividade NK pulmonar é suprimida pelo ozônio; a atividade NK esplênica é prejudicada pelo níquel)
- quimiotaxia de macrófagos e leucócitos polimorfonucleares e funções citotóxicas (o ozônio e o dióxido de nitrogênio prejudicam a atividade fagocítica dos macrófagos alveolares).
Alergia
Alergia pode ser definido como os efeitos adversos à saúde que resultam da indução e eliciação de respostas imunes específicas. Quando ocorrem reações de hipersensibilidade sem envolvimento do sistema imunológico, o termo pseudo-alergia é usado. No contexto da imunotoxicologia, a alergia resulta de uma resposta imune específica a produtos químicos e medicamentos de interesse. A capacidade de um produto químico para sensibilizar os indivíduos está geralmente relacionada com a sua capacidade de se ligar covalentemente às proteínas do corpo. As reações alérgicas podem assumir uma variedade de formas e diferem em relação aos mecanismos imunológicos subjacentes e à velocidade da reação. Quatro tipos principais de reações alérgicas foram reconhecidos: Reações de hipersensibilidade do tipo I, que são efetuadas pelo anticorpo IgE e onde os sintomas se manifestam dentro de minutos após a exposição do indivíduo sensibilizado. As reações de hipersensibilidade do tipo II resultam do dano ou destruição das células hospedeiras por anticorpos. Neste caso, os sintomas tornam-se aparentes dentro de horas. As reações de hipersensibilidade tipo III, ou Arthus, também são mediadas por anticorpos, mas contra antígenos solúveis, e resultam da ação local ou sistêmica de imunocomplexos. Tipo IV, ou hipersensibilidade do tipo retardado, as reações são efetuadas por linfócitos T e normalmente os sintomas se desenvolvem 24 a 48 horas após a exposição do indivíduo sensibilizado.
Os dois tipos de alergia química de maior relevância para a saúde ocupacional são a sensibilidade de contato ou alergia cutânea e a alergia do trato respiratório.
Hipersensibilidade de contato. Um grande número de produtos químicos é capaz de causar sensibilização da pele. Após a exposição tópica de um indivíduo suscetível a um alérgeno químico, uma resposta de linfócitos T é induzida nos gânglios linfáticos de drenagem. Na pele, o alérgeno interage direta ou indiretamente com as células de Langerhans epidérmicas, que transportam o produto químico para os gânglios linfáticos e o apresentam de forma imunogênica aos linfócitos T responsivos. Os linfócitos T ativados por alérgenos proliferam, resultando em expansão clonal. O indivíduo agora está sensibilizado e responderá a uma segunda exposição dérmica ao mesmo produto químico com uma resposta imune mais agressiva, resultando em dermatite alérgica de contato. A reação inflamatória cutânea que caracteriza a dermatite alérgica de contato é secundária ao reconhecimento do alérgeno na pele por linfócitos T específicos. Esses linfócitos tornam-se ativados, liberam citocinas e causam o acúmulo local de outros leucócitos mononucleares. Os sintomas se desenvolvem cerca de 24 a 48 horas após a exposição do indivíduo sensibilizado e, portanto, a dermatite alérgica de contato representa uma forma de hipersensibilidade do tipo retardado. Causas comuns de dermatite alérgica de contato incluem produtos químicos orgânicos (como 2,4-dinitroclorobenzeno), metais (como níquel e cromo) e produtos vegetais (como urushiol da hera venenosa).
Hipersensibilidade respiratória. A hipersensibilidade respiratória é geralmente considerada uma reação de hipersensibilidade do Tipo I. No entanto, as reações de fase tardia e os sintomas mais crônicos associados à asma podem envolver processos imunológicos mediados por células (Tipo IV). Os sintomas agudos associados à alergia respiratória são efetuados pelo anticorpo IgE, cuja produção é provocada após a exposição do indivíduo suscetível ao alérgeno químico indutor. O anticorpo IgE distribui-se sistemicamente e liga-se, via receptores de membrana, a mastócitos que se encontram em tecidos vascularizados, incluindo o trato respiratório. Após a inalação do mesmo produto químico, ocorrerá uma reação de hipersensibilidade respiratória. O alérgeno associa-se à proteína e liga-se e faz ligações cruzadas com o anticorpo IgE ligado aos mastócitos. Isso, por sua vez, causa a degranulação dos mastócitos e a liberação de mediadores inflamatórios, como histamina e leucotrienos. Tais mediadores causam broncoconstrição e vasodilatação, resultando em sintomas de alergia respiratória; asma e/ou rinite. Os produtos químicos conhecidos por causar hipersensibilidade respiratória no homem incluem anidridos ácidos (como anidrido trimelítico), alguns diisocianatos (como diisocianato de tolueno), sais de platina e alguns corantes reativos. Além disso, a exposição crônica ao berílio é conhecida por causar doença pulmonar de hipersensibilidade.
Autoimunidade
Autoimunidade pode ser definida como a estimulação de respostas imunes específicas dirigidas contra antígenos “próprios” endógenos. A autoimunidade induzida pode resultar de alterações no equilíbrio dos linfócitos T reguladores ou da associação de um xenobiótico com componentes normais do tecido, de modo a torná-los imunogênicos (“altered self”). Drogas e produtos químicos conhecidos por induzir ou exacerbar acidentalmente efeitos como os da doença autoimune (AD) em indivíduos suscetíveis são compostos de baixo peso molecular (peso molecular de 100 a 500) que geralmente são considerados não imunogênicos. O mecanismo da DA por exposição química é praticamente desconhecido. A doença pode ser produzida diretamente por meio de anticorpos circulantes, indiretamente por meio da formação de complexos imunes ou como consequência da imunidade mediada por células, mas provavelmente ocorre por meio de uma combinação de mecanismos. A patogênese é mais bem conhecida em distúrbios hemolíticos imunes induzidos por drogas:
- A droga pode se ligar à membrana dos glóbulos vermelhos e interagir com um anticorpo específico da droga.
- A droga pode alterar a membrana dos glóbulos vermelhos de modo que o sistema imunológico considere a célula estranha.
- A droga e seu anticorpo específico formam imunocomplexos que aderem à membrana das hemácias para produzir lesões.
- A sensibilização das hemácias ocorre devido à produção de autoanticorpos das hemácias.
Verificou-se que uma variedade de substâncias químicas e drogas, em particular as últimas, induzem respostas autoimunes (Kamüller, Bloksma e Seinen 1989). A exposição ocupacional a produtos químicos pode ocasionar incidentalmente síndromes semelhantes à DA. A exposição a cloreto de vinila monomérico, tricloroetileno, percloroetileno, resinas epóxi e pó de sílica pode induzir síndromes semelhantes à esclerodermia. Uma síndrome semelhante ao lúpus eritematoso sistêmico (LES) foi descrita após a exposição à hidrazina. A exposição ao diisocianato de tolueno tem sido associada à indução de púrpura trombocitopênica. Metais pesados, como o mercúrio, têm sido implicados em alguns casos de glomerulonefrite por imunocomplexos.
Avaliação de Risco Humano
A avaliação do estado imunológico humano é realizada principalmente usando sangue periférico para análise de substâncias humorais como imunoglobulinas e complemento, e de leucócitos sanguíneos para composição de subconjuntos e funcionalidade de subpopulações. Esses métodos são geralmente os mesmos usados para investigar a imunidade humoral e mediada por células, bem como a resistência inespecífica de pacientes com suspeita de imunodeficiência congênita. Para estudos epidemiológicos (por exemplo, de populações expostas ocupacionalmente), os parâmetros devem ser selecionados com base em seu valor preditivo em populações humanas, modelos animais validados e a biologia subjacente dos marcadores (ver tabela 1). A estratégia de triagem de efeitos imunotóxicos após exposição (acidental) a poluentes ambientais ou outros tóxicos depende muito das circunstâncias, como tipo de imunodeficiência esperada, tempo entre a exposição e a avaliação do estado imunológico, grau de exposição e número de indivíduos expostos. O processo de avaliação do risco imunotóxico de um determinado xenobiótico em humanos é extremamente difícil e muitas vezes impossível, devido em grande parte à presença de vários fatores de confusão de origem endógena ou exógena que influenciam a resposta dos indivíduos aos danos tóxicos. Isto é particularmente verdadeiro para estudos que investigam o papel da exposição química em doenças autoimunes, onde os fatores genéticos desempenham um papel crucial.
Tabela 1. Classificação dos testes para marcadores imunológicos
| Categoria de teste | Características | Testes específicos |
| Básico-geral Deve ser incluído com painéis gerais |
Indicadores de estado geral de saúde e sistema de órgãos | Nitrogênio ureico no sangue, glicose no sangue, etc. |
| básico-imune Deve ser incluído com painéis gerais |
Indicadores gerais do estado imunológico Custo relativamente baixo Os métodos de ensaio são padronizados entre os laboratórios Os resultados fora dos intervalos de referência são clinicamente interpretáveis |
hemograma completo Níveis séricos de IgG, IgA, IgM Fenótipos de marcadores de superfície para os principais subconjuntos de linfócitos |
| Focado/reflexo Deve ser incluído quando indicado por achados clínicos, exposições suspeitas ou resultados de testes anteriores |
Indicadores de funções/eventos imunológicos específicos O custo varia Os métodos de ensaio são padronizados entre os laboratórios Os resultados fora dos intervalos de referência são clinicamente interpretáveis |
Genótipo de histocompatibilidade Anticorpos contra agentes infecciosos IgE sérico total IgE específica para alérgenos Autoanticorpos Testes cutâneos para hipersensibilidade Explosão oxidativa de granulócitos Histopatologia (biópsia de tecido) |
| Estudos Deve ser incluído apenas com populações de controle e desenho de estudo cuidadoso |
Indicadores de funções/eventos imunológicos gerais ou específicos O custo varia; muitas vezes caro Os métodos de ensaio geralmente não são padronizados entre os laboratórios Os resultados fora dos intervalos de referência geralmente não são clinicamente interpretáveis |
Ensaios de estimulação in vitro Marcadores de superfície de ativação celular Concentrações séricas de citocinas Ensaios de clonalidade (anticorpo, celular, genético) Testes de citotoxicidade |
Como dados humanos adequados raramente estão disponíveis, a avaliação do risco de imunossupressão induzida por produtos químicos em humanos é, na maioria dos casos, baseada em estudos em animais. A identificação de potenciais xenobióticos imunotóxicos é realizada principalmente em estudos controlados em roedores. Os estudos de exposição in vivo apresentam, a esse respeito, a abordagem ideal para estimar o potencial imunotóxico de um composto. Isso se deve à natureza multifatorial e complexa do sistema imunológico e das respostas imunes. Estudos in vitro são de valor crescente na elucidação dos mecanismos de imunotoxicidade. Além disso, ao investigar os efeitos do composto usando células de origem animal e humana, podem ser gerados dados para comparação de espécies, que podem ser usados na abordagem do “paralelogramo” para melhorar o processo de avaliação de risco. Se houver dados disponíveis para os três pilares do paralelogramo (in vivo animal e in vitro animal e humano), pode ser mais fácil prever o resultado no restante pilar, ou seja, o risco em humanos.
Quando a avaliação do risco de imunossupressão induzida por produtos químicos depende apenas de dados de estudos em animais, uma abordagem pode ser seguida na extrapolação para o homem pela aplicação de fatores de incerteza ao nível de efeito adverso não observado (NOAEL). Este nível pode ser baseado em parâmetros determinados em modelos relevantes, como ensaios de resistência do hospedeiro e avaliação in vivo de reações de hipersensibilidade e produção de anticorpos. Idealmente, a relevância dessa abordagem para avaliação de risco requer confirmação por estudos em humanos. Esses estudos devem combinar a identificação e medição do tóxico, dados epidemiológicos e avaliações do estado imunológico.
Para prever a hipersensibilidade de contato, modelos de cobaias estão disponíveis e têm sido usados na avaliação de risco desde a década de 1970. Embora sensíveis e reprodutíveis, esses testes apresentam limitações por dependerem de avaliação subjetiva; isso pode ser superado por métodos mais novos e quantitativos desenvolvidos no mouse. Em relação à hipersensibilidade química induzida por inalação ou ingestão de alérgenos, testes devem ser desenvolvidos e avaliados quanto ao seu valor preditivo no homem. Quando se trata de definir níveis seguros de exposição ocupacional de alérgenos potenciais, deve-se levar em consideração a natureza bifásica da alergia: a fase de sensibilização e a fase de elicitação. A concentração necessária para provocar uma reação alérgica em um indivíduo previamente sensibilizado é consideravelmente menor do que a concentração necessária para induzir a sensibilização no indivíduo imunologicamente virgem, mas suscetível.
Como praticamente não existem modelos animais para prever a autoimunidade induzida por produtos químicos, deve-se dar ênfase ao desenvolvimento de tais modelos. Para o desenvolvimento de tais modelos, nosso conhecimento da autoimunidade induzida por produtos químicos em humanos deve ser avançado, incluindo o estudo de marcadores genéticos e do sistema imunológico para identificar indivíduos suscetíveis. Os seres humanos expostos a drogas que induzem a autoimunidade oferecem essa oportunidade.
Opções no Projeto de Estudo
O epidemiologista está interessado nas relações entre variáveis, principalmente exposição e variáveis de resultado. Normalmente, os epidemiologistas querem verificar se a ocorrência da doença está relacionada à presença de um determinado agente (exposição) na população. As formas como essas relações são estudadas podem variar consideravelmente. Pode-se identificar todas as pessoas que estão expostas a esse agente e acompanhá-las para medir a incidência da doença, comparando essa incidência com a ocorrência da doença em uma população adequada não exposta. Alternativamente, pode-se simplesmente amostrar entre os expostos e não expostos, sem ter uma enumeração completa deles. Ou, como uma terceira alternativa, pode-se identificar todas as pessoas que desenvolveram uma doença de interesse em um período de tempo definido (“casos”) e um grupo adequado de indivíduos livres de doença (uma amostra da população de origem dos casos) e verificar se os padrões de exposição diferem entre os dois grupos. O acompanhamento dos participantes do estudo é uma opção (nos chamados estudos longitudinais): nessa situação, existe um intervalo de tempo entre a ocorrência da exposição e o início da doença. Uma opção alternativa é uma seção transversal da população, onde tanto a exposição quanto a doença são medidas no mesmo ponto no tempo.
Neste artigo, é dada atenção aos desenhos de estudo comuns – coorte, caso-referente (caso-controle) e transversal. Para preparar o terreno para esta discussão, considere uma grande fábrica de rayon de viscose em uma cidade pequena. Foi iniciada uma investigação sobre se a exposição ao dissulfeto de carbono aumenta o risco de doença cardiovascular. A investigação tem várias opções de design, algumas mais e outras menos óbvias. Uma primeira estratégia é identificar todos os trabalhadores que foram expostos ao dissulfeto de carbono e acompanhá-los quanto à mortalidade cardiovascular.
Estudos de coortes
Um estudo de coorte abrange participantes de pesquisa que compartilham um evento comum, a exposição. Um estudo de coorte clássico identifica um grupo definido de pessoas expostas e, em seguida, todos são acompanhados e sua experiência de morbidade e/ou mortalidade é registrada. Além de uma exposição qualitativa comum, a coorte também deve ser definida em outros critério de eleição, como faixa etária, sexo (masculino ou feminino ou ambos), duração mínima e intensidade da exposição, ausência de outras exposições e similares, para aumentar a validade e eficiência do estudo. À entrada, todos os membros da coorte devem estar livres da doença em estudo, de acordo com o conjunto empírico de critérios usados para medir a doença.
Se, por exemplo, no estudo de coorte sobre os efeitos do dissulfeto de carbono na morbidade coronariana, a doença coronariana for medida empiricamente como infartos clínicos, aqueles que, na linha de base, tiveram um histórico de infarto coronariano devem ser excluídos da coorte. Por outro lado, anormalidades eletrocardiográficas sem história de infarto podem ser aceitas. No entanto, se o aparecimento de novas alterações eletrocardiográficas for a medida de resultado empírico, os membros da coorte também devem ter eletrocardiogramas normais na linha de base.
A morbidade (em termos de incidência) ou a mortalidade de uma coorte exposta deve ser comparada a uma coorte de referência que, idealmente, deve ser o mais semelhante possível à coorte exposta em todos os aspectos relevantes, exceto a exposição, para determinar o risco relativo de doença ou morte por exposição. Usar uma coorte semelhante, mas não exposta, como fornecedora da experiência de referência é preferível à (má) prática comum de comparar a morbidade ou mortalidade da coorte exposta com números nacionais padronizados por idade, porque a população em geral fica aquém de cumprir até mesmo os requisitos mais requisitos elementares para a validade da comparação. A Razão Padronizada de Morbidade (ou Mortalidade) (SMR), resultante dessa comparação, geralmente gera uma subestimação da verdadeira razão de risco por causa de um viés que opera na coorte exposta, levando à falta de comparabilidade entre as duas populações. Esse viés de comparação foi denominado “Efeito do Trabalhador Saudável”. No entanto, não é realmente um “efeito” verdadeiro, mas um viés de confusão negativa, que por sua vez surgiu da rotatividade seletiva de saúde em uma população empregada. (Pessoas com problemas de saúde tendem a sair ou nunca entrar em coortes “expostas”, sendo seu destino final frequentemente a seção de desempregados da população em geral.)
Como uma coorte “exposta” é definida como tendo uma certa exposição, apenas efeitos causados por essa única exposição (ou combinação de exposições) podem ser estudados simultaneamente. Por outro lado, o desenho de coorte permite o estudo de várias doenças ao mesmo tempo. Pode-se também estudar concomitantemente diferentes manifestações da mesma doença - por exemplo, angina, alterações no ECG, infartos clínicos do miocárdio e mortalidade coronariana. Embora adequado para testar hipóteses específicas (por exemplo, “a exposição ao dissulfeto de carbono causa doença cardíaca coronária”), um estudo de coorte também fornece respostas para a pergunta mais geral: “Quais doenças são causadas por esta exposição?”
Por exemplo, em um estudo de coorte investigando o risco de morrer de câncer de pulmão para trabalhadores de fundição, os dados de mortalidade são obtidos do registro nacional de causas de morte. Embora o estudo fosse determinar se o pó de fundição causa câncer de pulmão, a fonte de dados, com o mesmo esforço, também fornece informações sobre todas as outras causas de morte. Portanto, outros possíveis riscos à saúde podem ser estudados ao mesmo tempo.
O momento de um estudo de coorte pode ser retrospectivo (histórico) ou prospectivo (concorrente). Em ambos os casos, a estrutura do projeto é a mesma. Uma enumeração completa de pessoas expostas ocorre em algum ponto ou período no tempo, e o resultado é medido para todos os indivíduos por meio de um ponto final definido no tempo. A diferença entre prospectivo e retrospectivo está no momento do estudo. Se for retrospectivo, o ponto final já ocorreu; se for prospectivo, é preciso esperar por ele.
No projeto retrospectivo, a coorte é definida em algum ponto no passado (por exemplo, aqueles expostos em 1º de janeiro de 1961 ou aqueles que assumiram trabalhos expostos entre 1961 e 1970). A morbidade e/ou mortalidade de todos os membros da coorte é então seguido até o presente. Embora “todos” signifique que também aqueles que deixaram o emprego devem ser rastreados, na prática, uma cobertura de 100% raramente pode ser alcançada. No entanto, quanto mais completo o acompanhamento, mais válido é o estudo.
No desenho prospectivo, a coorte é definida no presente, ou durante algum período futuro, e a morbidade é seguida no futuro.
Ao fazer estudos de coorte, deve-se permitir tempo suficiente para o acompanhamento, a fim de que os pontos finais preocupantes tenham tempo suficiente para se manifestar. Às vezes, como os registros históricos podem estar disponíveis apenas por um curto período no passado, é desejável tirar proveito dessa fonte de dados porque isso significa que um período mais curto de acompanhamento prospectivo seria necessário antes que os resultados do estudo pudessem ser divulgados. acessível. Nessas situações, uma combinação de estudos de coorte retrospectivos e prospectivos pode ser eficiente. O layout geral das tabelas de frequência que apresentam dados de coorte é mostrado na tabela 1.
Tabela 1. O layout geral das tabelas de frequência apresentando dados de coorte
|
Componente da taxa de doença |
Coorte exposta |
coorte não exposta |
|
Casos de doença ou morte |
c1 |
c0 |
|
Número de pessoas na coorte |
N1 |
N0 |
A proporção observada de doentes na coorte exposta é calculada como:
![]()
e o da coorte de referência como:
![]()
A razão de taxas, então, é expressa como:

N0 e N1 são geralmente expressos em unidades de tempo por pessoa, em vez de como o número de pessoas em as populações. Anos-pessoa são calculados para cada indivíduo separadamente. Muitas vezes, pessoas diferentes entram na coorte durante um período de tempo, não na mesma data. Portanto, seus tempos de acompanhamento começam em datas diferentes. Da mesma forma, após sua morte, ou após a ocorrência do evento de interesse, eles não estão mais “em risco” e não devem continuar a contribuir pessoas-ano para o denominador.
Se o RR for maior que 1, a morbidade da coorte exposta é maior que a da coorte de referência e vice-versa. O RR é uma estimativa pontual e um intervalo de confiança (CI) deve ser calculado para ele. Quanto maior o estudo, mais estreito se tornará o intervalo de confiança. Se RR = 1 não for incluído no intervalo de confiança (por exemplo, o IC de 95% é 1.4 a 5.8), o resultado pode ser considerado “estatisticamente significativo” no nível de probabilidade escolhido (neste exemplo, α = 0.05).
Se a população geral for usada como população de referência, c0 é substituído pelo valor “esperado”, E(c1 ), derivado das taxas de morbidade ou mortalidade padronizadas por idade dessa população (ou seja, o número de casos que teriam ocorrido na coorte, caso a exposição de interesse não tivesse ocorrido). Isso produz a Taxa Padronizada de Mortalidade (ou Morbidade), SMR. Desta forma,
![]()
Também para o SMR, um intervalo de confiança deve ser calculado. É melhor fornecer essa medida em uma publicação do que um valor-p, porque o teste de significância estatística não faz sentido se a população em geral for a categoria de referência. Tal comparação acarreta um viés considerável (o efeito do trabalhador saudável mencionado acima), e o teste de significância estatística, originalmente desenvolvido para pesquisa experimental, é enganoso na presença de erro sistemático.
Suponha que a questão seja se o pó de quartzo causa câncer de pulmão. Normalmente, o pó de quartzo ocorre junto com outros carcinógenos, como os derivados de radônio e escape de diesel em minas ou hidrocarbonetos poliaromáticos em fundições. As pedreiras de granito não expõem os pedreiros a esses outros carcinógenos. Portanto, o problema é melhor estudado entre os pedreiros empregados em pedreiras de granito.
Suponha então que todos os 2,000 trabalhadores, tendo sido empregados por 20 pedreiras entre 1951 e 1960, estejam inscritos na coorte e sua incidência de câncer (alternativamente apenas mortalidade) seja acompanhada a partir de dez anos após a primeira exposição (para permitir um tempo de indução) e terminando em 1990. Este é um acompanhamento de 20 a 30 anos (dependendo do ano de entrada) ou, digamos, em média, de 25 anos da mortalidade (ou morbidade) por câncer entre 1,000 dos trabalhadores da pedreira que eram especificamente trabalhadores de granito. O histórico de exposição de cada membro da coorte deve ser registrado. Aqueles que deixaram as pedreiras devem ser rastreados e seu histórico de exposição posterior registrado. Em países onde todos os habitantes têm números de registro exclusivos, esse é um procedimento simples, regido principalmente pelas leis nacionais de proteção de dados. Onde não existe tal sistema, rastrear funcionários para fins de acompanhamento pode ser extremamente difícil. Onde existem registros apropriados de óbitos ou doenças, a mortalidade por todas as causas, todos os cânceres e locais específicos de câncer podem ser obtidos no registro nacional de causas de morte. (Para mortalidade por câncer, o registro nacional de câncer é uma fonte melhor porque contém diagnósticos mais precisos. Além disso, dados de incidência (ou morbidade) também podem ser obtidos.) As taxas de mortalidade (ou taxas de incidência de câncer) podem ser comparadas a “ números esperados”, calculados a partir de taxas nacionais usando como base as pessoas-ano da coorte exposta.
Suponha que 70 casos fatais de câncer de pulmão sejam encontrados na coorte, enquanto o número esperado (o número que teria ocorrido se não houvesse exposição) é 35. Então:
c1 = 70, E(c1) = 35
![]()
Assim, o SMR = 200, o que indica um aumento de duas vezes no risco de morrer de câncer de pulmão entre os expostos. Se dados detalhados de exposição estiverem disponíveis, a mortalidade por câncer pode ser estudada em função de diferentes tempos de latência (digamos, 10, 15, 20 anos), trabalho em diferentes tipos de pedreiras (diferentes tipos de granito), diferentes períodos históricos, diferentes exposições intensidades e assim por diante. No entanto, 70 casos não podem ser subdivididos em muitas categorias, porque o número que cai em cada uma rapidamente se torna muito pequeno para análise estatística.
Ambos os tipos de projetos de coorte têm vantagens e desvantagens. Um estudo retrospectivo pode, via de regra, medir apenas a mortalidade, porque geralmente faltam dados para manifestações mais leves. Os registros de câncer são uma exceção, e talvez alguns outros, como registros de AVC e registros de altas hospitalares, em que os dados de incidência também estejam disponíveis. A avaliação da exposição passada é sempre um problema e os dados de exposição geralmente são bastante fracos em estudos retrospectivos. Isso pode levar ao mascaramento do efeito. Por outro lado, como os casos já ocorreram, os resultados do estudo ficam disponíveis muito mais cedo; em, digamos, dois a três anos.
Um estudo prospectivo de coorte pode ser melhor planejado para atender às necessidades do pesquisador, e os dados de exposição podem ser coletados de forma precisa e sistemática. Várias manifestações diferentes de uma doença podem ser medidas. As medições da exposição e do resultado podem ser repetidas, e todas as medições podem ser padronizadas e sua validade verificada. No entanto, se a doença tiver uma longa latência (como o câncer), muito tempo – até 20 a 30 anos – precisará passar antes que os resultados do estudo possam ser obtidos. Muita coisa pode acontecer durante este tempo. Por exemplo, rotatividade de pesquisadores, melhorias nas técnicas de medição de exposição, reforma ou fechamento das usinas escolhidas para estudo e assim por diante. Todas essas circunstâncias colocam em risco o sucesso do estudo. Os custos de um estudo prospectivo também são geralmente mais altos do que os de um estudo retrospectivo, mas isso se deve principalmente ao número muito maior de medições (monitoramento de exposição repetida, exames clínicos e assim por diante) e não ao registro de óbito mais caro. Portanto, o custos por unidade de informação não excedem necessariamente os de um estudo retrospectivo. Diante de tudo isso, estudos prospectivos são mais indicados para doenças com latência bastante curta, necessitando de seguimento curto, enquanto estudos retrospectivos são melhores para doenças com latência longa.
Estudos de caso-controle (ou caso-referente)
Voltemos à fábrica de viscose rayon. Um estudo de coorte retrospectivo pode não ser viável se as listas dos trabalhadores expostos forem perdidas, enquanto um estudo de coorte prospectivo produziria resultados sólidos em muito tempo. Uma alternativa seria, então, a comparação entre os que morreram de doença coronariana no município, ao longo de um determinado período de tempo, e uma amostra da população total na mesma faixa etária.
O projeto de caso-controle clássico (ou caso-referente) é baseado na amostragem de uma população dinâmica (aberta, caracterizada por uma rotatividade de membros). Esta população pode ser a de um país inteiro, um distrito ou um município (como no nosso exemplo), ou pode ser a população definida administrativamente da qual os pacientes são internados em um hospital. A população definida fornece os casos e os controles (ou referentes).
A técnica consiste em reunir todos os casos da doença em questão existentes em um ponto no tempo (casos prevalentes), ou ocorreram durante um período definido significativo de tempo (casos incidentes). Os casos, portanto, podem ser extraídos de registros de morbidade ou mortalidade, ou coletados diretamente de hospitais ou outras fontes com diagnósticos válidos. Os controles são desenhados como um amostra da mesma população, seja entre não-casos ou de toda a população. Outra opção é selecionar pacientes com outra doença como controles, mas esses pacientes devem ser representativos da população de onde vieram os casos. Pode haver um ou mais controles (ou seja, referentes) para cada caso. A abordagem de amostragem difere dos estudos de coorte, que examinam toda a população. Nem é preciso dizer que os ganhos em termos de redução de custos dos projetos de caso-controle são consideráveis, mas é importante que a amostra seja representante de toda a população da qual os casos se originaram (ou seja, a “base do estudo”)—caso contrário, o estudo pode ser tendencioso.
Quando casos e controles são identificados, seus históricos de exposição são coletados por meio de questionários, entrevistas ou, em alguns casos, de registros existentes (por exemplo, registros de folha de pagamento dos quais históricos de trabalho podem ser deduzidos). Os dados podem ser obtidos dos próprios participantes ou, se já falecidos, de parentes próximos. Para garantir uma recordação simétrica, é importante que a proporção de casos e referentes mortos e vivos seja igual, porque parentes próximos geralmente fornecem uma história de exposição menos detalhada do que os próprios participantes. As informações sobre o padrão de exposição entre os casos são comparadas com as dos controles, fornecendo uma estimativa do odds ratio (OR), uma medida indireta da risco entre os expostos de contrair a doença em relação aos não expostos.
Como o projeto de caso-controle se baseia nas informações de exposição obtidas de pacientes com uma determinada doença (isto é, casos) juntamente com uma amostra de pessoas não doentes (isto é, controles) da população da qual os casos se originaram, a conexão com as exposições pode ser investigado apenas uma doença. Em contraste, este desenho permite o estudo concomitante do efeito de várias exposições diferentes. O estudo de caso referente é adequado para abordar questões de pesquisa específicas (por exemplo, “A doença coronariana é causada pela exposição ao dissulfeto de carbono?”), mas também pode ajudar a responder à pergunta mais geral: “Quais exposições podem causar esta doença ?”
A questão de saber se a exposição a solventes orgânicos causa câncer hepático primário é levantada (como exemplo) na Europa. Casos de câncer hepático primário, uma doença comparativamente rara na Europa, são mais bem coletados a partir de um registro nacional de câncer. Suponha que todos os casos de câncer ocorridos durante três anos formem a série de casos. A base populacional para o estudo é então um acompanhamento de três anos de toda a população do país europeu em questão. Os controles são desenhados como uma amostra de pessoas sem câncer de fígado da mesma população. Por razões de conveniência (o que significa que a mesma fonte pode ser usada para amostragem dos controles), pacientes com outro tipo de câncer, não relacionado à exposição a solventes, podem ser usados como controles. O câncer de cólon não tem relação conhecida com a exposição a solventes; portanto, esse tipo de câncer pode ser incluído entre os controles. (O uso de controles de câncer minimiza o viés de memória, pois a precisão da história fornecida por casos e controles é, em média, simétrica. No entanto, se alguma conexão atualmente desconhecida entre câncer de cólon e exposição a solventes fosse revelada posteriormente, esse tipo de controle causaria uma subestimação do verdadeiro risco - não um exagero dele.)
Para cada caso de câncer de fígado, dois controles são sorteados para obter maior poder estatístico. (Pode-se desenhar ainda mais controles, mas os fundos disponíveis podem ser um fator limitante. Se os fundos não fossem limitados, talvez até quatro controles seriam ótimos. Além de quatro, a lei dos retornos decrescentes se aplica.) Depois de obter a permissão apropriada dos dados autoridades de proteção, os casos e controles, ou seus parentes próximos, são abordados, geralmente por meio de um questionário enviado pelo correio, solicitando um histórico ocupacional detalhado com ênfase especial em uma lista cronológica dos nomes de todos os empregadores, departamentos de trabalho, tarefas de trabalho em empregos diferentes e o período de emprego em cada tarefa respectiva. Esses dados podem ser obtidos de parentes com alguma dificuldade; no entanto, produtos químicos específicos ou nomes comerciais geralmente não são bem lembrados pelos parentes. O questionário também deve incluir perguntas sobre possíveis dados de confusão, como uso de álcool, exposição a alimentos contendo aflatoxinas e infecção por hepatite B e C. Para obter uma taxa de resposta suficientemente alta, dois lembretes são enviados aos não respondentes em intervalos de três semanas. Isso geralmente resulta em uma taxa de resposta final superior a 70%. A história ocupacional é então revisada por um higienista industrial, sem conhecimento do caso do entrevistado ou status de controle, e a exposição é classificada em exposição alta, média, baixa, nenhuma e desconhecida a solventes. Os dez anos de exposição imediatamente anteriores ao diagnóstico de câncer são desconsiderados, porque não é biologicamente plausível que carcinógenos do tipo iniciador possam ser a causa do câncer se o tempo de latência for tão curto (embora os promotores, de fato, possam). Nesta fase também é possível diferenciar entre diferentes tipos de exposição a solventes. Como foi fornecida uma história profissional completa, também é possível explorar outras exposições, embora a hipótese inicial do estudo não as inclua. As razões de chance podem então ser calculadas para exposição a qualquer solvente, solventes específicos, misturas de solventes, diferentes categorias de intensidade de exposição e para diferentes janelas de tempo em relação ao diagnóstico de câncer. É aconselhável excluir da análise aqueles com exposição desconhecida.
Os casos e controles podem ser amostrados e analisados como série independente or grupos combinados. Matching significa que os controles são selecionados para cada caso com base em certas características ou atributos, para formar pares (ou conjuntos, se mais de um controle for escolhido para cada caso). A correspondência geralmente é feita com base em um ou mais desses fatores, como idade, estado vital, histórico de tabagismo, tempo de calendário do diagnóstico do caso e outros. Em nosso exemplo, os casos e controles são comparados por idade e estado vital. (O estado vital é importante, porque os próprios pacientes geralmente fornecem um histórico de exposição mais preciso do que parentes próximos, e a simetria é essencial por razões de validade.) Hoje, a recomendação é restringir a correspondência, porque esse procedimento pode introduzir resultados negativos (mascaramento de efeito) ) confuso.
Se um controle corresponde a um caso, o projeto é chamado de design de par combinado. Desde que os custos de estudar mais controles não sejam proibitivos, mais de um referente por caso melhora a estabilidade da estimativa do OR, o que torna o estudo mais eficiente em tamanho.
O layout dos resultados de um estudo de caso-controle não pareado é mostrado na tabela 2.
Tabela 2. Layout de amostra de dados de caso-controle
|
Classificação de exposição |
||
|
exposto |
Não exposto |
|
|
Cases |
c1 |
c0 |
|
Não-casos |
n1 |
n0 |
A partir dessa tabela, as chances de exposição entre os casos e as chances de exposição entre a população (os controles) podem ser calculadas e divididas para gerar a razão de chances de exposição, OR. Para os casos, a probabilidade de exposição é c1 / c0, e para os controles é n1 / n0. A estimativa do OR é então:
![]()
Se relativamente mais casos do que controles foram expostos, o OR é superior a 1 e vice-versa. Os intervalos de confiança devem ser calculados e fornecidos para o OR, da mesma forma que para o RR.
A título de exemplo, um centro de saúde ocupacional de uma grande empresa atende a 8,000 funcionários expostos a diversas poeiras e outros agentes químicos. Estamos interessados na conexão entre exposição à poeira mista e bronquite crônica. O estudo envolve o acompanhamento dessa população por um ano. Estabelecemos como critério diagnóstico para bronquite crônica “tosse matinal e produção de catarro por três meses durante dois anos consecutivos”. Os critérios para exposição “positiva” à poeira são definidos antes do início do estudo. Cada paciente que visita o centro de saúde e preenche esses critérios durante um período de um ano é um caso, e o próximo paciente que procura aconselhamento médico por problemas não pulmonares é definido como um controle. Suponha que 100 casos e 100 controles sejam incluídos durante o período do estudo. Deixe 40 casos e 15 controles serem classificados como tendo sido expostos a poeira. Então
c1 = 40, c0 = 60, n1 = 15 e n0 = 85.
Consequentemente,
![]()
No exemplo anterior, não foi considerada a possibilidade de confusão, que pode levar a uma distorção da OR devido a diferenças sistemáticas entre casos e controles em uma variável como a idade. Uma maneira de reduzir esse viés é combinar os controles com os casos por idade ou outros fatores suspeitos. Isso resulta em um layout de dados descrito na tabela 3.
Tabela 3. Layout de dados de caso-controle se um controle corresponder a cada caso
|
Referentes |
||
|
Cases |
Exposição (+) |
Exposição (-) |
|
Exposição (+) |
f+ + |
f+ - |
|
Exposição (-) |
f- + |
f- - |
A análise se concentra nos pares discordantes: ou seja, “caso exposto, controle não exposto” (f+–); e “caso não exposto, controle exposto” (f–+). Quando ambos os membros de um par são expostos ou não expostos, o par é desconsiderado. O OR em um desenho de estudo de pares combinados é definido como
![]()
Em um estudo sobre a associação entre câncer nasal e exposição à poeira de madeira, havia ao todo 164 pares de caso-controle. Em apenas um par, tanto o caso quanto o controle foram expostos, e em 150 pares, nem o caso nem o controle foram expostos. Esses pares não são mais considerados. O caso, mas não o controle, foi exposto em 12 pares, e o controle, mas não o caso, em um par. Conseqüentemente,
![]()
e como a unidade não está incluída nesse intervalo, o resultado é estatisticamente significativo, ou seja, há uma associação estatisticamente significativa entre câncer nasal e exposição ao pó de madeira.
Os estudos de caso-controle são mais eficientes do que os estudos de coorte quando o a doença é rara; eles podem, de fato, fornecer a única opção. No entanto, doenças comuns também podem ser estudadas por este método. Se o a exposição é rara, uma coorte baseada na exposição é o desenho epidemiológico preferível ou o único viável. Claro, estudos de coorte também podem ser realizados em exposições comuns. A escolha entre projetos de coorte e de caso-controle quando a exposição e a doença são comuns geralmente é decidida levando em conta considerações de validade.
Como os estudos de caso-controle dependem de dados de exposição retrospectiva, geralmente baseados na recordação dos participantes, seu ponto fraco é a imprecisão e a grosseria das informações de exposição, o que resulta em mascaramento de efeitos por meio de não diferencial (simétrica) classificação incorreta do status de exposição. Além disso, às vezes a recordação pode ser assimétrica entre casos e controles, casos geralmente considerados como lembrando “melhor” (ou seja, viés de recordação).
A recordação seletiva pode causar um viés de ampliação de efeito através diferencial (assimétrica) classificação incorreta do status de exposição. As vantagens dos estudos de caso-controle residem em sua relação custo-eficácia e em sua capacidade de fornecer uma solução para um problema de forma relativamente rápida. Devido à estratégia de amostragem, eles permitem a investigação de populações-alvo muito grandes (por exemplo, por meio de registros nacionais de câncer), aumentando assim o poder estatístico do estudo. Em países onde a legislação de proteção de dados ou a falta de bons registros populacionais e de morbidade dificultam a execução de estudos de coorte, estudos de caso-controle baseados em hospitais podem ser a única maneira prática de conduzir pesquisas epidemiológicas.
Amostragem de caso-controle dentro de uma coorte (desenhos de estudo de caso-controle aninhados)
Um estudo de coorte também pode ser projetado para amostragem em vez de acompanhamento completo. Esse projeto foi anteriormente chamado de estudo de caso-controle “aninhado”. Uma abordagem de amostragem dentro da coorte estabelece requisitos diferentes para a elegibilidade da coorte, porque as comparações agora são feitas dentro da mesma coorte. Isso deve, portanto, incluir não apenas trabalhadores altamente expostos, mas também trabalhadores menos expostos e até mesmo não expostos, a fim de fornecer contrastes de exposição dentro de si. É importante perceber essa diferença nos requisitos de elegibilidade ao montar a coorte. Se uma análise de coorte completa for realizada pela primeira vez em uma coorte cujos critérios de elegibilidade foram em “muita” exposição, e um estudo de caso-controle “aninhado” for feito posteriormente na mesma coorte, o estudo torna-se insensível. Isso introduz mascaramento de efeito porque os contrastes de exposição são insuficientes “por design” em virtude da falta de variabilidade na experiência de exposição entre os membros da coorte.
No entanto, desde que a coorte tenha uma ampla gama de experiências de exposição, a abordagem de caso-controle aninhado é muito atraente. Um reúne todos os casos surgidos na coorte ao longo do período de acompanhamento para formar a série de casos, enquanto apenas um amostra dos não-casos é desenhado para a série de controle. Os pesquisadores, então, como no projeto tradicional de controle de caso, coletam informações detalhadas sobre a experiência de exposição entrevistando casos e controles (ou seus parentes próximos), examinando as listas de funcionários dos empregadores, construindo uma matriz de exposição de trabalho, ou combinando duas ou mais dessas abordagens. Os controles podem ser combinados com os casos ou podem ser tratados como uma série independente.
A abordagem de amostragem pode ser menos dispendiosa em comparação com a obtenção de informações exaustivas sobre cada membro da coorte. Em particular, porque apenas uma amostra de controles é estudada, mais recursos podem ser dedicados a uma avaliação de exposição detalhada e precisa para cada caso e controle. No entanto, os mesmos problemas de poder estatístico prevalecem como nos estudos de coorte clássicos. Para alcançar poder estatístico adequado, a coorte deve sempre incluir um número “adequado” de casos expostos dependendo da magnitude do risco que deve ser detectado.
Desenhos de estudos transversais
No sentido científico, um desenho transversal é uma seção transversal da população de estudo, sem qualquer consideração dada ao tempo. Tanto a exposição quanto a morbidade (prevalência) são medidas no mesmo ponto no tempo.
Do ponto de vista etiológico, esse desenho de estudo é fraco, em parte porque lida com a prevalência em oposição à incidência. A prevalência é uma medida composta, dependendo tanto da incidência quanto da duração da doença. Isso também restringe o uso de estudos transversais para doenças de longa duração. Mais grave ainda é o forte viés negativo causado pela eliminação dependente da saúde do grupo exposto daquelas pessoas mais sensíveis aos efeitos da exposição. Portanto, os problemas etiológicos são melhor resolvidos por projetos longitudinais. De fato, estudos transversais não permitem nenhuma conclusão sobre se a exposição precedeu a doença ou vice-versa. A seção transversal é etiologicamente significativa apenas se existir uma verdadeira relação de tempo entre a exposição e o resultado, o que significa que a exposição atual deve ter efeitos imediatos. No entanto, a exposição pode ser medida transversalmente para que represente um período de tempo passado mais longo (por exemplo, o nível de chumbo no sangue), enquanto a medida do resultado é uma prevalência (por exemplo, velocidades de condução nervosa). O estudo, então, é uma mistura de um desenho longitudinal e transversal, em vez de um mero corte transversal da população do estudo.
Pesquisas descritivas transversais
Os inquéritos transversais são muitas vezes úteis para fins práticos e administrativos, e não para fins científicos. Os princípios epidemiológicos podem ser aplicados a atividades de vigilância sistemática no ambiente de saúde ocupacional, tais como:
- observação de morbidade em relação à ocupação, área de trabalho ou certas exposições
- inquéritos regulares aos trabalhadores expostos a riscos ocupacionais conhecidos
- exame de trabalhadores que entram em contato com novos riscos à saúde
- programas de monitoramento biológico
- pesquisas de exposição para identificar e quantificar perigos
- programas de triagem de diferentes grupos de trabalhadores
- avaliar a proporção de trabalhadores que necessitam de prevenção ou controle regular (por exemplo, pressão arterial, doença coronariana).
É importante escolher indicadores de morbidade representativos, válidos e específicos para todos os tipos de pesquisas. Uma pesquisa ou um programa de triagem pode usar apenas um número bastante pequeno de testes, em contraste com o diagnóstico clínico e, portanto, o valor preditivo do teste de triagem é importante. Métodos insensíveis falham em detectar a doença de interesse, enquanto métodos altamente sensíveis produzem muitos resultados falsos positivos. Não vale a pena rastrear doenças raras em um ambiente ocupacional. Todas as atividades de busca de casos (ou seja, triagem) também requerem um mecanismo para cuidar de pessoas com achados “positivos”, tanto em termos de diagnóstico quanto de terapia. Caso contrário, apenas a frustração resultará com um potencial para mais mal do que bem emergindo.
" ISENÇÃO DE RESPONSABILIDADE: A OIT não se responsabiliza pelo conteúdo apresentado neste portal da Web em qualquer idioma que não seja o inglês, que é o idioma usado para a produção inicial e revisão por pares do conteúdo original. Algumas estatísticas não foram atualizadas desde a produção da 4ª edição da Enciclopédia (1998)."