Categorías Niños

1. Sangre (3)

1. Sangre
Redactor del capítulo: Bernardo D. Goldstein
Índice del contenido
Mesas
Sistema Hematopoyético y Linfático
Bernardo D. Goldstein
Leucemia, Linfomas Malignos y Mieloma Múltiple
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Agentes o condiciones de trabajo que afectan la sangre
Bernardo D. Goldstein
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.

2. Cáncer (4)

2. Cáncer
Redactor del capítulo: paolo bofetta
Mesa de Contenidos
Mesas
Introducción
Neil Pearce, Paolo Boffetta y Manolis Kogevinas
Carcinógenos ocupacionales
Paolo Boffetta, Rodolfo Saracci, Manolis Kogevinas, Julian Wilbourn y Harri Vainio
Cáncer ambiental
Bruce K. Armstrong y Paolo Boffetta
Prevención
Por Gustavsson
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
- Cáncer ocupacional: datos clave
- Proporciones estimadas de cáncer (PAR) atribuibles a las ocupaciones
- Evaluación de la evidencia de carcinogenicidad en las Monografías de la IARC
- Grupos de clasificación de programas de monografías de IARC
- Grupo 1-Químicos cancerígenos para los humanos
- Grupo 2A: Sustancias químicas probablemente cancerígenas para los humanos
- Grupo 2B: Sustancias químicas posiblemente cancerígenas para los humanos
- Pesticidas evaluados en Monografías IARC, Volúmenes 1-63 (1972-1995)
- Medicamentos evaluados en IARC Monografías, Volúmenes 1-63 (1972-1995)
- Agentes ambientales/exposiciones conocidas o sospechadas de cáncer humano
- Industrias, ocupaciones, exposiciones que presentan un riesgo cancerígeno
- Industrias, occs., exps. con exceso de cáncer carcinógenos no definitivos
- Variaciones poblacionales registradas de la incidencia de algunos cánceres comunes

3. Sistema cardiovascular (7)

3. Sistema cardiovascular
Editores de capítulos: Lothar Heinemann y Gerd Heuchert
Índice del contenido
Tablas y Figuras
Introducción
Lothar Heinemann y Gerd Heuchert
Morbilidad y Mortalidad Cardiovascular en la Fuerza Laboral
Gottfried Enderlein y Lothar Heinemann
El concepto de factor de riesgo en la enfermedad cardiovascular
Lothar Heinemann, Gottfried Enderlein y Heide Stark
Programas de Rehabilitación y Prevención
Lothar Heinemann y Gottfried Enderlein
Riesgos físicos, químicos y biológicos
Factores físicos
Heide Stark y Gerd Heuchert
Materiales químicos peligrosos
Ulrike Tittelbach y Wolfram Dietmar Schneider
Peligros biológicos
Regina Jäckel, Ulrike Tittelbach y Wolfram Dietmar Schneider
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo
- Mortalidad por enfermedades cardiovasculares
- Tasas de mortalidad, grupos especiales de diagnóstico cardiovascular
- Tasa de enfermedad y reducción de la capacidad de trabajo
- Trabajo asociado a riesgos cardiovasculares
- Infecciones y enfermedades relacionadas con el trabajo
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

4. Sistema Digestivo (6)

4. Sistema digestivo
Editor del capítulo: Heikki Savolainen
Índice del contenido
Figuras
Sistema digestivo
G.Frada
boca y dientes
F. Gobbato
Hígado
Jorge Kazantzis
Úlcera péptica
KS cho
Cáncer de hígado
Timo Partanen, Timo Kauppinen, Paolo Boffetta y Elisabete Weiderpass
Cancer pancreatico
Timo Partanen, Timo Kauppinen, Paolo Boffetta y Elisabete Weiderpass
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

5. Salud mental (8)

5. Salud mental
Editores de capítulos: Joseph J. Hurrell, Lawrence R. Murphy, Steven L. Sauter y Lennart Levi
Índice del contenido
Tablas y Figuras
Trabajo y Salud Mental
Irene LD Houtman y Michiel AJ Kompier
Psicosis relacionada con el trabajo
Craig Stenberg, Judith Holder y Krishna Tallur
Estado de ánimo y afecto
Depresión
Jay Lasser y Jeffrey P. Kahn
Ansiedad relacionada con el trabajo
Randal D Beaton
Trastorno de estrés postraumático y su relación con la salud ocupacional y la prevención de lesiones
marca braverman
Estrés y Burnout y su Implicación en el Ambiente Laboral
Herbert J. Freudenberger
Trastornos cognitivos
Catalina A. Heaney
Karoshi: muerte por exceso de trabajo
takashi haratani
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Resumen esquemático de las estrategias de gestión y ejemplos
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

6. Sistema musculoesquelético (14)

6. Sistema musculoesquelético
Editores de capítulos: Hilkka Riihimäki y Eira Viikari-Juntura
Índice del contenido
Tablas y Figuras
General
Hilkka Riihimäki
Musculatura
Gisela Sjogaard
Tendones
Thomas J Armstrong
Huesos y articulaciones
david hamerman
Discos intervertebrales
Sally Roberts y Jill PG Urban
Región de la espalda baja
Hilkka Riihimäki
Región de la columna torácica
Jarl-Erik Michelsson
Cuello
Asa Kilbom
Shoulder
Mats Hagberg
codo
Eira Viikari Juntura
antebrazo, muñeca y mano
Eira Viikari Juntura
Cadera y rodilla
Eva Vingård
Pierna, Tobillo y Pie
Jarl-Erik Michelsson
Otras enfermedades
Marjatta Leirisalo-Repo
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
- Estructura-función de los componentes de la articulación
- Prevalencia de trastornos de la espalda, en finlandeses mayores de 30 años
- Reducir los riesgos de dolor lumbar en el trabajo
- Clasificación: trastornos de la espalda baja (Quebec Task Force)
- Movimientos permisibles de cabeza en conducción prolongada
- Incidencia de epicondilitis en varias poblaciones
- Incidencia de tenosinovitis/peritendinitis
- Osteoartrosis primaria de cadera en Malmö, Suecia
- Pautas para el tratamiento de la artritis reumatoide
- Infecciones conocidas por desencadenar artritis reactiva
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

7. Sistema Nervioso (9)

7. Sistema Nervioso
Redactor del capítulo: donna mergler
Índice del contenido
Tablas y Figuras
Sistema Nervioso: Resumen
Donna Mergler y José A. Valciukas
Anatomía y fisiología
José A. Valciukas
Agentes Neurotóxicos Químicos
Peter Arlien-Søborg y Leif Simonsen
Manifestaciones de intoxicación aguda y crónica temprana
donna mergler
Prevención de la neurotoxicidad en el trabajo
barry johnson
Síndromes clínicos asociados con neurotoxicidad
Roberto G. Feldman
Medición de los déficits neurotóxicos
donna mergler
Diagnóstico
Anna María Seppäläinen
Neuroepidemiología Ocupacional
Olav Axelson
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
- Nombres y funciones principales de cada par de nervios craneales
- Agrupación de efectos neurotóxicos en cuanto a neurotoxicidad.
- Gases asociados con efectos neurotóxicos
- Metales neurotóxicos y sus compuestos inorgánicos
- monómeros neurotóxicos
- Disolventes orgánicos asociados a neurotoxicidad
- Clases de pesticidas neurotóxicos comunes
- Otros productos químicos asociados con la neurotoxicidad
- Lista de verificación de síntomas crónicos
- Efectos neurofuncionales de la exposición a algunas neurotoxinas
- Exposiciones químicas y síndromes neurotóxicos asociados
- Algunas baterías "básicas" para evaluar los efectos neurotóxicos tempranos
- Árbol de decisión para la enfermedad neurotóxica
- Efectos neurofuncionales constantes de la exposición en el lugar de trabajo a algunas de las principales sustancias neurotóxicas
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

8. Sistema renal-urinario (2)

8. Sistema renal-urinario
Redactor del capítulo: George P. Hemstreet
Índice del contenido
Tablas y Figuras
Sistemas renales y urinarios
George P. Hemstreet
Cánceres renales y urinarios
Timo Partanen, Harri Vainio, Paolo Boffetta y Elisabete Weiderpass
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
- Enzimas del metabolismo de fármacos en el riñón
- Las causas más comunes de hematuria, por edad y sexo
- Criterios para la selección de biomarcadores
- Posibles biomarcadores vinculados a la lesión celular
- Insuficiencia renal aguda y ocupación
- Segmentos de la nefrona afectados por tóxicos seleccionados
- Aplicaciones de la citología urinaria
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

9. Sistema reproductivo (9)

9. Sistema reproductivo
Redactor del capítulo: Gracia Kawas Lemasters
Índice del contenido
Tablas y Figuras
Sistema Reproductivo: Introducción
Lowell E. Severo
Introducción a la función reproductiva masculina y femenina
Donald R Mattison
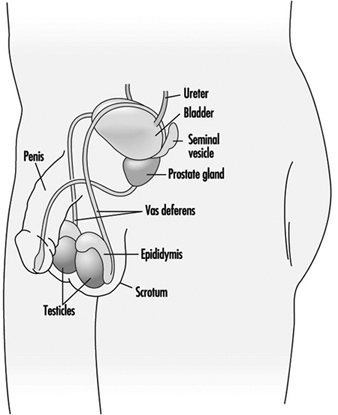
Sistema Reproductor Masculino y Toxicología
Steven Schrader y Grace Kawas Lemasters
Estructura del sistema reproductor femenino y vulnerabilidad de órganos diana
Donald R Mattison
Exposiciones ocupacionales maternas y resultados adversos del embarazo
Gracia Kawas Lemasters
Parto prematuro y trabajo
Nicole Mamelle
Exposición ocupacional y ambiental del recién nacido
Mary S. Wolff y Patrisha M. Woolard
Protección de la maternidad en la legislación
Marie-Claire Séguret
Recomendaciones para el embarazo y el trabajo en EE. UU.
leon j warshaw
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Exposiciones con múltiples criterios de valoración adversos
2. Estudios epidemiológicos de los efectos paternos en el resultado del embarazo
3. Tóxicos reproductivos femeninos potenciales
4. Definición de pérdida fetal y muerte infantil
5. Factores de pequeño para la edad gestacional y pérdida fetal
6. Fuentes identificadas de fatiga ocupacional
7. Riesgos relativos e índices de fatiga del parto prematuro
8. Riesgo de prematuridad por número de índices de fatiga laboral
9. Riesgos relativos y cambios en las condiciones de trabajo
10. Fuentes y niveles de exposición de los recién nacidos
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

10. Sistema respiratorio (18)

10. Sistema respiratorio
Editores de capítulos: Alois David y Gregory R. Wagner
Índice del contenido
Tablas y Figuras
Estructura y función
Morton Lippmann
Examen de función pulmonar
Ulf Ulfvarson y Monica Dahlqvist
Enfermedades Causadas por Irritantes Respiratorios y Químicos Tóxicos
David LS Ryon y William N. Rom
Asma ocupacional
George Friedman-Jiménez y Edward L. Petsonk
Enfermedades Causadas por Polvos Orgánicos
Ragnar Rylander y Richard SF Schilling
Enfermedad del berilio
Homayoun Kazemi
Neumoconiosis: Definición
alois david
Clasificación internacional de radiografías de neumoconiosis de la OIT
michel lesage
Etiopatogenia de las neumoconiosis
Patrick Sébastien y Raymond Bégin
Silicosis
John E. Parker y Gregory R. Wagner
Enfermedades pulmonares de los trabajadores del carbón
Michael D. Attfield, Edward L. Petsonk y Gregory R. Wagner
Enfermedades relacionadas con el asbesto
margaret r. becklake
Enfermedad del metal duro
Gerolamo Chiapino
Sistema respiratorio: la variedad de neumoconiosis
Steven R. Short y Edward L. Petsonk
Afección pulmonar obstructiva crónica
Kazimierz Marek y Jan E. Zejda
Efectos sobre la salud de las fibras artificiales
James E. Lockey y Clara S. Ross
Cáncer respiratorio
Paolo Boffetta y Elisabete Weiderpass
Infecciones pulmonares adquiridas en el trabajo
Anthony A. Marfin, Ann F. Hubbs, Karl J. Musgrave y John E. Parker
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Regiones del tracto respiratorio y modelos de deposición de partículas
2. Criterios de polvo inhalable, torácico y respirable
3. Resumen de irritantes respiratorios
4. Mecanismos de lesión pulmonar por sustancias inhaladas
5. Compuestos capaces de toxicidad pulmonar
6. Definición de caso médico de asma ocupacional
7. Pasos en la evaluación diagnóstica del asma en el lugar de trabajo
8. Agentes sensibilizantes que pueden causar asma ocupacional
9. Ejemplos de fuentes de peligros de la exposición al polvo orgánico
10. Agentes en polvos orgánicos con actividad biológica potencial
11. Enfermedades inducidas por polvos orgánicos y sus códigos CIE
12. Criterios diagnósticos de bisinosis
13. Propiedades del berilio y sus compuestos
14. Descripción de las radiografías estándar
15. Clasificación OIT 1980: Radiografías de neumoconiosis
16. Enfermedades y condiciones relacionadas con el asbesto
17. Principales fuentes comerciales, productos y usos del asbesto
18. Prevalencia de la EPOC
19. Factores de riesgo implicados en la EPOC
20. Pérdida de la función ventilatoria
21. Clasificación diagnóstica, bronquitis crónica y enfisema
22. Pruebas de función pulmonar en la EPOC
23. Fibras sinteticas
24. Carcinógenos respiratorios humanos establecidos (IARC)
25. Carcinógenos respiratorios humanos probables (IARC)
26. Enfermedades infecciosas respiratorias adquiridas ocupacionalmente
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

11. Sistemas sensoriales (8)

11. Sistemas sensoriales
Redactor del capítulo: Heikki Savolainen
Índice del contenido
Tablas y Figuras
La oreja
Marcel-André Boillat
Trastornos auditivos inducidos químicamente
pedro jacobsen
Trastornos auditivos inducidos físicamente
Pedro L. Pelmear
equilibrio
lucy yardley
Visión y Trabajo
Paule Rey y Jean-Jacques Meyer
Sabor
Abril E. Mott y Norman Mann
Olor
Abril E. Mott
Receptores cutáneos
Robert Dykes y Daniel McBain
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Cálculo típico de la pérdida funcional de un audiograma
2. Requerimientos visuales para diferentes actividades.
3. Valores de iluminancia recomendados para el diseño de iluminación
4. Requisitos visuales para un permiso de conducir en Francia
5. Agentes/procesos reportados para alterar el sistema del gusto
6. Agentes/procesos asociados con anomalías olfativas
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

12. Enfermedades de la piel (7)

12. Enfermedades de la piel
Redactor del capítulo: Louis Philippe Durocher
Índice del contenido
Tablas y Figuras
Descripción general: Enfermedades profesionales de la piel
Donald J Birmingham
Cáncer de piel no melanocítico
Elisabete Weiderpass, Timo Partanen, Paolo Boffetta
Melanoma maligno
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Dermatitis de contacto ocupacional
denis sasseville
Prevención de Dermatosis Laborales
Luis Felipe Durocher
Distrofia ungueal ocupacional
CD Calnan
Estigmas
H. Mierzecki
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Ocupaciones en riesgo
2. Tipos de dermatitis de contacto
3. Irritantes comunes
4. Alérgenos comunes de la piel
5. Factores predisponentes para la dermatitis ocupacional
6. Ejemplos de irritantes y sensibilizantes de la piel con ocupaciones
7. Dermatosis ocupacionales en Quebec en 1989
8. Factores de riesgo y sus efectos en la piel
9. Medidas colectivas (enfoque de grupo) para la prevención
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

13. Condiciones Sistémicas (3)

13. Condiciones Sistémicas
Redactor del capítulo: Howard M Kipen
Índice del contenido
Figuras
Condiciones Sistémicas: Una Introducción
Howard M Kipen
El síndrome del edificio enfermo
Michael J Hodgson
Sensibilidades químicas múltiples
marca r cullen
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.
Sistema Nervioso: Resumen
El conocimiento del sistema nervioso en general y del cerebro y el comportamiento humano en particular son de suma importancia para quienes se dedican a un entorno seguro y saludable. Las condiciones de trabajo y las exposiciones que afectan directamente las operaciones del cerebro influyen en la mente y el comportamiento. Para evaluar la información, tomar decisiones y reaccionar de manera consistente y razonable a las percepciones del mundo, se requiere que el sistema nervioso funcione correctamente y que el comportamiento no se vea dañado por condiciones peligrosas, como accidentes (p. ej., una caída de un mal diseñado). escalera) o la exposición a niveles peligrosos de sustancias químicas neurotóxicas.
El daño al sistema nervioso puede causar cambios en la información sensorial (pérdida de visión, audición, olfato, etc.), puede dificultar la capacidad de controlar el movimiento y las funciones corporales y/o puede afectar la capacidad del cerebro para tratar o almacenar información. Además, el funcionamiento alterado del sistema nervioso puede provocar trastornos conductuales o psicológicos. Los cambios de humor y personalidad son una ocurrencia común después de un daño físico u orgánico en el cerebro. A medida que se desarrolla nuestro conocimiento, aprendemos más sobre la forma en que se modifican los procesos del sistema nervioso. Las sustancias neurotóxicas pueden cruzar la barrera natural del cerebro e interferir directamente con su intrincado funcionamiento. Aunque algunas sustancias tienen una afinidad particular con ciertas áreas del sistema nervioso, la mayoría de las neurotoxinas tienen efectos generalizados, dirigidos a procesos celulares involucrados en el transporte de membrana, reacciones químicas celulares internas, liberación de sustancias secretoras, etc.
El daño a los diversos componentes del sistema nervioso puede ocurrir de diferentes maneras:
- lesión física directa por objetos que caen, colisiones, golpes o presión indebida sobre los nervios
- cambios en el ambiente interno, como falta de oxígeno debido a asfixiantes y exposición al calor
- interferencia en los procesos celulares a través de la acción química de sustancias, como metales, disolventes orgánicos y pesticidas
El desarrollo insidioso y multifacético de muchos trastornos del sistema nervioso requiere que las personas que trabajan en el campo de la salud ocupacional adopten enfoques diferentes pero complementarios para el estudio, comprensión, prevención y tratamiento del problema. Las alteraciones tempranas pueden detectarse en grupos de trabajadores activos y expuestos utilizando medidas sensibles de deterioro. La identificación de la disfunción inicial puede conducir a acciones preventivas. En estas últimas etapas se requiere un buen conocimiento clínico y el diagnóstico diferencial es fundamental para el adecuado tratamiento y cuidado de los trabajadores discapacitados.
Aunque las sustancias químicas se examinan mayoritariamente una por una, cabe recordar que en muchos lugares de trabajo se utilizan mezclas de sustancias químicas potencialmente neurotóxicas, lo que expone a los trabajadores a lo que se puede denominar un “cóctel”. En procesos como impresión, pintura, limpieza, en oficinas mal ventiladas, en laboratorios, aplicación de pesticidas, microelectrónica y muchos otros sectores, los trabajadores están expuestos a mezclas químicas. Aunque puede haber información de cada una de las sustancias por separado, hay que considerar la nocividad combinada y los posibles efectos aditivos o incluso sinérgicos sobre el sistema nervioso. En algunos casos de exposición múltiple, cada sustancia química en particular puede estar presente en cantidades muy pequeñas, incluso por debajo del nivel de detección de las técnicas de evaluación de la exposición; sin embargo, cuando se suman todos juntos, la concentración total puede ser muy alta.
El lector debe ser consciente de tres dificultades principales al revisar hechos sobre el sistema nervioso dentro del alcance de este Enciclopedia.
Primero, la comprensión de las enfermedades ocupacionales que afectan el sistema nervioso y el comportamiento ha cambiado sustancialmente a medida que se han desarrollado nuevos enfoques para ver las relaciones entre el cerebro y el comportamiento. El interés principal de la caracterización de los cambios morfológicos macroscópicos que ocurren debido a un traumatismo mecánico en el sistema nervioso, en particular, pero no exclusivamente, en el cerebro, fue seguido por un interés en la absorción de agentes neurotóxicos por parte del sistema nervioso; interés en el estudio de los mecanismos celulares de la patología del sistema nervioso; y finalmente, la búsqueda de la base molecular de estos procesos patológicos comenzó a crecer. Estos enfoques coexisten hoy y todos aportan información para evaluar las condiciones de trabajo que afectan el cerebro, la mente y el comportamiento.
En segundo lugar, la información generada por los neurocientíficos es asombrosa. La tercera edición del libro. Principios de las Ciencias Neurales editado por Kandel, Schwartz y Kessell que apareció en 1991, una de las revisiones más valiosas del campo, pesa 3.5 kg y tiene más de 1,000 páginas.
En tercer lugar, es muy difícil revisar el conocimiento sobre la organización funcional del sistema nervioso tal como se aplica a todos los nichos de la seguridad y salud en el trabajo. Hasta hace unos 25 años, los puntos de vista teóricos que respaldaban a los expertos en salud que se especializan en la detección, el seguimiento, la prevención y el tratamiento clínico de un trabajador que ha absorbido un agente neurotóxico a veces no se superponían con los puntos de vista teóricos sobre la salud de los trabajadores. trauma cerebral y las manifestaciones conductuales de daño cerebral mínimo. Las manifestaciones conductuales que se decía que eran consecuencia de la interrupción de vías químicas específicas en el cerebro eran territorio exclusivo del neurotoxicólogo; tanto el daño estructural del tejido de regiones específicas del cerebro, como estructuras neurales distantes vinculadas al área donde ocurrieron las lesiones, fueron explicaciones invocadas por los neurólogos. Solo en los últimos años están apareciendo puntos de vista convergentes.
Con esto en mente, este capítulo aborda temas importantes para la comprensión del sistema nervioso y los efectos de las condiciones del lugar de trabajo en su funcionamiento. Comienza con una descripción de la anatomía y la fisiología, seguida de una sección sobre neurotoxicidad, que revisa la exposición, los resultados y la prevención.
Dado que el sistema nervioso es central para el bienestar del cuerpo, muchos peligros no químicos también pueden afectar su funcionamiento normal. Muchos de estos se consideran en diferentes capítulos que tratan sobre estos peligros. Las lesiones traumáticas en la cabeza están incluidas en Primeros auxilios, el estrés por calor se considera en el artículo “Efectos del estrés por calor y el trabajo en el calor”, y la enfermedad por descompresión se revisa en el artículo “Estrés gravitacional”. Vibración mano-brazo (“vibración transmitida por la mano”) y movimiento repetitivo (“resultados crónicos, musculoesqueléticos”) en el capítulo Sistema musculoesquelético, que son factores de riesgo de neuropatías periféricas, también se consideran en estos apartados de la Enciclopedia.
El capítulo termina con una revisión de temas especiales y las perspectivas de futuras vías de investigación.
Anatomía y fisiología
Las células nerviosas son las unidades funcionales del sistema nervioso. Se cree que el sistema nervioso tiene diez mil millones de esas células, llamadas neuronas y glía, la glía está presente en mayor número que las neuronas.
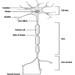
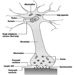
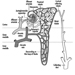
la neurona
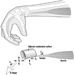
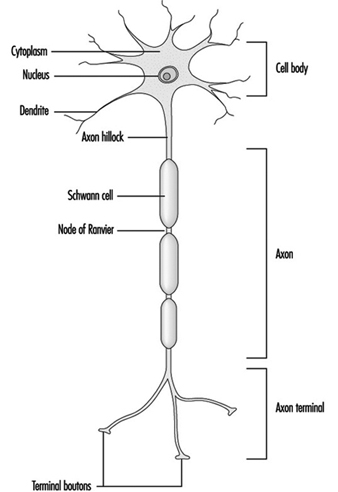
La figura 1 es un diagrama idealizado de una neurona con sus tres características estructurales más importantes: el cuerpo celular, las dendritas y el axón terminal.
Figura 1. La anatomía de la neurona
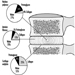
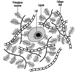
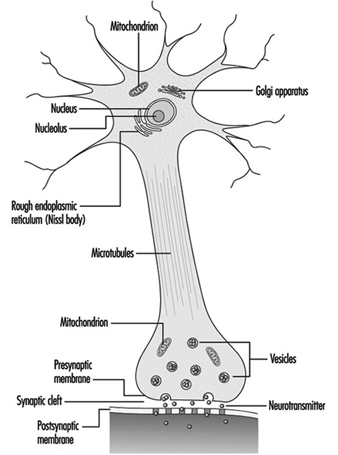
Las dendritas son procesos finamente ramificados que surgen cerca del cuerpo celular de una neurona. Las dendritas reciben efectos excitadores o inhibidores a través de mensajeros químicos llamados neurotransmisores. El citoplasma es el material del cuerpo celular en el que se encuentran los orgánulos, incluido el núcleo celular, y otras inclusiones Figura 2. El núcleo contiene la cromatina celular o material genético.
Figura 2. Los orgánulos
El núcleo de la célula nerviosa es atípico comparado con el de otras células vivas en que, aunque contiene el material genético ácido desoxirribonucleico (ADN), el ADN no está involucrado en el proceso de división celular; es decir, después de alcanzar la madurez, las células nerviosas no se dividen. (Una excepción a esta regla son las neuronas en el revestimiento de la nariz (epitelio olfativo).) El núcleo es rico en ácido ribonucleico (ARN), que es necesario para la síntesis de proteínas. Se han identificado tres tipos de proteínas: proteínas citosólicas, que forman los elementos fibrilares de la célula nerviosa; proteínas intracondriales, que generan energía para la actividad celular; y proteínas que forman membranas y productos secretores. Las neuronas ahora se conciben como células secretoras modificadas. Se forman gránulos secretores, se almacenan en vesículas sinápticas y luego se liberan como sustancias neurotransmisoras, los mensajeros químicos entre las células nerviosas.
Los elementos fibrilares, que forman el esqueleto de la neurona, participan en la función trófica de la neurona, actuando como vehículos de transmisión. El transporte axonal puede ser anterógrado (del cuerpo celular al axón terminal) y retrógrado (del axón terminal al cuerpo celular). De los más gruesos a los más delgados, se reconocen tres tipos de elementos fibrilares: microtúbulos, neurofilamentos y microfilamentos.
Células gliales
A diferencia de las neuronas, las células gliales, por sí mismas, no transmiten mensajes eléctricos. Hay dos tipos de células gliales: las macroglia y del microglia. La macroglia es el nombre que se le da a por lo menos tres tipos de células: astrocitos, oligodendrocitos y células ependimarias. Las células microgliales son principalmente células carroñeras para eliminar los desechos después de que se haya producido un daño neural o una infección.
Las células gliales también tienen características distintivas microscópicas y ultramicroscópicas. Las células gliales soportan físicamente a las neuronas, pero ahora también se empiezan a comprender una serie de propiedades fisiológicas. Entre las interacciones neuronales-gliales más importantes se encuentran el papel de las células gliales en el suministro de nutrientes a las neuronas, la eliminación de fragmentos de neuronas después de su muerte y, lo que es más importante, la contribución al proceso de comunicación química. Las células gliales, en marcado contraste con las neuronas, pueden dividirse y, por lo tanto, pueden reproducirse. Los tumores del sistema nervioso, por ejemplo, resultan de una reproducción anormal de las células gliales.
Mielina
Lo que aparece en la observación macroscópica del tejido neural como “materia gris” y “materia blanca” tiene una base microscópica y bioquímica. Microscópicamente, la materia gris contiene los cuerpos de las células neuronales, mientras que la materia blanca es donde se encuentran las fibras neurales o los axones. La apariencia "blanca" se debe a una vaina, compuesta de una sustancia grasa llamada mielina, que cubre estas fibras. La mielina de los nervios periféricos se origina en la membrana de la célula de Schwann que envuelve el axón. La mielina de las fibras del sistema nervioso central la proporcionan las membranas de los oligodendrocitos (una variedad de células gliales). Los oligodendrocitos suelen mielinizar varios axones, mientras que la célula de Schwann se asocia con un solo axón. Existe una discontinuidad de la vaina de mielina, designada como nódulos de Ranvier, entre las células de Schwann u oligodendrocitos continuos. Se estima que en la vía motora central más larga, hasta 2,000 células de Schwann forman la cubierta de mielina. La mielina, cuyo papel es facilitar la propagación del potencial de acción, puede ser un objetivo específico de los agentes neurotóxicos. Una clasificación morfológica de las sustancias neurotóxicas describe los cambios neuropatológicos característicos de la mielina como mielinopatías.
Función trófica de la neurona
Las funciones normales de la neurona incluyen la síntesis de proteínas, el transporte axonal, la generación y conducción del potencial de acción, la transmisión sináptica y la formación y mantenimiento de la mielina. Algunas de las funciones tróficas básicas de la neurona se describieron ya en el siglo XIX mediante la sección de los axones (axotomía). Entre los procesos descubiertos, uno de los más importantes fue la degeneración walleriana, en honor a Waller, el fisiólogo inglés que la describió.
La degeneración walleriana brinda una buena oportunidad para describir cambios bien conocidos en los orgánulos como resultado de daño traumático o tóxico. Entre paréntesis, los términos utilizados para describir la degeneración walleriana producida por axotomía traumática son los mismos que se utilizan para describir los cambios resultantes de agentes neurotóxicos. A nivel celular, los cambios neuropatológicos que resultan del daño tóxico al tejido neural son mucho más complejos que los que ocurren como resultado del daño traumático. Sólo recientemente se han observado cambios en las neuronas afectadas por agentes neurotóxicos.
Veinticuatro horas después del corte del axón, la característica más distintiva es la inflamación de ambos lados del trauma mecánico. La hinchazón resulta de la acumulación de fluidos y elementos membranosos en ambos lados del sitio de la lesión. Estos cambios no son diferentes a los observados en una carretera de doble sentido inundada por la lluvia con vehículos detenidos a ambos lados del área inundada. En esta analogía, los vehículos parados son la hinchazón. Después de unos días, se produce la regeneración de los axones envainados, es decir, los cubiertos con mielina. Los brotes crecen desde el muñón proximal moviéndose a un ritmo de 1 a 3 mm por día. En condiciones favorables, los brotes alcanzan el muñón distal (más alejado del cuerpo celular). Cuando se completa la renervación (unión de los muñones), se han restablecido las características básicas de la transmisión normal. El cuerpo celular de la neurona lesionada sufre cambios estructurales profundos en la síntesis de proteínas y el transporte axonal.
Si se dice que la neurobiología molecular es una disciplina joven, la neurobiología de los procesos neurotóxicos es aún más joven y aún está en pañales. Es cierto que ahora se comprende bien la base molecular de la acción de muchas neurotoxinas y agentes farmacológicos. Pero con algunas excepciones notables (p. ej., plomo, metilmercurio, acrilamida), se desconoce la base molecular de la toxicidad de la gran mayoría de los agentes ambientales y neurotóxicos. Por eso, en lugar de describir la neurobiología molecular de un grupo selecto de agentes neurotóxicos ocupacionales y ambientales, todavía nos vemos obligados a referirnos a las estrategias y ejemplos comparativamente abundantes de la neurofarmacología clásica o del trabajo en la fabricación moderna de medicamentos.
Neurotransmisores
Un neurotransmisor es una sustancia química que, cuando se libera de las terminales del axón por el potencial de acción, produce un cambio momentáneo en el potencial eléctrico cuando se estimula otra fibra nerviosa. Los neurotransmisores estimulan o inhiben las neuronas adyacentes o los órganos efectores, como los músculos y las glándulas. Los neurotransmisores conocidos y sus vías neuronales ahora se están estudiando intensamente, y constantemente se descubren nuevos. Ahora se sabe que algunos trastornos neurológicos y psiquiátricos son causados por cambios químicos en la neurotransmisión, por ejemplo, miastenia grave, enfermedad de Parkinson, ciertas formas de trastornos afectivos como la depresión, distorsión severa de los procesos de pensamiento como en la esquizofrenia y la enfermedad de Alzheimer. Aunque se han publicado excelentes informes aislados sobre el efecto de varios agentes neurotóxicos ambientales y ocupacionales sobre la neurotransmisión, el cuerpo de conocimiento es escaso en comparación con el existente para las enfermedades neuropsiquiátricas. Los estudios farmacológicos de las drogas fabricadas requieren una comprensión de cómo las drogas afectan la neurotransmisión. La fabricación de fármacos y la investigación en neurotransmisión están íntimamente relacionadas. Feldman y Quenzer (1984) resumieron las opiniones cambiantes sobre la acción de los fármacos.
Los efectos de los agentes neurotóxicos sobre la neurotransmisión se caracterizan por el lugar del sistema nervioso en el que actúan, sus receptores químicos, el curso temporal de sus efectos, si los agentes neurotóxicos facilitan, bloquean o inhiben la neurotransmisión, o si los agentes neurotóxicos alteran la terminación o eliminación de la acción farmacológica del neurotransmisor.
Una dificultad experimentada por los neurocientíficos es la necesidad de vincular procesos conocidos que ocurren a nivel molecular en la neurona con eventos a nivel celular, lo que a su vez puede explicar cómo ocurren los cambios neuropsicológicos normales y patológicos, como se establece claramente a continuación, que a un todavía se aplica en gran medida: “(A)l nivel molecular, a menudo es posible una explicación de la acción de un fármaco; a nivel celular, a veces es posible una explicación, pero a nivel conductual, nuestra ignorancia es abismal” (Cooper, Bloom y Roth 1986).
Los componentes principales del sistema nervioso
El conocimiento de los componentes principales del sistema nervioso es esencial para la comprensión de las manifestaciones neuropsicológicas macroscópicas de la enfermedad neurotóxica, la justificación del uso de técnicas específicas para la evaluación de las funciones del sistema nervioso y la comprensión de los mecanismos farmacológicos de la acción neurotóxica. Desde un punto de vista funcional, el sistema nervioso se puede dividir en dos compartimentos principales: el sistema nervioso somático transmite información sensorial (tacto, temperatura, dolor y posición de las extremidades, incluso cuando los ojos están cerrados) desde los segmentos del cuerpo y lleva las vías neurales que inervan y controlan el movimiento de los músculos esqueléticos, como los de los brazos, dedos, piernas y dedos del pie. Él sistema nervioso visceral controla los órganos internos que normalmente no están bajo la influencia de los vasos sanguíneos, la dilatación y constricción de las pupilas de los ojos, etc.
Desde un punto de vista anatómico, es necesario identificar cuatro componentes principales: el sistema nervioso central, la sistema nervioso periférico incluyendo los nervios craneales, el sistema autonómico y del sistema neuroendocrino.
El Sistema Nervioso Central
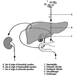
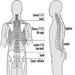
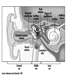
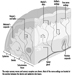
El sistema nervioso central contiene el cerebro y la médula espinal Figura 3. El cerebro se encuentra en la cavidad del cráneo y está protegido por las meninges. Se divide en tres componentes principales; en orden ascendente, es decir, desde la porción caudal (cola) a la cervical (cabeza) del sistema nervioso, son el cerebro posterior (también llamado rombencéfalo), el cerebro medio (mescencéfalo) y el cerebro anterior (proscencéfalo).
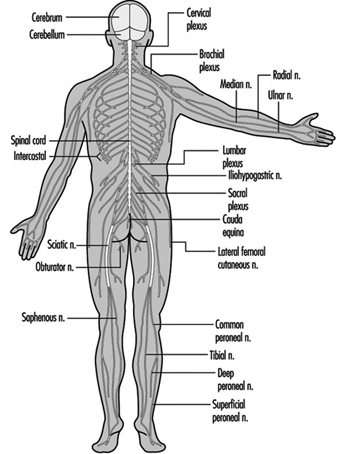
Figura 3. Las divisiones central y periférica del sistema nervioso.
el rombencéfalo
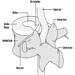
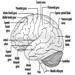
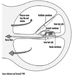
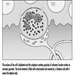
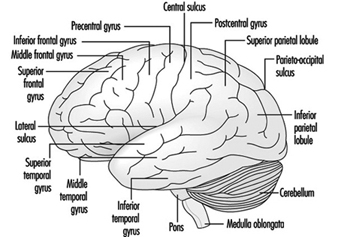
Los tres componentes principales del rombencéfalo son el bulbo raquídeo, la protuberancia y el cerebelo figura 4.
Figura 4. El cerebro visto desde un lado lateral.
El bulbo raquídeo contiene estructuras neurales que controlan la frecuencia cardíaca y la respiración, a veces los objetivos de los agentes neurotóxicos y las drogas que causan la muerte. Situado entre el bulbo raquídeo y el mesencéfalo, la protuberancia (puente) deriva su nombre del gran número de fibras que atraviesan su cara anterior en ruta hacia los hemisferios cerebelosos. El cerebelo, en latín, cerebro pequeño, tiene una apariencia característicamente corrugada. El cerebelo recibe información sensorial y envía mensajes motores esenciales para la coordinación motora. Es responsable (entre otras funciones) de la ejecución de movimientos finos. Esta programación, o programación, requiere la sincronización adecuada de las entradas sensoriales y las respuestas motoras. El cerebelo suele ser el objetivo de numerosos agentes neurotóxicos, por ejemplo, bebidas alcohólicas, muchos solventes industriales, plomo, que afectan las respuestas motoras.
El mesencéfalo
El cerebro medio es una parte estrecha del cerebro que conecta el cerebro posterior con el cerebro anterior. Las estructuras del mesencéfalo son el acueducto cerebral, el tectum, los pedúnculos cerebrales, la sustancia negra y el núcleo rojo. El acueducto cerebral es un canal que conecta el tercero con el cuarto ventrículo (cavidades del cerebro llenas de líquido); el líquido cefalorraquídeo (LCR) fluye a través de esta abertura.
el prosencéfalo
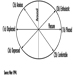
Esta parte del cerebro se subdivide en diencéfalo ("entre cerebro") y el cerebro. Las principales regiones del diencéfalo son el tálamo y el hipotálamo. “Tálamo” significa “cuarto interior”. Los tálamos están formados por agrupaciones neuronales, llamadas núcleos, que tienen cinco funciones principales:
- recibir información sensorial y enviarla a áreas primarias de la corteza cerebral
- enviar información sobre el movimiento en curso a las áreas motoras de la corteza cerebral
- enviar información sobre la actividad del sistema límbico a áreas de la corteza cerebral relacionadas con este sistema
- enviar información sobre la actividad intratalámica a las áreas de asociación de la corteza cerebral
- enviar información de la actividad de formación reticular del tronco encefálico a áreas extensas de la corteza cerebral.
El nombre hipotálamo significa “debajo del tálamo”. Forma la base del tercer ventrículo, un importante punto de referencia para la obtención de imágenes del cerebro. El hipotálamo es una estructura neuronal compleja y diminuta responsable de muchos aspectos del comportamiento, como los impulsos biológicos básicos, la motivación y la emoción. Es el vínculo entre el sistema nervioso y el neuroendocrino, que se revisará a continuación. La glándula pituitaria (también llamada hipófisis) está unida por neuronas a los núcleos hipotalámicos. Está bien establecido que las células nerviosas hipotalámicas realizan muchas funciones neurosecretoras. El hipotálamo está vinculado con muchas otras regiones importantes del cerebro, incluido el rinencéfalo, la corteza primitiva asociada originalmente con el olfato, y el sistema límbico, incluido el hipocampo.
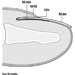
La corteza cerebral es el componente más grande del cerebro y consta de dos hemisferios cerebrales conectados por una masa de sustancia blanca llamada cuerpo calloso. La corteza cerebral es la capa superficial de cada hemisferio cerebral. Los surcos profundos de la corteza cerebral (los surcos central y lateral Figura 4) se toman como puntos de referencia para separar las regiones anatómicas del cerebro. El lóbulo frontal se encuentra frente al surco central. El lóbulo parietal comienza en la parte posterior del surco central y se encuentra junto al lóbulo occipital, que ocupa la porción posterior del cerebro. El lóbulo temporal comienza bien dentro del pliegue del surco lateral y se extiende hacia las caras ventrales de los hemisferios cerebrales. Dos componentes importantes del cerebro son los ganglios basales y el sistema límbico.
Los ganglios basales son núcleos, es decir, grupos de células nerviosas, ubicados hacia el centro del cerebro. Los ganglios basales comprenden los principales centros del sistema motor extrapiramidal. (El sistema piramidal, al que se contrapone el término, participa en el control voluntario del movimiento.) El sistema extrapiramidal se ve afectado selectivamente por muchos agentes neurotóxicos (p. ej., manganeso). En las últimas dos décadas, se han realizado importantes descubrimientos sobre el papel que desempeñan estos núcleos en varias enfermedades degenerativas neurales (p. ej., enfermedad de Parkinson, corea de Huntington).
El sistema límbico se compone de estructuras neurales enrevesadas que se ramifican en muchas direcciones y establecen conexiones con muchas regiones "antiguas" del cerebro, particularmente con el hipotálamo. Interviene en el control de la expresión emocional. Se cree que el hipocampo es una estructura donde ocurren muchos procesos de memoria.
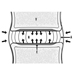
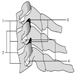
La medula espinal
La médula espinal es una estructura blanquecina situada dentro del canal vertebral. Se divide en cuatro regiones: cervical, torácica, lumbar y sacro-coxígea. Las dos características más fácilmente reconocibles de la médula espinal son la materia gris que contiene los cuerpos celulares de las neuronas y la materia blanca que contiene los axones mielinizados de las neuronas. La región ventral de la materia gris de la médula espinal contiene células nerviosas que regulan la función motora; la región media de la médula espinal torácica está asociada con funciones autonómicas. La porción dorsal recibe información sensorial de los nervios espinales.
El sistema nervioso periférico
El sistema nervioso periférico incluye aquellas neuronas que están fuera del sistema nervioso central. El termino periférico describe la distribución anatómica de este sistema, pero funcionalmente es artificial. Los cuerpos celulares de las fibras motoras periféricas, por ejemplo, se encuentran dentro del sistema nervioso central. En neurotoxicología experimental, clínica y epidemiológica, el término sistema nervioso periférico (PNS) describe un sistema que es selectivamente vulnerable a los efectos de agentes tóxicos y que es capaz de regenerarse.
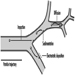
Los nervios espinales
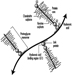
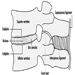
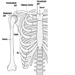
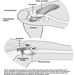
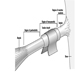
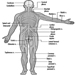
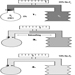
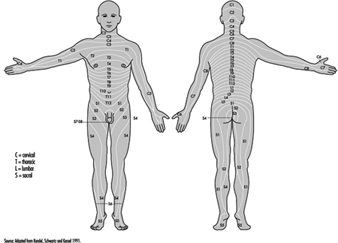
Las raíces ventral y dorsal son donde los nervios periféricos entran y salen de la médula espinal a lo largo de su longitud. Las vértebras adyacentes contienen aberturas para permitir que las fibras de la raíz que forman los nervios espinales salgan del canal espinal. Hay 31 pares de nervios espinales, que se nombran según la región de la columna vertebral a la que están asociados: 8 cervicales, 12 torácicos, 5 lumbares, 5 sacros y 1 coxígeo. Una metámera es una región del cuerpo inervada por un nervio espinal figura 5.
Figura 5. La distribución segmentaria de los nervios espinales (la metámera).
Examinando cuidadosamente las funciones motoras y sensoriales de las metámeras, los neurólogos pueden inferir la ubicación de las lesiones donde se ha producido el daño.
Tabla 1. Nombres y funciones principales de cada par de nervios craneales
| Nervio1 | Conduce impulsos | Clave |
| I. Olfativo | De la nariz al cerebro | Sentido del olfato |
| II. Óptico | Del ojo al cerebro | Visión |
| tercero oculomotor | Del cerebro a los músculos oculares | Movimientos oculares |
| IV. troclear | Del cerebro a los músculos oculares externos | Movimientos oculares |
| V. trigémino (o trifacial) |
Desde la piel y membrana mucosa de la cabeza y desde los dientes hasta el cerebro; también del cerebro a los músculos masticadores | Sensaciones de cara, cuero cabelludo y dientes; movimientos de masticación |
| VI. abducens | Del cerebro a los músculos oculares externos | Volviendo los ojos hacia afuera |
| VIII. Facial | De las papilas gustativas de la lengua al cerebro; del cerebro a los músculos de la cara | Sentido del gusto; contracción de los músculos de la expresión facial |
| VIII. Acústico | De oreja a cerebro | Audiencia; sensación de equilibrio |
| IX. glosofaríngeo | Desde la garganta y las papilas gustativas de la lengua hasta el cerebro; también desde el cerebro hasta los músculos de la garganta y las glándulas salivales | Sensaciones de garganta, gusto, movimientos de deglución, secreción de saliva. |
| X. vago | Desde la garganta, la laringe y los órganos de las cavidades torácica y abdominal hasta el cerebro; también del cerebro a los músculos de la garganta y a los órganos de las cavidades torácica y abdominal | Sensaciones de garganta, laringe y órganos torácicos y abdominales; deglución, producción de voz, ralentización de los latidos del corazón, aceleración del peristaltismo |
| XI. Accesorio espinal | Del cerebro a ciertos músculos de los hombros y el cuello | Movimientos de hombros; movimientos de giro de la cabeza |
| XII. hipogloso | Del cerebro a los músculos de la lengua | movimientos de la lengua |
1 La primera letra de las palabras de la siguiente oración son las primeras letras de los nombres de los nervios craneales: "En las diminutas cimas del viejo Olimpo, un finlandés y un alemán vieron algunos lúpulos". Muchas generaciones de estudiantes han usado esta oración u otra similar para recordar los nombres de los nervios craneales.
Los nervios craneales
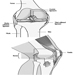
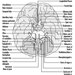
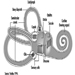
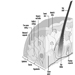
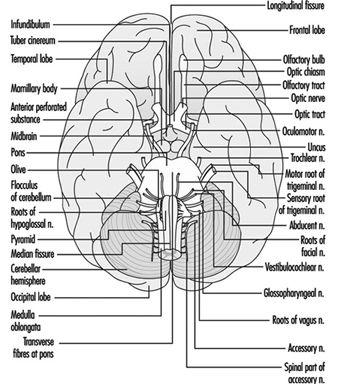
Tronco cerebral es un término amplio que designa la región del sistema nervioso que incluye el bulbo raquídeo, la protuberancia y el mesencéfalo. El tronco encefálico es una continuación de la médula espinal hacia arriba y hacia adelante (ventralmente). Es en esta región por donde entran y salen la mayoría de los nervios craneales. Hay 12 pares de nervios craneales; La Tabla 1 describe el nombre y la función principal de cada par y la Figura 6 muestra la entrada y salida de algunos nervios craneales en el cerebro.
Figura 6. El cerebro mostrado desde abajo con la entrada y salida de muchos nervios craneales.
El sistema nervioso autónomo
El sistema nervioso autónomo es la parte del sistema nervioso que controla la actividad de los componentes viscerales del cuerpo humano. Se llama “autonómico” porque realiza sus funciones automáticamente, lo que significa que su funcionamiento no se puede controlar fácilmente a voluntad. Desde un punto de vista anatómico, el sistema autónomo tiene dos componentes principales: el sistema nervioso simpático y el parasimpático. Los nervios simpáticos que controlan la actividad visceral surgen de las porciones torácica y lumbar de la médula espinal; Los nervios parasimpáticos surgen del tronco encefálico y la porción sacra de la médula espinal.
Desde un punto de vista fisiológico, no se puede hacer una sola generalización que se aplique a la manera en que los sistemas nerviosos simpático y parasimpático controlan los diferentes órganos del cuerpo. En la mayoría de los casos, los órganos viscerales están inervados por ambos sistemas y cada tipo tiene un efecto opuesto en un sistema de frenos y contrapesos. El corazón, por ejemplo, está inervado por nervios simpáticos cuya excitación produce una aceleración de los latidos del corazón, y por nervios parasimpáticos cuya excitación produce una disminución de los latidos del corazón. Cualquiera de los dos sistemas puede estimular o inhibir los órganos que inerva. En otros casos, los órganos están predominante o exclusivamente controlados por uno u otro sistema. Una función vital del sistema nervioso autónomo es el mantenimiento de la homeostasis (estado estable de equilibrio) y para la adaptación del cuerpo animal a su entorno externo. La homeostasis es el estado de equilibrio de las funciones corporales logrado por un proceso activo; el control de la temperatura corporal, el agua y los electrolitos son ejemplos de procesos homeostáticos.
Desde el punto de vista farmacológico, no existe un único neurotransmisor asociado con funciones simpáticas o parasimpáticas, como se creía en un tiempo. La antigua opinión de que la acetilcolina era el transmisor predominante del sistema autónomo tuvo que abandonarse cuando se encontraron nuevas clases de neurotransmisores y neuromoduladores (p. ej., dopamina, serotonina, purinas y varios neuropéptidos).
Los neurocientíficos han revivido recientemente el punto de vista conductual del sistema nervioso autónomo. El sistema nervioso autónomo está involucrado en la reacción instintiva de lucha o huida todavía presente en los humanos, que es, en su mayor parte, la base de las reacciones fisiológicas causadas por el estrés. Las interacciones entre el sistema nervioso y las funciones inmunológicas son posibles a través del sistema nervioso autónomo. Las emociones que se originan en el sistema nervioso autónomo se pueden expresar a través de los músculos esqueléticos.
El control autonómico de los músculos lisos.
Los músculos de las vísceras, excepto el corazón, son los músculos lisos. El músculo cardíaco tiene características tanto del músculo esquelético como del músculo liso. Al igual que los músculos esqueléticos, los músculos lisos también contienen las dos proteínas actina y, en menor proporción, miosina. A diferencia de los músculos esqueléticos, no presentan la organización regular de los sarcolemas, la unidad contráctil de la fibra muscular. El corazón es único en el sentido de que puede generar actividad miogénica; incluso después de que se hayan cortado sus inervaciones neuronales, puede contraerse y relajarse durante varias horas por sí mismo.
El acoplamiento neuromuscular en los músculos lisos difiere del de los músculos esqueléticos. En los músculos esqueléticos, la unión neuromuscular es el enlace entre el nervio y las fibras musculares. En el músculo liso no hay unión neuromuscular; las terminaciones nerviosas entran en el músculo y se extienden en todas las direcciones. Por lo tanto, los eventos eléctricos dentro del músculo liso son mucho más lentos que los de los músculos esqueléticos. Finalmente, el músculo liso tiene la característica única de exhibir contracciones espontáneas, como las que presenta el intestino. En gran medida, el sistema nervioso autónomo regula la actividad espontánea de los músculos lisos.
Los componentes centrales del sistema nervioso autónomo.
El papel principal del sistema nervioso autónomo es regular la actividad de los músculos lisos, el corazón, las glándulas del tracto digestivo, las glándulas sudoríparas y las glándulas suprarrenales y otras glándulas endocrinas. El sistema nervioso autónomo tiene un componente central, el hipotálamo, ubicado en la base del cerebro, donde se integran muchas funciones autónomas. Lo que es más importante, los componentes centrales del sistema autónomo están directamente involucrados en la regulación de los impulsos biológicos (regulación de la temperatura, hambre, sed, sexo, micción, defecación, etc.), la motivación, la emoción y, en gran medida, en las funciones "psicológicas". tales como estados de ánimo, afecto y sentimientos.
Sistema Neuroendocrino
Las glándulas son los órganos del sistema endocrino. Se llaman glándulas endocrinas porque sus mensajes químicos se envían dentro del cuerpo, directamente al torrente sanguíneo (en contraste con las glándulas exocrinas, como las glándulas sudoríparas, cuyas secreciones aparecen en la superficie exterior del cuerpo). El sistema endocrino proporciona un control lento pero duradero sobre los órganos y tejidos a través de mensajeros químicos llamados hormonas. Las hormonas son los principales reguladores del metabolismo corporal. Pero, debido a los vínculos íntimos entre los sistemas nerviosos central, periférico y autónomo, el sistema neuroendocrino—un término que captura vínculos tan complejos— ahora se concibe como un poderoso modificador de la estructura y función del cuerpo humano y el comportamiento.
Las hormonas se han definido como mensajeros químicos que se liberan de las células al torrente sanguíneo para ejercer su acción sobre las células diana a cierta distancia. Hasta hace poco, las hormonas se distinguían de los neurotransmisores, discutidos anteriormente. Estos últimos son mensajeros químicos liberados por las neuronas en una sinapsis entre las terminaciones nerviosas y otra neurona o un efector (es decir, un músculo o una glándula). Sin embargo, con el descubrimiento de que los neurotransmisores clásicos como la dopamina también pueden actuar como hormonas, la distinción entre neurotransmisores y hormonas es cada vez menos clara. Por tanto, basándose en consideraciones puramente anatómicas, las hormonas derivadas de las células nerviosas pueden denominarse neurohormonas. Desde un punto de vista funcional, el sistema nervioso puede considerarse como un verdadero sistema neurosecretor.
El hipotálamo controla las funciones endocrinas a través de un enlace con la glándula pituitaria (también llamada hipófisis, una glándula diminuta ubicada en la base del cerebro). Hasta mediados de la década de 1950, las glándulas endocrinas se consideraban un sistema separado gobernado por la glándula pituitaria, a menudo llamada "glándula maestra". En ese momento, se avanzó una hipótesis neurovascular que establecía el papel funcional de los factores hipotalámicos/hipofisarios en el control de la función endocrina. Desde este punto de vista, el hipotálamo endocrino proporciona la vía neuroendocrina común final en el control del sistema endocrino. Ahora se ha establecido firmemente que el propio sistema endocrino está regulado por el sistema nervioso central, así como por las entradas endocrinas. Por lo tanto, neuroendocrinología es ahora un término apropiado para describir la disciplina que estudia los roles integrados recíprocos de los sistemas nervioso y endocrino en el control de los procesos fisiológicos.
Con una comprensión cada vez mayor de la neuroendocrinología, las divisiones originales se están desmoronando. El hipotálamo, que se encuentra arriba y conectado a la glándula pituitaria, es el enlace entre los sistemas nervioso y endocrino, y muchas de sus células nerviosas realizan funciones secretoras. También está vinculado con otras regiones importantes del cerebro, incluido el rinencéfalo, la corteza primitiva asociada originalmente con el olfato o el sentido del olfato, y el sistema límbico, asociado con las emociones. Es en el hipotálamo donde se producen las hormonas liberadas por la hipófisis posterior. El hipotálamo también produce sustancias que se llaman hormonas liberadoras e inhibidoras. Éstos actúan sobre la adenohipófisis, provocando que ésta potencie o inhiba la producción de hormonas de la hipófisis anterior, que actúan sobre glándulas situadas en otros lugares (tiroides, corteza suprarrenal, ovarios, testículos y otras).
Agentes Neurotóxicos Químicos
Definición de neurotoxicidad
Neurotoxicidad se refiere a la capacidad de inducir efectos adversos en el sistema nervioso central, los nervios periféricos o los órganos sensoriales. Se considera que una sustancia química es neurotóxica si es capaz de inducir un patrón constante de disfunción neural o un cambio en la química o la estructura del sistema nervioso.
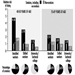
La neurotoxicidad generalmente se manifiesta como un continuo de síntomas y efectos, que dependen de la naturaleza de la sustancia química, la dosis, la duración de la exposición y las características del individuo expuesto. La gravedad de los efectos observados, así como la evidencia de neurotoxicidad, aumenta hasta los niveles 1 a 6, que se muestran en la Tabla 1. La exposición a corto plazo o en dosis bajas a un químico neurotóxico puede provocar síntomas subjetivos como dolor de cabeza y mareos, pero el efecto suele ser reversible. Al aumentar la dosis, pueden aparecer cambios neurológicos y eventualmente se generan cambios morfológicos irreversibles. El grado de anormalidad necesario para implicar la neurotoxicidad de un agente químico es un tema controvertido. De acuerdo con la definición, se considera un patrón consistente de disfunción neural o cambio en la química o estructura del sistema nervioso si hay evidencia bien documentada de efectos persistentes en el nivel 3, 4, 5 o 6 en la Tabla 1. Estos niveles reflejan el peso de la evidencia proporcionada por diferentes signos de neurotoxicidad. Las sustancias neurotóxicas incluyen elementos naturales como el plomo, el mercurio y el manganeso; compuestos biológicos como la tetrodotoxina (del pez globo, un manjar japonés) y el ácido domoico (de mejillones contaminados); y compuestos sintéticos que incluyen muchos pesticidas, solventes industriales y monómeros.
Tabla 1. Agrupación de efectos neurotóxicos para reflejar su fuerza relativa para establecer la neurotoxicidad
|
Nivel |
Agrupamiento |
Explicación/Ejemplos |
|
6 |
Cambios morfológicos |
Los cambios morfológicos incluyen muerte celular y axonopatía, así como cambios morfológicos subcelulares. |
|
5 |
Cambios neurológicos |
El cambio neurológico abarca hallazgos anormales en exámenes neurológicos en individuos individuales. |
|
4 |
Cambios fisiológicos/comportamentales |
Los cambios fisiológicos/comportamentales comprenden hallazgos experimentales en grupos de animales o humanos, como cambios en los potenciales evocados y EEG, o cambios en las pruebas psicológicas y conductuales. |
|
3 |
Cambios bioquímicos |
Los cambios bioquímicos cubren cambios en parámetros bioquímicos relevantes (p. ej., nivel de transmisor, contenido de proteína GFA (proteína ácida fibrilar glial) o actividades enzimáticas). |
|
21 |
Síntomas subjetivos irreversibles |
Síntomas subjetivos. No hay evidencia de anormalidad en el examen neurológico, psicológico u otro examen médico. |
|
11 |
Síntomas subjetivos reversibles |
Síntomas subjetivos. No hay evidencia de anormalidad en el examen neurológico, psicológico u otro examen médico. |
1 Solo humanos
Fuente: Modificado de Simonsen et al. 1994.
En los Estados Unidos se comercializan entre 50,000 100,000 y 1,000 1,600 productos químicos, y cada año se someten a evaluación entre 750 y 1985 nuevos productos químicos. Se sospecha que más de XNUMX productos químicos y varias clases o grupos de compuestos químicos son neurotóxicos (O'Donoghue XNUMX), pero nunca se han probado las propiedades neurotóxicas de la mayoría de los productos químicos. La mayoría de los productos químicos neurotóxicos conocidos disponibles en la actualidad han sido identificados por informes de casos o por accidentes.
Aunque los productos químicos neurotóxicos a menudo se producen para cumplir con usos específicos, la exposición puede provenir de varias fuentes: uso en casas particulares, en la agricultura y en las industrias, o del agua potable contaminada, etc. Se corrigieron las ideas preconcebidas a priori sobre qué compuestos neurotóxicos se espera que se encuentren en qué ocupaciones, por lo tanto, deben considerarse con precaución, y las siguientes citas deben considerarse como posibles ejemplos que incluyen algunos de los químicos neurotóxicos más comunes (Arlien-Søborg 1992; O 'Donoghue 1985; Spencer y Schaumburg 1980; OMS 1978).
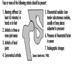
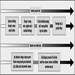
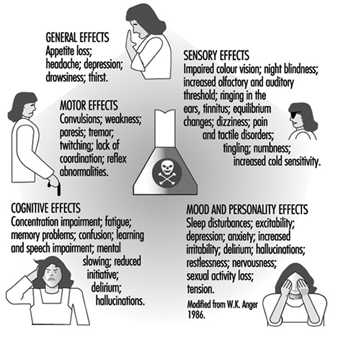
Síntomas de neurotoxicidad
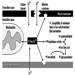
El sistema nervioso generalmente reacciona de manera bastante estereotipada a la exposición a sustancias neurotóxicas. Figura 1. A continuación se indican algunos síndromes típicos.
Figura 1. Efectos neurológicos y conductuales de la exposición a sustancias químicas neurotóxicas.
Polineuropatía
Esto es causado por el deterioro de la función nerviosa motora y sensorial que conduce a la debilidad de los músculos, con paresia generalmente más pronunciada en la periferia de las extremidades superiores e inferiores (manos y pies). Puede ocurrir parestesia previa o simultánea (hormigueo o entumecimiento en los dedos de manos y pies). Esto puede provocar dificultades para caminar o en la coordinación fina de manos y dedos. Los metales pesados, los solventes y los pesticidas, entre otros productos químicos, pueden provocar dicha discapacidad, aunque el mecanismo tóxico de estos compuestos sea totalmente diferente.
Encefalopatía
Esto es causado por un deterioro difuso del cerebro y puede resultar en fatiga; deterioro del aprendizaje, la memoria y la capacidad de concentración; ansiedad, depresión, aumento de la irritabilidad e inestabilidad emocional. Dichos síntomas pueden indicar un trastorno cerebral degenerativo difuso temprano, así como una encefalopatía tóxica crónica ocupacional. A menudo, el aumento de la frecuencia de los dolores de cabeza, los mareos, los cambios en el patrón de sueño y la reducción de la actividad sexual también pueden estar presentes desde las primeras etapas de la enfermedad. Dichos síntomas pueden desarrollarse después de una exposición prolongada y de bajo nivel a varios productos químicos diferentes, como solventes, metales pesados o sulfuro de hidrógeno, y también se observan en varios trastornos demenciales no relacionados con el trabajo. En algunos casos se pueden observar síntomas neurológicos más específicos (p. ej., parkinsonismo con temblor, rigidez de los músculos y ralentización de los movimientos, o síntomas cerebelosos como temblor y coordinación reducida de los movimientos de las manos y la marcha). Dichos cuadros clínicos se pueden ver después de la exposición a algunos químicos específicos como el manganeso o MPTP (1-metil-4-fenil-1,2,3,6-tetrahidropiridina) en la primera condición y tolueno o mercurio en la segunda.
Gases
Una amplia variedad de productos químicos con estructuras químicas totalmente diferentes son gases a temperatura normal y se ha demostrado que son neurotóxicos Tabla 3. Algunos de ellos son extremadamente tóxicos incluso en dosis muy pequeñas, e incluso se han utilizado como gases de guerra (fosgeno y cianuro); otros requieren dosis altas durante períodos más prolongados para producir síntomas (p. ej., dióxido de carbono). Algunos se usan para anestesia general (p. ej., óxido nitroso); otros se utilizan ampliamente en la industria y en agentes utilizados para la desinfección (p. ej., formaldehído). El primero puede inducir cambios irreversibles en el sistema nervioso después de una exposición repetida de bajo nivel, el segundo aparentemente produce solo síntomas agudos. La exposición en habitaciones pequeñas con mala ventilación es particularmente peligrosa. Algunos de los gases son inodoros, lo que los hace particularmente peligrosos (p. ej., monóxido de carbono). Como se muestra en la Tabla 2, algunos gases son constituyentes importantes en la producción industrial, mientras que otros son el resultado de una combustión incompleta o completa (p. ej., CO y CO2 respectivamente). Esto se ve en minería, acerías, centrales eléctricas, etc., pero también se puede ver en casas privadas con ventilación insuficiente. Esencial para el tratamiento es detener una mayor exposición y proporcionar aire fresco u oxígeno y, en casos graves, ventilación artificial.
Tabla 2. Gases asociados con efectos neurotóxicos
|
Química |
Ejemplos de fuente de exposición |
Industrias seleccionadas en riesgo |
Efectos1 |
|
Dióxido de carbono (CO2 ) |
Soldadura; fermentación; fabricación, almacenamiento y uso de hielo seco |
industria metalúrgica; minería; cervecerías |
M: Vasos dilatados A: Dolor de cabeza; disnea; temblor; pérdida de consciencia C: Apenas |
|
El monóxido de carbono (CO) |
Reparación de autos; soldadura; fusión de metales; conductores; bomberos |
industria metalúrgica; minería; transportación; central eléctrica |
M: Privación de oxígeno A: Dolor de cabeza; somnolencia; pérdida de consciencia |
|
Sulfuro de hidrógeno (H2S) |
Fumigación de invernadero; estiércol; pescadores; descarga de pescado; manejo de alcantarillado |
Agricultura; pesca; trabajo de alcantarillado |
M: Bloqueo del metabolismo oxidativo A: Pérdida de consciencia C: Encefalopatía |
|
Cianuro (HCN) |
electrosoldadura; tratamiento superficial galvánico con níquel; cobre y plata; fumigación de barcos, casas alimentos y suelo en invernaderos |
industria metalúrgica; industria química; guardería; minería; fábrica de gas |
M: Bloqueo de enzimas respiratorias A: Disnea; caída de la presión arterial; convulsiones; pérdida de consciencia; muerte C: encefalopatía; ataxia; neuropatía (p. ej., después de comer cavasava) Incapacidad laboral incierta |
|
Óxido nitroso (N2O) |
Anestesia general durante la operación; narcosis ligera en el cuidado dental y el parto |
Hospitales (anestesia); dentistas; Partera |
M: Cambio agudo en la membrana de las células nerviosas; degeneración de las células nerviosas después de una exposición prolongada A: mareos; somnolencia; pérdida de consciencia C: Entumecimiento de los dedos de manos y pies; coordinación reducida; encefalopatía |
1 M: mecanismo; A: efectos agudos; C: efectos crónicos.
Neuropatía: disfunción de las fibras nerviosas periféricas motoras y sensoriales.
Encefalopatía: disfunción cerebral debida a un deterioro generalizado del cerebro.
Ataxia: alteración de la coordinación motora.
Metales
Por regla general, la toxicidad de los metales aumenta con el aumento del peso atómico, siendo el plomo y el mercurio particularmente tóxicos. Los metales generalmente se encuentran en la naturaleza en bajas concentraciones, pero en ciertas industrias se utilizan en grandes cantidades (ver Tabla 3) y pueden generar riesgo laboral para los trabajadores. Además, se encuentran cantidades considerables de metales en las aguas residuales y pueden generar un riesgo ambiental para los residentes cercanos a las plantas, pero también a mayores distancias. A menudo, los metales (o, por ejemplo, los compuestos orgánicos de mercurio) se incorporan a la cadena alimentaria y se acumulan en peces, aves y animales, lo que representa un riesgo para los consumidores. La toxicidad y la forma en que el organismo manipula los metales puede depender de la estructura química. Los metales puros pueden absorberse por inhalación o contacto con la piel de vapor (mercurio) y/o partículas pequeñas (plomo), o por vía oral (plomo). Compuestos inorgánicos de mercurio (p. ej., HgCl2) se absorben principalmente por vía oral, mientras que los compuestos orgánicos metálicos (p. ej., tetraetilo de plomo) se absorben principalmente por inhalación o por contacto con la piel. La carga corporal puede reflejarse hasta cierto punto en la concentración de metal en la sangre o la orina. Esta es la base para el control biológico. En el tratamiento debe recordarse que especialmente el plomo se libera muy lentamente de los depósitos en el cuerpo. La cantidad de plomo en los huesos normalmente se reducirá solo un 50% en 10 años. Esta liberación puede acelerarse mediante el uso de agentes quelantes: BAL (dimercapto-1-propanol), Ca-EDTA o penicilamina.
Tabla 3. Metales y sus compuestos inorgánicos asociados a neurotoxicidad
|
Química |
Ejemplos de fuente de exposición |
Industrias seleccionadas en riesgo |
Efectos1 |
|
Lidera |
Derritiendo; soldadura; molienda; reparar; acristalamiento; plastificante |
trabajos en metal; minería; plantas de acumuladores; reparación de autos; astilleros; trabajadores del vidrio; cerámica; cerámica; el plastico |
M: Deterioro del metabolismo oxidativo de las células nerviosas y la glía A: Dolor abdominal; dolor de cabeza; encefalopatía; convulsiones C: encefalopatía; polineuropatía, incluida la mano caída |
|
Elemental de Mercurio |
Electrólisis; instrumentos eléctricos (giroscopio; manómetro; termómetro; batería; bombilla eléctrica; tubos, etc.); relleno de amalgama |
plantas de cloro-álcali; minería; electrónica; odontología; producción de polímeros; industria del papel y la pulpa |
M: Deterioro en múltiples sitios en las células nerviosas A: inflamación pulmonar; dolor de cabeza; deterioro del habla C: Inflamación de las encías; pérdida de apetito; encefalopatía; incluyendo temblor; irritabilidad |
|
calomelano Hg2Cl2 |
Laboratorios |
A: Baja toxicidad aguda efectos tóxicos crónicos, ver arriba |
|
|
Sublimar HgCl2 |
Sistema |
hospitales; clínicas; laboratorios |
M: Degeneración renal aguda tubular y glomerular. Muy tóxico incluso en pequeñas dosis orales, letal hasta 30 mg/kg de peso C: Véase más arriba. |
|
Magnesio |
Fusión (aleación de acero); corte; soldadura en acero; pilas secas |
minería de manganeso; producción de acero y aluminio; industria metalúrgica; producción de baterías; industria química; fábrica de ladrillos |
M: Frecuencia no conocida, posibles cambios en la dopamina y las catecolaminas en los ganglios basales en el centro del cerebro A: Disforia C: Encefalopatía incluyendo parkinsonismo; psicosis; pérdida de apetito; irritabilidad; dolor de cabeza; debilidad |
|
Aluminio |
Metalurgia; molienda; pulido |
Industria del metal |
M: Desconocido C: Posiblemente encefalopatía |
1 M: mecanismo; A: efectos agudos; C: efectos crónicos.
Neuropatía: disfunción de las fibras nerviosas periféricas motoras y sensoriales.
Encefalopatía: disfunción cerebral debida a un deterioro generalizado del cerebro.
Monómeros
Los monómeros constituyen un grupo amplio y heterogéneo de productos químicos reactivos utilizados para la síntesis química y la producción de polímeros, resinas y plásticos. Los monómeros comprenden compuestos aromáticos polihalogenados tales como p-clorobenceno y 1,2,4-triclorobenceno; disolventes orgánicos insaturados como estireno y viniltolueno, acrilamida y compuestos relacionados, fenoles, ɛ-caprolactama y ζ-aminobutirolactama. Algunos de los monómeros neurotóxicos ampliamente utilizados y su efecto sobre el sistema nervioso se enumeran en la Tabla 3. La exposición ocupacional a los monómeros neurotóxicos puede tener lugar en las industrias que fabrican, transportan y utilizan productos químicos y productos plásticos. Durante la manipulación de polímeros que contienen monómeros restantes y durante el moldeado en astilleros y en clínicas dentales, tiene lugar una exposición sustancial a monómeros neurotóxicos. Tras la exposición a estos monómeros, la absorción puede tener lugar durante la inhalación (p. ej., disulfuro de carbono y estireno) o por contacto con la piel (p. ej., acrilamida). Dado que los monómeros son un grupo heterogéneo de productos químicos, es probable que existan varios mecanismos diferentes de toxicidad. Esto se refleja en las diferencias en los síntomas (Tabla 4).
Tabla 4. Monómeros neurotóxicos
|
Compuesto |
Ejemplos de fuente de exposición |
Industrias seleccionadas en riesgo |
Efectos1 |
|
acrilamida |
Empleados expuestos al monómero |
Producción de polímeros; operaciones de tunelización y perforación |
M: Transporte axonal alterado C: polineuropatía; mareo; temblor y ataxia |
|
Acrilonitrilo |
Accidentes en laboratorios e industrias; fumigacion de casas |
Producción de polímeros y caucho; síntesis química |
A: hiperexcitabilidad; salivación; vómitos; cianosis; ataxia; respiración dificultosa |
|
Disulfuro de carbono |
Producción de caucho y rayón viscosa. |
Industrias de caucho y rayón viscosa |
M: Es probable que se deteriore el transporte axonal y la actividad enzimática C: Neuropatía periférica; encefalopatía; dolor de cabeza; vértigo; trastornos gastrointestinales |
|
Estireno |
Producción de plásticos reforzados con vidrio; fabricación y transporte de monómeros; uso de resinas y revestimientos que contienen estireno |
Industria química; producción de fibra de vidrio; industria de polímeros |
M: Desconocido A: depresión del sistema nervioso central; dolor de cabeza C: polineuropatía; encefalopatía; pérdida de la audición |
|
Viniltolueno |
Producción de resina; compuestos insecticidas |
Industria química y de polímeros |
C: polineuropatía; velocidad de conducción nerviosa motora reducida |
1 M: mecanismo; A: efectos agudos; C: efectos crónicos.
Neuropatía: disfunción de las fibras nerviosas periféricas motoras y sensoriales.
Encefalopatía: disfunción cerebral debida a un deterioro generalizado del cerebro.
Ataxia: alteración de la coordinación motora.
Disolventes orgánicos
Disolventes orgánicos es una designación común para un gran grupo de más de 200 compuestos químicos lipofílicos capaces de disolver grasas, aceites, ceras, resinas, caucho, asfalto, filamentos de celulosa y materiales plásticos. Suelen ser fluidos a temperatura ambiente con puntos de ebullición por debajo de 200 a 250°C, y se evaporan fácilmente. Se absorben principalmente a través de los pulmones, pero algunos también pueden penetrar en la piel. Por su lipofilia se distribuyen a órganos ricos en grasa. Por lo tanto, se encuentran altas concentraciones en la grasa corporal, la médula ósea, el hígado y el cerebro, que también pueden actuar como reservorios de solventes. El coeficiente de partición octanol/agua puede indicar si se esperan altas concentraciones en el cerebro. El mecanismo de toxicidad aún no se conoce, pero se han previsto varias posibilidades: bloquear enzimas importantes en la descomposición metabólica de la glucosa y, por lo tanto, reducir la energía disponible para el procesamiento neuronal; reduciendo la formación de energía en las mitocondrias; cambiar las membranas neuronales, lo que conduce a un deterioro de la función de los canales iónicos; Enlentecimiento del flujo axonal. El cloruro de metileno se metaboliza a CO, que bloquea el transporte de oxígeno en la sangre. Grandes grupos de trabajadores en una gran variedad de profesiones están expuestos diariamente o al menos con frecuencia (ver Tabla 5). En algunos países, el consumo de solventes orgánicos ha disminuido en algunas ocupaciones debido a mejoras higiénicas y sustitución (p. ej., pintores de casas, trabajadores de la industria gráfica, trabajadores del metal), mientras que en otras ocupaciones el patrón de exposición ha cambiado pero la cantidad total de solventes orgánicos se ha mantenido sin cambios. Por ejemplo, el tricloroetileno ha sido reemplazado por 1,1,1-tricloroetano y freón. Por lo tanto, los disolventes siguen siendo un problema higiénico importante en muchos lugares de trabajo. Las personas corren un riesgo particular cuando se exponen en habitaciones pequeñas con poca ventilación y con altas temperaturas, lo que aumenta la evaporación. El trabajo físico aumenta la captación pulmonar de disolventes. En varios países (en particular, los países nórdicos), se ha otorgado compensación a los trabajadores que han desarrollado encefalopatía tóxica crónica luego de una exposición prolongada y de bajo nivel a solventes.
Tabla 5. Disolventes orgánicos asociados a neurotoxicidad
|
Química |
Ejemplos de fuente de exposición |
Industrias seleccionadas en riesgo |
Efectos1 |
|
Hidrocarburos clorados: tricloroetileno; 1,1,1-tricloroetano; tetracloroetileno |
desengrasado; galvanoplastia; pintura; impresión; limpieza; anestesia general y ligera |
industria metalúrgica; industria gráfica; industria electrónica; tintorerías; anestesistas |
M: Desconocido A: Síntomas prenarcóticos C: encefalopatía; polineuropatía; afección del trigémino (TRI); pérdida de la audición |
|
Cloruro de metileno |
Extracción, incluida la extracción de cafeína; removedor de pintura |
Industria de alimentos; pintores; industria grafica |
M: Metabolismo ® CO A: Síntomas prenarcóticos; coma C: Encefalopatía |
|
Cloruro de metilo |
fabricacion y reparacion de heladeras |
Producción de refrigeradores; industria del caucho; industria del plastico |
M: Desconocido A: Síntomas prenarcóticos; pérdida de consciencia; muerte C: Encefalopatía |
|
tolueno |
Impresión; limpieza; desengrasado; galvanoplastia; pintura; pintura con pistola |
industria gráfica; industria electrónica |
M: Desconocido A: Síntomas prenarcóticos C: encefalopatía; disfunción cerebelosa; polineuropatía; pérdida de la audición; disturbio visual |
|
xileno |
Impresión; síntesis de anhídrido ftálico; pintura; procedimientos de laboratorio de histología |
industria gráfica; industria del plástico; laboratorios de histología |
M: Desconocido A: Síntomas prenarcóticos C: encefalopatía; disturbio visual; pérdida de la audición |
|
Estireno |
Polimerización; moldura |
Industria del plástico; producción de fibra de vidrio |
M: Desconocido A: Síntomas prenarcóticos C: encefalopatía; polineuropatía; pérdida de la audición |
|
Hexacarbonos: n-hexano; metilbutilcetona (MBK); metiletilcetona (MEK) |
pegado; impresión; revestimiento de plástico; pintura; extracción |
industria del cuero y del calzado; industria gráfica; pintor; laboratorios |
M: Deterioro del transporte axonal A: prenarcótico C: polineuropatía; encefalopatía |
|
Disolventes varios: freón 113 |
Producción y reparación de frigoríficos; Limpieza en seco; desengrasante |
Producción de refrigeradores; industria metalúrgica; industria electrónica; Limpieza en seco |
M: Desconocido A: Síntomas prenarcóticos leves C: Encefalopatía |
|
Éter dietílico; halotano |
Anestésicos generales (enfermeras; médicos) |
hospitales; clínicas |
M: Desconocido A: Síntomas prenarcóticos C: Encefalopatía |
|
Disulfuro de carbono |
Ver monómeros |
Ver monómeros |
Ver monómeros |
|
Mezclas: white spirit y thinner |
Pintura; desengrasado; limpieza; impresión; impregnación; tratamiento de superficies |
industria metalúrgica; industria gráfica; industria de la madera; pintores |
M: Desconocido A: Síntomas prenarcóticos C: Encefalopatía |
1 M: mecanismo; A: efectos agudos; C: efectos crónicos.
Neuropatía: disfunción de las fibras nerviosas periféricas motoras y sensoriales.
Encefalopatía: disfunción cerebral debido a un deterioro generalizado del cerebro
Los pesticidas
Los pesticidas se utiliza como un término genérico para cualquier producto químico diseñado para matar grupos de plantas o animales que son un peligro para la salud humana o pueden causar pérdidas económicas. Incluye insecticidas, fungicidas, rodenticidas, fumigantes y herbicidas. Aproximadamente 5 mil millones de libras de productos pesticidas compuestos por más de 600 ingredientes pesticidas activos se usan anualmente en la agricultura en todo el mundo. Los plaguicidas organofosforados, carbamatos y organoclorados junto con los piretroides, los herbicidas clorofenoxi y los compuestos orgánicos metálicos utilizados como fungicidas tienen propiedades neurotóxicas (Cuadro 6). Entre los muchos químicos diferentes que se usan como rodenticidas, algunos (p. ej., estricnina, fosfuro de zinc y talio) también son neurotóxicos. La exposición ocupacional a los pesticidas neurotóxicos se asocia principalmente con el trabajo agrícola, como el manejo de pesticidas y el trabajo con cultivos tratados, pero los exterminadores, los empleados que fabrican y formulan pesticidas, los trabajadores de carreteras y ferrocarriles, así como los trabajadores de invernaderos, silvicultura y viveros pueden tener un riesgo sustancial de estar expuesto a pesticidas neurotóxicos también. Los niños, que constituyen una proporción significativa de la mano de obra agrícola, son especialmente vulnerables porque su sistema nervioso no está completamente desarrollado. Los efectos agudos de los plaguicidas generalmente están bien descritos y, a menudo, se observan efectos duraderos tras la exposición repetida o la exposición a una sola dosis alta (Tabla 6), pero el efecto de la exposición subclínica repetida es incierto.
Tabla 6. Clases de pesticidas neurotóxicos comunes, exposición, efectos y síntomas asociados
|
Compuesto |
Ejemplos de fuente de exposición |
Industrias seleccionadas en riesgo |
Efectos1 |
|
Compuestos organofosforados: Beomil; Demetón; diclorvos; paratión de etilo; mevinfos; fosfolano; terbufos; malatión |
Manejo; tratamiento de cultivos; trabajar con cultivos tratados; trabajador portuario |
Agricultura; silvicultura; químico; jardinería |
M: Inhibición de la acetilcolinesterasa A: Hiperactividad; parálisis neuromuscular; discapacidad visual; dificultad para respirar; inquietud; debilidad; vómitos; convulsiones |
|
Carbamatos: Aldicarb; carbarilo; carbofurano; Propoxur |
M: Axonopatía por neurotoxicidad retardada2 C: polineuropatía; entumecimiento y hormigueo en los pies; debilidad muscular; alteración sensorial; parálisis |
||
|
Organoclorados: Aldrin; dieldrín; DDT; endrín; heptacloro; lindano; metoxicloro; mirex; toxafeno |
Consultar más arriba |
Consultar más arriba |
A: Excitabilidad; detención; mareo; dolor de cabeza; confusión; pérdida del equilibrio; debilidad; ataxia; temblores; convulsiones; coma C: Encefalopatía |
|
Piretroides |
Consultar más arriba |
Consultar más arriba |
M: Alteración del flujo de iones de sodio a través de la membrana celular nerviosa A: Disparo repetido de la célula nerviosa; temblor; convulsión |
|
2,4-D |
Herbicida |
Agricultura |
C: Polineuropatía |
|
Hidróxido de trietilestaño |
Tratamiento de superficies; manipulación de madera tratada |
Madera y productos de madera |
A: Dolor de cabeza; debilidad; parálisis; alteraciones visuales C: polineuropatía; efectos del SNC |
|
Bromuro de metilo |
Fumigar |
invernaderos; insecticida; fabricación de refrigeradores |
M: Desconocido A: Trastornos visuales y del habla; delirio; convulsión C: Encefalopatía |
1 M: mecanismo; A: efectos agudos; C: efectos crónicos.
Neuropatía: disfunción de las fibras nerviosas periféricas motoras y sensoriales.
Encefalopatía: disfunción cerebral debida a un deterioro generalizado del cerebro.
Ataxia: alteración de la coordinación motora.
2 Principalmente fosfatos o fosfonatos.
Otros productos químicos
Varios productos químicos diferentes que no encajan en los grupos mencionados anteriormente también poseen neurotoxicidad. Algunos de estos se utilizan como pesticidas pero también en diferentes procesos industriales. Algunos tienen efectos neurotóxicos agudos y crónicos bien documentados; otros tienen efectos agudos obvios, pero los efectos crónicos están mal examinados. En la Tabla 7 se enumeran ejemplos de estos productos químicos, sus usos y efectos.
Tabla 7. Otras sustancias químicas asociadas con neurotoxicidad
|
Química |
Ejemplos de fuente de exposición |
Industrias seleccionadas en riesgo |
Efectos1 |
|
Ácido bórico |
Soldadura; flujos; preservación |
Metal; vaso |
A: Delirio; convulsión C: Depresión del SNC. |
|
El disulfiram |
Farmacéutica |
Caucho |
C: Fatiga; neuropatía periférica; somnolencia |
|
Hexaclorofeno |
Jabones antibacterianos |
Química |
C: edema del SNC; daño a los nervios periféricos |
|
Hydrazine |
Agentes reductores |
Químico; Ejército |
A: Excitación; pérdida de apetito; temblor; convulsión |
|
Fenol/Cresol |
Antisépticos |
Plástica; resinas; químico; hospitales; laboratorios |
M: Desnaturaliza proteínas y enzimas. A: Pérdida de reflejos; debilidad; temblor; transpiración; coma C: pérdida de apetito; perturbación mental; zumbido en los oídos |
|
Piridina |
Desnaturalización de etanol |
Químico; textil |
A: depresión del SNC; Depresión mental; fatiga; pérdida de apetito C: Irritabilidad; trastornos del sueño; polineuropatía; visión doble |
|
Plomo tetraetilo |
Aditivo de gasolina |
Químico; transporte |
C: Irritabilidad; debilidad; temblor; dificultades de visión |
|
Arsina |
baterías; insecticida; derritiendo |
Fundición; cristalería; cerámica; fabricación de papel |
M: Deterioro de la función enzimática A: Sensación reducida; paresia; convulsión; coma C: Deterioro motor; ataxia; pérdida del sentido de la vibración; polineuropatía |
|
Litio |
aditivo de aceite; farmacéutico |
Petroquímico |
C.A: pérdida de apetito; zumbido en los oídos; visión borrosa; temblor; ataxia |
|
Selenio |
Derritiendo; producción de rectificadores; vulcanización; aceites de corte; antioxidante |
Electrónico; obras de vidrio; industria metalúrgica; industria del caucho |
A: Delirio; anosmia C: Olor a ajo; polineuropatía; nerviosismo |
|
talio |
Rodenticida |
Vaso; productos de vidrio |
A: pérdida de apetito; cansancio; somnolencia; sabor metálico; entumecimiento; ataxia |
|
Telurio |
Derritiendo; producción de caucho; Catalizador |
Metal; químico; caucho; electrónico |
A: Dolor de cabeza; somnolencia; neuropatía C: Olor a ajo; sabor metálico; parkinsonismo; depresión |
|
Vanadio |
Fusión |
Minería; producción de acero; industria química |
A: pérdida de apetito; zumbido en los oídos; somnolencia, temblor C: Depresión; temblor; ceguera |
1 M: mecanismo; A: efectos agudos; C: efectos crónicos.
Neuropatía: disfunción de las fibras nerviosas periféricas motoras y sensoriales.
Encefalopatía: disfunción cerebral debida a un deterioro generalizado del cerebro.
Ataxia: alteración de la coordinación motora
Manifestaciones de intoxicación aguda y crónica temprana
El conocimiento actual de las manifestaciones a corto y largo plazo de la exposición a sustancias neurotóxicas proviene de estudios experimentales en animales y estudios de cámara humana, estudios epidemiológicos de trabajadores activos y jubilados y/o enfermos, estudios e informes clínicos, así como desastres a gran escala. , como los ocurridos en Bhopal, tras una fuga de isocianato de metilo, y en Minamata, por envenenamiento con metilmercurio.
La exposición a sustancias neurotóxicas puede producir efectos inmediatos (agudos) y/o efectos a largo plazo (crónicos). En ambos casos, los efectos pueden ser reversibles y desaparecer con el tiempo tras la reducción o el cese de la exposición, o resultar en daños permanentes e irreversibles. La gravedad del deterioro agudo y crónico del sistema nervioso depende de la dosis de exposición, que incluye tanto la cantidad como la duración de la exposición. Al igual que el alcohol y las drogas recreativas, muchas sustancias neurotóxicas pueden ser inicialmente excitatorias, produciendo una sensación de bienestar o euforia y/o acelerando las funciones motoras; a medida que la dosis aumenta en cantidad o en tiempo, estas mismas neurotoxinas deprimen el sistema nervioso. De hecho, la narcosis (un estado de estupor o insensibilidad) es inducida por un gran número de sustancias neurotóxicas, que alteran la mente y deprimen el sistema nervioso central.
Intoxicación aguda
Los efectos agudos reflejan la respuesta inmediata a la sustancia química. La gravedad de los síntomas y los trastornos resultantes depende de la cantidad que llegue al sistema nervioso. Con exposiciones leves, los efectos agudos son leves y transitorios y desaparecen cuando cesa la exposición. Dolor de cabeza, cansancio, mareos, dificultad para concentrarse, sensación de embriaguez, euforia, irritabilidad, mareos y reflejos lentos son los tipos de síntomas experimentados durante la exposición a sustancias químicas neurotóxicas. Aunque estos síntomas son reversibles, cuando la exposición se repite día tras día, los síntomas también reaparecen. Además, dado que la sustancia neurotóxica no se elimina inmediatamente del cuerpo, los síntomas pueden persistir después del trabajo. Los síntomas informados en una estación de trabajo en particular son un buen reflejo de la interferencia química con el sistema nervioso y deben considerarse una señal de advertencia de una posible sobreexposición; deben iniciarse medidas preventivas para reducir los niveles de exposición.
Si la exposición es muy alta, como puede ocurrir con derrames, fugas, explosiones y otros accidentes, los síntomas y signos de intoxicación son debilitantes (dolor de cabeza intenso, confusión mental, náuseas, mareos, falta de coordinación, visión borrosa, pérdida del conocimiento); si la exposición es lo suficientemente alta, los efectos pueden ser duraderos y posiblemente provocar coma y la muerte.
Los trastornos agudos relacionados con los pesticidas son una ocurrencia común entre los trabajadores agrícolas en los países productores de alimentos, donde se usan grandes cantidades de sustancias tóxicas como insecticidas, fungicidas, nematicidas y herbicidas. Los organofosforados, carbamatos, organoclorados, piretro, piretrina, paraquat y diquat se encuentran entre las principales categorías de plaguicidas; sin embargo, hay miles de formulaciones de pesticidas que contienen cientos de ingredientes activos diferentes. Algunos pesticidas, como el maneb, contienen manganeso, mientras que otros se disuelven en solventes orgánicos. Además de los síntomas mencionados anteriormente, la intoxicación aguda por organofosforados y carbamatos puede ir acompañada de salivación, incontinencia, convulsiones, espasmos musculares, diarrea, alteraciones visuales, así como dificultades respiratorias y frecuencia cardíaca acelerada; estos son el resultado de un exceso del neurotransmisor acetilcolina, que ocurre cuando estas sustancias atacan una sustancia química llamada colinesterasa. La colinesterasa sanguínea disminuye proporcionalmente al grado de intoxicación aguda por organofosforados o carbamatos.
Con algunas sustancias, como los pesticidas organofosforados y el monóxido de carbono, las exposiciones agudas de alto nivel pueden producir un deterioro retardado de ciertas partes del sistema nervioso. Para los primeros, pueden presentarse entumecimiento y hormigueo, debilidad y desequilibrio unas semanas después de la exposición, mientras que para los segundos puede producirse un deterioro neurológico tardío, con síntomas de confusión mental, ataxia, incoordinación motora y paresia. Los episodios agudos repetidos de niveles elevados de monóxido de carbono se han asociado con parkinsonismo en etapas posteriores de la vida. Es posible que las altas exposiciones a ciertas sustancias químicas neurotóxicas puedan estar asociadas con un mayor riesgo de trastornos neurodegenerativos más adelante en la vida.
Envenenamiento Crónico
El reconocimiento de los peligros de los productos químicos neurotóxicos ha llevado a muchos países a reducir los niveles de exposición permisibles. Sin embargo, para la mayoría de los productos químicos, aún se desconoce el nivel en el que no se producirán efectos adversos durante la exposición a largo plazo. La exposición repetida a niveles bajos o medios de sustancias neurotóxicas durante muchos meses o años puede alterar las funciones del sistema nervioso de manera insidiosa y progresiva. La interferencia continua con los procesos moleculares y celulares hace que las funciones neurofisiológicas y psicológicas sufran alteraciones lentas, que en las primeras etapas pueden pasar desapercibidas, ya que existen grandes reservas en el circuito del sistema nervioso y el daño puede, en las primeras etapas, compensarse con nuevos aprendizajes.
Por tanto, la lesión inicial del sistema nervioso no se acompaña necesariamente de trastornos funcionales y puede ser reversible. Sin embargo, a medida que el daño progresa, los síntomas y signos, a menudo de naturaleza inespecífica, se hacen evidentes y las personas pueden buscar atención médica. Finalmente, el deterioro puede volverse tan severo que se manifieste un claro síndrome clínico, generalmente irreversible.
La figura 1 esquematiza el continuo de deterioro de la salud asociado a la exposición a sustancias neurotóxicas. La progresión de la disfunción neurotóxica depende tanto de la duración como de la concentración de la exposición (dosis), y puede verse influida por otros factores del lugar de trabajo, el estado de salud individual y la susceptibilidad, así como el estilo de vida, en particular el consumo de alcohol y la exposición a sustancias neurotóxicas utilizadas en pasatiempos, como colas aplicadas en el montaje de muebles o construcción de maquetas de plástico, pinturas y decapantes.
Figura 1. Deterioro de la salud en un continuo con dosis crecientes
Se adoptan diferentes estrategias para la identificación de enfermedades relacionadas con neurotoxinas entre trabajadores individuales y para la vigilancia del deterioro temprano del sistema nervioso entre trabajadores activos. El diagnóstico clínico se basa en una constelación de signos y síntomas, junto con el historial médico y de exposición de un individuo; deben descartarse sistemáticamente etiologías distintas de la exposición. Para la vigilancia de la disfunción temprana entre los trabajadores activos, el retrato grupal de la disfunción es importante. Muy a menudo, el patrón de disfunción observado para el grupo será similar al patrón de deterioro clínicamente observado en la enfermedad. Es algo así como sumar alteraciones tempranas y leves para producir una imagen de lo que le está sucediendo al sistema nervioso. El patrón o perfil de la respuesta temprana general proporciona una indicación de la especificidad y el tipo de acción de la sustancia o mezcla neurotóxica particular. En lugares de trabajo con exposición potencial a sustancias neurotóxicas, la vigilancia de la salud de grupos de trabajadores puede resultar especialmente útil para la prevención y actuación en el lugar de trabajo con el fin de evitar el desarrollo de enfermedades más graves (ver Figura 2). Los estudios de lugares de trabajo realizados en todo el mundo, con trabajadores activos expuestos a sustancias neurotóxicas específicas o a mezclas de varios productos químicos, han proporcionado información valiosa sobre las manifestaciones tempranas de disfunción del sistema nervioso en grupos de trabajadores expuestos.
Figura 2. Prevención de la neurotoxicidad en el trabajo.
Primeros síntomas de intoxicación crónica
Los estados de ánimo alterados suelen ser los primeros síntomas de los cambios iniciales en el funcionamiento del sistema nervioso. La irritabilidad, la euforia, los cambios de humor repentinos, el cansancio excesivo, los sentimientos de hostilidad, la ansiedad, la depresión y la tensión se encuentran entre los estados de ánimo más frecuentemente asociados con las exposiciones neurotóxicas. Otros síntomas incluyen problemas de memoria, dificultades de concentración, dolores de cabeza, visión borrosa, sensación de embriaguez, mareos, lentitud, sensación de hormigueo en manos o pies, pérdida de libido, etc. Aunque en las primeras etapas estos síntomas no suelen ser lo suficientemente graves como para interferir con el trabajo, reflejan una disminución del bienestar y afectan la capacidad de disfrutar plenamente de las relaciones familiares y sociales. A menudo, debido a la naturaleza no específica de estos síntomas, los trabajadores, los empleadores y los profesionales de la salud en el trabajo tienden a ignorarlos y buscan causas distintas a la exposición en el lugar de trabajo. De hecho, tales síntomas pueden contribuir o agravar una situación personal ya difícil.
En los lugares de trabajo donde se utilizan sustancias neurotóxicas, los trabajadores, empleadores y personal de seguridad y salud en el trabajo deben estar particularmente atentos a la sintomatología de intoxicación temprana, indicativa de vulnerabilidad del sistema nervioso a la exposición. Se han desarrollado cuestionarios de síntomas para estudios en el lugar de trabajo y vigilancia de lugares de trabajo donde se usan sustancias neurotóxicas. La Tabla 1 contiene un ejemplo de dicho cuestionario.
Tabla 1. Lista de verificación de síntomas crónicos
Síntomas experimentados en el último mes
1. ¿Se ha cansado más fácilmente de lo esperado para el tipo de actividad que realiza?
2. ¿Se ha sentido mareado o mareado?
3. ¿Ha tenido dificultad para concentrarse?
4. ¿Ha estado confundido o desorientado?
5. ¿Ha tenido problemas para recordar cosas?
6. ¿Tus familiares han notado que tienes problemas para recordar cosas?
7. ¿Ha tenido que tomar notas para recordar cosas?
8. ¿Le ha resultado difícil entender el significado de los periódicos?
9. ¿Se ha sentido irritable?
10. ¿Se ha sentido deprimido?
11. ¿Ha tenido palpitaciones del corazón incluso cuando no se está esforzando?
12. ¿Ha tenido una convulsión?
13. ¿Ha estado durmiendo con más frecuencia de lo habitual para usted?
14. ¿Ha tenido dificultad para conciliar el sueño?
15. ¿Le ha molestado la falta de coordinación o la pérdida del equilibrio?
16. ¿Ha tenido alguna pérdida de fuerza muscular en las piernas o los pies?
17. ¿Ha tenido alguna pérdida de fuerza muscular en sus brazos o manos?
18. ¿Ha tenido dificultad para mover los dedos o agarrar cosas?
19. ¿Ha tenido entumecimiento de las manos y hormigueo en los dedos durante más de un día?
20. ¿Ha tenido entumecimiento en las manos y hormigueo en los dedos de los pies durante más de un día?
21. ¿Ha tenido dolores de cabeza al menos una vez a la semana?
22. ¿Ha tenido dificultades para conducir a casa desde el trabajo porque se sintió mareado o cansado?
23. ¿Se ha sentido “colocado” por los productos químicos utilizados en el trabajo?
24. ¿Ha tenido menor tolerancia al alcohol (tarda menos en emborracharse)?
Fuente: Tomado de Johnson 1987.
Cambios motores, sensoriales y cognitivos tempranos en el envenenamiento crónico
Con el aumento de la exposición, se pueden observar cambios en las funciones motoras, sensoriales y cognitivas en trabajadores expuestos a sustancias neurotóxicas, que no presentan evidencia clínica de anormalidad. Dado que el sistema nervioso es complejo y ciertas áreas son vulnerables a sustancias químicas específicas, mientras que otras son sensibles a la acción de una gran cantidad de agentes tóxicos, una amplia gama de funciones del sistema nervioso pueden verse afectadas por un solo agente tóxico o una mezcla de agentes tóxicos. neurotoxinas. Tiempo de reacción, coordinación mano-ojo, memoria a corto plazo, memoria visual y auditiva, atención y vigilancia, destreza manual, vocabulario, cambio de atención, fuerza de agarre, velocidad motora, firmeza de la mano, estado de ánimo, visión del color, percepción vibrotáctil, audición y olfato se encuentran entre las muchas funciones que se ha demostrado que son alteradas por diferentes sustancias neurotóxicas.
Se ha proporcionado información importante sobre el tipo de déficits tempranos que resultan de la exposición al comparar el desempeño entre trabajadores expuestos y no expuestos y con respecto al grado de exposición. Anger (1990) brinda una excelente revisión de la investigación neuroconductual en el lugar de trabajo hasta 1989. La Tabla 2, adaptada de este artículo, brinda un ejemplo del tipo de déficit neurofuncional que se ha observado consistentemente en grupos de trabajadores activos expuestos a algunos de los más sustancias neurotóxicas comunes.
Tabla 2. Efectos neurofuncionales consistentes de la exposición en el lugar de trabajo a algunas de las principales sustancias neurotóxicas
|
Disolventes orgánicos mixtos |
disulfuro de carbono |
Estireno |
Organofos- |
Lidera |
Mercurio |
|
|
Acquisition |
+ |
|
|
|
+ |
|
|
Afectar |
+ |
|
+ |
|
+ |
|
|
Categorización |
+ |
|
|
|
|
|
|
Codificación |
+ |
+ |
|
|
+ |
+ |
|
visión de color |
+ |
|
+ |
|
|
|
|
Cambio de concepto |
+ |
|
|
|
|
|
|
Distracción |
|
|
|
|
+ |
|
|
Intelligence |
+ |
+ |
|
+ |
+ |
+ |
|
Salud Cerebral |
+ |
+ |
+ |
+ |
+ |
+ |
|
Coordinación motriz |
+ |
+ |
+ |
|
+ |
+ |
|
La velocidad del motor |
+ |
+ |
+ |
|
+ |
+ |
|
Sensibilidad al contraste visual cercano |
+ |
|
|
|
|
|
|
Umbral de percepción del olor |
+ |
|
|
|
|
|
|
Identificación de olores |
+ |
|
|
|
+ |
|
|
Personalidad |
+ |
+ |
|
|
|
+ |
|
Relaciones espaciales |
+ |
+ |
|
|
+ |
|
|
Umbral vibrotáctil |
+ |
|
|
+ |
|
+ |
|
Vigilancia |
+ |
+ |
|
|
+ |
|
|
Campo visual |
|
|
|
|
+ |
+ |
|
Vocabulario |
|
|
|
|
+ |
|
Fuente: Adaptado de Anger 1990.
Aunque en esta etapa en el continuo del bienestar a la enfermedad, la pérdida no está en el rango clínicamente anormal, puede haber consecuencias relacionadas con la salud asociadas con tales cambios. Por ejemplo, la disminución de la vigilancia y la reducción de los reflejos pueden poner a los trabajadores en mayor peligro de sufrir accidentes. El olfato se utiliza para identificar fugas y saturación de la máscara (apertura del cartucho), y la pérdida aguda o crónica del olfato hace que uno sea menos apto para identificar una situación potencialmente peligrosa. Los cambios de humor pueden interferir con las relaciones interpersonales en el trabajo, socialmente y en el hogar. Estas etapas iniciales de deterioro del sistema nervioso, que se pueden observar examinando grupos de trabajadores expuestos y comparándolos con trabajadores no expuestos o con respecto a su grado de exposición, reflejan una disminución del bienestar y pueden predecir el riesgo de enfermedades neurológicas más graves. problemas en el futuro.
Salud mental en intoxicaciones crónicas
Los trastornos neuropsiquiátricos se han atribuido durante mucho tiempo a la exposición a sustancias neurotóxicas. Las descripciones clínicas van desde trastornos afectivos, incluidas la ansiedad y la depresión, hasta manifestaciones de comportamiento psicótico y alucinaciones. La exposición aguda de alto nivel a muchos metales pesados, solventes orgánicos y pesticidas puede producir delirio. Se ha descrito la “locura por manganeso” en personas expuestas a largo plazo al manganeso, y el conocido síndrome del “sombrerero loco” resulta de la intoxicación por mercurio. La encefalopatía tóxica tipo 2a, caracterizada por un cambio sostenido en la personalidad que implica fatiga, labilidad emocional, control de los impulsos y estado de ánimo y motivación general, se ha asociado con la exposición a disolventes orgánicos. Cada vez hay más evidencia de estudios clínicos y de población de que los trastornos de personalidad persisten en el tiempo, mucho después de que cesa la exposición, aunque otros tipos de deterioro pueden mejorar.
En el continuo del bienestar a la enfermedad, los cambios de humor, la irritabilidad y el cansancio excesivo suelen ser los primeros indicios de sobreexposición a sustancias neurotóxicas. Aunque los síntomas neuropsiquiátricos se examinan de forma rutinaria en los estudios en el lugar de trabajo, rara vez se presentan como un problema de salud mental con posibles consecuencias en el bienestar mental y social. Por ejemplo, los cambios en el estado de salud mental afectan el comportamiento de uno, contribuyendo a relaciones interpersonales difíciles y desacuerdos en el hogar; estos a su vez pueden agravar el estado mental. En lugares de trabajo con programas de ayuda para empleados, diseñados para ayudar a los empleados con problemas personales, la ignorancia de los posibles efectos en la salud mental de la exposición a sustancias neurotóxicas puede conducir a que el tratamiento se ocupe de los efectos en lugar de la causa. Es interesante notar que entre los muchos brotes informados de "histeria colectiva" o enfermedad psicógena, las industrias con exposición a sustancias neurotóxicas están sobrerrepresentadas. Es posible que estas sustancias, que en su mayor parte no se midieron, contribuyeron a los síntomas informados.
Las manifestaciones de salud mental de la exposición a neurotoxinas pueden ser similares a las que son causadas por factores estresantes psicosociales asociados con una mala organización del trabajo, así como reacciones psicológicas a accidentes, sucesos muy estresantes e intoxicaciones graves, denominado trastorno de estrés postraumático (como se analiza en otra parte de este artículo). Enciclopedia). Una buena comprensión de la relación entre los problemas de salud mental y las condiciones de trabajo es importante para iniciar acciones preventivas y curativas adecuadas.
Consideraciones generales en la evaluación de la disfunción neurotóxica temprana
Al evaluar la disfunción temprana del sistema nervioso entre los trabajadores activos, se deben tener en cuenta una serie de factores. En primer lugar, muchas de las funciones neuropsicológicas y neurofisiológicas que se examinan disminuyen con la edad; algunos están influenciados por la cultura o el nivel educativo. Estos factores deben tenerse en cuenta al considerar la relación entre la exposición y las alteraciones del sistema nervioso. Esto se puede hacer comparando grupos con un estatus sociodemográfico similar o usando métodos estadísticos de ajuste. Sin embargo, hay ciertas trampas que deben evitarse. Por ejemplo, los trabajadores mayores pueden tener un historial laboral más prolongado y se ha sugerido que algunas sustancias neurotóxicas pueden acelerar el envejecimiento. La segregación laboral puede confinar a los trabajadores, las mujeres y las minorías con poca educación en trabajos con mayor exposición. En segundo lugar, el consumo de alcohol, tabaco y drogas, que contienen sustancias neurotóxicas, también pueden afectar los síntomas y el rendimiento. Una buena comprensión del lugar de trabajo es importante para desentrañar los diferentes factores que contribuyen a la disfunción del sistema nervioso y la implementación de medidas preventivas.
Prevención de la neurotoxicidad en el trabajo
Un trabajador que no esté expuesto a una sustancia neurotóxica nunca desarrollará efectos neurotóxicos adversos para la salud a causa de esa sustancia. La exposición cero conduce a una protección total contra los efectos neurotóxicos para la salud. Esta es la esencia de todas las medidas de prevención primaria.
Pruebas de toxicidad
Los nuevos compuestos químicos introducidos en el lugar de trabajo y en los entornos laborales ya deberían haber sido probados para determinar su neurotoxicidad. Si no se realizan las pruebas de toxicidad previas a la comercialización, se puede producir el contacto de los trabajadores y efectos potencialmente adversos para la salud. La introducción de metil n-butilcetona en un lugar de trabajo en los Estados Unidos es un ejemplo clásico de los posibles peligros de la introducción de neurotóxicos no probados en el lugar de trabajo (Spencer y Schaumburg 1980).
Controles de ingeniería
Los controles de ingeniería (p. ej., sistemas de ventilación, instalaciones de producción cerradas) son los mejores medios para mantener la exposición de los trabajadores por debajo de los límites de exposición permisibles. Los procesos químicos cerrados que evitan que todos los tóxicos se liberen en el ambiente del lugar de trabajo son los ideales. Si esto no es posible, los sistemas de ventilación cerrados que expulsan los vapores del aire ambiental y están diseñados para alejar el aire contaminado de los trabajadores son útiles cuando están bien diseñados, mantenidos adecuadamente y operados correctamente.
Equipo de Protección Personal
En situaciones donde los controles de ingeniería no estén disponibles para reducir el contacto de los trabajadores con neurotóxicos, se debe proporcionar equipo de protección personal. Debido a que los neurotóxicos en el lugar de trabajo son muchos y las rutas de exposición difieren según el lugar de trabajo y las condiciones de trabajo, el tipo de equipo de protección personal debe seleccionarse cuidadosamente para la situación en cuestión. Por ejemplo, el neurotóxico plomo puede ejercer su toxicidad cuando se respira polvo cargado de plomo y cuando se ingieren partículas de plomo en los alimentos o el agua. Por lo tanto, el equipo de protección personal debe proteger contra ambas vías de exposición. Esto significaría equipo de protección respiratoria y adopción de medidas de higiene personal para evitar el consumo de alimentos o bebidas contaminados con plomo. Para muchos neurotóxicos (como los solventes industriales), la absorción de la sustancia a través de la piel intacta es una ruta principal de exposición. Por lo tanto, se deben proporcionar guantes impermeables, delantales y otro equipo apropiado para evitar la absorción por la piel. Esto se sumaría a los controles de ingeniería o al equipo de protección respiratoria personal. Se debe realizar una planificación considerable para adaptar el equipo de protección personal al trabajo específico que se está realizando.
Controles administrativos
Los controles administrativos consisten en esfuerzos gerenciales para reducir los riesgos en el lugar de trabajo a través de la planificación, capacitación, rotación de empleados en los sitios de trabajo, cambios en los procesos de producción y sustitución de productos (Urie 1992), así como el cumplimiento estricto de todas las reglamentaciones existentes.
Derecho a saber de los trabajadores
Si bien el empleador tiene la responsabilidad de proporcionar un lugar de trabajo o experiencia laboral que no perjudique la salud de los trabajadores, los trabajadores tienen la responsabilidad de seguir las reglas del lugar de trabajo destinadas a protegerlos. Los trabajadores deben estar en condiciones de saber qué acciones tomar para protegerse. Esto significa que los trabajadores tienen derecho a saber sobre la neurotoxicidad de las sustancias con las que entran en contacto y qué medidas de protección pueden tomar.
Vigilancia de la Salud del Trabajador
Cuando las condiciones lo permitan, los trabajadores deberían someterse a exámenes médicos periódicos. Una evaluación periódica por médicos del trabajo u otros médicos especialistas constituye una vigilancia de la salud del trabajador. Para los trabajadores que se sabe que trabajan con o cerca de neurotóxicos, los médicos deben conocer los efectos de la exposición. Por ejemplo, la exposición de bajo nivel a muchos solventes orgánicos producirá síntomas de fatiga, trastornos del sueño, dolores de cabeza y alteraciones de la memoria. Para dosis altas de plomo, la caída de la muñeca y el deterioro de los nervios periféricos serían signos de intoxicación por plomo. Cualquier signo y síntoma de intoxicación por neurotóxicos debe dar como resultado la reasignación del trabajador a un área libre del neurotóxico y los esfuerzos para reducir los niveles del neurotóxico en el lugar de trabajo.
Síndromes clínicos asociados con neurotoxicidad
Los síndromes neurotóxicos, provocados por sustancias que afectan negativamente al tejido nervioso, constituyen uno de los diez principales trastornos ocupacionales en los Estados Unidos. Los efectos neurotóxicos constituyen la base para establecer criterios de límites de exposición para aproximadamente el 40% de los agentes considerados peligrosos por el Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH) de los Estados Unidos.
Una neurotoxina es cualquier sustancia capaz de interferir con la función normal del tejido nervioso, causando un daño celular irreversible y/o dando como resultado la muerte celular. Dependiendo de sus propiedades particulares, una neurotoxina dada atacará sitios seleccionados o elementos celulares específicos del sistema nervioso. Esos compuestos, que son no polares, tienen una mayor solubilidad en lípidos y, por lo tanto, tienen un mayor acceso al tejido nervioso que los productos químicos altamente polares y menos solubles en lípidos. El tipo y tamaño de las células y los diversos sistemas de neurotransmisores afectados en diferentes regiones del cerebro, los mecanismos de desintoxicación protectores innatos, así como la integridad de las membranas celulares y los orgánulos intracelulares influyen en las respuestas neurotóxicas.
Las neuronas (la unidad celular funcional del sistema nervioso) tienen una alta tasa metabólica y corren el mayor riesgo de daño neurotóxico, seguidas por los oligodendrocitos, los astrocitos, la microglía y las células del endotelio capilar. Los cambios en la estructura de la membrana celular deterioran la excitabilidad e impiden la transmisión de impulsos. Los efectos tóxicos alteran la forma de las proteínas, el contenido de fluidos y la capacidad de intercambio iónico de las membranas, lo que provoca la inflamación de las neuronas, los astrocitos y el daño de las delicadas células que recubren los capilares sanguíneos. La alteración de los mecanismos de los neurotransmisores bloquea el acceso a los receptores postsinápticos, produce falsos efectos de los neurotransmisores y altera la síntesis, el almacenamiento, la liberación, la recaptación o la inactivación enzimática de los neurotransmisores naturales. Así, las manifestaciones clínicas de la neurotoxicidad están determinadas por una serie de factores diferentes: las características físicas de la sustancia neurotóxica, la dosis de exposición a la misma, la vulnerabilidad del blanco celular, la capacidad del organismo para metabolizar y excretar la toxina, y por la capacidades reparadoras de las estructuras y mecanismos afectados. La Tabla 1 enumera varias exposiciones químicas y sus síndromes neurotóxicos.
Tabla 1. Exposiciones químicas y síndromes neurotóxicos asociados
|
Neurotoxina |
Fuentes de exposición |
Diagnostico clinico |
Locus de la patología1 |
|
Metales |
|||
|
Arsénico |
plaguicidas; pigmentos; pintura antiincrustante; industria de galvanoplastia; fruto de mar; fundiciones; semiconductores |
Aguda: encefalopatía Crónico: neuropatía periférica |
Desconocido (a) axón (c) |
|
Lidera |
Soldar; perdigones de plomo; whisky ilícito; insecticidas; taller de carrocería; fabricación de baterías de almacenamiento; fundiciones, fundiciones; pintura a base de plomo; tuberías de plomo |
Aguda: encefalopatía Crónico: encefalopatía y neuropatía periférica |
vasos sanguíneos (a) axón (c) |
|
Magnesio |
Hierro, industria del acero; operaciones de soldadura; operaciones de acabado de metales; fertilizantes; fabricantes de fuegos artificiales, fósforos; fabricantes de pilas secas |
Aguda: encefalopatía Crónico: parkinsonismo |
Desconocido (a) Neuronas de los ganglios basales (c) |
|
Mercurio |
Instrumentos cientificos; equipo eléctrico; amalgamas; industria de galvanoplastia; fotografía; fabricación de fieltro |
Aguda: cefalea, náuseas, aparición de temblor Crónico: ataxia, neuropatía periférica, encefalopatía |
Desconocido (a) axón (c) Desconocido |
|
Estaño |
industria conservera; soldar; componentes electrónicos; plásticos de polivinilo; fungicidas |
Agudo: defectos de memoria, convulsiones, desorientación Crónico: encefalomielopatía |
Neuronas del sistema límbico (a y c) mielina (c) |
|
disolventes |
|||
|
Disulfuro de carbono |
Fabricantes de rayón viscosa; conservantes; textiles; adhesivo de goma; barnices; industria de la galvanoplastia |
Aguda: encefalopatía Crónico: neuropatía periférica, parkinsonismo |
Desconocido (a) axón (c) Desconocido |
|
n-hexano, metilbutilcetona |
pinturas; lacas; barnices; compuestos para limpiar metales; tintas de secado rápido; removedores de pintura; pegamentos, adhesivos |
Agudo: narcosis Crónica: neuropatía periférica, desconocida (a) Axón (c), |
|
|
Percloroetileno |
removedores de pintura; desengrasantes; agentes de extracción; industria de limpieza en seco; industria textil |
Agudo: narcosis Crónico: neuropatía periférica, encefalopatía |
Desconocido (a) axón (c) Desconocido |
|
tolueno |
disolventes de caucho; agentes de limpieza; colas; fabricantes de benceno; gasolina, combustibles de aviación; pinturas, diluyentes de pintura; lacas |
Agudo: narcosis Crónico: ataxia, encefalopatía |
Desconocido (a) Cerebelo (c) Desconocido |
|
Tricloroetileno |
desengrasantes; industria de la pintura; barnices; quitamanchas; proceso de descafeinado; industria de limpieza en seco; disolventes de caucho |
Agudo: narcosis Crónico: encefalopatía, neuropatía craneal |
Desconocido (a) Desconocido axón (c) |
|
Insecticidas |
|||
|
Organofosforados |
Fabricación y aplicación de la industria agrícola. |
Aguda: intoxicación colinérgica Crónico: ataxia, parálisis, neuropatía periférica |
Acetilcolinesterasa (a) Largos tramos de médula espinal (c) axón (c) |
|
Carbamatos |
Fabricación y aplicación de polvos antipulgas para la industria agrícola. |
Aguda: intoxicación colinérgica Crónica: temblor, neuropatía periférica |
Acetilcolinesterasa (a) Sistema dopaminérgico (c) |
1 (a), agudo; (c), crónico.
Fuente: Modificado de Feldman 1990, con permiso del editor.
Establecer un diagnóstico de un síndrome neurotóxico y diferenciarlo de enfermedades neurológicas de etiología no neurotóxica requiere una comprensión de la patogenia de los síntomas neurológicos y los signos y síntomas observados; una conciencia de que ciertas sustancias son capaces de afectar el tejido nervioso; documentación de la exposición; evidencia de presencia de neurotoxina y/o metabolitos en tejidos de un individuo afectado; y la delimitación cuidadosa de una relación de tiempo entre la exposición y la aparición de los síntomas con la subsiguiente disminución de los síntomas una vez finalizada la exposición.
La prueba de que una sustancia en particular ha alcanzado un nivel de dosis tóxica suele faltar después de que aparecen los síntomas. A menos que se realice una vigilancia ambiental continua, es necesario un alto índice de sospecha para reconocer los casos de lesión neurotoxicológica. Identificar síntomas atribuibles al sistema nervioso central y/o periférico puede ayudar al clínico a centrarse en ciertas sustancias, que tienen una mayor predilección por una u otra parte del sistema nervioso, como posibles culpables. Convulsiones, debilidad, temblor/espasmos, anorexia (pérdida de peso), alteración del equilibrio, depresión del sistema nervioso central, narcosis (estado de estupor o inconsciencia), alteración visual, alteración del sueño, ataxia (incapacidad para coordinar los movimientos voluntarios de los músculos), fatiga y los trastornos táctiles son síntomas comúnmente informados después de la exposición a ciertos químicos. Las constelaciones de síntomas forman síndromes asociados con la exposición a neurotóxicos.
Síndromes de comportamiento
En algunos trabajadores se han descrito trastornos con características predominantemente conductuales que van desde la psicosis aguda, la depresión y la apatía crónica. Es fundamental diferenciar el deterioro de la memoria asociado a otras enfermedades neurológicas, como la enfermedad de Alzheimer, la arterioesclerosis o la presencia de un tumor cerebral, de los déficits cognitivos asociados a la exposición a tóxicos de disolventes orgánicos, metales o insecticidas. Los trastornos transitorios de la conciencia o las crisis epilépticas con o sin afectación motora asociada deben identificarse como un diagnóstico primario independiente de los trastornos de la conciencia de apariencia similar relacionados con los efectos neurotóxicos. Los síndromes tóxicos subjetivos y conductuales como dolor de cabeza, vértigo, fatiga y cambio de personalidad se manifiestan como encefalopatía leve con embriaguez y pueden indicar la presencia de exposición a monóxido de carbono, dióxido de carbono, plomo, zinc, nitratos o solventes orgánicos mixtos. Las pruebas neuropsicológicas estandarizadas son necesarias para documentar elementos de deterioro cognitivo en pacientes con sospecha de encefalopatía tóxica, y estos deben diferenciarse de los síndromes demenciales causados por otras patologías. Las pruebas específicas utilizadas en las baterías de pruebas diagnósticas deben incluir una amplia muestra de pruebas de función cognitiva que generarán predicciones sobre el funcionamiento y la vida diaria del paciente, así como pruebas que hayan demostrado previamente ser sensibles a los efectos de neurotoxinas conocidas. Estas baterías estandarizadas deben incluir pruebas que hayan sido validadas en pacientes con tipos específicos de daño cerebral y déficits estructurales, para separar claramente estas condiciones de los efectos neurotóxicos. Además, las pruebas deben incluir medidas de control interno para detectar la influencia de la motivación, la hipocondría, la depresión y las dificultades de aprendizaje, y deben contener un lenguaje que tenga en cuenta los efectos culturales y educativos.
Existe un continuo de deterioro del sistema nervioso central leve a grave que experimentan los pacientes expuestos a sustancias tóxicas:
- Síndrome afectivo orgánico (Efecto Tipo I), en el que predominan los trastornos leves del estado de ánimo como queja principal del paciente, con características más consistentes con las de los trastornos afectivos orgánicos de tipo depresivo. Este síndrome parece ser reversible después del cese de la exposición al agente agresor.
- Encefalopatía tóxica crónica leve, en el que, además de los trastornos del estado de ánimo, es más prominente el deterioro del sistema nervioso central. Los pacientes tienen evidencia de alteración de la memoria y la función psicomotora que puede confirmarse mediante pruebas neuropsicológicas. Además, se pueden observar características de discapacidad visoespacial y formación de conceptos abstractos. Las actividades de la vida diaria y el rendimiento laboral se ven afectados.
- Cambio sostenido de personalidad o estado de ánimo (Efecto Tipo IIA) or deterioro de la función intelectual (Tipo II) se puede ver En la encefalopatía crónica leve por sustancias tóxicas, el curso es insidioso. Las características pueden persistir después del cese de la exposición y desaparecer gradualmente, mientras que en algunos individuos se puede observar un deterioro funcional persistente. Si la exposición continúa, la encefalopatía puede progresar a una etapa más grave.
- In Encefalopatía tóxica crónica grave (Efecto de tipo III) se notan las demencias con la agravación global de la memoria y otros problemas cognitivos. Los efectos clínicos de la encefalopatía tóxica no son específicos de un agente determinado. La encefalopatía crónica asociada a tolueno, plomo y arsénico no es diferente de la de otras etiologías tóxicas. Sin embargo, la presencia de otros hallazgos asociados (trastornos visuales con alcohol metílico) puede ayudar a diferenciar los síndromes de acuerdo con etiologías químicas particulares.
Los trabajadores expuestos a disolventes durante largos períodos de tiempo pueden presentar alteraciones permanentes del funcionamiento del sistema nervioso central. Dado que se ha informado un exceso de síntomas subjetivos, que incluyen dolor de cabeza, fatiga, problemas de memoria, pérdida de apetito y dolores de pecho difusos, a menudo es difícil confirmar este efecto en cualquier caso individual. Un estudio epidemiológico que comparó a pintores de casas expuestos a solventes con trabajadores industriales no expuestos mostró, por ejemplo, que los pintores tenían puntajes promedio significativamente más bajos en las pruebas psicológicas que miden la capacidad intelectual y la coordinación psicomotora que los sujetos de referencia. Los pintores también tuvieron un desempeño significativamente más bajo de lo esperado en las pruebas de memoria y tiempo de reacción. También fueron evidentes las diferencias entre los trabajadores expuestos durante varios años al combustible para aviones y los trabajadores no expuestos, en pruebas que requerían mucha atención y alta velocidad motora sensorial. También se han informado alteraciones en el rendimiento psicológico y cambios de personalidad entre los pintores de automóviles. Estos incluían memoria visual y verbal, reducción de la reactividad emocional y bajo rendimiento en las pruebas de inteligencia verbal.
Más recientemente, un controvertido síndrome neurotóxico, sensibilidad química múltiple, ha sido descrito. Dichos pacientes desarrollan una variedad de características que involucran múltiples sistemas de órganos cuando están expuestos incluso a niveles bajos de varias sustancias químicas que se encuentran en el lugar de trabajo y el medio ambiente. Los trastornos del estado de ánimo se caracterizan por depresión, fatiga, irritabilidad y falta de concentración. Estos síntomas reaparecen con la exposición a estímulos predecibles, provocados por sustancias químicas de diversas clases estructurales y toxicológicas, ya niveles mucho más bajos que los que provocan respuestas adversas en la población general. Muchos de los síntomas de la sensibilidad química múltiple son compartidos por personas que muestran solo una forma leve de alteración del estado de ánimo, dolor de cabeza, fatiga, irritabilidad y olvido cuando están en un edificio con mala ventilación y con la liberación de gases de sustancias volátiles de materiales de construcción sintéticos. y alfombras. Los síntomas desaparecen cuando salen de estos ambientes.
Alteraciones de la conciencia, convulsiones y coma.
Cuando el cerebro se ve privado de oxígeno, por ejemplo, en presencia de monóxido de carbono, dióxido de carbono, metano o agentes que bloquean la respiración de los tejidos, como el ácido cianhídrico, o aquellos que causan una impregnación masiva del nervio, como ciertos solventes orgánicos, las alteraciones de la conciencia puede resultar. La pérdida del conocimiento puede estar precedida por convulsiones en trabajadores expuestos a sustancias anticolinesterásicas como los insecticidas organofosforados. Las convulsiones también pueden ocurrir con la encefalopatía por plomo asociada con la inflamación del cerebro. Las manifestaciones de toxicidad aguda posteriores al envenenamiento por organofosforados tienen manifestaciones en el sistema nervioso autónomo que preceden a la aparición de mareos, dolor de cabeza, visión borrosa, miosis, dolor torácico, aumento de las secreciones bronquiales y convulsiones. Estos efectos parasimpáticos se explican por la acción inhibidora de estas sustancias tóxicas sobre la actividad de la colinesterasa.
Trastornos del movimiento
Se han observado lentitud de movimiento, aumento del tono muscular y anomalías posturales en trabajadores expuestos a manganeso, monóxido de carbono, disulfuro de carbono y la toxicidad de un subproducto de meperidina, 1-metil-4-fenil-1,2,3,6 -tetrahidropiridina (MPTP). A veces, los individuos pueden parecer tener la enfermedad de Parkinson. Parkinsonismo secundario a exposición a sustancias tóxicas tiene características de otros trastornos nerviosos como corea y atetosis. En estos casos no se observa el típico temblor de "pastillas rodantes" y, por lo general, los casos no responden bien al fármaco levodopa. La discinesia (deterioro del poder del movimiento voluntario) puede ser un síntoma común del envenenamiento por bromometano. Pueden observarse movimientos espasmódicos de los dedos, la cara, los músculos peribucales y el cuello, así como espasmos en las extremidades. El temblor es común después del envenenamiento por mercurio. Se observa un temblor más obvio asociado con ataxia (falta de coordinación de la acción muscular) en individuos después de la inhalación de tolueno.
opsoclono Es un movimiento ocular anormal que es espasmódico en todas las direcciones. Esto se observa a menudo en la encefalitis del tronco encefálico, pero también puede ser una característica posterior a la exposición a la clordecona. La anormalidad consiste en ráfagas irregulares de sacudidas simultáneas repentinas, involuntarias y rápidas de ambos ojos de manera conjugada, posiblemente multidireccional en individuos gravemente afectados.
Dolor de cabeza
Las quejas comunes de dolor de cabeza después de la exposición a varios vapores metálicos como el zinc y otros vapores de solventes pueden deberse a la vasodilatación (ensanchamiento de los vasos sanguíneos), así como al edema cerebral (hinchazón). La experiencia del dolor es común a estas condiciones, así como a las condiciones de monóxido de carbono, hipoxia (bajo nivel de oxígeno) o dióxido de carbono. Se cree que el “síndrome del edificio enfermo” causa dolores de cabeza debido al exceso de dióxido de carbono presente en un área mal ventilada.
La neuropatía periférica
Las fibras nerviosas periféricas que cumplen funciones motoras comienzan en las neuronas motoras en el asta ventral de la médula espinal. Los axones motores se extienden periféricamente a los músculos que inervan. Una fibra nerviosa sensorial tiene su cuerpo celular nervioso en el ganglio de la raíz dorsal o en la sustancia gris dorsal de la médula espinal. Habiendo recibido información de la periferia detectada en los receptores distales, los impulsos nerviosos se conducen centralmente a los cuerpos de las células nerviosas donde se conectan con las vías de la médula espinal que transmiten información al tronco encefálico y los hemisferios cerebrales. Algunas fibras sensoriales tienen conexiones inmediatas con fibras motoras dentro de la médula espinal, proporcionando una base para la actividad refleja y respuestas motoras rápidas a sensaciones nocivas. Estas relaciones sensoriomotoras existen en todas las partes del cuerpo; los nervios craneales son los equivalentes de los nervios periféricos que surgen en las neuronas del tronco encefálico, en lugar de las de la médula espinal. Las fibras nerviosas sensoriales y motoras viajan juntas en haces y se conocen como nervios periféricos.
Los efectos tóxicos de las fibras nerviosas periféricas se pueden dividir en los que afectan principalmente a los axones (axonopatías), los que están implicados en la pérdida sensoriomotora distal y los que afectan principalmente a la vaina de mielina y las células de Schwann. Las axonopatías son evidentes en etapas tempranas en las extremidades inferiores, donde los axones son más largos y están más alejados del cuerpo de la célula nerviosa. La desmielinización aleatoria ocurre en segmentos entre los nódulos de Ranvier. Si ocurre suficiente daño axonal, se produce una desmielinización secundaria; mientras se conserven los axones, puede ocurrir la regeneración de las células de Schwann y la remielinización. Un patrón que se observa con frecuencia en las neuropatías tóxicas es la axonopatía distal con desmielinización segmentaria secundaria. La pérdida de mielina reduce la velocidad de conducción de los impulsos nerviosos. Por lo tanto, el inicio gradual de hormigueo intermitente y entumecimiento que progresa a falta de sensibilidad y sensaciones desagradables, debilidad muscular y atrofia resulta del daño a las fibras motoras y sensoriales. Los reflejos tendinosos reducidos o ausentes y los patrones anatómicamente consistentes de pérdida sensorial, que involucran las extremidades inferiores más que las superiores, son características de la neuropatía periférica.
Se pueden notar debilidades motoras en las extremidades distales y progresar a una marcha inestable e incapacidad para agarrar objetos. Las porciones distales de las extremidades están más afectadas, pero los casos graves también pueden producir debilidad o atrofia de los músculos proximales. Los grupos de músculos extensores están involucrados antes que los flexores. Los síntomas a veces pueden progresar durante algunas semanas, incluso después de la eliminación de la exposición. El deterioro de la función nerviosa puede persistir durante varias semanas después de la eliminación de la exposición.
Según el tipo y la gravedad de la neuropatía, es útil un examen electrofisiológico de los nervios periféricos para documentar el deterioro de la función. Se puede observar una disminución de la velocidad de conducción, amplitudes reducidas de los potenciales de acción sensoriales o motores, o latencias prolongadas. El enlentecimiento de las velocidades de conducción motora o sensorial generalmente se asocia con la desmielinización de las fibras nerviosas. La preservación de los valores normales de velocidad de conducción en presencia de atrofia muscular sugiere neuropatía axonal. Se producen excepciones cuando hay una pérdida progresiva de fibras nerviosas motoras y sensoriales en la neuropatía axonal que afecta a la velocidad de conducción máxima como resultado de la caída de las fibras nerviosas de mayor diámetro y conducción más rápida. Las fibras regeneradoras ocurren en etapas tempranas de recuperación en las axonopatías, en las que la conducción se enlentece, especialmente en los segmentos distales. El estudio electrofisiológico de pacientes con neuropatías tóxicas debe incluir mediciones de velocidad de conducción motora y sensorial en las extremidades superiores e inferiores. Se debe prestar especial atención a las características de conducción principalmente sensoriales del nervio sural en la pierna. Esto es de gran valor cuando se utiliza el nervio sural para la biopsia, proporcionando una correlación anatómica entre la histología de las fibras nerviosas objeto de burla y las características de conducción. Un estudio electrofisiológico diferencial de las capacidades de conducción de los segmentos proximales frente a los segmentos distales de un nervio es útil para identificar una axonopatía tóxica distal o para localizar un bloqueo neuropático de la conducción, probablemente debido a la desmielinización.
Comprender la fisiopatología de una polineuropatía neurotóxica sospechada tiene un gran valor. Por ejemplo, en pacientes con neuropatía causada por n-hexano y metilbutilcetona, las velocidades de conducción nerviosa motora se reducen, pero en algunos casos, los valores pueden caer dentro del rango normal si solo se estimulan y utilizan como resultado medido las fibras de activación más rápida. . Dado que los solventes de hexacarbono neurotóxicos causan degeneración axonal, surgen cambios secundarios en la mielina y explican la reducción general en la velocidad de conducción a pesar del valor dentro del rango normal producido por las fibras conductoras preservadas.
Las técnicas electrofisiológicas incluyen pruebas especiales además de los estudios de velocidad de conducción directa, amplitud y latencia. Los potenciales evocados somatosensoriales, los potenciales evocados auditivos y los potenciales evocados visuales son formas de estudiar las características de los sistemas de conducción sensorial, así como los nervios craneales específicos. El circuito aferente-eferente se puede probar usando pruebas de reflejo de parpadeo que involucran las respuestas del quinto nervio craneal al séptimo músculo craneal inervado; Los reflejos H implican vías reflejas motoras segmentarias. La estimulación por vibración selecciona las fibras más grandes de las fibras más pequeñas. Están disponibles técnicas electrónicas bien controladas para medir el umbral necesario para provocar una respuesta y luego determinar la velocidad de viaje de esa respuesta, así como la amplitud de la contracción muscular, o la amplitud y el patrón de un potencial de acción sensorial evocado. . Todos los resultados fisiológicos deben evaluarse a la luz del cuadro clínico y con una comprensión del proceso fisiopatológico subyacente.
Conclusión
La diferenciación de un síndrome neurotóxico de una enfermedad neurológica primaria plantea un desafío formidable para los médicos en el ámbito laboral. Obtener una buena anamnesis, mantener un alto grado de sospecha y un adecuado seguimiento de un individuo, así como de grupos de individuos, es necesario y gratificante. El reconocimiento temprano de enfermedades relacionadas con agentes tóxicos en su entorno o con una exposición ocupacional particular es fundamental, ya que un diagnóstico adecuado puede conducir a la eliminación temprana de los peligros de una exposición continua a una sustancia tóxica, evitando posibles daños neurológicos irreversibles. Además, el reconocimiento de los primeros casos afectados en un entorno particular puede generar cambios que protegerán a otros que aún no se han visto afectados.
Medición de los déficits neurotóxicos
Baterías de prueba neurofuncional
Durante mucho tiempo se han observado signos y síntomas neurológicos subclínicos entre trabajadores activos expuestos a neurotoxinas; sin embargo, es solo desde mediados de la década de 1960 que los esfuerzos de investigación se han centrado en el desarrollo de baterías de pruebas sensibles capaces de detectar cambios leves y sutiles que están presentes en las primeras etapas de la intoxicación, en las funciones perceptuales, psicomotoras, cognitivas, sensoriales y motoras. , y afectar.
La primera batería de pruebas neuroconductuales para su uso en estudios en el lugar de trabajo fue desarrollada por Helena Hänninen, pionera en el campo de los déficits neuroconductuales asociados con la exposición tóxica (Hänninen Test Battery) (Hänninen y Lindstrom 1979). Desde entonces, se han realizado esfuerzos en todo el mundo para desarrollar, refinar y, en algunos casos, informatizar baterías de pruebas neuroconductuales. Anger (1990) describe cinco baterías de pruebas neuroconductuales en el lugar de trabajo de Australia, Suecia, Gran Bretaña, Finlandia y los Estados Unidos, así como dos baterías de detección de neurotóxicos de los Estados Unidos, que se han utilizado en estudios de trabajadores expuestos a neurotoxinas. Además, el sistema computarizado de evaluación neuroconductual (NES) y el sistema sueco de evaluación del desempeño (SPES) se han utilizado ampliamente en todo el mundo. También existen baterías de prueba diseñadas para evaluar las funciones sensoriales, incluidas medidas de visión, umbral de percepción vibrotáctil, olfato, audición y balanceo (Mergler 1995). Los estudios de varios agentes neurotóxicos que utilizan una u otra de estas baterías han contribuido en gran medida a nuestro conocimiento del deterioro neurotóxico temprano; sin embargo, las comparaciones entre estudios han sido difíciles debido a que se utilizan diferentes pruebas y las pruebas con nombres similares pueden administrarse utilizando un protocolo diferente.
En un intento de estandarizar la información de los estudios sobre sustancias neurotóxicas, un comité de trabajo de la Organización Mundial de la Salud (OMS) propuso la noción de una batería "central" (Johnson 1987). Sobre la base de los conocimientos adquiridos en el momento de la reunión (1985), se seleccionaron una serie de pruebas para formar la Batería de pruebas básicas neuroconductuales (NCTB, por sus siglas en inglés), una batería relativamente económica, administrada a mano, que se ha utilizado con éxito en muchos países (Anger et al. 1993). Las pruebas que componen esta batería se eligieron para cubrir dominios específicos del sistema nervioso, que previamente habían demostrado ser sensibles al daño neurotóxico. Un grupo de trabajo de la Agencia de Sustancias Tóxicas y Registro de Enfermedades de los Estados Unidos (Hutchison et al. 1992) ha propuesto una batería central más reciente, que comprende pruebas tanto administradas a mano como computarizadas. Ambas baterías se presentan en la Tabla 1.
Tabla 1. Ejemplos de baterías "básicas" para la evaluación de efectos neurotóxicos tempranos
|
Batería de prueba básica neuroconductual (NCTB)+ |
orden de prueba |
Agencia para Sustancias Tóxicas y Registro de Enfermedades Batería de Pruebas de Neurocomportamiento Ambiental para Adultos (AENTB)+ |
||
|
dominio funcional |
Test |
dominio funcional |
Test |
|
|
Estabilidad motora |
Apuntar (Persecución Apuntar II) |
1 |
Visión |
Agudeza visual, sensibilidad al contraste cercano |
|
Velocidad de atención/respuesta |
Tiempo de reacción simple |
2 |
Visión de color (prueba desaturada Lanthony D-15) |
|
|
Velocidad motora perceptiva |
Símbolo de dígito (WAIS-R) |
3 |
Somatosensorial |
Umbral de percepción vibrotáctil |
|
Destreza manual |
Santa Ana (Versión Helsinki) |
4 |
Fuerza motora |
Dinamómetro (incluida la evaluación de la fatiga) |
|
Percepción visual/memoria |
Retención visual de Benton |
5 |
Coordinación motriz |
Santa Ana |
|
memoria auditiva |
Intervalo de dígitos (WAIS-R, WMS) |
6 |
Función intelectual superior |
Matrices progresivas de Raven (revisadas) |
|
Afectar |
POMS (Perfil de Estados de Ánimo) |
7 |
Coordinación motriz |
Prueba de toqueteo (una mano)1 |
|
8 |
Atención sostenida (cognitiva), velocidad (motora) |
Tiempo de reacción simple (SRT) (extendido)1 |
||
|
9 |
Codificación cognitiva |
Símbolo-dígito con recuperación retardada1 |
||
|
10 |
Aprendizaje y memoria |
Aprendizaje de dígitos en serie1 |
||
|
11 |
Índice de nivel educativo |
Vocabulario1 |
||
|
12 |
Humor |
Escala de estado de ánimo1 |
||
1 Disponible en versión informatizada; WAIS = Escala de Inteligencia para Adultos de Wechsler; WMS = Escala de memoria de Wechsler.
Los autores de ambas baterías centrales destacan que, aunque las baterías son útiles para estandarizar los resultados, de ninguna manera proporcionan una evaluación completa de las funciones del sistema nervioso. Se deben usar pruebas adicionales según el tipo de exposición; por ejemplo, una batería de pruebas para evaluar la disfunción del sistema nervioso entre los trabajadores expuestos al manganeso incluiría más pruebas de las funciones motoras, en particular aquellas que requieren movimientos alternos rápidos, mientras que una para los trabajadores expuestos al metilmercurio incluiría pruebas de campo visual. La elección de las pruebas para cualquier lugar de trabajo en particular debe hacerse sobre la base de los conocimientos actuales sobre la acción de la toxina o toxinas particulares a las que están expuestas las personas.
Las baterías de pruebas más sofisticadas, administradas e interpretadas por psicólogos capacitados, son una parte importante de la evaluación clínica del envenenamiento por neurotóxicos (Hart 1988). Incluye pruebas de capacidad intelectual, atención, concentración y orientación, memoria, viso-perceptivas, constructivas y motrices, lenguaje, funciones conceptuales y ejecutivas, y bienestar psicológico, así como una evaluación de posibles simulacros. El perfil de actuación del paciente se examina a la luz del historial médico y psicológico pasado y presente, así como del historial de exposición. El diagnóstico final se basa en una constelación de déficits interpretados en relación con el tipo de exposición.
Medidas de Estado Emocional y Personalidad
Los estudios de los efectos de las sustancias neurotóxicas suelen incluir medidas de trastornos afectivos o de la personalidad, en forma de cuestionarios de síntomas, escalas del estado de ánimo o índices de personalidad. El NCTB, descrito anteriormente, incluye el Perfil de estados de ánimo (POMS), una medida cuantitativa del estado de ánimo. Utilizando 65 adjetivos calificativos de estados de ánimo de los últimos 8 días, se derivan los grados de tensión, depresión, hostilidad, vigor, fatiga y confusión. La mayoría de los estudios comparativos sobre la exposición a neurotóxicos en el lugar de trabajo indican diferencias entre los expuestos y los no expuestos. Un estudio reciente de trabajadores expuestos al estireno muestra relaciones dosis-respuesta entre el nivel de ácido mandélico en la orina después del turno, un indicador biológico del estireno, y escalas de puntuación de tensión, hostilidad, fatiga y confusión (Sassine et al. 1996).
Las pruebas de afecto y personalidad más largas y sofisticadas, como el Índice de personalidad multifásico de Minnesota (MMPI), que reflejan tanto los estados emocionales como los rasgos de personalidad, se han utilizado principalmente para la evaluación clínica, pero también en estudios en el lugar de trabajo. El MMPI también proporciona una evaluación de la exageración de los síntomas y las respuestas inconsistentes. En un estudio de trabajadores de microelectrónica con antecedentes de exposición a sustancias neurotóxicas, los resultados del MMPI indicaron niveles clínicamente significativos de depresión, ansiedad, preocupaciones somáticas y trastornos del pensamiento (Bowler et al. 1991).
Medidas electrofisiológicas
La actividad eléctrica generada por la transmisión de información a lo largo de las fibras nerviosas y de una célula a otra, se puede registrar y utilizar para determinar lo que sucede en el sistema nervioso de las personas expuestas a sustancias tóxicas. La interferencia con la actividad neuronal puede ralentizar la transmisión o modificar el patrón eléctrico. Los registros electrofisiológicos requieren instrumentos precisos y se realizan con mayor frecuencia en un laboratorio o en un hospital. Sin embargo, se han realizado esfuerzos para desarrollar más equipos portátiles para su uso en estudios en el lugar de trabajo.
Las medidas electrofisiológicas registran una respuesta global de un gran número de fibras nerviosas y/o fibras, y debe existir una gran cantidad de daño antes de que pueda registrarse adecuadamente. Por lo tanto, para la mayoría de las sustancias neurotóxicas, los síntomas, así como los cambios sensoriales, motores y cognitivos, generalmente pueden detectarse en grupos de trabajadores expuestos antes de que se observen diferencias electrofisiológicas. Para el examen clínico de personas con sospecha de trastornos neurotóxicos, los métodos electrofisiológicos proporcionan información sobre el tipo y la extensión del daño del sistema nervioso. Seppalaïnen (1988) proporciona una revisión de las técnicas electrofisiológicas utilizadas en la detección de neurotoxicidad temprana en humanos.
La velocidad de conducción nerviosa de los nervios sensoriales (que van hacia el cerebro) y los nervios motores (que se alejan del cerebro) se mide mediante electroneurografía (ENG). Estimulando en diferentes posiciones anatómicas y registrando en otra, se puede calcular la velocidad de conducción. Esta técnica puede proporcionar información sobre las grandes fibras mielinizadas; el enlentecimiento de la velocidad de conducción ocurre cuando hay desmielinización. Con frecuencia se han observado velocidades de conducción reducidas entre trabajadores expuestos al plomo, en ausencia de síntomas neurológicos (Maizlish y Feo 1994). Las velocidades de conducción lentas de los nervios periféricos también se han asociado con otras neurotoxinas, como mercurio, hexacarbonos, disulfuro de carbono, estireno, metil-n-butilcetona, metiletilcetona y ciertas mezclas de solventes. El nervio trigémino (un nervio facial) se ve afectado por la exposición al tricloroetileno. Sin embargo, si la sustancia tóxica actúa principalmente sobre fibras poco mielinizadas o amielínicas, las velocidades de conducción suelen permanecer normales.
La electromiografía (EMG) se utiliza para medir la actividad eléctrica en los músculos. Se han observado anormalidades electromiográficas entre trabajadores expuestos a sustancias como n-hexano, disulfuro de carbono, metil-n-butilcetona, mercurio y ciertos pesticidas. Estos cambios a menudo van acompañados de cambios en ENG y síntomas de neuropatía periférica.
Los cambios en las ondas cerebrales se evidencian mediante electroencefalografía (EEG). En pacientes con intoxicación por disolventes orgánicos, se han observado anomalías de onda lenta locales y difusas. Algunos estudios reportan evidencia de alteraciones del EEG relacionadas con la dosis entre trabajadores activos, con exposición a mezclas de solventes orgánicos, estireno y disulfuro de carbono. Los pesticidas organoclorados pueden causar ataques epilépticos, con anomalías en el EEG. Se han informado cambios en el EEG con la exposición a largo plazo a plaguicidas organofosforados y fosfuro de zinc.
Los potenciales evocados (EP) proporcionan otro medio para examinar la actividad del sistema nervioso en respuesta a un estímulo sensorial. Los electrodos de registro se colocan en el área específica del cerebro que responde a los estímulos particulares, y se registran la latencia y la amplitud del potencial lento relacionado con el evento. Se ha observado una latencia aumentada y/o amplitudes máximas reducidas en respuesta a estímulos visuales, auditivos y somatosensoriales para una amplia gama de sustancias neurotóxicas.
La electrocardiografía (ECG o EKG) registra los cambios en la conducción eléctrica del corazón. Aunque no se usa con frecuencia en estudios de sustancias neurotóxicas, se han observado cambios en las ondas de ECG entre personas expuestas al tricloroetileno. Los registros electrooculográficos (EOG) de los movimientos oculares han mostrado alteraciones entre los trabajadores expuestos al plomo.
Técnicas de imágenes cerebrales
En los últimos años se han desarrollado diferentes técnicas para la obtención de imágenes cerebrales. Las imágenes de tomografía computarizada (TC) revelan la anatomía del cerebro y la médula espinal. Se han utilizado para estudiar la atrofia cerebral entre trabajadores y pacientes expuestos a solventes; sin embargo, los resultados no son consistentes. La resonancia magnética nuclear (RMN) examina el sistema nervioso usando un poderoso campo magnético. Es particularmente útil clínicamente para descartar un diagnóstico alternativo, como los tumores cerebrales. La tomografía por emisión de positrones (PET), que produce imágenes de procesos bioquímicos, se ha utilizado con éxito para estudiar los cambios en el cerebro inducidos por la intoxicación por manganeso. La tomografía computarizada por emisión de fotón único (SPECT) proporciona información sobre el metabolismo cerebral y puede resultar una herramienta importante para comprender cómo actúan las neurotoxinas en el cerebro. Todas estas técnicas son muy costosas y no están fácilmente disponibles en la mayoría de los hospitales o laboratorios de todo el mundo.
Diagnóstico
El diagnóstico de la enfermedad neurotóxica no es fácil. Los errores suelen ser de dos tipos: o no se reconoce que un agente neurotóxico es la causa de los síntomas neurológicos, o los síntomas neurológicos (y especialmente neurocomportamentales) se diagnostican erróneamente como resultado de una exposición neurotóxica ocupacional. Ambos errores pueden ser peligrosos ya que un diagnóstico temprano es importante en el caso de una enfermedad neurotóxica, y el mejor tratamiento es evitar una mayor exposición para el caso individual y la vigilancia de la condición de otros trabajadores para prevenir su exposición a la misma. peligro. Por otro lado, a veces se puede generar una alarma indebida en el lugar de trabajo si un trabajador afirma tener síntomas graves y sospecha que la causa es una exposición química pero, de hecho, el trabajador está equivocado o el peligro no está realmente presente para los demás. También existe una razón práctica para procedimientos de diagnóstico correctos, ya que en muchos países, el diagnóstico y el tratamiento de enfermedades profesionales y la pérdida de la capacidad laboral y la invalidez causadas por esas enfermedades están cubiertos por seguros; por lo tanto, la compensación financiera puede ser cuestionada, si los criterios de diagnóstico no son sólidos. En la Tabla 1 se proporciona un ejemplo de un árbol de decisión para la evaluación neurológica.
Tabla 1. Árbol de decisión para enfermedad neurotóxica
I. Nivel, duración y tipo de exposición pertinente
II. Síntomas apropiados que aumentan insidiosamente los síntomas del sistema nervioso central (SNC) o periférico (SNP)
tercero Signos y pruebas adicionales Disfunción del SNC: neurología, pruebas de psicología Disfunción del SNC: prueba sensorial cuantitativa, estudios de conducción nerviosa
IV. Otras enfermedades excluidas en el diagnóstico diferencial
Exposición y síntomas
Los síndromes neurotóxicos agudos ocurren principalmente en situaciones accidentales, cuando los trabajadores están expuestos a corto plazo a niveles muy altos de una sustancia química oa una mezcla de sustancias químicas, generalmente por inhalación. Los síntomas habituales son vértigo, malestar y posible pérdida de conciencia como consecuencia de la depresión del sistema nervioso central. Cuando se retira al sujeto de la exposición, los síntomas desaparecen con bastante rapidez, a menos que la exposición haya sido tan intensa que ponga en peligro la vida, en cuyo caso puede seguir el coma y la muerte. En estas situaciones el reconocimiento del peligro debe ocurrir en el lugar de trabajo, y la víctima debe ser sacada al aire libre inmediatamente.
En general, los síntomas neurotóxicos surgen después de exposiciones a corto o largo plazo y, a menudo, a niveles de exposición ocupacional relativamente bajos. En estos casos, los síntomas agudos pueden haber ocurrido en el trabajo, pero la presencia de síntomas agudos no es necesaria para hacer el diagnóstico de encefalopatía tóxica crónica o neuropatía tóxica. Sin embargo, los pacientes a menudo informan dolor de cabeza, mareos o irritación de las mucosas al final de la jornada laboral, pero estos síntomas desaparecen inicialmente durante la noche, el fin de semana o las vacaciones. Una lista de verificación útil se puede encontrar en la Tabla 2.
Tabla 2. Efectos neurofuncionales consistentes de la exposición en el lugar de trabajo a algunas de las principales sustancias neurotóxicas
|
Disolventes orgánicos mixtos |
Disulfuro de carbono |
Estireno |
Organofos- |
Lidera |
Mercurio |
|
|
Acquisition |
+ |
|
|
|
+ |
|
|
Afectar |
+ |
|
+ |
|
+ |
|
|
Categorización |
+ |
|
|
|
|
|
|
Codificación |
+ |
+ |
|
|
+ |
+ |
|
visión de color |
+ |
|
+ |
|
|
|
|
Cambio de concepto |
+ |
|
|
|
|
|
|
Distracción |
|
|
|
|
+ |
|
|
Intelligence |
+ |
+ |
|
+ |
+ |
+ |
|
Salud Cerebral |
+ |
+ |
+ |
+ |
+ |
+ |
|
Coordinación motriz |
+ |
+ |
+ |
|
+ |
+ |
|
La velocidad del motor |
+ |
+ |
+ |
|
+ |
+ |
|
Sensibilidad al contraste visual cercano |
+ |
|
|
|
|
|
|
Umbral de percepción del olor |
+ |
|
|
|
|
|
|
Identificación de olores |
+ |
|
|
|
+ |
|
|
Personalidad |
+ |
+ |
|
|
|
+ |
|
Relaciones espaciales |
+ |
+ |
|
|
+ |
|
|
Umbral vibrotáctil |
+ |
|
|
+ |
|
+ |
|
Vigilancia |
+ |
+ |
|
|
+ |
|
|
Campo visual |
|
|
|
|
+ |
+ |
|
Vocabulario |
|
|
|
|
+ |
|
Fuente: Adaptado de Anger 1990.
Suponiendo que el paciente ha estado expuesto a sustancias químicas neurotóxicas, el diagnóstico de enfermedad neurotóxica comienza con los síntomas. En 1985, un grupo de trabajo conjunto de la Organización Mundial de la Salud y el Consejo Nórdico de Ministros discutió el tema de la intoxicación crónica por solventes orgánicos y encontró un conjunto de síntomas centrales, que se encuentran en la mayoría de los casos (OMS/Consejo Nórdico 1985). Los síntomas centrales son fatigabilidad, pérdida de memoria, dificultades de concentración y pérdida de iniciativa. Estos síntomas suelen comenzar después de un cambio básico en la personalidad, que se desarrolla gradualmente y afecta la energía, el intelecto, la emoción y la motivación. Entre otros síntomas de la encefalopatía tóxica crónica se encuentran la depresión, disforia, labilidad emocional, dolor de cabeza, irritabilidad, trastornos del sueño y mareos (vértigo). Si también hay compromiso del sistema nervioso periférico, se desarrolla entumecimiento y posiblemente debilidad muscular. Dichos síntomas crónicos duran al menos un año después de que finaliza la exposición.
Examen clínico y pruebas
El examen clínico debe incluir un examen neurológico, donde se debe prestar atención al deterioro de las funciones nerviosas superiores, como la memoria, la cognición, el razonamiento y la emoción; a funciones cerebelosas alteradas, como temblor, marcha, estación y coordinación; ya las funciones nerviosas periféricas, especialmente la sensibilidad a la vibración y otras pruebas de sensibilidad. Las pruebas psicológicas pueden proporcionar medidas objetivas de las funciones del sistema nervioso superior, incluidas las funciones psicomotoras, de memoria a corto plazo, de razonamiento verbal y no verbal y de percepción. En el diagnóstico individual las pruebas deben incluir algunas pruebas que den una pista sobre el nivel intelectual premórbido de la persona. El historial de desempeño escolar y el desempeño laboral anterior, así como las posibles pruebas psicológicas administradas previamente, por ejemplo, en relación con el servicio militar, pueden ayudar en la evaluación del nivel normal de desempeño de la persona.
El sistema nervioso periférico se puede estudiar con pruebas cuantitativas de modalidades sensoriales, vibración y termosensibilidad. Los estudios de velocidad de conducción nerviosa y la electromiografía a menudo pueden revelar neuropatía en una etapa temprana. En estas pruebas se debe hacer especial hincapié en las funciones de los nervios sensoriales. La amplitud del potencial de acción sensorial (SNAP) disminuye con más frecuencia que la velocidad de conducción sensorial en las neuropatías axonales, y la mayoría de las neuropatías tóxicas son de carácter axonal. Los estudios neurorradiológicos como la tomografía computarizada (TC) y la resonancia magnética nuclear (RMN) por lo general no revelan nada pertinente a la encefalopatía tóxica crónica, pero pueden ser útiles en el diagnóstico diferencial.
En el diagnóstico diferencial se deben considerar otras enfermedades neurológicas y psiquiátricas. Deben descartarse demencias de otra etiología, así como síntomas depresivos y de estrés de diversas causas. Puede ser necesaria una consulta psiquiátrica. El abuso de alcohol es un factor de confusión relevante; el uso excesivo de alcohol provoca síntomas similares a los de la exposición a solventes, y por otro lado hay trabajos que indican que la exposición a solventes puede inducir al abuso de alcohol. También hay que descartar otras causas de neuropatía, especialmente neuropatías por atrapamiento, diabetes y enfermedad renal; también el alcohol causa neuropatía. Es más probable que la combinación de encefalopatía y neuropatía tenga un origen tóxico que cualquiera de estos por separado.
En la decisión final, la exposición debe evaluarse nuevamente. ¿Hubo exposición relevante, teniendo en cuenta el nivel, la duración y la calidad de la exposición? Es más probable que los disolventes induzcan el síndrome psicoorgánico o la encefalopatía tóxica; los hexacarbonos, sin embargo, por lo general primero causan neuropatía. El plomo y algunos otros metales causan neuropatía, aunque la afectación del SNC puede detectarse más tarde.
Neuroepidemiología Ocupacional
Olav Axelson*
*Adaptado de Axelson 1996.
Los primeros conocimientos sobre los efectos neurotóxicos de las exposiciones ocupacionales aparecieron a través de observaciones clínicas. Los efectos observados fueron más o menos agudos y se referían a la exposición a metales como el plomo y el mercurio o disolventes como el disulfuro de carbono y el tricloroetileno. Con el tiempo, sin embargo, se han evaluado los efectos más crónicos y clínicamente menos evidentes de los agentes neurotóxicos mediante métodos de examen modernos y estudios sistemáticos de grupos más grandes. Aún así, la interpretación de los hallazgos ha sido controvertida y debatida, como los efectos crónicos de la exposición a solventes (Arlien-Søborg 1992).
Las dificultades encontradas al interpretar los efectos neurotóxicos crónicos dependen tanto de la diversidad y vaguedad de los síntomas y signos como del problema asociado de definir una entidad de enfermedad adecuada para estudios epidemiológicos concluyentes. Por ejemplo, en la exposición a solventes, los efectos crónicos pueden incluir problemas de memoria y concentración, cansancio, falta de iniciativa, responsabilidad afectiva, irritabilidad y, a veces, mareos, dolor de cabeza, intolerancia al alcohol y reducción de la libido. Los métodos neurofisiológicos también han revelado varios trastornos funcionales, nuevamente difíciles de condensar en una sola entidad patológica.
De manera similar, también parece ocurrir una variedad de efectos neuroconductuales debido a otras exposiciones ocupacionales, como exposición moderada al plomo o soldadura con alguna exposición al aluminio, plomo y manganeso o exposición a pesticidas. Nuevamente también existen signos neurofisiológicos o neurológicos, entre otros, polineuropatía, temblor y alteración del equilibrio, en individuos expuestos a organoclorados, organofosforados y otros insecticidas.
En vista de los problemas epidemiológicos que implica definir una entidad de enfermedad entre los muchos tipos de efectos neuroconductuales a los que se hace referencia, también se ha vuelto natural considerar algunos trastornos neuropsiquiátricos clínicamente más o menos bien definidos en relación con las exposiciones ocupacionales.
Desde la década de 1970, varios estudios se han centrado especialmente en la exposición a disolventes y el síndrome psicoorgánico, cuando su gravedad es incapacitante. Más recientemente, también la demencia de Alzheimer, la esclerosis múltiple, la enfermedad de Parkinson, la esclerosis lateral amiotrófica y afecciones relacionadas han atraído el interés en la epidemiología ocupacional.
Con respecto a la exposición a solventes y el síndrome psico-orgánico (o encefalopatía crónica tóxica en medicina laboral clínica, cuando la exposición se toma en cuenta para el diagnóstico), el problema de definir una entidad de enfermedad adecuada fue evidente y primero llevó a considerar en bloque los diagnósticos de encefalopatía, demencia y atrofia cerebral, pero también se incluyeron neurosis, neurastenia y nervositas como no necesariamente distintos entre sí en la práctica médica (Axelson, Hane y Hogstedt 1976). Recientemente, entidades patológicas más específicas, como la demencia orgánica y la atrofia cerebral, también se han asociado con la exposición a disolventes (Cherry, Labréche y McDonald 1992). Sin embargo, los hallazgos no han sido totalmente consistentes, ya que no apareció un exceso de "demencia presenil" en un estudio de referencia de casos a gran escala en los Estados Unidos con hasta 3,565 casos de diversos trastornos neuropsiquiátricos y 83,245 1990 referencias hospitalarias (Brackbill, Maizlish y Fischbach 45). Sin embargo, en comparación con los albañiles, hubo un exceso de alrededor del XNUMX % de trastornos neuropsiquiátricos incapacitantes entre los pintores varones blancos, excepto los pintores con aerosol.
Las exposiciones ocupacionales también parecen desempeñar un papel en trastornos más específicos que el síndrome psicoorgánico. Por lo tanto, en 1982, se indicó por primera vez en la industria italiana del calzado una asociación entre la esclerosis múltiple y la exposición a solventes de los pegamentos (Amaducci et al. 1982). Esta relación ha sido fortalecida considerablemente por estudios adicionales en Escandinavia (Flodin et al. 1988; Landtblom et al. 1993; Grönning et al. 1993) y en otros lugares, por lo que 13 estudios con alguna información sobre exposición a solventes podrían ser considerados en una revisión ( Landtblom et al. 1996). Diez de estos estudios proporcionaron suficientes datos para su inclusión en un metanálisis, mostrando un riesgo de casi el doble de esclerosis múltiple entre las personas expuestas a disolventes. Algunos estudios también asocian la esclerosis múltiple con el trabajo radiológico, la soldadura y el trabajo con herbicidas fenoxi (Flodin et al. 1988; Landtblom et al. 1993). La enfermedad de Parkinson parece ser más común en áreas rurales (Goldsmith et al. 1990), especialmente en edades más jóvenes (Tanner 1989). Más interesante aún, un estudio de Calgary, Canadá, mostró un riesgo triple de exposición a herbicidas (Semchuk, Love y Lee 1992).
Todas las personas del caso que recordaron exposiciones específicas informaron exposición a herbicidas fenoxi o tiocarbamatos. Uno de ellos recordó la exposición al paraquat, que es químicamente similar al MPTP (N-metil-4-fenil-1,2,3,6-tetrahidropiridina), un inductor de un síndrome similar al de Parkinson. Sin embargo, aún no se ha encontrado que los trabajadores de paraquat padezcan dicho síndrome (Howard 1979). Los estudios de referencia de casos de Canadá, China, España y Suecia han indicado una relación con la exposición a químicos industriales, pesticidas y metales no especificados, especialmente manganeso, hierro y aluminio (Zayed et al. 1990).
En un estudio de los Estados Unidos, apareció un mayor riesgo de enfermedad de las neuronas motoras (que abarca la esclerosis lateral amiotrófica, la parálisis bulbar progresiva y la atrofia muscular progresiva) en relación con la soldadura blanda y blanda (Armon et al. 1991). La soldadura también apareció como un factor de riesgo, al igual que el trabajo con electricidad, y también el trabajo con agentes de impregnación en un estudio sueco (Gunnarsson et al. 1992). La heredabilidad de las enfermedades neurodegenerativas y tiroideas, combinada con la exposición a solventes y el sexo masculino, mostró un riesgo de hasta 15.6. Otros estudios también indican que la exposición al plomo y los solventes podría ser importante (Campbell, Williams y Barltrop 1970; Hawkes, Cavanagh y Fox 1989; Chio, Tribolo y Schiffer 1989; Sienko et al. 1990).
Para la enfermedad de Alzheimer, no apareció ninguna indicación clara de ningún riesgo ocupacional en un metanálisis de once estudios de referencia de casos (Graves et al. 1991), pero más recientemente se relacionó un mayor riesgo con el trabajo manual (Fratiglioni et al. 1993). ). Otro nuevo estudio, que incluyó también las edades más antiguas, indicó que la exposición a solventes podría ser un factor de riesgo bastante fuerte (Kukull et al. 1995). La sugerencia reciente de que la enfermedad de Alzheimer podría estar relacionada con la exposición a campos electromagnéticos fue quizás aún más sorprendente (Sobel et al. 1995). Es probable que ambos estudios estimulen el interés en varias investigaciones nuevas en las líneas indicadas.
Por lo tanto, en vista de las perspectivas actuales en neuroepidemiología ocupacional, como se ha esbozado brevemente, parece haber una razón para realizar estudios adicionales relacionados con el trabajo de diferentes trastornos neurológicos y neuropsiquiátricos, hasta ahora más o menos descuidados. No es improbable que existan algunos efectos contribuyentes de varias exposiciones ocupacionales, de la misma manera que hemos visto para muchos tipos de cáncer. Además, al igual que en la investigación etiológica del cáncer, de la epidemiología ocupacional se pueden obtener nuevas pistas que sugieran las causas últimas o los mecanismos desencadenantes de algunos de los trastornos neurológicos graves.
Sistemas renales y urinarios
Los sistemas renal y urinario se componen de una serie compleja de órganos que juntos funcionan para filtrar los desechos de la sangre y fabricar, almacenar y descargar la orina. Estos sistemas de órganos son vitales para la homeostasis a través del mantenimiento del equilibrio de líquidos, el equilibrio ácido-base y la presión arterial. Los órganos primarios del sistema renal-urinario son los dos riñones y la vejiga urinaria. En el proceso de filtrado de los productos de desecho de la sangre, los riñones están potencialmente expuestos a altas concentraciones de sustancias tóxicas endógenas y exógenas. Así, algunas células renales están expuestas a concentraciones mil veces superiores a las de la sangre.
Los problemas que resultan en daño al riñón pueden ser prerrenales (afectan el suministro de sangre al riñón), renales (afectan al propio riñón) o posrenales (afectan cualquier punto a lo largo del camino que la orina viaja desde el riñón hasta el final). de la uretra o del pene). Los problemas posrenales suelen ser de naturaleza obstructiva; un sitio común de obstrucción es la próstata, yuxtapuesta entre la vejiga y la uretra. Las enfermedades preexistentes de la próstata, la vejiga o los uréteres, en particular infecciones, obstrucciones o cuerpos extraños como cálculos, pueden comprometer la función renal y aumentar la susceptibilidad a defectos adquiridos o genéticos.
Comprender la microanatomía y los mecanismos moleculares de los riñones y la vejiga es importante para evaluar la susceptibilidad, monitorear y prevenir exposiciones ocupacionales. Los tóxicos parecen dirigirse a partes específicas del riñón o la vejiga y dan como resultado la expresión de biomarcadores específicos directamente relacionados con el segmento dañado. Históricamente, la predisposición a la enfermedad se ha visto desde la perspectiva epidemiológica de identificar un grupo de trabajadores en riesgo. Hoy, con una mejor comprensión de los mecanismos fundamentales de la enfermedad, la evaluación del riesgo individual mediante el uso de biomarcadores de susceptibilidad, exposición, efecto y enfermedad está en el horizonte. Surgen nuevos problemas éticos debido a la presión para desarrollar estrategias rentables para proteger a los trabajadores de los riesgos laborales. La presión surge, en parte, porque las pruebas genéticas están ganando aceptación para evaluar la predisposición a la enfermedad y los biomarcadores de exposición y efecto pueden servir como puntos finales intermedios en los que la intervención puede ser beneficiosa. El propósito de este capítulo es proporcionar una revisión médica de los sistemas renal y urinario a partir de la cual se podrían establecer pautas para evaluar y reducir el riesgo individual en el lugar de trabajo, teniendo debidamente en cuenta los aspectos éticos involucrados.
Anatomía y fisiopatología del riñón
El riñón humano es un órgano complejo cuya función es filtrar los desechos de la sangre a través de la producción de orina. Los dos riñones también realizan una variedad de otras funciones vitales, incluido el mantenimiento de la homeostasis, la regulación de la presión arterial, la presión osmótica y el equilibrio ácido-base. Los riñones reciben el 25% del gasto cardíaco total de sangre, lo que los expone potencialmente a toxinas endógenas y exógenas.
Los riñones están ubicados a cada lado de la columna vertebral en la parte inferior de la espalda. Cada uno pesa unos 150 gramos y tiene el tamaño aproximado de una naranja. El riñón consta de tres capas: la corteza (capa externa), la médula y la pelvis renal. La sangre fluye hacia la corteza y la médula a través de la arteria renal y se ramifica en arterias cada vez más pequeñas. Cada una de las arterias termina en una unidad de filtración de sangre llamada nefrona. Un riñón sano contiene aproximadamente 1.2 millones de nefronas, ubicadas estratégicamente dentro de la corteza y la médula.
Una nefrona consiste en el glomérulo (un grupo de pequeños vasos sanguíneos) rodeado por la cápsula de Bowman (una membrana de dos capas) que se abre en un túbulo contorneado. La porción fluida de la sangre, el plasma, es forzada a través del glomérulo hacia la cápsula de Bowman y luego, como plasma filtrado, pasa al túbulo contorneado. Aproximadamente el 99% del agua y los nutrientes esenciales que se han filtrado son reabsorbidos por las células del túbulo y pasan a los capilares que rodean el túbulo contorneado. La sangre sin filtrar que permanece en el glomérulo también fluye hacia los capilares y regresa a través de la vena renal al corazón.
Las nefronas aparecen como conductos largos en forma de bucle compuestos por múltiples segmentos, cada uno de los cuales realiza una variedad de funciones diferentes diseñadas para mantener los mecanismos homeostáticos del cuerpo. La figura 1 muestra una nefrona y su orientación dentro de la corteza renal y la médula. Cada segmento de nefrona tiene un suministro de sangre diferencial que regula el gradiente iónico. Ciertos productos químicos pueden afectar directamente a segmentos específicos de la nefrona de forma aguda o crónica, según el tipo y la dosis de exposición al xenobiótico. Dependiendo del segmento de la microanatomía objetivo, varios aspectos de la función renal pueden verse afectados.
Figura 1. Relaciones entre el suministro vascular, el glomérulo y los componentes tubulares de la nefrona y la orientación de estos componentes dentro de la corteza y la médula renales
Los vasos sanguíneos que llegan al riñón suministran únicamente los elementos glomerulares y tubulares, entregando desechos para ser filtrados y absorbiendo nutrientes, proteínas y electrolitos, además de suministrar oxígeno para la viabilidad del órgano. El noventa por ciento del flujo sanguíneo se dirige a la corteza, con un gradiente decreciente hacia la médula. Tal flujo sanguíneo diferencial y el posicionamiento de las unidades de nefrona son vitales para el mecanismo de contracorriente que concentra aún más la orina y las nefrotoxinas potenciales.
El glomérulo se coloca entre las arteriolas aferente y eferente. Las arteriolas eferentes forman una red de capilares alrededor de cada unidad de nefrona con la excepción de la yuxtaposición del túbulo distal adyacente al suministro de sangre aferente del glomérulo. Los túbulos aferentes y eferentes enervados por los nervios simpáticos responden a la estimulación autonómica y mediadores hormonales como la vasopresión y la hormona antidiurética (ADH). Un área llamada mácula densa, parte del aparato yuxtaglomerular, produce renina, un mediador de la presión arterial, en respuesta a los cambios osmóticos y la presión arterial. Las enzimas hepáticas convierten la renina en un octapéptido, la angiotensina II, que regula el flujo sanguíneo a los riñones y se dirige preferentemente a las arteriolas aferentes y las células mesangiales del glomérulo.
El glomérulo solo permite el paso de proteínas de cierto tamaño con carga definida durante la filtración. La filtración de plasma está controlada por un equilibrio de presión osmótica e hidrostática. Moléculas de azúcar especializadas, glicosaminoglicanos, proporcionan carga aniónica negativa que inhibe, por fuerzas electrostáticas, la filtración de materiales cargados negativamente. La capa de tres células de la membrana basal glomerular consta de múltiples procesos de pie que aumentan el área de absorción y crean los poros a través de los cuales pasa el filtrado. El daño a la membrana basal especializada o al endotelio capilar puede permitir que la albúmina, un tipo de proteína, se derrame en cantidades mayores en la orina. La presencia de una cantidad excesiva de albúmina u otras microproteínas en la orina sirve como marcador de daño glomerular o tubular.
El intersticio renal es el espacio entre las unidades de nefrona y es más prominente en la porción medular central que en la corteza externa. Dentro del intersticio hay células intersticiales que están muy cerca de los vasos sanguíneos medulares y las células de los túbulos. Con el envejecimiento puede haber una mayor prominencia de las células intersticiales en la corteza con fibrosis y cicatrización asociadas. Las células intersticiales contienen gotitas de lípidos y pueden participar en el control de la presión arterial con la liberación de factores de relajación o constricción vasculares. La enfermedad crónica del intersticio puede afectar a los glomérulos y los túbulos o, por el contrario, la enfermedad de los glomérulos y los túbulos puede afectar al intersticio. Por lo tanto, en la enfermedad renal terminal a veces es difícil definir con precisión los mecanismos patológicos de la insuficiencia renal.
Los túbulos colectores proximales absorben el 80% del sodio, agua y cloruro, y el 100% de la urea. Cada túbulo proximal tiene tres segmentos, siendo el último segmento (P-3) el más vulnerable a la exposición a xenobióticos (sustancias extrañas tóxicas). Cuando las células proximales están dañadas por metales pesados como el cromo, la capacidad de concentración del riñón se ve afectada y la orina puede estar más diluida. La toxicidad en el segmento P-3 da como resultado la liberación en la orina de enzimas, como la fosfatasa alcalina intestinal, la N-acetil-beta-D-glucosaminidasa (NAG) o la proteína de Tamm-Horsfall, que está asociada con la fosfatasa alcalina intestinal. borde de las células del túbulo proximal aumentando el área de absorción efectiva.
Diagnóstico y pruebas de nefrotoxicidad
La creatinina sérica es otra sustancia filtrada por el glomérulo pero mínimamente absorbida por los túbulos proximales. El daño al glomérulo da como resultado su incapacidad para eliminar las toxinas producidas por el cuerpo y hay una acumulación de creatinina sérica. Debido a que la creatinina sérica es un producto del metabolismo muscular y dependiente de la masa corporal del paciente, tiene baja sensibilidad y especificidad para medir la función renal, pero se usa con frecuencia porque es conveniente. Una prueba más sensible y específica es cuantificar el filtrado midiendo el aclaramiento de creatinina (Cr); el aclaramiento de creatinina en orina sérica se calcula mediante la fórmula general CCr=UCr V/PCr, Donde UCrV es la cantidad de Cr excretada por unidad de tiempo y PCr es la concentración plasmática de Cr. Sin embargo, el aclaramiento de creatinina es más complejo en términos de muestreo para la prueba y, por lo tanto, no es práctico para las pruebas ocupacionales. Las pruebas de depuración de isótopos realizadas mediante marcaje radiactivo de compuestos como el ortoyodohipurato, que también son depurados por el riñón, también son eficaces, pero no prácticas ni rentables en el entorno laboral. La función diferencial de los riñones individuales se puede determinar utilizando exploraciones nucleares renales diferenciales o cateterismo selectivo de ambos riñones mediante el paso de un catéter desde la vejiga hasta el riñón a través del uréter. Sin embargo, estos métodos tampoco se emplean fácilmente para pruebas en el lugar de trabajo a gran escala. Debido a que la función renal puede reducirse entre un 70 y un 80 % antes de una elevación detectable de la creatinina sérica, y debido a que otras pruebas existentes son poco prácticas o costosas, se necesitan biomarcadores no invasivos para detectar exposiciones intermitentes agudas a dosis bajas en el riñón. En la sección sobre biomarcadores se analiza una serie de biomarcadores para detectar daño renal a dosis bajas o cambios tempranos asociados con la carcinogénesis.
Aunque las células del túbulo proximal absorben el 80% de los líquidos, el mecanismo de contracorriente y los túbulos colectores distales ajustan con precisión la cantidad de líquidos absorbidos mediante la regulación de la ADH. La ADH se libera de la glándula pituitaria en lo profundo del cerebro y responde a las presiones osmóticas y al volumen de líquido. Los compuestos exógenos como el litio pueden dañar los conductos colectores distales y provocar diabetes insípida renal (emisión de orina diluida). Los trastornos genéticos hereditarios también pueden causar este defecto. Los xenobióticos normalmente afectan a ambos riñones, pero surgen complejidades de interpretación cuando las exposiciones son difíciles de documentar o cuando hay una enfermedad renal preexistente. En consecuencia, las exposiciones accidentales a dosis altas han servido como marcadores para identificar compuestos nefrotóxicos en muchos casos. La mayoría de las exposiciones ocupacionales ocurren a dosis bajas y están enmascaradas por la filtración de reserva y la capacidad compensatoria de reparación (hipertrofia) del riñón. El desafío que queda es detectar exposiciones a dosis bajas clínicamente no detectadas por los métodos actuales.
Anatomía y fisiopatología de la vejiga
La vejiga urinaria es una bolsa hueca en la que se almacena la orina; normalmente, se contrae a demanda para el vaciado controlado a través de la uretra. La vejiga está ubicada en la parte frontal e inferior de la cavidad pélvica. La vejiga está unida a ambos lados de los dos riñones por tubos peristálticos musculares, los uréteres, que transportan la orina desde los riñones hasta la vejiga. La pelvis renal, los uréteres y la vejiga están revestidos con epitelio de transición. La capa externa del urotelio consta de células paraguas recubiertas con una capa de carbohidratos, glicosaminoglicanos (GAG). Las células de transición se extienden hasta la membrana basal de la vejiga. Las células basales profundas están protegidas por las células paraguas, pero si la capa protectora de GAG está dañada, las células basales son susceptibles de lesión por los componentes urinarios. La microanatomía del epitelio de transición le permite expandirse y contraerse, e incluso con el desprendimiento normal de las células paraguas, se mantiene la integridad protectora de las células basales.
El sistema neurológico equilibrado que regula el almacenamiento y el vaciado puede dañarse durante electrochoques u otros traumatismos, como lesiones de la médula espinal, que se produzcan en el lugar de trabajo. Una de las principales causas de muerte entre los tetrapléjicos es la pérdida de la función de la vejiga, lo que resulta en un daño renal crónico secundario a la infección y la formación de cálculos. Es frecuente la infección crónica por vaciado incompleto debido a causas neurógenas u obstructivas, como fractura pélvica u otro traumatismo de la uretra y formación de estenosis subsiguiente. La infección bacteriana persistente o la formación de cálculos que resultan en condiciones malignas e inflamatorias crónicas de la vejiga pueden ser causadas por una resistencia reducida (es decir, susceptibilidad) a las exposiciones exógenas en el lugar de trabajo.
Las moléculas asociadas con el daño y la reparación dentro de la vejiga sirven como posibles marcadores de punto final intermedio para las condiciones tóxicas y malignas porque ocurren muchas alteraciones bioquímicas durante los cambios relacionados con el desarrollo del cáncer. Al igual que el riñón, las células de la vejiga tienen sistemas enzimáticos activos, como el citocromo P-450, que pueden activar o desactivar xenobióticos. La actividad funcional de las enzimas está determinada por herencia genética y exhibe polimorfismo genético. La orina eliminada contiene células exfoliadas del riñón, los uréteres, la vejiga, la próstata y la uretra. Estas células proporcionan objetivos, mediante el uso de biomarcadores, para evaluar los cambios en la patología renal y de la vejiga. Recordar el comentario de Virchow de que todas las enfermedades empiezan en las células centra nuestra atención en la importancia de las células, que son el espejo molecular de los episodios de exposición.
Toxicología Ambiental y Ocupacional
Un volumen considerable de datos epidemiológicos respalda la relación causal de las exposiciones ocupacionales en el cáncer de vejiga, pero las contribuciones precisas de las exposiciones en el lugar de trabajo a la insuficiencia renal y el cáncer de riñón son difíciles de estimar. En un informe reciente, se estimó que hasta el 10 % de las enfermedades renales en etapa terminal podrían atribuirse a exposiciones en el lugar de trabajo, pero los resultados son difíciles de validar debido a los peligros ambientales y químicos cambiantes, las variaciones en los criterios de diagnóstico y el período de latencia a menudo prolongado. entre la exposición y la enfermedad. Se estima que la función de dos tercios de las nefronas de ambos riñones puede perderse antes de que el daño renal sea clínicamente evidente. Sin embargo, cada vez hay más pruebas de que lo que antes se pensaba que eran causas socioeconómicas o étnicas de la nefrotoxicidad pueden ser de hecho ambientales, lo que añade validez al papel de las sustancias tóxicas en el desarrollo de la enfermedad.
La nefrotoxicidad puede estar directamente relacionada con el xenobiótico, o el xenobiótico puede pasar por una activación o inactivación de un solo paso o de varios pasos en el riñón o el hígado. La activación de los xenobióticos está regulada por conjuntos complejos de enzimas identificadas como Fase I, II y Auxiliar. Una enzima de Fase I es el sistema oxidativo P-450 que actúa a través de vías de reducción o hidrólisis. Las enzimas de la fase II catalizan la conjugación, mientras que las enzimas auxiliares regulan el metabolismo de los fármacos (la Tabla 1 enumera estas enzimas). Varios modelos animales han proporcionado información sobre los mecanismos metabólicos, y los estudios de cortes de riñón y microdisección de las unidades de nefronas renales en cultivo de tejidos aportan información sobre los mecanismos patológicos. Sin embargo, las variables individuales y de especies son considerables y, aunque los mecanismos pueden ser similares, se requiere precaución al extrapolar los resultados a los humanos en el lugar de trabajo. Los temas principales ahora son determinar qué xenobióticos son nefrotóxicos y/o cancerígenos, y en qué sitios objetivo, y desarrollar métodos para identificar con mayor precisión la toxicidad subclínica en el sistema renal-urinario.
Tabla 1. Enzimas del metabolismo de fármacos en el riñón1
| ENZIMAS | ||
| fase I | Fase II | Auxiliar |
| Citocromo P-450 | Esterasa | peróxidos de GSH |
| Monooxigenasa que contiene FAD microsomal | N-Acetiltransferasa | GSSG reductasa |
| Alcohol y aldehído deshidrogenasas | GSH S-transferasa | Superóxido dismutasa |
| Epóxido hidrolasa | Tiol S-metil-transferasa | Catalase |
| Prostaglandina sintasa | UDP glucuronosiltransferasa | DT-diaforasa |
| Monoamina oxidasa | sulfotransferasa | Vías generadoras de NADPH |
1 Las enzimas de fase I catalizan la oxidación, reducción o hidrólisis.
Las enzimas de fase II generalmente catalizan la conjugación.
Las enzimas auxiliares funcionan de manera secundaria o de apoyo para facilitar el metabolismo de los fármacos.
Fuente: Consejo Nacional de Investigación 1995.
Trastornos renales y urinarios no malignos
La glomerulonefritis es una condición reactiva inflamatoria de la membrana basal glomerular o del endotelio capilar. Las formas aguda y crónica de la enfermedad son causadas por una variedad de condiciones infecciosas, autoinmunes o inflamatorias o por exposición a agentes tóxicos. La glomerulonefritis se asocia con vasculitis, ya sea sistémica o limitada al riñón. El daño crónico secundario al glomérulo también ocurre durante un ciclo intenso de ataque desde la nefrotoxicidad al intersticio de las células del túbulo. Las medias lunas glomerulares epiteliales o las formas proliferativas son un sello distintivo de la glomerulonefritis en las muestras de biopsia renal. La sangre, los cilindros de glóbulos rojos (RBC) o las proteínas en la orina y la hipertensión son síntomas de glomerulonefritis. Puede ocurrir un cambio en las proteínas de la sangre con la disminución de ciertas fracciones del complemento sérico, un conjunto complejo de proteínas que interactúan involucradas en el sistema inmunológico, las defensas del huésped y las funciones de coagulación. La evidencia directa e indirecta respalda la importancia de los xenobióticos como factor causal de la glomerulonefritis.
El glomérulo evita que los glóbulos rojos que transportan oxígeno pasen a través de su filtro. Después de la centrifugación, la orina normal contiene solo un glóbulo rojo en 10 ml cuando se observa con un microscopio óptico de alta potencia. Cuando los glóbulos rojos se filtran a través del filtro glomerular y tal vez se vuelven dismórficos individualmente, se forman cilindros de glóbulos rojos que asumen la forma cilíndrica de las nefronas colectoras.
En apoyo de la importancia de las toxinas como factor etiológico en la glomerulonefritis, los estudios epidemiológicos revelan una mayor evidencia de exposiciones tóxicas en pacientes que se han sometido a diálisis o que han sido diagnosticados con glomerulonefritis. La evidencia de lesión glomerular por exposición aguda a hidrocarburos es rara, pero se ha observado en estudios epidemiológicos, con cocientes de probabilidades que oscilan entre 2.0 y 15.5. Un ejemplo de toxicidad aguda es la enfermedad de Goodpasture, que resulta de la estimulación con hidrocarburos de la producción de anticuerpos contra las proteínas del hígado y los pulmones que reaccionan de forma cruzada con la membrana basal. La exacerbación del síndrome nefrótico, grandes cantidades de proteína en la orina, también se ha observado en individuos expuestos nuevamente a solventes orgánicos, mientras que otros estudios revelan una relación histórica con un espectro de trastornos renales. Otros disolventes, como los agentes desengrasantes, las pinturas y los pegamentos, están implicados en formas más crónicas de la enfermedad. El conocimiento de los mecanismos de excreción y reabsorción de solventes ayuda a identificar biomarcadores porque incluso un daño mínimo en los glomérulos da como resultado una mayor fuga de glóbulos rojos en la orina. Aunque los glóbulos rojos en la orina son un signo cardinal de lesión glomerular, es importante descartar otras causas de hematuria.
Nefritis intersticial y tubular. Como se mencionó anteriormente, la etiología de la enfermedad renal crónica terminal suele ser difícil de determinar. Puede ser de origen principalmente glomerular, tubular o intersticial y ocurrir debido a múltiples episodios agudos o procesos crónicos de dosis bajas. La nefritis intersticial crónica implica fibrosis y atrofia tubular. En su forma aguda, la enfermedad se expresa por un marcado infiltrado inflamatorio acompañado de una acumulación de líquido en los espacios intersticiales. La nefritis intersticial puede afectar principalmente al intersticio, o manifestarse como un evento secundario de una lesión tubular crónica, o puede deberse a causas posrenales, como la obstrucción. La prostaglandina-A sintasa, una enzima, se encuentra principalmente en el intersticio y está asociada con el retículo endoplásmico, una parte de la maquinaria proteica de la célula. Ciertos xenobióticos, como la bencidina y los nitrofuranos, son cosustratos reductores de la prostaglandina sintasa y son tóxicos para el intersticio tubular.
Se pueden producir lesiones tubulares e intersticiales por exposición a cadmio, plomo o una variedad de disolventes orgánicos. La mayoría de las exposiciones son crónicas, a dosis bajas y la toxicidad queda enmascarada por la reserva de función renal y la capacidad del riñón para recuperar algunas funciones. La nefritis intersticial también puede deberse a una lesión vascular causada, por ejemplo, por una exposición crónica al monóxido de carbono. Las células del túbulo proximal son las más vulnerables a las sustancias tóxicas en la sangre debido a la intensa exposición a las toxinas que se filtran a través del glomérulo, los sistemas enzimáticos internos que activan las sustancias tóxicas y el transporte selectivo de sustancias tóxicas. El epitelio en los diversos segmentos del túbulo proximal tiene cualidades ligeramente diferentes de enzimas peroxidasa lisosomal y otros compuestos de la maquinaria genética. Por lo tanto, la exposición al cromo puede provocar lesiones tanto intersticiales como tubulares. El daño a los túbulos colectores puede ocurrir cuando enzimas específicas activan varios xenobióticos como cloroformo, paracetamol y p-aminofenol, y antibióticos como Loradine. Un resultado secundario del daño a los conductos colectores es la incapacidad del riñón para acidificar la orina y el subsiguiente desarrollo de un estado ácido metabólico.
Diabetes insípida nefrogénica, la condición en la que la orina se vuelve diluida, puede ser genética o adquirida. La forma genética implica mutaciones de los receptores ADH que se localizan en la membrana lateral basal de los conductos colectores, en el asa descendente de Henle. ADH afina la reabsorción de agua y ciertos iones como el potasio. La diabetes insípida adquirida puede afectar las células del túbulo o el intersticio asociado, los cuales pueden estar afectados por una variedad de condiciones. La diabetes insípida nefrogénica puede acompañar a la nefropatía terminal debido a la afectación difusa del intersticio. En consecuencia, el intersticio no puede mantener un entorno hipertónico para el movimiento pasivo del agua desde los conductos colectores tubulares. Las condiciones que pueden causar cambios intersticiales difusos son la pielonefritis, la anemia de células falciformes y la uropatía obstructiva. La posible asociación de estas condiciones en relación con la exposición ocupacional es una mayor susceptibilidad del riñón a los xenobióticos. Se ha identificado un número limitado de compuestos nefrotóxicos que se dirigen especialmente a las células del túbulo colector. La frecuencia, la nicturia (micción más frecuente por la noche) y la polidipsia (sed crónica) son síntomas de la diabetes insípida nefrogénica. El movimiento de fluidos a través de las células del conducto colector da como resultado canales que se forman en respuesta a la ADH, lo que afecta la función microtubular de las células; en consecuencia, fármacos como la colchicina pueden afectar la ADH. Dos fármacos que parecen actuar mediante mecanismos ligeramente diferentes para corregir la ADH son la hidroclorotiazida y la indometacina, un inhibidor de la prostaglandina sintasa.
La diabetes insípida inducida por litio se correlaciona con la duración de la terapia con litio, el nivel sérico promedio de litio y la dosis total de carbonato de litio. Curiosamente, el litio se concentra en los conductos colectores y afecta al AMP cíclico, parte de la vía de la bomba metabólica de energía. La exposición a otros compuestos como metoxiflurano y demeclociclina, el último de los cuales se usa para el tratamiento del acné, también produce diabetes insípida nefrogénica a través de una vía alternativa que hace que las células epiteliales no respondan a la ADH.
Hipertensión, o presión arterial elevada, la segunda causa más común de enfermedad renal terminal, se asocia con múltiples vías etiológicas. La hipertensión puede ser causada por nefropatía diabética, nefropatía obstructiva, glomerulonefritis, poliquistosis renal, pielonefritis y vasculitis, y muchas de esas enfermedades están asociadas con la exposición a compuestos tóxicos. Un número limitado de exposiciones ocupacionales están directamente asociadas con la hipertensión. Uno es el plomo, que causa isquemia y lesiones vasculares renales. El mecanismo de la hipertensión inducida por plomo probablemente esté regulado por el aparato yuxtaglomerular, la liberación de renina y la escisión de la renina por las enzimas hepáticas en angiotensina II. Los fármacos implicados en la hipertensión incluyen anfetaminas, estrógenos y anticonceptivos orales, esteroides, cis-platino, alcohol y antidepresivos tricíclicos. La hipertensión puede ser de inicio gradual o de naturaleza aguda y maligna. La hipertensión maligna en la que la presión diastólica es superior a 110 mm Hg se asocia a náuseas, vómitos y cefalea intensa, y constituye una urgencia médica. Hay numerosos fármacos disponibles para el tratamiento de la hipertensión, pero el tratamiento excesivo puede provocar una disminución de la perfusión renal y una mayor pérdida de la función renal. Siempre que sea posible, la retirada del nefrotóxico es el tratamiento de elección.
Diagnóstico diferencial de hematuria y proteinuria
La hematuria (glóbulos rojos en la orina) y la piuria (glóbulos blancos en la orina) son síntomas primarios de muchas enfermedades del sistema urinario-renal, y para fines categóricos pueden considerarse biomarcadores celulares no específicos. Debido a su importancia, se analizan por separado aquí. Un desafío para el médico ocupacional es determinar si la hematuria significa una condición médica subyacente permanente que puede ser potencialmente mortal o si es atribuible a exposiciones ocupacionales. La evaluación clínica de la hematuria requiere estandarización y determinación de si es de origen prerrenal, renal o posrenal.
La hematuria puede derivarse de lesiones en el riñón per se o en cualquier lugar a lo largo del trayecto de la orina. Los sitios de origen incluyen el riñón, la pelvis renal colectora, los uréteres, la vejiga, la próstata y la uretra. Debido a las enfermedades graves asociadas con la hematuria, un solo episodio justifica una evaluación médica o urológica. Más de un glóbulo rojo por campo de gran aumento puede ser una señal de enfermedad, pero se puede pasar por alto una hematuria significativa en el análisis microscópico en presencia de orina hipotónica (diluida) que puede lisar los glóbulos rojos. La pseudo-hematuria puede ser causada por remolachas, bayas, colorantes vegetales y uratos concentrados. La hematuria inicial sugiere un origen uretral, la hematuria terminal suele ser de origen prostático y la sangre durante la micción proviene de la vejiga, el riñón o el uréter. La hematuria macroscópica se asocia a tumores vesicales en el 21% de los casos, pero la hematuria microscópica se asocia con mucha menos frecuencia (2.2 a 12.5%).
Encontrar células dismórficas cuando se evalúa cuantitativamente la hematuria sugiere un origen del tracto superior, particularmente cuando se asocia con cilindros de glóbulos rojos. Comprender la hematuria en relación con la proteinuria proporciona información adicional. El dispositivo de filtración glomerular excluye casi por completo las proteínas de un peso molecular superior a 250,000 Daltons, mientras que las proteínas de bajo peso molecular se filtran libremente y se absorben normalmente por las células del túbulo. La presencia de proteínas de alto peso molecular en la orina sugiere hemorragia del tracto inferior, mientras que las proteínas de bajo peso molecular se asocian con lesión tubular. La evaluación de la proporción de α-microglobulina a albúmina y α-macroglobulina a albúmina ayuda a delinear la nefropatía intersticial glomerular de la tubular y la hemorragia del tracto inferior potencialmente asociada con la neoplasia urotelial y otras causas posrenales, como las infecciones del tracto urinario.
Surge un problema de diagnóstico especial cuando dos o más procesos de enfermedad que causan los mismos síntomas están presentes al mismo tiempo. Por ejemplo, la hematuria se observa tanto en la neoplasia urotelial como en las infecciones del tracto urinario. En un paciente con ambas enfermedades, si la infección es tratada y resuelta, el cáncer permanecería. Por lo tanto, es importante identificar la verdadera causa de los síntomas. La hematuria está presente en el 13 % de las poblaciones examinadas; aproximadamente el 20% de las personas tienen trastornos renales o vesicales significativos y el 10% de ellos desarrollarán una neoplasia maligna genitourinaria. En consecuencia, la hematuria es un importante biomarcador de enfermedad que debe evaluarse adecuadamente.
La interpretación clínica de la hematuria se ve reforzada por el conocimiento de la edad y el sexo del paciente, como se indica en la Tabla 2, que muestra las causas de la hematuria en relación con la edad y el sexo del paciente. Otras causas de hematuria incluyen trombosis de la vena renal, hipercalciuria y vasculitis, así como traumatismos como trotar u otros deportes y eventos o exposiciones ocupacionales. La evaluación clínica de la hematuria requiere una radiografía del riñón, pielografía intravenosa (PIV), para descartar enfermedades del tracto superior, incluidos cálculos renales y tumores, y una cistoscopia (observación de la vejiga a través de un instrumento iluminado) para descartar vejiga, próstata o urotelio. cánceres Las causas vaginales sutiles deben excluirse en las mujeres. Independientemente de la edad del paciente, está indicada una evaluación clínica si se produce hematuria y, dependiendo de la etiología identificada, pueden estar indicadas evaluaciones de seguimiento secuenciales.
Tabla 2. Causas más frecuentes de hematuria por edad y sexo
| 0–20 años | 40–60 años (mujeres) |
| Glomerulonefritis aguda Infección aguda del tracto urinario Anomalías congénitas del tracto urinario con obstrucción |
Infección aguda del tracto urinario Cálculos Tumor de vejiga |
| 20–40 años | 60+ años (hombres) |
| Infección aguda del tracto urinario Cálculos Tumor de vejiga |
Hiperplasia prostática benigna Tumor de vejiga Infección aguda del tracto urinario |
| 40–60 años (hombres) | 60+ años (mujeres) |
| Tumor de vejiga Cálculos Infección aguda del tracto urinario |
Tumores de vejiga Infección aguda del tracto urinario |
Fuente: Wyker 1991.
El uso de biomarcadores identificados recientemente junto con la citología convencional para la evaluación de la hematuria ayuda a asegurar que no se pase por alto ninguna malignidad oculta o incipiente (consulte la siguiente sección sobre biomarcadores). Para el especialista ocupacional, es importante determinar si la hematuria es el resultado de una exposición tóxica o de una malignidad oculta. El conocimiento de la exposición y la edad del paciente son parámetros críticos para tomar una decisión de manejo clínico informada. Un estudio reciente ha demostrado que, juntos, la hematuria y el análisis de biomarcadores en células urinarias exfoliadas de la vejiga fueron los dos mejores marcadores para detectar lesiones vesicales premalignas. La hematuria se observa en todos los casos de lesión glomerular, solo en el 60% de los pacientes con cáncer de vejiga y solo en el 15% de los pacientes con neoplasias malignas del propio riñón. Por tanto, la hematuria sigue siendo un síntoma cardinal de la enfermedad renal y posrenal, pero el diagnóstico final puede ser complejo.
Pruebas de nefrotoxicidad: biomarcadores
Históricamente, el control de las toxinas en el entorno laboral ha sido el método principal para identificar el riesgo. Sin embargo, no se conocen todos los tóxicos y, por lo tanto, no se pueden controlar. Además, la susceptibilidad es un factor que determina si los xenobióticos afectarán a las personas.
Figura 2. Categorías de biomarcadores.
Los biomarcadores brindan nuevas oportunidades para definir el riesgo individual. Con fines descriptivos y para proporcionar un marco de interpretación, los biomarcadores se han clasificado de acuerdo con el esquema que se muestra en la Figura 2. Como en otras enfermedades, los biomarcadores de nefrotoxicidad y toxicidad genitourinaria pueden estar relacionados con la susceptibilidad, la exposición, el efecto o la enfermedad. Los biomarcadores pueden ser genotípicos o fenotípicos y pueden ser funcionales, celulares o solubles en orina, sangre u otros fluidos corporales. Ejemplos de marcadores solubles son proteínas, enzimas, citocinas y factores de crecimiento. Los biomarcadores pueden ensayarse como gen, mensaje o producto proteico. Estos sistemas variables se suman a la complejidad de la evaluación y selección de biomarcadores. Una ventaja de ensayar la proteína es que es la molécula funcional. El gen puede no estar transcrito y la cantidad de mensaje puede no corresponder al producto proteico. En la Tabla 3 se muestra una lista de criterios para la selección de biomarcadores.
Tabla 3. Criterios para la selección de biomarcadores
| Utilidad clínica | Consideraciones de ensayo |
| biomarcador fuerte | Estabilidad del reactivo |
| Sensibilidad | Costo del reactivo |
| Especificidad | Requisitos de fijación |
| Valor predictivo negativo | Reproducibilidad del ensayo |
| Valor predictivo positivo | Parámetros sensibles a la máquina |
| Rol funcional | Contribución al perfil de biomarcadores |
| Secuencia en oncogénesis | Adaptabilidad a la automatización |
Fuente: Hemstreet et al. 1996.
El compromiso científico internacional para mapear el genoma humano hecho posible por los avances en biología molecular estableció la base para identificar biomarcadores de susceptibilidad. La mayoría de los casos de enfermedades humanas, especialmente las que resultan de la exposición ambiental a sustancias tóxicas, involucran una constelación de genes que reflejan una marcada diversidad genética (polimorfismo genético). Un ejemplo de dicho producto génico, como se mencionó anteriormente, es el sistema enzimático oxidativo P-450 que puede metabolizar xenobióticos en el hígado, el riñón o la vejiga. Los factores de susceptibilidad también pueden controlar el mecanismo básico para la reparación del ADN, influir en la susceptibilidad de varias vías de señalización importantes para la tumorigénesis (es decir, factores de crecimiento) o estar relacionados con condiciones hereditarias que predisponen a la enfermedad. Un ejemplo importante de un factor de susceptibilidad hereditario es el fenotipo de acetilación lenta o rápida que regula la acetilación y la inactivación de ciertas aminas aromáticas que se sabe que causan cáncer de vejiga. Los biomarcadores de susceptibilidad pueden incluir no solo genes que regulan la activación de xenobióticos, sino también protooncogenes y oncogenes supresores. El control del crecimiento de las células tumorales implica varios sistemas complejos que interactúan. Estos incluyen un equilibrio de oncogenes positivos (proto) y oncogenes negativos (supresores). Los protooncogenes controlan el crecimiento y desarrollo celular normal, mientras que los oncogenes supresores controlan la división y diferenciación celular normal. Otros genes pueden contribuir a condiciones preexistentes, como la propensión a la insuficiencia renal provocada por condiciones subyacentes, como la poliquistosis renal.
Un biomarcador de exposición puede ser el propio xenobiótico, el metabolito metabólico o marcadores como los aductos de ADN. En algunos casos, el biomarcador puede unirse a una proteína. Los biomarcadores de exposición también pueden ser biomarcadores de efecto, si el efecto es transitorio. Si un biomarcador de efecto persiste, puede convertirse en un biomarcador de enfermedad. Los biomarcadores de efecto útiles tienen una alta asociación con un tóxico y son indicativos de exposición. Para la detección de enfermedades, la expresión del biomarcador en una secuencia cercana al inicio de la enfermedad tendrá la mayor especificidad. La sensibilidad y la especificidad esperadas de un biomarcador dependen del riesgo frente al beneficio de la intervención. Por ejemplo, un biomarcador como la actina F, un marcador de diferenciación de proteínas del citoesqueleto, que aparece alterado en la carcinogénesis temprana, puede tener poca especificidad para la detección de estados precancerosos porque no todos los individuos con un marcador anormal progresarán a la enfermedad. Sin embargo, puede ser útil para seleccionar individuos y monitorearlos mientras se someten a quimioprevención, siempre que la terapia no sea tóxica. Comprender el marco de tiempo y el vínculo funcional entre los biomarcadores individuales es extremadamente importante para la evaluación del riesgo individual y para comprender los mecanismos de carcinogénesis y nefrotoxicidad.
Biomarcadores de nefrotoxicidad
Los biomarcadores de nefrotoxicidad pueden estar relacionados con la etiología de la insuficiencia renal (es decir, prerrenal, renal o posrenal) y los mecanismos implicados en la patogenia del proceso. Este proceso incluye daño celular y reparación. La lesión tóxica puede afectar las células, los glomérulos, el intersticio o los túbulos con la liberación de los biomarcadores correspondientes. Los xenobióticos pueden afectar a más de un compartimento o pueden causar cambios en los biomarcadores debido a la interdependencia de las células dentro del compartimento. Los cambios inflamatorios, los procesos autoinmunes y los procesos inmunológicos promueven aún más la liberación de biomarcadores. Los xenobióticos pueden tener como objetivo un compartimento en algunas circunstancias y otro en diferentes condiciones. Un ejemplo es el mercurio, que es, de forma aguda, nefrotóxico para el túbulo proximal, mientras que de forma crónica afecta a las arteriolas. La respuesta a la lesión se puede dividir en varias categorías principales que incluyen hipertrofia, proliferación, degeneración (necrosis y apoptosis, o muerte celular programada) y alteraciones de la membrana.
La mayoría de los factores de susceptibilidad están relacionados con la enfermedad renal no asociada a xenobióticos. Sin embargo, el 10% de los casos de insuficiencia renal se atribuyen a exposiciones ambientales a compuestos tóxicos o a la inducción iatrogénica por diversos compuestos, como antibióticos, o procedimientos como la administración de contraste de rayos X de riñón a un diabético. En el lugar de trabajo, la identificación de la insuficiencia renal subclínica antes de un posible estrés nefrotóxico adicional tiene una utilidad práctica potencial. Si se sospecha que un compuesto es xenobiótico y produce un efecto específicamente en la vía causal de la enfermedad, existe la posibilidad de una intervención para revertir el efecto. Por lo tanto, los biomarcadores de efecto eliminan muchos de los problemas de calcular la exposición y definir la susceptibilidad individual. El análisis estadístico de los biomarcadores de efecto en relación con los biomarcadores de susceptibilidad y exposición debería mejorar la especificidad de los marcadores. Cuanto más específico sea el biomarcador de efecto, menor será el requisito de un tamaño de muestra grande para identificar científicamente las toxinas potenciales.
Los biomarcadores de efecto son la clase más importante de marcadores y relacionan la exposición con la susceptibilidad y la enfermedad. Anteriormente hemos abordado la combinación de biomarcadores celulares y solubles para diferenciar entre la hematuria que se origina en el tracto superior o en el tracto inferior. En la Tabla 4 se muestra una lista de biomarcadores solubles potencialmente relacionados con la nefrotoxicidad celular. Hasta la fecha, ninguno de ellos solo o como paneles de múltiples biomarcadores detecta la toxicidad subclínica con la sensibilidad adecuada. Algunos problemas con el uso de biomarcadores solubles son la falta de especificidad, la inestabilidad enzimática, el efecto de dilución de la orina, las variaciones en la función renal y las interacciones de proteínas no específicas que pueden enturbiar la especificidad del análisis.
Tabla 4. Biomarcadores potenciales relacionados con la lesión celular
|
Factores inmunológicos: -Anticuerpos humorales y fragmentos de anticuerpos; componentes de la cascada del complemento y factores de coagulación -Linfocitos celulares, fagocitos mononucleares y otros efectores derivados de la médula (esinófilos, basófilos, neutrófilos y plaquetas) Linfoquinas Antígenos mayores de histocompatibilidad Factores de crecimiento y citocinas: factor de crecimiento derivado de plaquetas, factor de crecimiento epidérmico, factor de crecimiento transformante (TGF), factor de necrosis tumoral, interleucina-1, etc. Mediadores lipídicos: prostaglandinas Endotelina |
Componentes de la matriz extracelular: -Colágenos -Procolágeno -Laminina -Fibronectina Especies reactivas de oxígeno y nitrógeno Factores de transcripción y protooncogenes: c-myc, c-fos, c-jun, c-Haras, c-Ki-ras y Egr-1 Proteínas de choque térmico |
Fuente: Finn, Hemstreet et al. en el Consejo Nacional de Investigación 1995.
Un factor de crecimiento soluble con aplicación clínica potencial es el factor de crecimiento epidérmico urinario (EGF), que puede ser excretado por el riñón y también está alterado en pacientes con carcinoma de células transicionales de la vejiga. Se ha investigado la cuantificación de las enzimas urinarias, pero su utilidad se ha visto limitada por la incapacidad para determinar el origen de la enzima y la falta de reproducibilidad del ensayo. El uso de enzimas urinarias y su aceptación generalizada ha sido lento debido a los criterios restrictivos mencionados anteriormente. Las enzimas evaluadas incluyen alaminopeptidasa, NAG y fosfatasa alcalina intestinal. NAG es quizás el marcador más ampliamente aceptado para monitorear la lesión de las células del túbulo proximal debido a su localización en el segmento S3 del túbulo. Debido a que se desconoce la célula de origen precisa y la causa patológica de la actividad enzimática urinaria, la interpretación de los resultados es difícil. Además, los fármacos, los procedimientos de diagnóstico y las enfermedades coexistentes, como el infarto de miocardio, pueden enturbiar la interpretación.
Un enfoque alternativo es usar biomarcadores de anticuerpos monoclonales para identificar y cuantificar las células tubulares en la orina de varias áreas del segmento de la nefrona. La utilidad de este enfoque dependerá del mantenimiento de la integridad de la célula para la cuantificación. Esto requiere una fijación y una manipulación de la muestra adecuadas. Ahora hay disponibles anticuerpos monoclonales que se dirigen a células del túbulo específicas y distinguen, por ejemplo, las células del túbulo proximal de las células del túbulo distal o las células del túbulo contorneado. La microscopía de transmisión no puede resolver de manera efectiva las diferencias entre los leucocitos y varios tipos de células tubulares en contraste con la microscopía electrónica que ha sido efectiva para detectar el rechazo de trasplantes. Técnicas como el análisis cuantitativo de imágenes de fluorescencia de alta velocidad de células tubulares teñidas con anticuerpos monoclonales deberían resolver este problema. En un futuro próximo, debería ser posible detectar la nefrotoxicidad subclínica con un alto grado de certeza a medida que se produce la exposición.
Biomarcadores de enfermedad maligna
Los cánceres sólidos surgen en muchos casos de un campo de células alteradas bioquímicamente que pueden o no estar alteradas histológica o citológicamente. Tecnologías como el análisis cuantitativo de imágenes de fluorescencia capaces de detectar biomarcadores asociados con condiciones premalignas con certeza brindan el horizonte para la quimioprevención dirigida. Las alteraciones bioquímicas pueden ocurrir en un proceso variado u ordenado. Fenotípicamente, estos cambios se expresan mediante una progresión morfológica gradual de atipia a displasia y finalmente a malignidad manifiesta. conocimiento de la “rol funcional” de un biomarcador y “cuando en la secuencia de tumorigénesis se expresa” ayuda a definir su utilidad para identificar enfermedades premalignas, realizar un diagnóstico temprano y desarrollar un panel de biomarcadores para predecir la recurrencia y la progresión del tumor. Un paradigma para la evaluación de biomarcadores está evolucionando y requiere la identificación de perfiles de biomarcadores únicos y múltiples.
El cáncer de vejiga parece desarrollarse a lo largo de dos vías separadas: una vía de bajo grado aparentemente asociada con alteraciones en el cromosoma 9 y una segunda vía asociada con el gen supresor P-53 alterado genéticamente en el cromosoma 17. Claramente, múltiples factores genéticos están relacionados con el desarrollo del cáncer. y definir los factores genéticos en cada individuo es una tarea difícil, particularmente cuando la vía genética debe estar vinculada a una complejidad de exposiciones quizás múltiples. En estudios epidemiológicos, las exposiciones durante intervalos prolongados han sido difíciles de reconstruir. Se están identificando baterías de marcadores fenotípicos y genotípicos para definir individuos en riesgo en cohortes ocupacionales. Un perfil de biomarcadores fenotípicos y su relación con el cáncer de vejiga se muestra en la Figura 3, que ilustra que la actina G, una proteína precursora de la proteína actina F del citoesqueleto, es un marcador de diferenciación temprana y puede estar seguida por alteraciones secuenciales de otros intermediarios. marcadores de punto final como M344, DD23 y ploidía de ADN. Quedan por determinarse los paneles de biomarcadores más fuertes para detectar enfermedades premalignas y cáncer manifiesto, y para el pronóstico. A medida que se definen los criterios bioquímicos sensibles a las máquinas, puede ser posible detectar el riesgo de enfermedad en puntos prescritos en el continuo de la enfermedad.
Figura 3. Cuatro biomarcadores, G-actina, P-300, DD23 y ADN, en relación con la progresión tumoral y la respuesta al tratamiento quirúrgico y quimioprevención.
Diagnóstico y manejo de la enfermedad renal-urinaria relacionada con el trabajo
Enfermedad renal preexistente
Los cambios en los sistemas de atención de la salud en todo el mundo ponen de relieve los problemas de asegurabilidad y protección de los trabajadores frente a una exposición adicional. La enfermedad renal preexistente significativa se manifiesta por un aumento de la creatinina sérica, glucosuria (azúcar en la orina), proteinuria, hematuria y orina diluida. Es necesario descartar inmediatamente causas sistémicas subyacentes como diabetes e hipertensión y, dependiendo de la edad del paciente, investigar otras etiologías congénitas como quistes múltiples en el riñón. Así, el análisis de orina, tanto tira reactiva como microscópico, para la detección de alteraciones bioquímicas y celulares, es de utilidad para el médico del trabajo. Las pruebas de creatinina sérica y aclaramiento de creatinina están indicadas si una hematuria, piuria o proteinuria significativas sugieren una patología subyacente.
Múltiples factores son importantes para evaluar el riesgo de progresión de la enfermedad crónica o insuficiencia renal aguda. La primera es la limitación inherente o adquirida del riñón para resistir la exposición a xenobióticos. La respuesta del riñón al nefrotóxico, como un aumento en la cantidad de tóxico absorbido o alteraciones en el metabolismo renal, puede estar influenciada por una condición preexistente. De particular importancia es una disminución en la función desintoxicante en los muy jóvenes o muy viejos. En un estudio, la susceptibilidad a la exposición ocupacional se correlacionó altamente con antecedentes familiares de enfermedad renal, lo que significa la importancia de la predisposición hereditaria. Las condiciones subyacentes, como la diabetes y la hipertensión, aumentan la susceptibilidad. Las condiciones raras, como el lupus eritematoso y la vasculitis, pueden ser factores de susceptibilidad adicionales. En la mayoría de los casos, el aumento de la susceptibilidad es multifactorial y frecuentemente implica una batería de agresiones que ocurren solas o simultáneamente. Por lo tanto, el médico del trabajo debe conocer los antecedentes familiares de enfermedad renal del paciente y las condiciones preexistentes que afectan la función renal, así como cualquier enfermedad vascular o cardíaca, particularmente en trabajadores de edad avanzada.
Fallo renal agudo
La insuficiencia renal aguda puede deberse a causas prerrenales, renales o posrrenales. La condición generalmente es causada por un insulto agudo que resulta en una pérdida rápida y progresiva de la función renal. Cuando se elimina el nefrotóxico o el factor causal desencadenante, se recupera progresivamente la función renal con una disminución gradual de la creatinina sérica y una mejor capacidad de concentración renal. En la Tabla 5 se muestra una lista de causas ocupacionales de insuficiencia renal aguda. La insuficiencia renal aguda por exposición a dosis altas de xenobióticos ha sido útil para señalar posibles causas etiológicas que también pueden contribuir a formas más crónicas de enfermedad renal progresiva. La insuficiencia renal aguda por obstrucción del tracto de salida causada por enfermedad benigna o malignidad es relativamente rara, pero las causas quirúrgicas pueden contribuir con mayor frecuencia. La ecografía de las vías superiores delimita el problema de la obstrucción, cualquiera que sea el factor contribuyente. La insuficiencia renal asociada con drogas o tóxicos ocupacionales da como resultado una tasa de mortalidad de aproximadamente 37%; el resto de los individuos afectados mejoran en varios grados.
Tabla 5. Principales causas de insuficiencia renal aguda de origen laboral
| isquemia renal | necrosis tubular | Hemoglobinuria, mioglobinuria |
| Choque traumático Choque anafiláctico Intoxicación aguda por monóxido de carbono Golpe de calor |
Mercurio Cromo Arsénico Ácido oxálico tartratos Etilenglicol Tetracloruro de carbono tetracloroetano |
Arsina Síndrome de aplastamiento Golpeado por un rayo |
Fuente: Crepet 1983.
La insuficiencia renal aguda puede atribuirse a una variedad de causas prerrenales que tienen como tema subyacente la isquemia renal resultante de una perfusión renal disminuida prolongada. La insuficiencia cardíaca y la obstrucción de la arteria renal son dos ejemplos. La necrosis tubular puede ser causada por un número cada vez mayor de nefrotóxicos presentes en el lugar de trabajo. Los herbicidas y pesticidas han sido implicados en una serie de estudios. En un informe reciente, el envenenamiento por cicuta resultó en la deposición de miosina y actina a partir de la descomposición de las células musculares en los túbulos y una disminución aguda de la función renal. El endosulfán, un insecticida, y el acetato de trifenilestaño (TPTA), un organoestaño, se clasificaron inicialmente como neurotoxinas, pero recientemente se informó que están asociados con la necrosis tubular. Los informes anecdóticos de casos adicionales ponen en perspectiva la necesidad de encontrar biomarcadores para identificar sustancias tóxicas subclínicas más sutiles que quizás aún no hayan resultado en exposiciones tóxicas a dosis altas.
Los signos y síntomas de insuficiencia renal aguda son: falta de diuresis (anuria); oliguria (disminución de la producción de orina); disminución de la capacidad de concentración renal; y/o un aumento del potasio sérico que puede detener el corazón en un estado relajado (paro diastólico). El tratamiento implica el apoyo clínico y, siempre que sea posible, la eliminación de la exposición al tóxico. El aumento del potasio sérico o la retención excesiva de líquidos son los dos indicadores principales para la hemodiálisis o la diálisis peritoneal, y la elección depende de la estabilidad cardiovascular del paciente y del acceso vascular para la hemodiálisis. El nefrólogo, médico especialista renal, es clave en la estrategia de manejo de estos pacientes que también pueden requerir la atención de un especialista en cirugía urológica.
El tratamiento a largo plazo de los pacientes después de la insuficiencia renal depende en gran medida del grado de recuperación y rehabilitación y del estado general de salud del paciente. Es deseable volver al trabajo limitado y evitar las condiciones que estresarán la condición subyacente. Los pacientes con hematuria persistente o piuria requieren un control cuidadoso, posiblemente con biomarcadores, durante los 2 años posteriores a la recuperación.
enfermedad renal cronica
La enfermedad renal crónica o en etapa terminal es con mayor frecuencia el resultado de un proceso subclínico crónico y en curso que involucra una multiplicidad de factores, la mayoría de los cuales son poco conocidos. La glomerulonefritis, las causas cardiovasculares y la hipertensión son los principales factores contribuyentes. Otros factores incluyen la diabetes y los nefrotóxicos. Los pacientes presentan elevaciones progresivas del nitrógeno ureico sérico en sangre, creatinina, potasio sérico y oliguria (disminución de la diuresis). Se necesitan biomarcadores mejorados o paneles de biomarcadores para identificar con mayor precisión la nefrotoxicidad subclínica. Para el médico ocupacional, los métodos de evaluación deben ser no invasivos, altamente específicos y reproducibles. Ningún biomarcador único ha cumplido hasta ahora estos criterios para ser práctico a gran escala clínica.
La enfermedad renal crónica puede resultar de una variedad de nefrotóxicos, cuya patogenia se comprende mejor para algunos que para otros. En la Tabla 6 se muestra una lista de nefrotóxicos y sitios de toxicidad. Como se mencionó, las toxinas pueden tener como objetivo los glomérulos, los segmentos de los túbulos o las células intersticiales. Los síntomas de la exposición a xenobióticos pueden incluir hematuria, piuria, glucosuria, aminoácidos en la orina, micción frecuente y disminución de la diuresis. No se han definido los mecanismos precisos del daño renal para muchos nefrotóxicos, pero la identificación de biomarcadores específicos de nefrotoxicidad debería ayudar a abordar este problema. Aunque la prevención de la vasoconstricción proporciona cierta protección al riñón, la lesión tubular persiste en la mayoría de los casos. Como ejemplo, la toxicidad del plomo es principalmente de origen vascular, mientras que el cromo en dosis bajas afecta las células del túbulo proximal. Estos compuestos parecen afectar la maquinaria metabólica de la célula. Se han implicado múltiples formas de mercurio en la nefrotoxicidad elemental aguda. El cadmio, a diferencia del mercurio y como muchos otros nefrotóxicos ocupacionales, se dirige primero a las células del túbulo proximal.
Tabla 6. Segmentos de la nefrona afectados por tóxicos seleccionados
|
Túbulo proximal Antibióticos -Cefalosporinas Los aminoglucósidos Antineoplásticos -Nitrosoureas -Cisplatino y análogos Agentes de contraste radiográfico hidrocarburos halogenados -Clorotrifluoroetileno -Hexafluoropropeno -Hexaclorobutadieno -tricloroetileno -Cloroformo -Tetracloruro de carbono Ácido maleico Citrinina Metales -Mercurio -Nitrato de uranilo -Cadmio -Cromo |
Glomérulo Complejos inmunes antibióticos aminoglucósidos Aminonucleósido de puromicina Adriamicina La penicilamina Túbulo distal/conducto colector -Litio -Tetraciclinas -Anfotericina -Fluoruro -metoxiflurano
Papila -Aspirina -fenacetina -Paracetamol -Agentes antiinflamatorios no esteroideos -2-bromoetilamina |
Fuente: Tarloff y Goldstein 1994.
Más...
Cánceres renales y urinarios
Cancer de RIÑON
Epidemiología
Históricamente, el cáncer de riñón se ha utilizado para referirse a todas las neoplasias malignas del sistema renal (carcinoma de células renales [RCC], ICD-9 189.0; pelvis renal, ICD-9 189.1; y uréter, ICD-9 189.2) o solo RCC. Esta categorización ha llevado a cierta confusión en los estudios epidemiológicos, lo que ha dado lugar a la necesidad de analizar los datos informados previamente. El RCC comprende del 75 al 80% del total, siendo el resto principalmente carcinomas de células de transición de la pelvis renal y el uréter. La separación de estos dos tipos de cáncer es adecuada ya que la patogenia del CCR y del carcinoma de células de transición es bastante diferente, y los factores de riesgo epidemiológicos son distintos, al igual que los signos y síntomas de las dos enfermedades. Esta sección se centra en RCC.
El principal factor de riesgo identificado para el cáncer de riñón es el tabaquismo, seguido de factores de riesgo ocupacionales y ambientales sospechados pero mal definidos. Se estima que la eliminación del tabaquismo disminuiría la incidencia de cáncer de riñón en un 30 a 40% en los países industrializados, pero los determinantes ocupacionales del CCR no están bien establecidos. Se ha estimado que el riesgo atribuible de la población debido a exposiciones ocupacionales está entre cero, según la carcinogénesis reconocida, y el 21 %, según un estudio multicéntrico de casos y controles en múltiples sitios en el área de Montreal de Canadá. Los primeros biomarcadores de efecto en asociación con los biomarcadores de exposición deberían ayudar a aclarar factores de riesgo importantes. En estudios epidemiológicos se ha encontrado que varias ocupaciones e industrias conllevan un mayor riesgo de cáncer renal. Sin embargo, con la posible excepción de los agentes utilizados en la limpieza en seco y las exposiciones en la refinación de petróleo, la evidencia disponible no es consistente. El análisis estadístico de los datos de exposición epidemiológica en relación con los biomarcadores de susceptibilidad y efecto aclarará causas etiológicas adicionales.
Varios estudios epidemiológicos han asociado industrias, ocupaciones y exposiciones ocupacionales específicas con mayores riesgos de carcinoma de células renales. El patrón que emerge de estos estudios no es completamente consistente. La refinación de petróleo, la imprenta, la limpieza en seco y la conducción de camiones son ejemplos de trabajos asociados con un riesgo excesivo de cáncer de riñón. Los agricultores generalmente muestran un menor riesgo de RCC, pero un estudio danés vinculó la exposición a largo plazo a insecticidas y herbicidas con un exceso de riesgo de RCC de casi cuatro veces. Este hallazgo requiere confirmación en datos independientes, incluida la especificación de la posible naturaleza causal de la asociación. Otros productos sospechosos de estar asociados con RCC incluyen: varios derivados de hidrocarburos y solventes; productos de la refinación del petróleo; productos derivados del petróleo, alquitrán y brea; escape de gasolina; combustible para aviones; emisiones de motores a reacción y diesel; compuestos de arsénico; cadmio; compuestos de cromo (VI); compuestos inorgánicos de plomo; y asbesto. Los estudios epidemiológicos han asociado la exposición ocupacional al vapor de gasolina con el riesgo de cáncer de riñón, algunos en forma de respuesta a la dosis, un fenómeno observado en la rata macho por exposición al vapor de gasolina sin plomo. Estos hallazgos ganan algo de peso potencial, dada la exposición humana generalizada a los vapores de gasolina en las estaciones de servicio minoristas y el reciente aumento en la incidencia de cáncer de riñón. La gasolina es una mezcla compleja de hidrocarburos y aditivos, incluido el benceno, que es un carcinógeno humano conocido.
El riesgo de cáncer de riñón no está consistentemente relacionado con la clase social, aunque un mayor riesgo ocasionalmente se ha asociado con un estatus socioeconómico más alto. Sin embargo, en algunas poblaciones se observó un gradiente inverso y en otras aún no surgió un patrón claro. Posiblemente estas variaciones pueden estar relacionadas con el estilo de vida. Los estudios con personas migrantes muestran una modificación en el riesgo de CCR hacia el nivel de la población del país de acogida, lo que sugiere que los factores ambientales son importantes en el desarrollo de esta malignidad.
A excepción del nefroblastoma (tumor de Wilms), que es un cáncer infantil, el cáncer de riñón suele aparecer después de los 40 años. Se estima que en 127,000 ocurrieron a nivel mundial 1.7 1985 nuevos casos de cáncer de riñón (incluidos el CCR y el carcinoma de células de transición (TCC) de la pelvis renal y el uréter), lo que corresponde al 1985 % de la incidencia mundial total de cáncer. La incidencia del cáncer de riñón varía entre las poblaciones . Se han informado tasas altas tanto para hombres como para mujeres en América del Norte, Europa, Australia y Nueva Zelanda; tasas bajas en Melanesia, África central y oriental y Asia sudoriental y oriental. La incidencia del cáncer de riñón ha ido en aumento en la mayoría de los países occidentales, pero se ha estancado en unos pocos. La incidencia de cáncer de riñón estandarizada por edad en XNUMX fue más alta en América del Norte y Europa occidental, septentrional y oriental, y más baja en África, Asia (excepto en hombres japoneses) y el Pacífico. El cáncer de riñón es más frecuente en hombres que en mujeres y se encuentra entre los diez cánceres más frecuentes en varios países.
El carcinoma de células de transición (CCT) de la pelvis renal se asocia con agentes etiológicos similares al cáncer de vejiga, que incluyen infección crónica, cálculos y analgésicos que contienen fenacetina. La nefropatía balcánica, una nefropatía lentamente progresiva, crónica y mortal que prevalece en los países balcánicos, se asocia con altas tasas de tumores de la pelvis renal y el uréter. Se desconocen las causas de la nefropatía de los Balcanes. La exposición excesiva a la ocratoxina A, que se considera posiblemente cancerígena para los seres humanos, se ha asociado con el desarrollo de la nefropatía de los Balcanes, pero no se puede excluir el papel de otros agentes nefrotóxicos. La ocratoxina A es una toxina producida por hongos que se pueden encontrar en muchos alimentos, en particular cereales y productos derivados del cerdo.
Detección y diagnóstico del cáncer de riñón
El patrón de signos y síntomas del CCR varía entre los pacientes, incluso hasta la etapa en que aparece la metástasis. Debido a la ubicación de los riñones y la movilidad de los órganos contiguos a la masa en expansión, estos tumores suelen ser muy grandes en el momento de la detección clínica. Aunque la hematuria es el síntoma principal del CCR, el sangrado ocurre tarde en comparación con los tumores de células de transición debido a la ubicación intrarrenal del CCR. El CCR ha sido considerado el “sueño del médico” pero la “maldición del cirujano” debido a la interesante constelación de síntomas relacionados con los síndromes paraneoplásicos. Se han notificado sustancias que aumentan el recuento de glóbulos rojos, calcio y factores que imitan la función anormal de las glándulas suprarrenales, y se han observado masa abdominal, pérdida de peso, fatiga, dolor, anemia, función hepática anormal e hipertensión. Los médicos solicitan una tomografía axial computarizada (TAC) del abdomen y una ecografía cada vez con mayor frecuencia, por lo que se estima que el 20 % de los CCR se diagnostican por casualidad como resultado de la evaluación de otros problemas médicos.
La evaluación clínica de un caso de RCC consiste en un examen físico para identificar una masa en el flanco, que ocurre en el 10% de los pacientes. Una radiografía de riñón con contraste puede delinear una masa renal y la naturaleza sólida o quística generalmente se aclara mediante ecografía o tomografía computarizada. Los tumores son muy vascularizados y tienen un aspecto característico cuando se inyecta en la arteria material de contraste radiopaco. La arteriografía se realiza para embolizar el tumor si es muy grande o para definir el suministro de sangre arterial si se prevé una nefrectomía parcial. La aspiración con aguja fina se puede utilizar para tomar muestras de RCC sospechoso.
Los tumores RCC localizados se extirpan quirúrgicamente con ganglios linfáticos regionales y, quirúrgicamente, es importante la ligadura temprana de la arteria y la vena. Sintomáticamente, el paciente puede mejorar al extirpar tumores grandes o sangrantes que han hecho metástasis, pero esto no mejora la supervivencia. Para los tumores metastásicos, el control del dolor localizado puede lograrse con radioterapia, pero el tratamiento de elección para la enfermedad metastásica son los modificadores de la respuesta biológica (interleucina-2 o α-interferón), aunque ocasionalmente la quimioterapia se usa sola o en combinación con otras terapias.
Marcadores como el gen del cáncer en el cromosoma 3 observado en familias con cáncer y en la enfermedad de von Hippel-Lindau pueden servir como biomarcadores de susceptibilidad. Aunque se han informado antígenos marcadores tumorales para el RCC, actualmente no hay forma de detectarlos de manera confiable en la orina o la sangre con sensibilidad y especificidad adecuadas. La baja prevalencia de esta enfermedad en la población general requiere una prueba de alta especificidad y sensibilidad para la detección temprana de la enfermedad. Las cohortes ocupacionales en riesgo podrían potencialmente ser examinadas con ultrasonido. La evaluación de este tumor sigue siendo un desafío para el científico básico, el epidemiólogo molecular y el médico por igual.
Cáncer de vejiga
Epidemiología
Más del 90% de los cánceres de vejiga en Europa y América del Norte son carcinomas de células de transición (TCC). El carcinoma de células escamosas y el adenocarcinoma representan el 5 y el 1%, respectivamente, del cáncer de vejiga en estas regiones. La distribución de tipos histopatológicos en el cáncer de vejiga es sorprendentemente diferente en regiones como el Medio Oriente y África, donde el cáncer de vejiga está asociado con la infección por esquistosomas. Por ejemplo, en Egipto, donde la esquistosomiasis es endémica y el cáncer de vejiga es el principal problema oncogénico, el tipo más común es el carcinoma de células escamosas, pero la incidencia de CCT está aumentando con el aumento de la prevalencia del tabaquismo. La discusión que sigue se centra en TCC.
El cáncer de vejiga sigue siendo una enfermedad de gran importancia. Representaba alrededor del 3.5% de todas las neoplasias malignas del mundo en 1980. En 1985, se estimó que el cáncer de vejiga ocupaba el puesto 11 en frecuencia a escala mundial, siendo el octavo cáncer más frecuente entre los hombres, con un total esperado de 243,000 casos nuevos. Hay una incidencia máxima en la séptima década de la vida y, en todo el mundo, la proporción entre hombres y mujeres es de alrededor de tres a uno. La incidencia ha ido en aumento en casi todas las poblaciones de Europa, especialmente en los hombres. En Dinamarca, donde las tasas de incidencia anual se encuentran entre las más altas del mundo, 45 por 100,000 12 en hombres y 100,000 por 8 9 en mujeres, la tendencia reciente ha sido un aumento adicional de 5 a XNUMX % cada XNUMX años. En Asia, las altísimas tasas entre los chinos de Hong Kong han disminuido constantemente, pero en ambos sexos la incidencia de cáncer de vejiga sigue siendo mucho más alta que en otras partes de Asia y más del doble que entre los chinos de Shanghái o Singapur. Las tasas de cáncer de vejiga entre los chinos en Hawái también son altas.
El tabaquismo es el factor etiológico individual más importante en el cáncer de vejiga, y las exposiciones ocupacionales ocupan el segundo lugar. Se ha estimado que el tabaco es responsable de un tercio de todos los casos de cáncer de vejiga fuera de las regiones donde prevalece la infección por esquistosomas. El número de casos de cáncer de vejiga atribuidos en 1985 al tabaquismo se ha estimado en más de 75,000 en todo el mundo y puede representar el 50% del cáncer de vejiga en las poblaciones occidentales. El hecho de que todas las personas que fuman cantidades similares no desarrollen cáncer de vejiga al mismo ritmo sugiere que los factores genéticos son importantes para controlar la susceptibilidad. Dos aminas aromáticas, 4-aminobifenilo y 2-naftilamina, son carcinógenos asociados con el tabaquismo; estos se encuentran en concentraciones más altas en el “tabaco negro” (curado al aire) que en la “mezcla de tabaco” (curado al aire caliente). El humo pasivo aumenta los aductos en la sangre y la relación dosis-respuesta de la formación de aductos se ha correlacionado con un mayor riesgo de cáncer de vejiga. Se han observado niveles más altos de formación de aductos en fumadores de cigarrillos que son acetiladores lentos en comparación con acetiladores rápidos, lo que sugiere que el estado de acetilación heredado genéticamente puede ser un biomarcador importante de susceptibilidad. La menor incidencia de cáncer de vejiga en razas negras en comparación con las razas blancas puede atribuirse a la conjugación de intermediarios metabólicos cancerígenos por sulfotransferasas que producen electrófilos. Los sulfatos fenólicos desintoxicados pueden proteger el urotelio. Se ha informado que la actividad de la sulfotransferasa hepática para las N-hidroxiarilaminas es mayor en los negros que en los blancos. Esto puede resultar en una disminución en la cantidad de N-hidroximetabolitos libres para funcionar como carcinógenos.
El cáncer de vejiga ocupacional es uno de los primeros cánceres ocupacionales conocidos y mejor documentados. El primer caso identificado de cáncer de vejiga ocupacional apareció unos 20 años después del inicio de la industria de tintes sintéticos en Alemania. Numerosas otras ocupaciones han sido identificadas en los últimos 25 años como riesgos laborales de cáncer de vejiga. Las exposiciones ocupacionales pueden contribuir hasta en un 20% de los cánceres de vejiga. Los trabajadores ocupacionalmente expuestos incluyen aquellos que trabajan con brea de hulla, gasificación de carbón y producción de caucho, aluminio, auramina y magenta, así como también aquellos que trabajan como peluqueros y barberos. Se ha demostrado que las aminas aromáticas causan cáncer de vejiga en los trabajadores de muchos países. Entre esta clase de productos químicos destacan la 2-naftilamina, la bencidina, el 4-nitrobifenilo y la 3,3r´-diclorobencidina. Otras dos aminas aromáticas, la 4,4´-metilendianilina (MDA) y la 4,4´-metilen-bis-2-cloroanilina (MOCA) se encuentran entre los carcinógenos de la vejiga más utilizados. Otros carcinógenos asociados con exposiciones industriales son en gran parte indeterminados; sin embargo, las aminas aromáticas están frecuentemente presentes en el lugar de trabajo.
Detección y diagnóstico del cáncer de vejiga
La detección del cáncer de vejiga continúa recibiendo atención en la búsqueda para diagnosticar el cáncer de vejiga antes de que se vuelva sintomático y, presumiblemente, menos susceptible de tratamiento curativo. La citología de orina miccional y el análisis de orina para hematuria se han considerado pruebas de detección candidatas. Una pregunta fundamental para la detección es cómo identificar los grupos de alto riesgo y luego a las personas dentro de estos grupos. Los estudios epidemiológicos identifican grupos en riesgo, mientras que los biomarcadores identifican potencialmente a individuos dentro de grupos. En general, la detección ocupacional del cáncer de vejiga con pruebas de hematuria y citología de Papanicolaou ha sido ineficaz.
La detección mejorada del cáncer de vejiga puede ser posible mediante la prueba de hemastick de 14 días descrita por Messing y colaboradores. Se observó una prueba positiva al menos una vez en el 84 % de 31 pacientes con cáncer de vejiga al menos 2 meses antes del diagnóstico cistoscópico de la enfermedad. Esta prueba tiene una tasa de falsos positivos del 16 al 20% y la mitad de estos pacientes no tienen enfermedad urológica. El bajo costo puede hacer de esta una prueba útil en una pantalla de dos niveles en combinación con biomarcadores y citología (Waples y Messing 1992).
En un estudio reciente, el anticuerpo monoclonal DD23 mediante análisis cuantitativo de imágenes de fluorescencia detectó cáncer de vejiga en células uroepiteliales exfoliadas. Se logró una sensibilidad del 85 % y una especificidad del 95 % en una mezcla de carcinomas de células de transición de bajo y alto grado, incluidos los tumores TaT1. El antígeno asociado al tumor M344 junto con la ploidía del ADN tenía una sensibilidad cercana al 90 %.
Estudios recientes indican que combinar biomarcadores con pruebas de hematuria puede ser el mejor enfoque. En la Tabla 1 se resume una lista de las aplicaciones de la citología urinaria de fluorescencia cuantitativa en combinación con biomarcadores. Los cambios celulares tempranos genéticos, bioquímicos y morfológicos asociados con condiciones premalignas respaldan el concepto de que las personas en riesgo pueden identificarse años antes del desarrollo de una enfermedad manifiesta. malignidad. Los biomarcadores de susceptibilidad en combinación con biomarcadores de efecto prometen detectar individuos en riesgo con una precisión aún mayor. Estos avances son posibles gracias a las nuevas tecnologías capaces de cuantificar los cambios moleculares fenotípicos y genotípicos a nivel de una sola célula, identificando así a los individuos en riesgo. La evaluación del riesgo individual facilita el control estratificado y rentable de grupos seleccionados para la quimioprevención dirigida.
Tabla 1. Aplicaciones de la citología urinaria
Detección de CIS1 y cáncer de vejiga
Seguimiento de la terapia quirúrgica:
Monitoreo de la vejiga después de TURBT2
Monitoreo del tracto urinario superior
Monitoreo de remanente uretral
Monitoreo de la derivación urinaria
Monitoreo de la terapia intravesical
Selección de la terapia intravesical
Supervisión del efecto de la terapia con láser
Evaluación de pacientes con hematuria
Establecer la necesidad de una cistoscopia
Detección de poblaciones de alto riesgo:
Grupos de exposición ocupacional
Grupos de abuso de drogas en riesgo de cáncer de vejiga
Criterios de decisión para:
Cistectomía
Resección ureteral segmentaria versus nefroureterectomía
Otras indicaciones:
Detección de fístula vesicoentérica
Tumores extraurológicos que invaden el tracto urinario
Definición de agentes quimiopreventivos eficaces
Vigilancia de la quimioterapia eficaz
1 CIS, carcinoma in situ.
2 TURBT, resección transuretral por tumor vesical.
Fuente: Hemstreet et al. 1996.
Los signos y síntomas del cáncer de vejiga son similares a los de la infección del tracto urinario y pueden incluir dolor al orinar, evacuación frecuente y sangre y pus en la orina. Debido a que los síntomas de una infección del tracto urinario pueden presagiar un tumor de vejiga, particularmente cuando se asocian con hematuria macroscópica en pacientes mayores, se necesita la confirmación de la presencia de bacterias y una gran conciencia por parte del médico examinador. Cualquier paciente tratado por una infección del tracto urinario que no se resuelve de inmediato debe ser derivado a un especialista en urología para una evaluación adicional.
La evaluación diagnóstica del cáncer de vejiga primero requiere una pielografía intravenosa (PIV) para excluir una enfermedad del tracto superior en la pelvis renal o los uréteres. La confirmación del cáncer de vejiga requiere observar la vejiga con una luz (cistoscopio) con múltiples biopsias realizadas con un instrumento iluminado a través de la uretra para determinar si el tumor es no invasivo (es decir, papilar o CIS) o invasivo. Las biopsias aleatorias de la vejiga y la uretra prostática ayudan a definir la cancerización del campo y los cambios del efecto de campo. Los pacientes con enfermedad no invasiva requieren una estrecha vigilancia, ya que corren el riesgo de recurrencias posteriores, aunque la progresión de estadio y grado es poco común. Los pacientes que presentan cáncer de vejiga que ya es de alto grado o invasivo en la lámina propia tienen un riesgo igualmente alto de recurrencia, pero la progresión de la etapa es mucho más probable. Por lo tanto, suelen recibir instilación intravesical de agentes inmuno o quimioterapéuticos después de la resección transuretral. Los pacientes con tumores que invaden la capa muscular propia o más allá tienen muchas más probabilidades de tener metástasis y rara vez pueden tratarse con medios conservadores. Sin embargo, incluso cuando se trata con cistectomía total (la terapia estándar para el cáncer de vejiga que invade los músculos), entre el 20 y el 60 % finalmente sucumben a la enfermedad, casi siempre debido a la metástasis. Cuando la metástasis regional o distal está presente en el momento del diagnóstico, las tasas de supervivencia a 5 años caen al 35 y 9%, respectivamente, a pesar del tratamiento agresivo. La quimioterapia sistémica para el cáncer de vejiga metastásico está mejorando con tasas de respuesta completa informadas del 30 %. Estudios recientes sugieren que la quimioterapia antes de la cistectomía puede mejorar la supervivencia en pacientes seleccionados.
La estadificación del cáncer de vejiga predice el potencial biológico de progresión, metástasis o recurrencia en el 70% de los casos. La estadificación del cáncer de vejiga generalmente requiere una tomografía computarizada para descartar metástasis en el hígado, una gammagrafía ósea con radioisótopos para excluir la diseminación al hueso y una radiografía de tórax o una tomografía computarizada para excluir la metástasis pulmonar. Continúa la búsqueda de biomarcadores en el tumor y el campo del cáncer de vejiga que predecirán qué tumores harán metástasis o reaparecerán. La accesibilidad de las células vesicales exfoliadas en muestras anuladas es prometedora para el uso de biomarcadores para monitorear la recurrencia y para la prevención del cáncer.
Sistema Reproductivo: Introducción
La toxicidad reproductiva masculina y femenina son temas de creciente interés en la consideración de los riesgos para la salud ocupacional. Toxicidad reproductiva ha sido definida como la ocurrencia de efectos adversos en el sistema reproductivo que pueden resultar de la exposición a agentes ambientales. La toxicidad puede expresarse como alteraciones en los órganos reproductores y/o el sistema endocrino relacionado. Las manifestaciones de tal toxicidad pueden incluir:
- alteraciones en el comportamiento sexual
- fertilidad reducida
- resultados adversos del embarazo
- modificaciones de otras funciones que dependen de la integridad del sistema reproductivo.
Los mecanismos subyacentes a la toxicidad para la reproducción son complejos. Se han probado más sustancias xenobióticas y se ha demostrado que son tóxicas para el proceso reproductivo masculino que para el femenino. Sin embargo, no se sabe si esto se debe a las diferencias subyacentes en la toxicidad oa la mayor facilidad para estudiar los espermatozoides que los ovocitos.
Toxicidad para el desarrollo
La toxicidad para el desarrollo se ha definido como la aparición de efectos adversos en el organismo en desarrollo que pueden resultar de la exposición antes de la concepción (cualquiera de los padres), durante el desarrollo prenatal o después del nacimiento hasta el momento de la maduración sexual. Los efectos adversos del desarrollo pueden detectarse en cualquier momento de la vida del organismo. Las principales manifestaciones de la toxicidad del desarrollo incluyen:
- muerte del organismo en desarrollo
- anormalidad estructural
- crecimiento alterado
- deficiencia funcional.
En la siguiente discusión, toxicidad del desarrollo se utilizará como un término que incluye todo para referirse a las exposiciones a la madre, el padre o el producto de la concepción que conducen a un desarrollo anormal. El termino teratogénesis se utilizará para referirse más específicamente a las exposiciones del concepto que producen una malformación estructural. Nuestra discusión no incluirá los efectos de las exposiciones postnatales en el desarrollo.
Mutagénesis
Además de la toxicidad reproductiva, la exposición a cualquiera de los padres antes de la concepción tiene el potencial de resultar en defectos de desarrollo a través de mutagénesis, cambios en el material genético que se transmite de padres a hijos. Dichos cambios pueden ocurrir a nivel de genes individuales oa nivel cromosómico. Los cambios en los genes individuales pueden dar como resultado la transmisión de mensajes genéticos alterados, mientras que los cambios a nivel cromosómico pueden dar como resultado la transmisión de anomalías en el número o la estructura de los cromosomas.
Es interesante que algunas de las pruebas más sólidas del papel de las exposiciones previas a la concepción en las anomalías del desarrollo provienen de estudios de exposiciones paternas. Por ejemplo, el síndrome de Prader-Willi, un defecto congénito caracterizado por hipotonicidad en el período neonatal y, posteriormente, obesidad marcada y problemas de conducta, se ha asociado con exposiciones ocupacionales paternas a hidrocarburos. Otros estudios han mostrado asociaciones entre exposiciones paternas previas a la concepción a agentes físicos y malformaciones congénitas y cánceres infantiles. Por ejemplo, la exposición ocupacional paterna a la radiación ionizante se ha asociado con un mayor riesgo de defectos del tubo neural y un mayor riesgo de leucemia infantil, y varios estudios han sugerido asociaciones entre la exposición ocupacional paterna a campos electromagnéticos antes de la concepción y los tumores cerebrales infantiles (Gold y Sever 1994). ). Al evaluar los riesgos reproductivos y de desarrollo de las exposiciones en el lugar de trabajo, se debe prestar mayor atención a los posibles efectos entre los hombres.
Es muy probable que algunos defectos de etiología desconocida involucren un componente genético que puede estar relacionado con la exposición de los padres. Debido a las asociaciones demostradas entre la edad del padre y las tasas de mutación, es lógico creer que otros factores y exposiciones paternos pueden estar asociados con mutaciones genéticas. La asociación bien establecida entre la edad materna y la no disyunción cromosómica, que da como resultado anomalías en el número cromosómico, sugiere un papel significativo de las exposiciones maternas en las anomalías cromosómicas.
A medida que aumenta nuestra comprensión del genoma humano, es probable que podamos rastrear más defectos de desarrollo hasta cambios mutagénicos en el ADN de genes individuales o cambios estructurales en porciones de cromosomas.
teratogénesis
Los efectos adversos sobre el desarrollo humano de la exposición del producto de la concepción a agentes químicos exógenos han sido reconocidos desde el descubrimiento de la teratogenicidad de la talidomida en 1961. Wilson (1973) ha desarrollado seis "principios generales de teratología" que son relevantes para esta discusión. Estos principios son:
- Las manifestaciones finales del desarrollo anormal son la muerte, la malformación, el retraso del crecimiento y el trastorno funcional.
- La susceptibilidad del producto de la concepción a los agentes teratogénicos varía según la etapa de desarrollo en el momento de la exposición.
- Los agentes teratogénicos actúan de maneras específicas (mecanismos) sobre células y tejidos en desarrollo al iniciar la embriogénesis anormal (patogénesis).
- Las manifestaciones de desarrollo anormal aumentan en grado desde el nivel sin efecto hasta el nivel totalmente letal a medida que aumenta la dosis.
- El acceso de las influencias ambientales adversas a los tejidos en desarrollo depende de la naturaleza del agente.
- La susceptibilidad a un teratógeno depende del genotipo del embrión y de la forma en que el genotipo interactúa con los factores ambientales.
Los primeros cuatro de estos principios se discutirán con mayor detalle, al igual que la combinación de los principios 1, 2 y 4 (resultado, tiempo de exposición y dosis).
Espectro de resultados adversos asociados con la exposición
Hay un espectro de resultados adversos potencialmente asociados con la exposición. Estudios ocupacionales que se enfocan en un solo resultado de riesgo pasando por alto otros efectos reproductivos importantes.
La Figura 1 enumera algunos ejemplos de resultados de desarrollo potencialmente asociados con la exposición a teratógenos ocupacionales. Los resultados de algunos estudios ocupacionales han sugerido que las malformaciones congénitas y los abortos espontáneos están asociados con las mismas exposiciones, por ejemplo, gases anestésicos y solventes orgánicos.
El aborto espontáneo es un resultado importante a considerar porque puede resultar de diferentes mecanismos a través de varios procesos patogénicos. Un aborto espontáneo puede ser el resultado de toxicidad para el embrión o el feto, alteraciones cromosómicas, efectos de un solo gen o anomalías morfológicas. Es importante tratar de diferenciar entre conceptos cariotípicamente normales y anormales en estudios de abortos espontáneos.
Figura 1. Anormalidades del desarrollo y resultados reproductivos potencialmente asociados con exposiciones ocupacionales.
Momento de la exposición
El segundo principio de Wilson relaciona la susceptibilidad al desarrollo anormal con el tiempo de exposición, es decir, la edad gestacional del concepto. Este principio ha sido bien establecido para la inducción de malformaciones estructurales y los períodos sensibles para la organogénesis son conocidos para muchas estructuras. Teniendo en cuenta una gama ampliada de resultados, el período sensible durante el cual se puede inducir cualquier efecto debe extenderse a lo largo de la gestación.
Al evaluar la toxicidad del desarrollo ocupacional, la exposición debe determinarse y clasificarse para el período crítico apropiado, es decir, la(s) edad(es) gestacional(es), para cada resultado. Por ejemplo, es probable que los abortos espontáneos y las malformaciones congénitas estén relacionados con la exposición en el primer y segundo trimestre, mientras que el bajo peso al nacer y los trastornos funcionales como los trastornos convulsivos y el retraso mental tienen más probabilidades de estar relacionados con la exposición en el segundo y tercer trimestre.
Mecanismos teratogénicos
El tercer principio es la importancia de considerar los mecanismos potenciales que podrían iniciar la embriogénesis anormal. Se han sugerido varios mecanismos diferentes que podrían conducir a la teratogénesis (Wilson 1977). Éstas incluyen:
- cambios mutacionales en las secuencias de ADN
- anomalías cromosómicas que conducen a cambios estructurales o cuantitativos en el ADN
- alteración o inhibición del metabolismo intracelular, por ejemplo, bloqueos metabólicos y falta de coenzimas, precursores o sustratos para la biosíntesis
- interrupción de la síntesis de ADN o ARN
- interferencia con la mitosis
- interferencia con la diferenciación celular
- fracaso de las interacciones célula a célula
- fracaso de las migraciones celulares
- muerte celular por efectos citotóxicos directos
- efectos sobre la permeabilidad de la membrana celular y los cambios osmolares
- disrupción física de células o tejidos.
Al considerar los mecanismos, los investigadores pueden desarrollar agrupaciones de resultados biológicamente significativas. Esto también puede proporcionar información sobre posibles teratógenos; por ejemplo, las relaciones entre carcinogénesis, mutagénesis y teratogénesis se han discutido durante algún tiempo. Desde la perspectiva de evaluar los riesgos reproductivos ocupacionales, esto es de particular importancia por dos razones distintas: (1) las sustancias que son cancerígenas o mutagénicas tienen una mayor probabilidad de ser teratogénicas, lo que sugiere que se debe prestar especial atención a los efectos reproductivos de tales sustancias y (2) los efectos sobre el ácido desoxirribonucleico (ADN), que producen mutaciones somáticas, se cree que son mecanismos tanto para la carcinogénesis como para la teratogénesis.
Dosis y Resultado
El cuarto principio relacionado con la teratogénesis es la relación entre el resultado y la dosis. Este principio está claramente establecido en muchos estudios con animales, y Selevan (1985) ha discutido su relevancia potencial para la situación humana, señalando la importancia de múltiples resultados reproductivos dentro de rangos de dosis específicos y sugiriendo que una relación dosis-respuesta podría reflejarse en un aumento tasa de un resultado particular con el aumento de la dosis y/o un cambio en el espectro de los resultados observados.
Con respecto a la teratogénesis y la dosis, existe una preocupación considerable acerca de los trastornos funcionales resultantes de los posibles efectos conductuales de la exposición prenatal a agentes ambientales. La teratología del comportamiento animal se está expandiendo rápidamente, pero la teratología ambiental del comportamiento humano se encuentra en una etapa relativamente temprana de desarrollo. En la actualidad, existen limitaciones críticas en la definición y determinación de los resultados conductuales apropiados para los estudios epidemiológicos. Además, es posible que las exposiciones de bajo nivel a los tóxicos del desarrollo sean importantes para algunos efectos funcionales.
Múltiples resultados y tiempo de exposición y dosis
De particular importancia con respecto a la identificación de los riesgos para el desarrollo en el lugar de trabajo son los conceptos de resultados múltiples y tiempo y dosis de exposición. Sobre la base de lo que sabemos sobre la biología del desarrollo, está claro que existen relaciones entre los resultados reproductivos, como el aborto espontáneo y el retraso del crecimiento intrauterino y las malformaciones congénitas. Además, se han demostrado efectos múltiples para muchos tóxicos del desarrollo (tabla 1).
Tabla 1. Ejemplos de exposiciones asociadas con múltiples puntos finales reproductivos adversos
| Exposición | Resultado | |||
| Aborto espontáneo | Malformación congénita | Bajo peso al nacer | Discapacidades del desarrollo | |
| Alcohol | X | X | X | X |
| Anestésico gases de efecto |
X | X | ||
| Lidera | X | X | X | |
| Disolventes orgánicos | X | X | X | |
| Fumar | X | X | X | |
Relevantes a esto son las cuestiones del tiempo de exposición y las relaciones dosis-respuesta. Durante mucho tiempo se ha reconocido que el período embrionario durante el cual ocurre la organogénesis (de dos a ocho semanas después de la concepción) es el momento de mayor sensibilidad a la inducción de malformaciones estructurales. El período fetal desde las ocho semanas hasta el término es el momento de la histogénesis, con un rápido aumento en el número de células y la diferenciación celular durante este tiempo. Es entonces cuando es más probable que se induzcan anomalías funcionales y retraso del crecimiento. Es posible que pueda haber relaciones entre la dosis y la respuesta durante este período en el que una dosis alta podría provocar un retraso del crecimiento y una dosis más baja podría provocar un trastorno funcional o conductual.
Toxicidad del desarrollo mediada por hombres
Aunque generalmente se considera que la toxicidad para el desarrollo es el resultado de la exposición de la hembra y el producto de la concepción, es decir, los efectos teratogénicos, cada vez hay más evidencia de estudios en animales y humanos sobre los efectos en el desarrollo mediados por machos. Los mecanismos propuestos para tales efectos incluyen la transmisión de sustancias químicas del padre al producto de la concepción a través del líquido seminal, la contaminación indirecta de la madre y el producto de la concepción por sustancias transportadas desde el lugar de trabajo al entorno doméstico a través de la contaminación personal y, como se señaló anteriormente, exposiciones paternas previas a la concepción. que resultan en cambios genéticos transmisibles (mutaciones).
Introducción a la Función Reproductiva Masculina y Femenina
La toxicidad para la reproducción tiene muchas diferencias únicas y desafiantes con respecto a la toxicidad para otros sistemas. Mientras que otras formas de toxicidad ambiental generalmente implican el desarrollo de una enfermedad en un individuo expuesto, debido a que la reproducción requiere la interacción entre dos individuos, la toxicidad reproductiva se expresará dentro de una unidad reproductiva o pareja. Este aspecto único, dependiente de la pareja, aunque obvio, hace que la toxicología reproductiva sea distinta. Por ejemplo, es posible que la exposición a un tóxico por parte de un miembro de una pareja reproductiva (p. ej., el hombre) se manifieste por un resultado reproductivo adverso en el otro miembro de la pareja (p. ej., mayor frecuencia de abortos espontáneos). Cualquier intento de abordar las causas ambientales de la toxicidad reproductiva debe abordar el aspecto específico de la pareja.
Hay otros aspectos únicos que reflejan los desafíos de la toxicología reproductiva. A diferencia de la función renal, cardíaca o pulmonar, la función reproductiva ocurre de manera intermitente. Esto significa que las exposiciones ocupacionales pueden interferir con la reproducción pero pasar desapercibidas durante los períodos en los que no se desea la fertilidad. Esta característica intermitente puede dificultar la identificación de un tóxico reproductivo en humanos. Otra característica única de la reproducción, que se deriva directamente de la consideración anterior, es que la evaluación completa de la integridad funcional del sistema reproductivo requiere que la pareja intente el embarazo.
Sistema Reproductor Masculino y Toxicología
La espermatogénesis y la espermiogénesis son los procesos celulares que producen células sexuales masculinas maduras. Estos procesos tienen lugar dentro de los túbulos seminíferos de los testículos del macho sexualmente maduro, como se muestra en la Figura 1. Los túbulos seminíferos humanos tienen de 30 a 70 cm de largo y de 150 a 300 mm de diámetro (Zaneveld 1978). Las espermatogonias (células madre) se sitúan a lo largo de la membrana basal de los túbulos seminíferos y son las células básicas para la producción de espermatozoides.
Figura 1. El sistema reproductor masculino
Los espermatozoides maduran a través de una serie de divisiones celulares en las que las espermatogonias proliferan y se convierten en espermatocitos primarios. Los espermatocitos primarios en reposo migran a través de uniones estrechas formadas por las células de Sertoli hacia el lado luminal de esta barrera testicular. Cuando los espermatocitos alcanzan la barrera de la membrana en los testículos, la síntesis de ADN, el material genético en el núcleo de la célula, está esencialmente completa. Cuando los espermatocitos primarios se encuentran realmente con la luz del túbulo seminífero, estos experimentan un tipo especial de división celular que ocurre solo en las células germinales y se conoce como meiosis. La división celular meiótica da como resultado la división de los pares de cromosomas en el núcleo, de modo que cada célula germinal resultante contiene solo una copia de cada hebra cromosómica en lugar de un par coincidente.
Durante la meiosis, los cromosomas cambian de forma al condensarse y volverse filamentosos. En un momento dado, la membrana nuclear que los rodea se rompe y los husos microtubulares se unen a los pares cromosómicos, lo que hace que se separen. Esto completa la primera división meiótica y se forman dos espermatocitos secundarios haploides. Luego, los espermatocitos secundarios se someten a una segunda división meiótica para formar un número igual de espermátidas portadoras de cromosomas X e Y.
La transformación morfológica de las espermátidas en espermatozoides se denomina espermiogénesis. Cuando se completa la espermiogénesis, la célula de Sertoli libera cada espermatozoide en la luz de los túbulos seminíferos mediante un proceso denominado espermiación. Los espermatozoides migran a lo largo del túbulo hasta la rete testis y hacia la cabeza del epidídimo. Los espermatozoides que salen de los túbulos seminíferos son inmaduros: incapaces de fertilizar un óvulo e incapaces de nadar. Los espermatozoides liberados en la luz del túbulo seminífero están suspendidos en un líquido producido principalmente por las células de Sertoli. Los espermatozoides concentrados suspendidos dentro de este fluido fluyen continuamente desde los túbulos seminíferos, a través de ligeros cambios en el medio iónico dentro de la rete testis, a través de los conductos eferentes y hacia el epidídimo. El epidídimo es un solo tubo muy enrollado (de cinco a seis metros de largo) en el que los espermatozoides pasan de 12 a 21 días.
Dentro del epidídimo, los espermatozoides adquieren progresivamente motilidad y capacidad fecundante. Esto puede deberse a la naturaleza cambiante del fluido en suspensión en el epidídimo. Es decir, a medida que las células maduran, el epidídimo absorbe componentes del líquido, incluidas las secreciones de las células de Sertoli (p. ej., proteína fijadora de andrógenos), aumentando así la concentración de espermatozoides. El epidídimo también contribuye con sus propias secreciones al líquido de suspensión, incluidas las sustancias químicas glicerilfosforilcolina (GPC) y carnitina.
La morfología del esperma continúa transformándose en el epidídimo. La gotita citoplasmática se desprende y el núcleo del espermatozoide se condensa aún más. Si bien el epidídimo es el principal reservorio de almacenamiento de esperma hasta la eyaculación, alrededor del 30% de los espermatozoides en una eyaculación se han almacenado en los conductos deferentes. La eyaculación frecuente acelera el paso de los espermatozoides a través del epidídimo y puede aumentar la cantidad de espermatozoides inmaduros (estériles) en el eyaculado (Zaneveld 1978).
Eyaculación
Una vez dentro de los conductos deferentes, los espermatozoides son transportados por las contracciones musculares de la eyaculación más que por el flujo de líquido. Durante la eyaculación, los fluidos son expulsados a la fuerza de las glándulas sexuales accesorias dando lugar al plasma seminal. Estas glándulas no expulsan sus secreciones al mismo tiempo. Más bien, la glándula bulbouretral (de Cowper) primero expulsa un líquido transparente, seguido de las secreciones prostáticas, los líquidos concentrados en espermatozoides de los epidídimos y la ampolla de los conductos deferentes y, finalmente, la fracción más grande, principalmente de las vesículas seminales. Así, el plasma seminal no es un fluido homogéneo.
Acciones tóxicas sobre la espermatogénesis y la espermiogénesis
Los tóxicos pueden interrumpir la espermatogénesis en varios puntos. Los más dañinos, debido a su irreversibilidad, son los tóxicos que matan o alteran genéticamente (más allá de los mecanismos de reparación) las espermatogonias o las células de Sertoli. Los estudios en animales han sido útiles para determinar la etapa en la que un tóxico ataca el proceso espermatogénico. Estos estudios emplean exposición a corto plazo a un tóxico antes del muestreo para determinar el efecto. Al conocer la duración de cada etapa espermatogénica, se puede extrapolar para estimar la etapa afectada.
El análisis bioquímico del plasma seminal proporciona información sobre la función de las glándulas sexuales accesorias. Los productos químicos que son secretados principalmente por cada una de las glándulas sexuales accesorias se seleccionan típicamente para que sirvan como marcador para cada glándula respectiva. Por ejemplo, el epidídimo está representado por GPC, las vesículas seminales por fructosa y la glándula prostática por zinc. Tenga en cuenta que este tipo de análisis proporciona solo información general sobre la función glandular y poca o ninguna información sobre los demás constituyentes secretores. La medición del pH y la osmolalidad del semen proporciona información general adicional sobre la naturaleza del plasma seminal.
El plasma seminal puede analizarse para detectar la presencia de un tóxico o su metabolito. Se han detectado metales pesados en el plasma seminal utilizando espectrofotometría de absorción atómica, mientras que los hidrocarburos halogenados se han medido en fluido seminal mediante cromatografía de gases después de la extracción o filtración con limitación de proteínas (Stachel et al. 1989; Zikarge 1986).
La viabilidad y motilidad de los espermatozoides en el plasma seminal es típicamente un reflejo de la calidad del plasma seminal. Las alteraciones en la viabilidad de los espermatozoides, medida por exclusión de tinción o por hinchazón hipoosmótica, o alteraciones en los parámetros de motilidad de los espermatozoides sugerirían efectos tóxicos postesticulares.
Los análisis de semen también pueden indicar si la producción de espermatozoides se ha visto afectada por un tóxico. El recuento de espermatozoides y la morfología de los espermatozoides proporcionan índices de la integridad de la espermatogénesis y la espermiogénesis. Por lo tanto, el número de espermatozoides en el eyaculado está directamente relacionado con el número de células germinales por gramo de testículo (Zukerman et al. 1978), mientras que la morfología anormal es probablemente el resultado de una espermiogénesis anormal. Los espermatozoides muertos o los espermatozoides inmóviles a menudo reflejan los efectos de los eventos postesticulares. Por lo tanto, el tipo o momento de un efecto tóxico puede indicar el objetivo del tóxico. Por ejemplo, la exposición de ratas macho al 2-metoxietanol resultó en una reducción de la fertilidad después de cuatro semanas (Chapin et al. 1985). Esta evidencia, corroborada por el examen histológico, indica que el objetivo de la toxicidad es el espermatocito (Chapin et al. 1984). Si bien no es ético exponer intencionalmente a los seres humanos a posibles tóxicos para la reproducción, los análisis de semen de eyaculados en serie de hombres expuestos inadvertidamente durante un breve período de tiempo a posibles tóxicos pueden proporcionar información útil similar.
La exposición ocupacional al 1,2-dibromocloropropano (DBCP) redujo la concentración de esperma en los eyaculados de una mediana de 79 millones de células/ml en hombres no expuestos a 46 millones de células/ml en trabajadores expuestos (Whorton et al. 1979). Al retirar a los trabajadores de la exposición, aquellos con recuentos reducidos de espermatozoides experimentaron una recuperación parcial, mientras que los hombres que habían sido azoospérmicos permanecieron estériles. La biopsia testicular reveló que el objetivo de DBCP eran las espermatogonias. Esto corrobora la gravedad del efecto cuando las células madre son el objetivo de los tóxicos. No hubo indicios de que la exposición de los hombres a DBCP estuviera asociada con un resultado adverso del embarazo (Potashnik y Abeliovich 1985). Otro ejemplo de un tóxico dirigido a la espermatogénesis/espermiogénesis fue el estudio de trabajadores expuestos al dibromuro de etileno (EDB). Tenían más espermatozoides con cabezas cónicas y menos espermatozoides por eyaculado que los controles (Ratcliffe et al. 1987).
El daño genético es difícil de detectar en el esperma humano. Varios estudios en animales que utilizan el ensayo letal dominante (Ehling et al. 1978) indican que la exposición paterna puede producir un resultado adverso en el embarazo. Los estudios epidemiológicos de grandes poblaciones han demostrado una mayor frecuencia de abortos espontáneos en mujeres cuyos maridos trabajaban como mecánicos de vehículos motorizados (McDonald et al. 1989). Dichos estudios indican la necesidad de métodos para detectar daño genético en el esperma humano. Estos métodos están siendo desarrollados por varios laboratorios. Estos métodos incluyen sondas de ADN para discernir mutaciones genéticas (Hecht 1987), cariotipo de cromosomas espermáticos (Martin 1983) y evaluación de la estabilidad del ADN mediante citometría de flujo (Evenson 1986).
Figura 2. Exposiciones asociadas positivamente con efectos adversos en la calidad del semen
La figura 2 enumera las exposiciones que se sabe que afectan la calidad del esperma y la tabla 1 proporciona un resumen de los resultados de los estudios epidemiológicos de los efectos paternos en los resultados reproductivos.
Tabla 1. Estudios epidemiológicos de los efectos paternos en el resultado del embarazo
| Referencia | Tipo de exposición u ocupación | Asociación con la exposición1 | Efecto |
| Estudios de población basados en registros | |||
| Lindbohm et al. 1984 | disolventes | – | Aborto espontáneo |
| Lindbohm et al. 1984 | Estación de servicio | + | Aborto espontáneo |
| Daniell y Vaughan 1988 | Disolventes orgánicos | – | Aborto espontáneo |
| McDonald et al. 1989 | La Mecánica | + | Aborto espontáneo |
| McDonald et al. 1989 | Procesamiento de alimentos | + | defectos de desarrollo |
| Lindbohm et al. 1991a | Óxido de etileno | + | Aborto espontáneo |
| Lindbohm et al. 1991a | refinería de petróleo | + | Aborto espontáneo |
| Lindbohm et al. 1991a | Impregnaciones de madera | + | Aborto espontáneo |
| Lindbohm et al. 1991a | Productos químicos de caucho | + | Aborto espontáneo |
| Olsen et al. 1991 | Metales | + | Riesgo de cáncer infantil |
| Olsen et al. 1991 | maquinistas | + | Riesgo de cáncer infantil |
| Olsen et al. 1991 | Smiths | + | Riesgo de cáncer infantil |
| Kristensen et al. 1993 | disolventes | + | Parto prematuro |
| Kristensen et al. 1993 | plomo y solventes | + | Parto prematuro |
| Kristensen et al. 1993 | Lidera | + | Muerte perinatal |
| Kristensen et al. 1993 | Lidera | + | Morbilidad del niño varón |
| Estudios de casos y controles | |||
| kucera 1968 | Industria de la impresión | (+) | Labio leporino |
| kucera 1968 | Pintar | (+) | Paladar hendido |
| Olsen 1983 | Pintar | + | Daño al sistema nervioso central |
| Olsen 1983 | disolventes | (+) | Daño al sistema nervioso central |
| Sever et al. 1988 | Radiación de bajo nivel | + | Defectos del tubo neural |
| Taskinen et al. 1989 | Disolventes orgánicos | + | Aborto espontáneo |
| Taskinen et al. 1989 | Hidrocarbonos aromáticos | + | Aborto espontáneo |
| Taskinen et al. 1989 | Dust | + | Aborto espontáneo |
| Garner et al. 1990 | La radiación | + | Leucemia infantil |
| Bonde 1992 | Soldadura | + | Tiempo hasta la concepción |
| Wilkins y sumideros 1990 | Agricultura | (+) | tumor cerebral infantil |
| Wilkins y sumideros 1990 | Construcción | (+) | tumor cerebral infantil |
| Wilkins y sumideros 1990 | Procesamiento de alimentos/tabaco | (+) | tumor cerebral infantil |
| Wilkins y sumideros 1990 | Metal | + | tumor cerebral infantil |
| Lindböhmn et al. 1991b | Lidera | (+) | Aborto espontáneo |
| Sallmen et al. 1992 | Lidera | (+) | Defectos congénitos |
| Veulemans et al. 1993 | Éter de etilenglicol | + | Espermiograma anormal |
| Chia y col. 1992 | Metales | + | Cadmio en semen |
1 – ninguna asociación significativa; (+) asociación marginalmente significativa; + asociación significativa.
Fuente: Adaptado de Taskinen 1993.
Sistema Neuroendocrino
El funcionamiento general del sistema reproductivo está controlado por el sistema nervioso y las hormonas producidas por las glándulas (el sistema endocrino). El eje neuroendocrino reproductivo del varón involucra principalmente el sistema nervioso central (SNC), la glándula pituitaria anterior y los testículos. Las entradas del SNC y de la periferia están integradas por el hipotálamo, que regula directamente la secreción de gonadotropinas por parte de la hipófisis anterior. Las gonadotropinas, a su vez, actúan principalmente sobre las células de Leydig dentro del intersticio y las células de Sertoli y germinales dentro de los túbulos seminíferos para regular la espermatogénesis y la producción de hormonas en los testículos.
Eje hipotálamo-pituitario
El hipotálamo secreta la neurohormona hormona liberadora de gonadotropina (GnRH) en la vasculatura porta hipofisaria para su transporte a la glándula pituitaria anterior. La secreción pulsátil de este decapéptido provoca la liberación concomitante de hormona luteinizante (LH) y, con menor sincronía y una quinta parte de la potencia, la liberación de hormona folículo estimulante (FSH) (Bardin 1986). Existe evidencia sustancial para apoyar la presencia de una hormona liberadora de FSH separada, aunque todavía no se ha aislado ninguna (Savy-Moore y Schwartz 1980; Culler y Negro-Vilar 1986). Estas hormonas son secretadas por la glándula pituitaria anterior. La LH actúa directamente sobre las células de Leydig para estimular la síntesis y liberación de testosterona, mientras que la FSH estimula la aromatización de testosterona a estradiol por parte de las células de Sertoli. La estimulación gonadotrópica provoca la liberación de estas hormonas esteroides en la vena espermática.
La secreción de gonadotropina es, a su vez, controlada por la testosterona y el estradiol a través de mecanismos de retroalimentación negativa. La testosterona actúa principalmente sobre el hipotálamo para regular la secreción de GnRH y, por lo tanto, reduce la frecuencia del pulso, principalmente, de la liberación de LH. El estradiol, por otro lado, actúa sobre la glándula pituitaria para reducir la magnitud de la liberación de gonadotropinas. A través de estos bucles de retroalimentación endocrina, la función testicular en general y la secreción de testosterona en particular se mantienen en un estado relativamente estable.
Eje pituitario-testicular
La LH y la FSH generalmente se consideran necesarias para la espermatogénesis normal. Presumiblemente, el efecto de la LH es secundario a la inducción de altas concentraciones intratesticulares de testosterona. Por lo tanto, la FSH de la hipófisis y la testosterona de las células de Leydig actúan sobre las células de Sertoli dentro del epitelio de los túbulos seminíferos para iniciar la espermatogénesis. La producción de espermatozoides persiste, aunque se reduce cuantitativamente, después de eliminar la LH (y presumiblemente las altas concentraciones intratesticulares de testosterona) o la FSH. La FSH es necesaria para iniciar la espermatogénesis en la pubertad y, en menor medida, para reiniciar la espermatogénesis detenida (Matsumoto 1989; Sharpe 1989).
El sinergismo hormonal que sirve para mantener la espermatogénesis puede implicar el reclutamiento por parte de la FSH de espermatogonias diferenciadas para entrar en la meiosis, mientras que la testosterona puede controlar etapas posteriores específicas de la espermatogénesis. La FSH y la testosterona también pueden actuar sobre las células de Sertoli para estimular la producción de uno o más factores paracrinos que pueden afectar el número de células de Leydig y la producción de testosterona por estas células (Sharpe 1989). La FSH y la testosterona estimulan la síntesis de proteínas por parte de las células de Sertoli, incluida la síntesis de proteína fijadora de andrógenos (ABP), mientras que la FSH sola estimula la síntesis de aromatasa e inhibina. La ABP se secreta principalmente en el líquido de los túbulos seminíferos y se transporta a la porción proximal de la cabeza del epidídimo, posiblemente sirviendo como transportador local de andrógenos (Bardin 1986). La aromatasa cataliza la conversión de testosterona en estradiol en las células de Sertoli y en otros tejidos periféricos.
La inhibina es una glicoproteína que consta de dos subunidades diferentes unidas por disulfuro, a y b. Aunque la inhibina inhibe preferentemente la liberación de FSH, también puede atenuar la liberación de LH en presencia de estimulación con GnRH (Kotsugi et al. 1988). FSH y LH estimulan la liberación de inhibina con una potencia aproximadamente igual (McLachlan et al. 1988). Curiosamente, la inhibina se secreta en la sangre de la vena espermática en forma de pulsos que son sincrónicos con los de la testosterona (Winters 1990). Esto probablemente no refleja las acciones directas de la LH o la testosterona sobre la actividad de las células de Sertoli, sino más bien los efectos de otros productos de las células de Leydig secretados en los espacios intersticiales o en la circulación.
La prolactina, que también es secretada por la glándula pituitaria anterior, actúa sinérgicamente con la LH y la testosterona para promover la función reproductiva masculina. La prolactina se une a receptores específicos en la célula de Leydig y aumenta la cantidad de complejo receptor de andrógenos dentro del núcleo de los tejidos sensibles a los andrógenos (Baker et al. 1977). La hiperprolactinemia se asocia con reducciones del tamaño de los testículos y la próstata, el volumen del semen y las concentraciones circulantes de LH y testosterona (Segal et al. 1979). La hiperprolactinemia también se ha asociado con impotencia, aparentemente independiente de la alteración de la secreción de testosterona (Thorner et al. 1977).
Si se miden metabolitos de hormonas esteroides en la orina, se debe considerar la posibilidad de que la exposición que se está estudiando pueda alterar el metabolismo de los metabolitos excretados. Esto es especialmente pertinente ya que la mayoría de los metabolitos se forman en el hígado, un objetivo de muchas sustancias tóxicas. El plomo, por ejemplo, redujo la cantidad de esteroides sulfatados que se excretaban en la orina (Apostoli et al. 1989). Los niveles sanguíneos de ambas gonadotropinas se elevan durante el sueño cuando el varón entra en la pubertad, mientras que los niveles de testosterona mantienen este patrón diurno durante la edad adulta en los hombres (Plant 1988). Por lo tanto, las muestras de sangre, orina o saliva deben recolectarse aproximadamente a la misma hora del día para evitar variaciones debidas a los patrones secretores diurnos.
Los efectos evidentes de la exposición tóxica dirigida al sistema neuroendocrino reproductivo tienen más probabilidades de revelarse a través de manifestaciones biológicas alteradas de los andrógenos. Las manifestaciones significativamente reguladas por andrógenos en el hombre adulto que pueden detectarse durante un examen físico básico incluyen: (1) retención de nitrógeno y desarrollo muscular; (2) mantenimiento de los genitales externos y órganos sexuales accesorios; (3) mantenimiento de la laringe agrandada y cuerdas vocales engrosadas que causan la voz masculina; (4) crecimiento de barba, vello axilar y púbico y recesión del vello temporal y calvicie; (5) libido y rendimiento sexual; (6) proteínas específicas de órganos en tejidos (p. ej., hígado, riñones, glándulas salivales); y (7) conducta agresiva (Bardin 1986). Las modificaciones en cualquiera de estos rasgos pueden indicar que la producción de andrógenos se ha visto afectada.
Ejemplos de efectos tóxicos
El plomo es un ejemplo clásico de un tóxico que afecta directamente al sistema neuroendocrino. Las concentraciones séricas de LH se elevaron en hombres expuestos al plomo durante menos de un año. Este efecto no progresó en hombres expuestos durante más de cinco años. Los niveles séricos de FSH no se vieron afectados. Por otro lado, los niveles séricos de ABP se elevaron y los de testosterona total se redujeron en hombres expuestos al plomo durante más de cinco años. Los niveles séricos de testosterona libre se redujeron significativamente después de la exposición al plomo durante tres a cinco años (Rodamilans et al. 1988). Por el contrario, las concentraciones séricas de LH, FSH, testosterona total, prolactina y 17-cetosteroides neutros totales no se alteraron en los trabajadores con niveles circulantes de plomo más bajos, aunque se alteró la frecuencia de distribución del conteo de espermatozoides (Assennato et al. 1986). .
La exposición de los pintores de astilleros al 2-etoxietanol también redujo el conteo de espermatozoides sin un cambio simultáneo en las concentraciones séricas de LH, FSH o testosterona (Welch et al. 1988). Por lo tanto, los tóxicos pueden afectar la producción de hormonas y las medidas de esperma de forma independiente.
Los trabajadores masculinos involucrados en la fabricación del nematocida DBCP experimentaron niveles séricos elevados de LH y FSH y reducción del recuento de espermatozoides y la fertilidad. Aparentemente, estos efectos son secuelas de las acciones del DBCP sobre las células de Leydig para alterar la producción o la acción de los andrógenos (Mattison et al. 1990).
Varios compuestos pueden ejercer toxicidad en virtud de la similitud estructural con las hormonas esteroides reproductivas. Por lo tanto, al unirse al receptor endocrino respectivo, los tóxicos pueden actuar como agonistas o antagonistas para alterar las respuestas biológicas. La clordecona (Kepone), un insecticida que se une a los receptores de estrógeno, redujo el conteo y la motilidad de los espermatozoides, detuvo la maduración de los espermatozoides y redujo la libido. Si bien es tentador sugerir que estos efectos se deben a que la clordecona interfiere con las acciones de los estrógenos a nivel neuroendocrino o testicular, en estos estudios no se demostró que los niveles séricos de testosterona, LH y FSH se alteraran de manera similar a los efectos de la terapia con estradiol. . El DDT y sus metabolitos también exhiben propiedades esteroides y podría esperarse que alteren la función reproductiva masculina al interferir con las funciones de las hormonas esteroides. Los xenobióticos como los bifenilos policlorados, los bifenilos polibromados y los pesticidas organoclorados también pueden interferir con las funciones reproductivas masculinas al ejercer una actividad agonista/antagonista estrogénica (Mattison et al. 1990).
función sexual
La función sexual humana se refiere a las actividades integradas de los testículos y las glándulas sexuales secundarias, los sistemas de control endocrino y los componentes conductuales y psicológicos de la reproducción (libido) basados en el sistema nervioso central. La erección, la eyaculación y el orgasmo son tres eventos distintos, independientes, fisiológicos y psicodinámicos que normalmente ocurren simultáneamente en los hombres.
Hay pocos datos confiables disponibles sobre los efectos de la exposición ocupacional en la función sexual debido a los problemas descritos anteriormente. Se ha demostrado que las drogas afectan cada una de las tres etapas de la función sexual masculina (Fabro 1985), lo que indica la posibilidad de que las exposiciones ocupacionales ejerzan efectos similares. Los antidepresivos, los antagonistas de la testosterona y los estimulantes de la liberación de prolactina reducen eficazmente la libido en los hombres. Los fármacos antihipertensivos que actúan sobre el sistema nervioso simpático inducen impotencia en algunos hombres, pero sorprendentemente, priapismo en otros. La fenoxibenzamina, un antagonista adrenoceptivo, se ha utilizado clínicamente para bloquear la emisión seminal pero no el orgasmo (Shilon, Paz y Homonnai 1984). Los fármacos antidepresivos anticolinérgicos permiten la emisión seminal mientras bloquean la eyección seminal y el orgasmo, lo que da como resultado que el plasma seminal se filtre desde la uretra en lugar de ser expulsado.
Las drogas recreativas también afectan la función sexual (Fabro 1985). El etanol puede reducir la impotencia al tiempo que mejora la libido. La cocaína, la heroína y las altas dosis de cannabinoides reducen la libido. Los opiáceos también retrasan o deterioran la eyaculación.
La amplia y variada gama de productos farmacéuticos que se ha demostrado que afectan el sistema reproductivo masculino respalda la idea de que los productos químicos que se encuentran en el lugar de trabajo también pueden ser tóxicos para la reproducción. Se necesitan métodos de investigación que sean confiables y prácticos para las condiciones de estudio de campo para evaluar esta importante área de toxicología reproductiva.
" EXENCIÓN DE RESPONSABILIDAD: La OIT no se responsabiliza por el contenido presentado en este portal web que se presente en un idioma que no sea el inglés, que es el idioma utilizado para la producción inicial y la revisión por pares del contenido original. Ciertas estadísticas no se han actualizado desde la producción de la 4ª edición de la Enciclopedia (1998)."